果汁饮料中6种苯系物的顶空气相色谱分析
陈艳彬,铁军,宋曦,念红丽
(1.长治学院生物科学与技术系,山西长治046011;2.陇东学院农林科技学院,甘肃庆阳745000;3.北京市经济管理学校,北京100036)
由于塑料制品的良好性能和低廉的价格,使其在食品领域应用广泛。然而食品包装用的塑料制品含有多种有机残留物,例如苯系物,会对人体健康造成一定的危害[1]。塑料与食品接触过程中有害物质易溶出并迁移到食品中,严重危害人体健康。苯系物对人的神经和心血管系统有明显的毒性,对造血机能有抑制作用,如白血球减少、贫血等[2]。
果汁中的苯系物主要是原料水、包装材料、环境污染以及果汁中的添加剂在加工过程中衍生而成。目前国内外对于饮用水中苯及其同系物的检测方法报道较多[3-6],对果汁饮料中苯的检测鲜见报道。顶空气相色谱法具有灵敏度高、操作简单、不需要特殊设备等优点,是一种符合“绿色分析化学”要求的分析手段。因此本文研究了用顶空气相色谱法测定果汁饮料中苯系物的含量。
1 材料与方法
1.1 仪器、试剂和样品
1.1.1 仪器
Clarus 600型气相色谱仪:美国 PerkinElmer公司,配 FID检测器;OV-1701毛细管色谱柱:50 m×0.20 mm×0.32 μm;FFAP(50 m×0.25 mm×0.5 μm):兰州化物所;AutoHS自动顶空进样器:成都科林分析技术有限公司。
1.1.2 试剂
苯、甲苯、邻二甲苯、间二甲苯、对二甲苯、异丙苯6种苯系物标准品,纯度99.5%:上海安谱科技有限公司;甲醇(色谱纯):德国 Merck公司;氯化钠(分析纯):天津市红岩化学试剂厂,550℃烘2 h,干燥器内保存备用。
1.1.3 样品
各种果汁:购于大型超市。
1.2 分析条件
1.2.1 色谱分析条件
色谱柱:FFAP 柱(50 m×0.25 mm×0.5 μm);
检测器:氢火焰离子检测器(FID),温度230℃;
程序升温:初始温度 70℃(5 min),7℃/min至130 ℃(3 min);
进样口:温度 200℃,柱流量,0.75 mL/min,分流进样,分流比 5∶1;
载气:高纯氮气(99.999%)。
1.2.2 顶空分析条件
炉温50℃时恒温30 min,针温85℃,传输线85℃,加压置换 1min,进样 4 s,载气压力 2.0×105Pa。
1.3 方法
1.3.1 混合标准溶液的配制
分别准确量取6种苯系物标准品适量,用甲醇溶解后转移到 10 mL容量瓶中,甲醇定容,配成相应的混合标准储备液,4℃下密封保存。用前采用梯度稀释法将标准储备液逐级稀释。
1.3.2 样品分析
取15种不同的果汁饮料样品各 5 mL于22 mL顶空瓶中,均加入2.0 g氯化钠混匀,密封后进行测定分析。
2 结果与讨论
2.1 色谱柱的选择
色谱柱对混合物的分离主要取决于色谱柱中固定相的选择性和极性[7]。为了实现苯系物的完全分离,分别选取了中极性毛细管 OV-1701、强极性毛细管柱FFAP两种色谱柱进行分离,结果发现 OV-1701柱存在间、对二甲苯难分离,FFAP则能对苯系物各组分实现完全基线分离,各色谱峰峰形对称,分离度高,是实现分离和分析6种苯系物的理想柱子。本试验选择FFAP柱。

图1 FFAP色谱柱对卤代烃的分离色谱图Fig.1 Chromatogram of benzene substances on FFAP
2.2 顶空测定条件的选择
2.2.1 平衡温度的影响
样品的平衡温度与蒸气压直接相关,它影响分配系数[8],样品中组分的蒸汽分压随平衡温度升高而加大,提高加热温度就可以提高灵敏度。试验对顶空平衡温度进行了选择,考察了 40、45、50、55、60 ℃不同平衡温度对测定结果的影响,以不同平衡温度下各被测组分的峰面积来表示方法的检测灵敏度,结果见图2。

图2 平衡温度和峰面积的关系Fig.2 Relationship between equilibrium temperature and peak areas
由图2结果可以看出:随着温度的升高,峰面积有所增大,灵敏度也有所提高,但平衡温度超过50℃时变化趋于平缓。且随着温度的逐渐升高,水蒸气增多,测定结果的重复性降低,高温容易将水蒸气带入色谱系统,对仪器造成损害。因此综合样品的稳定性、重复性和仪器等条件,选择50℃为平衡温度。
2.2.2 平衡时间的影响
被测样品在选定的平衡温度下热平衡时,各被测组分需经过一定的时间才能建立气-液平衡。试验在选定顶空平衡温度为50℃的情况下对平衡时间进行了选择,考察了 10、20、30、40、50 min 不同平衡时间对测定结果的影响,以不同平衡时间下各被测组分的峰面积来表示方法的检测灵敏度,结果见图3。

图3 平衡时间和峰面积的关系Fig.3 Relationship between equilibrium time and peak areas
由图3结果表明:随着时间的增加,混合标样的峰面积增大,从30 min~50 min峰面积变化平缓,为保证样品的平行性和重复性,选择30 min为平衡时间。
2.2.3 针温和传输线温度的选择
针温和传输线温度对分析结果也有重要的影响,温度太低会使一部分的样品在管路中冷凝和吸附被消耗在传输线管壁上。试验选择在50℃时平衡30 min,在针温和传输线温度分别为 65、75、85、95、105 ℃下进样测定,结果见图4。
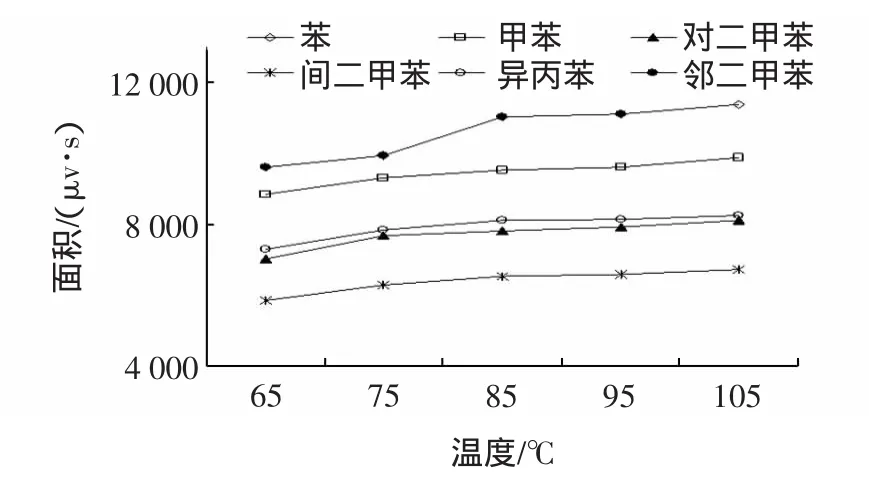
图4 针温和传输线温度和峰面积的关系Fig.4 Relationship between needle,transmission-line temperature and peak areas
由图4结果可以看出,6种苯系物的峰面积随着针温、传输线温度升高而增大,当温度达到85℃后变化趋于平缓,针温和传输线温度对于峰面积的影响相对于平衡温度和平衡时间较小。本试验选择针温和传输线温度为85℃。
2.2.4 样品基体的选择
氯化钠具有提高溶液的离子强度,降低有机化合物在水中溶解度的作用[9],试验对同一样品分别加入1、1.5、2.0、2.5、3 g 氯化钠进行分析,同时做未加盐的顶空分析,结果发现加盐后灵敏度大幅度提高,而且随氯化钠加入量的增加而增大,当氯化钠加入量为2.0g时样品溶液呈现饱和状态,灵敏度达到最大,本试验选择加2.0 g氯化钠。
2.3 超声时间的选择
由于饮料基质与苯系物标准溶液基质不同,饮料中的各种复杂组分容易使样品加标回收率降低,本试验考察了将样品密封加热前超声0、5、10、15 min的处理,试验结果见表1。
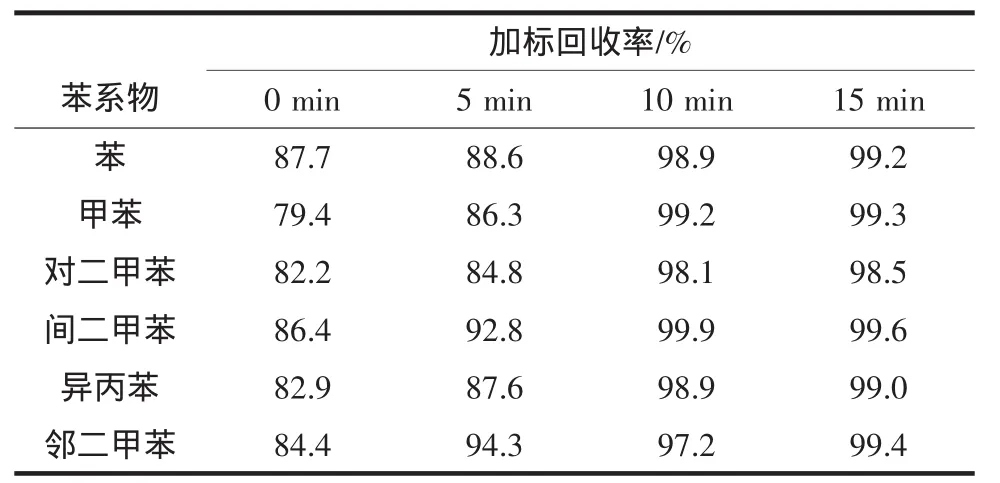
表1 不同超声时间下的回收率Table 1 The recovery results of different ultrasonic time
由表1结果可以看出,超声处理可以明显提高样品的加标回收率,随着超声时间的延长样品的加标回收率呈逐渐上升趋势,当超声时间超过10 min时变化趋于缓慢,本实验选择将样品在加热前超声10 min。这可能是因为超声减少了饮料复杂的样品基体对测定结果的影响,使饮料中的苯系物更好地挥发出来,提高了测定灵敏度和准确度。
2.4 方法评价
2.4.1 方法线性范围和检出限
线性范围是待测物浓度与仪器的响应信号(峰高或峰面积)呈线性关系并且能满足定量要求的浓度范围[10]。准确吸取不同浓度的6种苯系物混合标准溶液5 mL进行分析测定,以峰面积(Y)对相应组分的质量浓度(ρ)进行线性分析,得到各组分的线性方程与相关系数如表2所示。以信噪比为S/N=2时各组分浓度为最低检测限,结果见表2。

表2 6种苯系物的线性方程、相关系数和检测限Table 2 Linear equations,crrelation and linear ranges of 6 benzene substances
由表2结果可知,6种苯系物有良好的线性关系,R 值在 0.993~0.999 之间,检测限在 2.1 μg/L~9.8 μg/L之间。
2.4.2 方法的回收率和精密度
采用标准添加法,在5 mL饮料样品中加入2.0 g氯化钠,分别添加低、中、高3个浓度水平的标准溶液,按照上述方法进样分析。回收率和相对标准偏差结果 见表3。

表3 苯系物在样品中的回收率及方法精密度(n=6)Table 3 Recoveries and analytixal precision of benzene substances determination in sample(n=6)
由表3结果可知6种苯系物具有较高的回收率,在 89.4%~99.5% 之间,RSD在2.8%~7.5% 之间,具有良好的精密度。
2.4.3 实际样品分析
采用顶空-气相色谱法对市售 15种果汁饮料进行分析,均未检测出。说明市售的果汁饮料是安全可靠的。
3 结论与讨论
1)FFAP柱能实现6种苯系物的完全分离,且各色谱峰峰形对称,分离度高。
2)顶空测定条件为平衡温度为50℃时平衡30min,针温和传输线温度为85℃。
3)方法具有良好的线性关系,R值在 0.993~0.999之间,检测限在 2.1 μg/L~9.8 μg/L 之间。
4)方法具有良好的回收率和精密度,回收率在89.4%~99.5% 之间,RSD在2.8%~7.5%之间。
采用顶空气相色谱法测定果汁饮料中苯系物,该分析方法准确、简便、快速,可以用于实际样品的检测分析。
[1] 李伟,许华,常宇文,等.顶空-气相色谱法同时测定塑料食品包装袋中11种有机溶剂残留量[J].化学试剂,2007,29(8):481-482
[2] 顾寿永,夏昭林.苯致血液毒性易感性标志物研究进展[J].职业卫生与应急救援,2004,22(1):6-8
[3] 华树岸,黄秋艳,李志涛.吹扫捕集-气相色谱-质谱联用测定城市饮用水中苯系物[J].光谱实验室,2005,22(3):641-644
[4] 魏复盛,齐文启.水和废水监测分析方法[M].北京:中国环境科学出版社,2002,500-516
[5] RezaeeM,Assad i Y,H osse ini M M,et al.Determination of organic compounds in water using dispersive liquid-liquid microextraction[J].Journal of Chromatography A,2006,23(4):1116:1-9
[6] 贾薇,刘丽,赵蕾,等.气相色谱-质谱法检测水中苯系物[J].中国公共卫生,2003,19(11):1375-1376
[7] 饶竹,李松,佟柏龄,等.顶空气相色谱法测定地层水中的苯系物[J].岩矿测试,2004(2):97-101
[8] 陈小丽,陈敏,梁春霞.顶空气相色谱法测定水中三氯甲烷及四氯化碳[J].中国热带医学,2009,9(1):155-156
[9]陈淑彩,孙仕萍.顶空气相色谱法测定饮用水中多种挥发性有机物[J].中国卫生检验杂志,2008,18(9):1792-1793
[10]呼世斌,李敬慈.分析化学[M].北京:世界图书出版公司,1996:20-26

