正交试验优选双花抗病毒口服液提取工艺
胡玉良 杨素红 邓健安
(广州中医药大学附属中山中医院,广东 中山 528400)
正交试验优选双花抗病毒口服液提取工艺
胡玉良 杨素红 邓健安
(广州中医药大学附属中山中医院,广东 中山 528400)
目的:优选双花抗病毒口服液的提取工艺。方法:采用L9(34)正交试验筛选提取工艺;以加水量(A)、提取时间(B)、浸泡时间(C)作为考察因素,以挥发油提取量为指标,优选广藿香、鱼腥草、连翘3味药材的挥发油提取工艺;以加水量(A)、浸泡时间(B)、提取时间(C)、提取次数(D)为考察因素,以绿原酸和连翘苷含量为指标,优选药材的水提工艺。结果:挥发油最佳提取工艺为:加10倍量水,直接提取4小时;水提取最佳工艺为:加8倍量水,浸泡0.5小时,煎煮2次,每次1.5小时。结论:优选得到的提取工艺质量稳定、可行。
双花抗病毒口服液;挥发油;绿原酸;连翘苷;提取工艺;正交试验
双花抗病毒口服液为本院院内制剂,由金银花、野菊花、鱼腥草、板蓝根、广藿香、连翘等11味中药组成。由于目前制剂制备工艺为水煮醇沉,鱼腥草、广藿香、连翘等药材挥发油含量高,有效成分易流失,故采用水蒸气蒸馏法先行提取挥发油,药渣再与其余中药进行水提的工艺路线[1],对主要工艺参数进行正交试验,筛选出最佳的提取工艺。
1 仪器与试药
挥发油提取器(上海求精玻璃仪器厂);DZTW型调温电热套(北京市永光明医疗仪器厂);BS224S型电子天平(北京赛多利斯仪器系统有限公司d=0.000 1 g);Agilent 1100系列高效液相色谱仪;绿原酸对照品(批号:110753-201314,中国药品生物制品检验所);连翘苷对照品(批号:110821-201213,中国药品生物制品检验所);甲醇、乙腈为色谱纯;水为重蒸馏水。其余试剂为分析纯。所用药材均购于广东致信药业有限公司,经鉴定符合《中国药典》2010年版规定。
2 方法与结果
2.1 挥发油提取工艺研究[2]
2.1.1 正交试验设计选用对挥发油提取影响较大的加水量(A)、提取时间(B)和浸泡时间(C)作为考察因素,每个因素设计3个水平,采用L9(34)正交表进行试验,见表1。
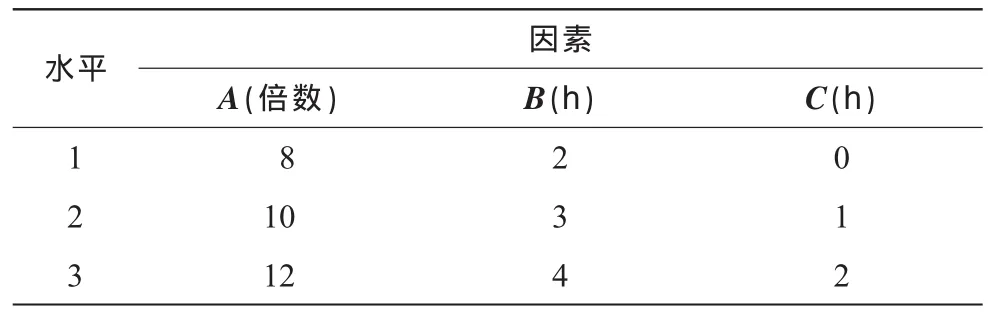
表1 正交试验因素和水平
2.1.2 试验方法与结果取连翘30 g、鱼腥草30 g、广藿香15 g,按表1试验序列号各条件分别进行提取,收集挥发油,读取挥发油量。结果见表2,方差分析结果见表3。
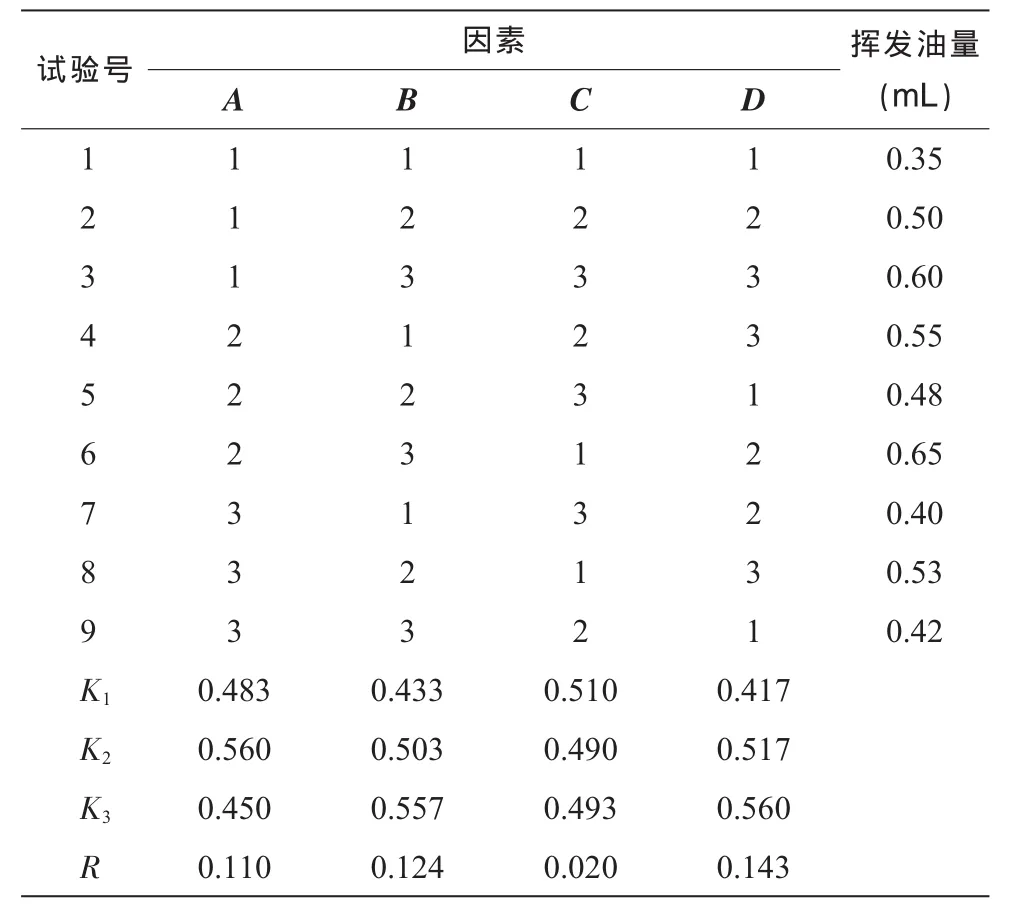
表2 挥发油提取工艺正交试验结果
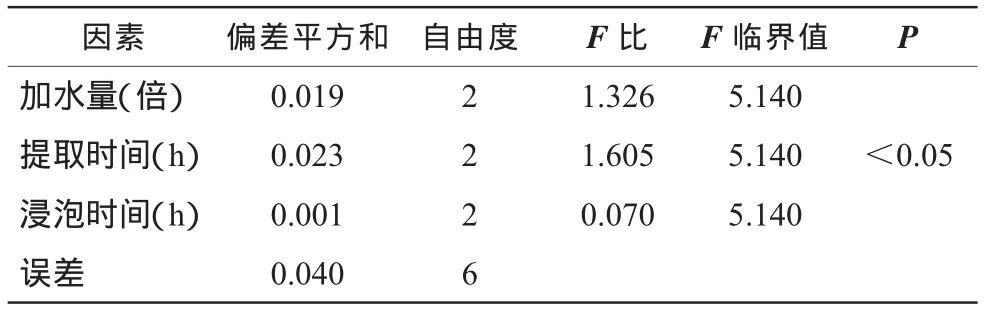
表3 挥发油提取工艺方差分析
2.1.3 结果分析由表2可知,影响实验因素依次为:B> A>C,且A2>A1>A3,B3> B2> B1[13],C1> C3> C2,可初步得到最佳工艺条件为A2B3C1。由表 3方差分析也可以看出提取时间对挥发油的提取量有显著性影响(P<0.05),而其他两个因素对挥发油提取量的影响都无显著性意义(P>0.05),故A2B3C1为挥发油提取工艺最佳方案。
2.1.4 验证试验取药材按正交试验得到的最佳工艺进行验证,即加入10倍水,提取4小时,平行试验3次。为考察提取是否完全,试验后再提取1小时。结果见表 4。
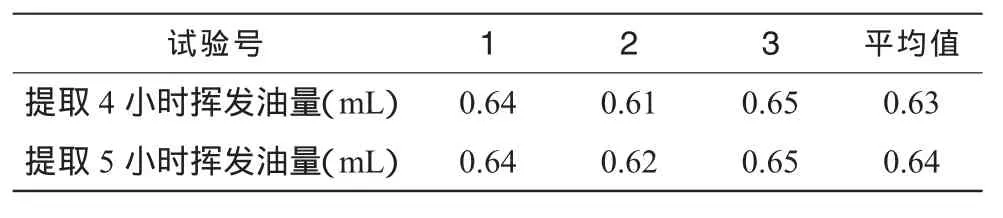
表4 挥发油提取工艺验证试验结果
由表4可知,提取4小时挥发油已提取完全,所选提取条件稳定可行。
2.2 水提工艺研究[3]
2.2.1 正交试验设计水提工艺选取了加水量(A)、浸泡时间(B)、提取时间(C)和提取次数(D)作为考察因素,每个因素分别设计3个水平,以绿原酸和连翘苷含量为评价指标,采用 L9(34)正交表进行试验。见表5。
表5 水提工艺正交试验设计因素和水平
按照处方比例,称取除连翘、鱼腥草、广藿香外的药材,加入提取挥发油后的药渣,按照正交试验安排表进行试验,收集提取液,合并提取液和提取挥发油后的药液,滤过,滤液浓缩至100 mL,即得样品。
2.2.2 绿原酸含量的测定[4]
2.2.2.1 色谱条件 色谱柱为 Boston Green ODS(4.6 mm×250 mm,5 μm),流动相为乙腈-0.1%磷酸溶液(12∶88),检测波长327 nm,柱温30℃,流速1.0 mL/min[15]。色谱见图1。
2.2.2.2 供试品溶液的制备 精密量取样品2 mL,置50 mL棕色量瓶中,加50%甲醇溶液至刻度,摇匀,滤过,取续滤液,即得。
2.2.2.3 对照品溶液的制备 精密称取 11.2 mg绿原酸对照品,置100 mL棕色量瓶中,用甲醇溶解并定容至刻度,即得0.112 mg/mL的对照品储备液。精密量取2 mL置10 mL棕色量瓶中,加甲醇稀释至刻度,摇匀,作为对照品溶液。
2.2.2.4 测定法 分别精密量取对照品溶液及供试品溶液各20 μL注入液相色谱仪,测定绿原酸含量。
2.2.3 连翘苷含量的测定[4]
2.2.3.1 色谱条件 色谱柱为 Boston Green ODS(4.6 mm ×250 mm,5 μm),流动相为乙腈-水(25∶75),检测波长 277 nm,柱温 30 ℃,流速1.0 mL/min[16]。色谱见图2。
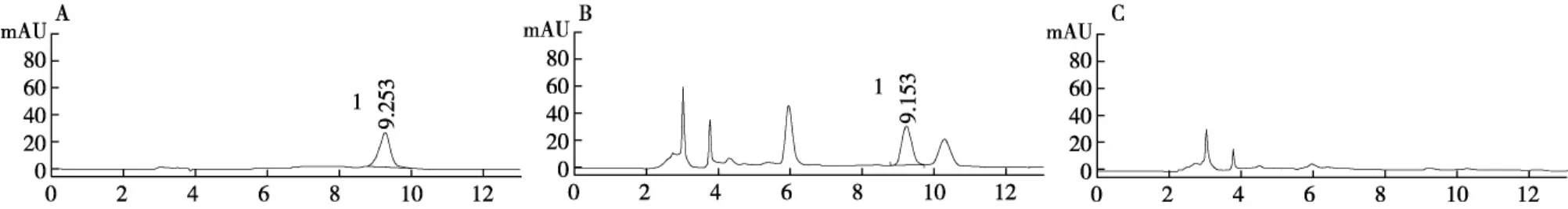
图1 绿原酸的高效液相色谱
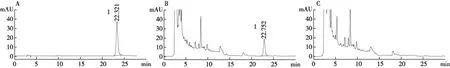
图2 连翘苷的高效液相色谱
2.2.3.2 供试品溶液的制备 精密量取样品1 mL,加在中性氧化铝柱(100~ 120目,1 g,内径为1 cm)上,用90%乙醇80 mL洗脱,收集洗脱液,浓缩至干,残渣用50%甲醇溶解,转移至2 mL量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得。
2.2.3.3 对照品溶液的制备 精密称取连翘苷对照品10.5 mg,置50 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得0.21 mg/mL对照品储备溶液。精密量取2 mL置10 mL棕色量瓶中,加甲醇稀释至刻度,摇匀,作为对照品溶液。
2.2.3.4 测定法 分别精密量取对照品溶液及供试品溶液各20 μL注入液相色谱仪,测定连翘苷含量。
2.2.4 结果与分析正交试验结果及方差分析情况见表6~ 8。
表6直观分析结果表明,提取次数是最主要的影响因素。以绿原酸含量为指标,根据各因素各水平的K值比较,初步确定最佳工艺为 A3B2C2D3,即药材加 12倍水,浸泡 0.5 h,提取 3次,每次1.5 h;以连翘苷含量为指标,根据各因素各水平的K值比较,初步确定最佳工艺为A1B2C2D3,即药材加8倍水,浸泡0.5 h,提取3次,每次1.5 h。从表7、表8方差分析可知,提取时间对绿原酸含量和连翘苷含量都有显著影响,加水量只对连翘苷含量有显著意义,从节约成本角度来看,最终确定水提取工艺为 A1B2C2D2,即药材加 8倍水,浸泡0.5 h,提取 2次,每次1.5 h。
2.2.5 验证试验根据所选的最佳提取工艺进行3次验证试验。绿原酸含量分别为 0.157,0.156,0.147 mg/mL,平均含量为0.153 mg/mL。连翘苷含量分别为0.117,0.113,0.111 mg/mL,平均含量为0.114 mg/mL。说明该工艺科学合理,质量稳定。
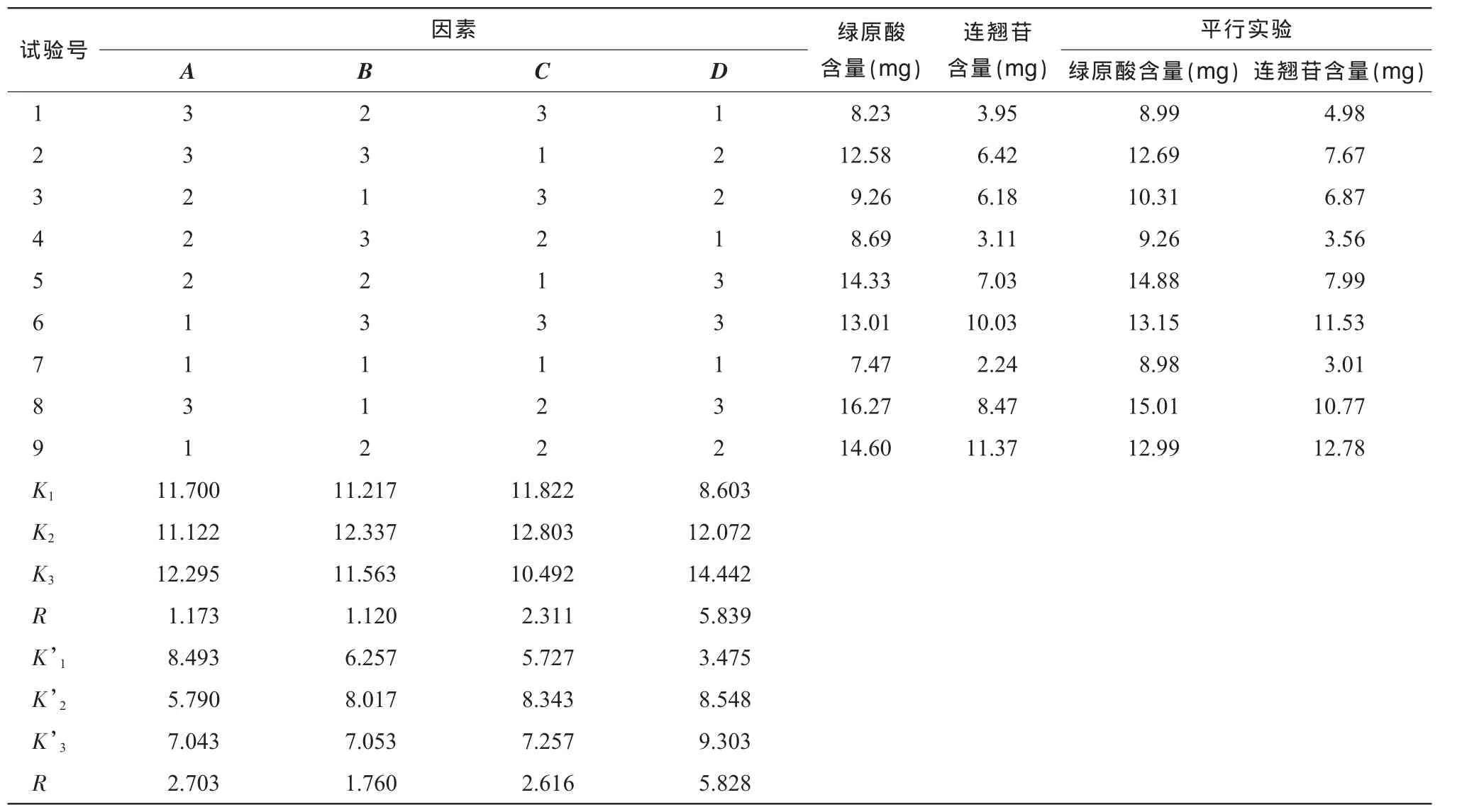
表6 水提工艺正交试验结果
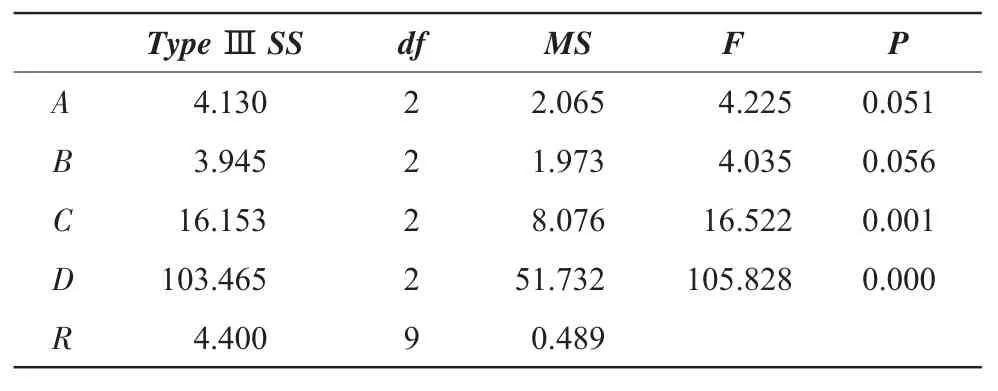
表7 绿原酸含量方差分析(R2=0.967;调整R2=0.937)
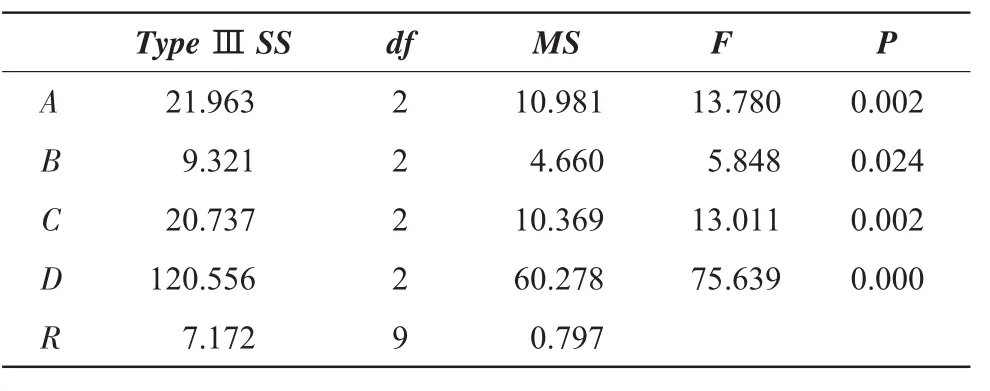
表8 连翘苷含量方差分析(R2=0.960;调整R2=0.925)
3 讨论
连翘为果实类药材,有效成分的提出比较慢,但提取挥发油时已经经历了一次水提,有效成分已经大部分被提取了,在水提工艺中,又被提取两次,连翘苷基本提取完全。金银花和野菊花为花类药材,有效成分的提出比较快,水提两次也基本提取完全。
对按原工艺进行3次试验和按优选工艺验证试验的样品进行质量比较,结果原工艺样品中挥发油鉴别斑点均弱于优选工艺样品;绿原酸含量分别为 0.138,0.129,0.140 mg/mL,平均含量为0.136 mg/mL,连翘苷含量分别为 0.101,0.105,0.098 mg/mL,平均含量为 0.101 mg/mL,均低于优选工艺样品。证明优选工艺能够提高制剂有效成分的得率,提高了制剂质量。
[1] 宋敏,李峰,李清芳.抗病毒口服液制备工艺及临床疗效评价[J].河南大学学报(医学科学版),2001,20(4):44-45.
[2] 邓丽明,林华庆,刘国宏,等.抗病毒口服液挥发油提取工艺的研究[J].广东药学院学报,2007,23(2):119-120.
[3] 王剑林,王冰.正交设计优选抗病毒口服液的提取工艺[J].亚太传统医药,2010,8(6):28-30.
[4] 国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010.
Optimization of Extraction Process of Shuanghua Kangbingdu Oral Liquid by Orthogonal Test
Hu Yuliang,Yang Suhong,Deng Jianan
(Zhongshan Hospital of Guangzhou University of TCM,Guangdong Zhongshan 528400,China)
Objective:To study the optimal extraction process of shuanghua kangbingdu oral liquid.Methods:Orthogonal design was carried for screening the extraction process.Water volume,extracting time and soaking time were used as the investigating factors and the yield of volatile oil as index to select the optimal extracting condition for volatile oil from patchouli,houttuynia cordata and forsythia,and with water addition,soaking time,extraction time and extraction times as factors,and the content of phillyrin in chlorogenic acid as the evaluation index to select the optimal extracting process for water.Results:The optimal extraction conditions for volatile oil included 4 hours of extraction with 10 times of water volume,the optimal extracting process for water was 0.5 hour of soaking time with 8 times of water volume and decoction 2 times,1.5 hour each time.Conclusion:The optimized extraction process is stable with a good feasibility.
Shuanghua Kangbingdu Oral Liquid;Volatile Oil;Chlorogenic Acid;Forsythin;Extraction Process;Orthogonal Test
10.3969/j.issn.1672-5433.2014.10.004
2014-07-10)
中山市医学科研项目(2014A020274)
胡玉良,女,主管药师。研究方向:制剂工艺与质量标准。通讯作者E-mail:hyliang2010@139.com

