灵芝三萜酸组分高效液相色谱指纹图谱初探
魏晓霞 李鹏 孙红 庄捷
(1福建省立医院药学部,福建福州 350001;2福建医科大学药学院天然药物学系,350004)
灵芝三萜酸组分高效液相色谱指纹图谱初探
魏晓霞1李鹏2孙红1庄捷1
(1福建省立医院药学部,福建福州 350001;2福建医科大学药学院天然药物学系,350004)
目的:建立灵芝三萜酸组分(GLA)的指纹图谱,为其质量控制提供依据。方法:使用植物组织破碎法提取GLA,利用高效液相色谱法建立GLA的指纹图谱。结果:GLA高效液相色谱指纹图谱中有8个峰为其主要特征,其α值分别为0.68,0.73,0.90,0.95,1.00,1.12,1.36,1.46。结论:所建立的RP-HPLC指纹图谱分析方法可为GLA的质量控制提供理论依据。
灵芝三萜酸;指纹图谱;高效液相色谱法
灵芝(Ganoderma lucidum[Leys.ex Fr.]Karst)为多孔菌科(polyproraceae)、灵芝属(Ganoderma)真菌植物赤芝(Ganoderma lucidum[Leys.ex Fr.] Karst)或紫芝(Ganoderma japonicum[Fr.]Lloyd)的干燥子实体[1]。灵芝性温、味甘,多分布于闽、贵、云、冀、苏、吉、浙等省,在我国已有悠久的药用历史,始载于《神农本草经》,具有补中益气、扶正固本、滋补强壮之功效,是一种珍贵的中药材[2]。三萜类化合物是灵芝主要成分之一。其中灵芝三萜酸组分(GLA)是灵芝三萜中的一大类成分,具有多种药理活性,前期研究发现其具有一定抗肿瘤[3]和保肝作用[4],本实验利用反相高效液相色谱(RP-HPLC)技术,建立GLA的高效液相色谱指纹图谱,为GLA的质量控制提供实验依据。
1 仪器与药品
1.1 药材
灵芝子实体精粉,3批次(批号GC-L3-20120821、GC-L3-20120922、GC-L3-20121010),由福建仙芝楼生物科技有限公司提供。
1.2 试剂
乙腈、甲醇为色谱纯(国药集团化学试剂有限公司);无水乙醇、乙酸乙酯、石油醚、冰乙酸均为分析纯(国药集团化学试剂有限公司);碳酸氢钠为化学纯(国药集团化学试剂有限公司)。
1.3 仪器
AB204-E电子分析天平(Mettler Toledo公司);JHBE-50型闪式提取器(北京金鼐科技发展有限公司);HH-4型数显恒温水浴锅(国华电器有限公司);RE-52A旋转蒸发器(上海亚荣生化仪器厂);Agilent 1100高效液相色谱仪(美国Agilent公司),配二极管阵列检测器,自动进样器;处理软件(Agilent化学工作站)。
2 方法
2.1 供试品制备
将灵芝子实体精粉经无水乙醇闪式提取、抽滤与减压蒸馏后,无水乙醇提取浸膏拌硅藻土后,以石油醚索氏提取除杂后再用乙酸乙酯提取,乙酸乙酯提取液用饱和NaHCO3溶液萃取,NaHCO3层酸化后再用乙酸乙酯萃取,减压浓缩真空干燥即得GLA[5]。共制备3批次来源于灵芝子实体精粉的GLA样品备用。参照《中华人民共和国药典》RP-HPLC的有关规定[6],精确称取GLA样品,用乙腈配成10 mg/mL供试品,0.45 μm微孔滤膜过滤,RP-HPLC进样量5 μL。
2.2 色谱条件
依利特C18色谱柱(250 mm×4.6 mm,5 μm);填料Hypersil ODS 25 μm(柱号E1720569);流动相甲醇-水(含2%乙酸),梯度洗脱条件见表1;检测波长252 nm;进样量5 μL;流速0.8 mL/min;柱温35℃。

表1 线性梯度洗脱条件(体积百分比%)
2.3 HPLC分析
取3批次供试品溶液5 μL,注入高效液相色谱仪,自动积分记录色谱图(图1、图2、图3)和各色谱峰的保留时间,以面积归一化法计算各色谱峰的相对峰面积。
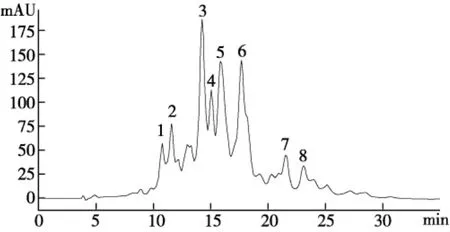
图1 GLA的RP-HPLC图(批次GC-L3-20120821)
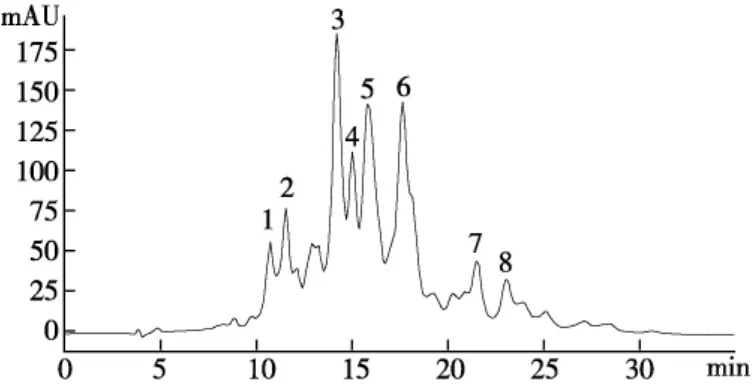
图2 GLA的RP-HPLC图(批次:GC-L3-20120922)
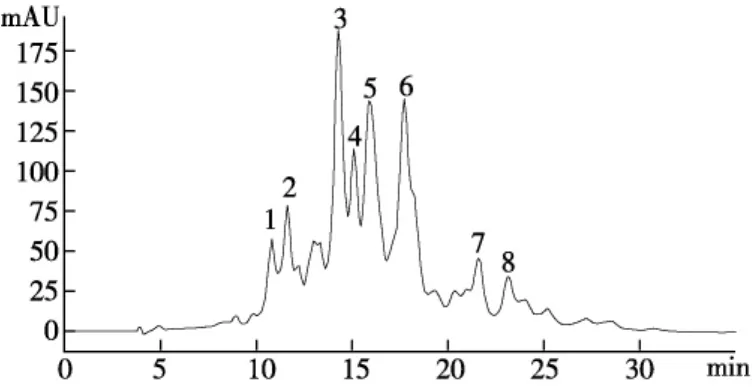
图3 GLA的RP-HPLC图(批次:GC-L3-20121010)
2.4 相对保留值指纹图谱的确定
选择一个保留时间居中且在各样品中均存在的色谱峰作为参照物,指定它的相对保留时间(relative retention time)α=1,并分别求出样品中各组分的相对保留值为:
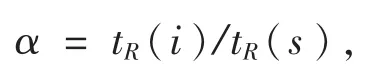
式中tR(i)为各组分的出峰时间,tR(s)为参照峰的出峰时间。
以某一样品的色谱峰总面积为分母,各样品中每个色谱峰面积为分子,求得该色谱峰的相对峰面积(ratio of peak area,RA),将它标在其α值项下,最后将各样品的α按由小到大的次序依次排列成行。每个样品色谱峰的相对保留值α和相对峰面积RA构成了其HPLC的指纹特征。
2.5 方法学考察
2.5.1 精密度试验取同一GLA样品,按2.1制备供试品,连续进样5次,考察主要色谱峰的α和RA的一致性。相对标准偏差(RSD)是试验可信度的一种考察标准,根据检测数据,计算各自的RSD。
2.5.2 稳定性试验取同一GLA样品,按2.1制备供试品,分别在0 h,4 h,8 h,12 h和16 h检测指纹图谱,考察主要色谱峰的α和RA的一致性,并计算各自的RSD。
2.5.3 重现性试验取同一批号GLA样品5份,按2.1制备供试品,考察主要色谱峰的α和RA的一致性,并计算各自的RSD。
3 结果
3.1 GLA色谱图
按2.3进行HPLC分析,得到3批次GLA高效液相色谱图,见图1、图2、图3。
3.2 指纹峰的标定
采用α标定指纹峰,以5号色谱峰作为参照峰,计算各待测峰的α及RA。结果见表2,表3。3批次GLA供试品中含量较高的峰集中在0.90~1.11区域,α值为0.90(峰3),0.95(峰4),1.00(峰5),1.12(峰6)处有4个较强峰;0.68(峰1),0.73(峰2),1.36(峰7),1.46(峰8)处有4个中等强峰。这8个色谱峰的RA均占总峰面积的3.3%以上,说明这8个峰的含量较高,可能是GLA组分中的主要成分。

表2 GLA指纹图谱共有峰相对保留时间(α)
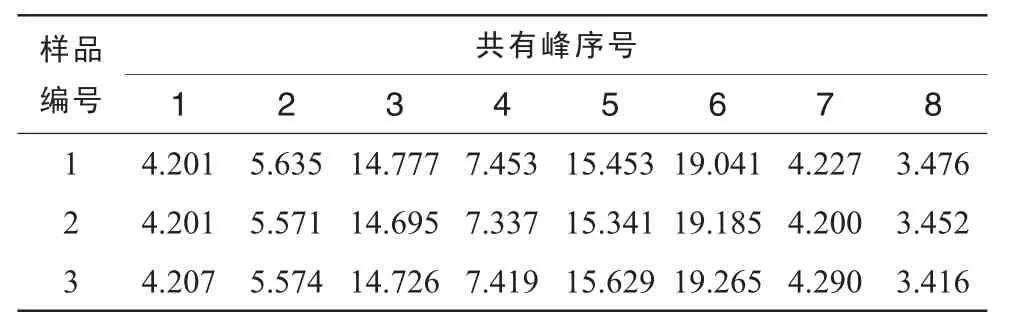
表3 GLA指纹图谱共有峰相对峰面积(RA)
3.3 仪器精密度
分别取同一供试品溶液5 μL,连续进样5次,色谱峰均自动积分。比较不同色谱图中主要色谱峰的α和RA。结果表明,所标定色谱峰的α和RA基本一致,RSD均小于3%,符合指纹图谱的检测要求[7]。说明仪器系统精密度良好。见表4。
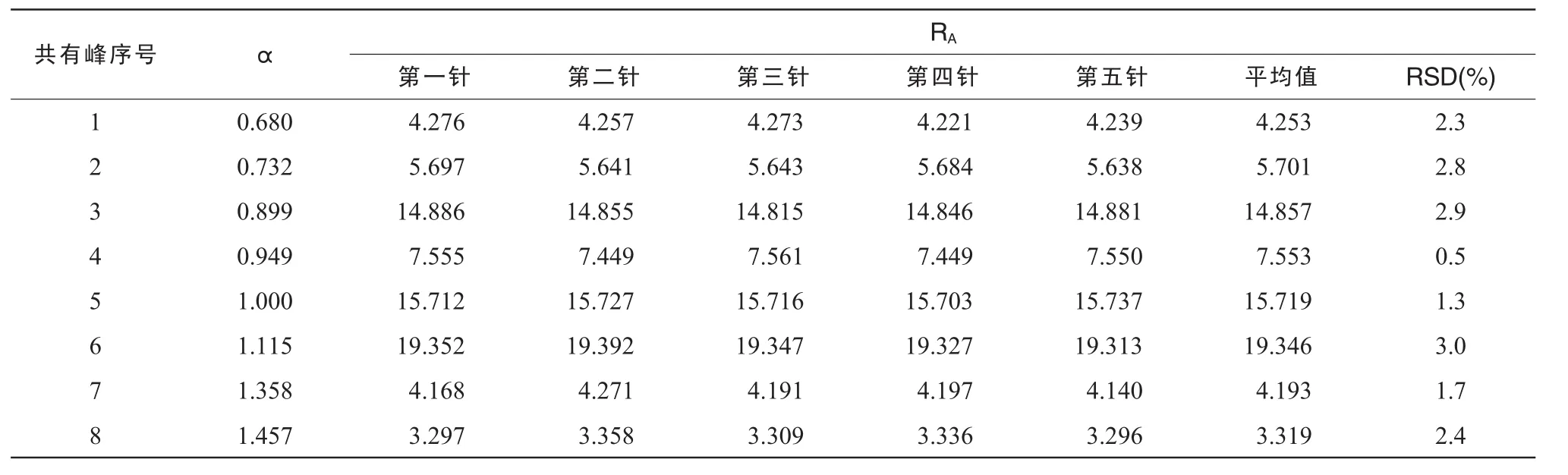
表4 GLA的精密度实验数据
3.4 稳定性试验
分别取同一供试品溶液5 μL,每隔4 h进样一次,16 h内连续进样5次,色谱峰均自动积分。比较不同色谱图中主要色谱峰的α和RA。结果表明,所标定色谱峰的α和RA基本一致,RSD均小于3%,符合指纹图谱的检测要求[6]。说明GLA样品性能比较稳定。见表5。
3.5 重现性试验
取同一批号灵芝子实体精粉,按2.1项下方法制备5份供试品溶液。每份样品进样5 μL,色谱峰均自动积分。结果表明,所标定色谱峰的α和RA基本一致,RSD均小于3%,符合指纹图谱的检测要求。所考察的共有色谱峰的重现性良好。见表6。
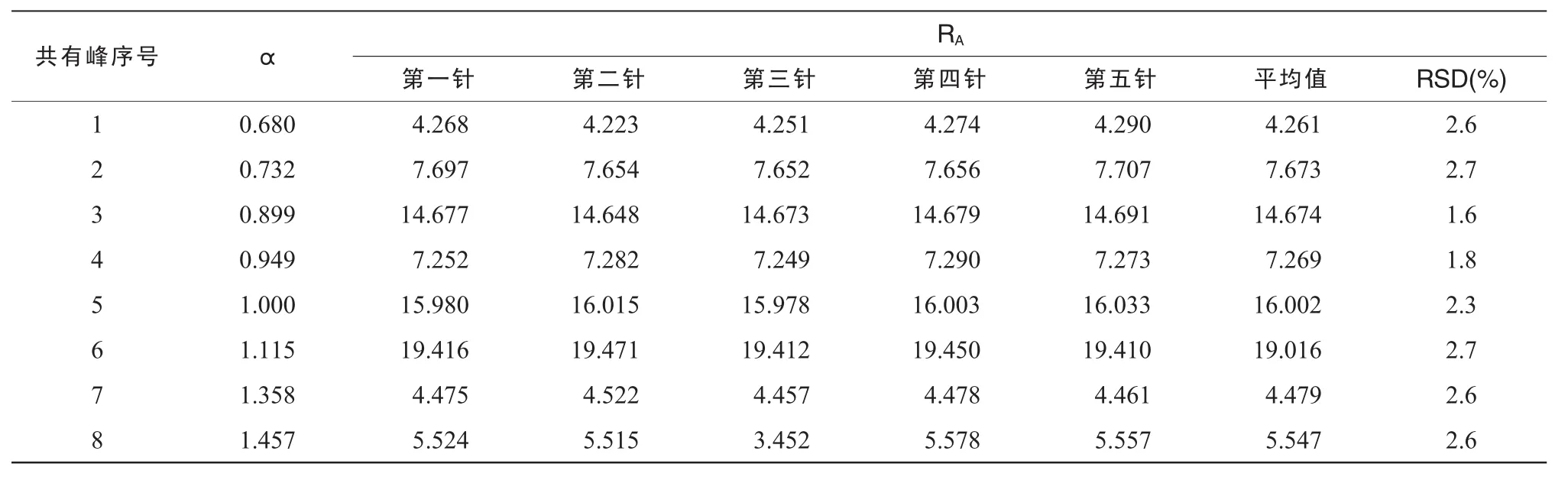
表5 稳定性实验数据

表6 GLA重现性实验数据
4 讨论
中药的药效是所含有的多种化学成分通过多靶点、多环节发挥综合作用的结果,GLA的药效是多种灵芝三萜酸类成分共同起作用的结果。仅分析测定一种或某几种灵芝三萜酸来评价其质量是不全面的,本文建立的GLA高效液相色谱指纹图谱是GLA中三萜酸类成分整体的综合表达,更能全面评价GLA的质量。因此,GLA的RP-HPLC指纹图谱是控制GLA质量的有效手段,具有一定必要性和先进性。本文所建立的方法得到的色谱指纹图谱多数峰未达到基线分离,因此不适用于GLA的定量控制,但可以作为GLA质量控制中的定性控制方法。通过测定一种或某几种灵芝三萜酸来作为GLA质量的定量控制方法,再结合本文建立的GLA质量的定性控制方法,可以全面控制GLA质量。3批次GLA样品的指纹图谱,各主要色谱峰的α分别为0.68,0.73,0.90,0.95,1.00,1.12,1.36,1.46。这8个色谱峰为3批次供试品的共有指纹峰,是鉴别GLA样品的必要条件之一。
[1]国家药典委员会.中华人民共和国药典(2010年版)一部[S].北京:中国医药科技出版社,2010:174.
[2]江苏新医学院.中药大辞典[M].上海:上海科学技术出版社,1985:1180-1182.
[3]魏晓霞,李鹏,许建华,等.灵芝三萜组分GLA体内外抗肿瘤作用的研究[J].福建医科大学学报,2010,44(6):417-418.
[4]李鹏,魏晓霞,南婷婷,等.灵芝三萜酸对小鼠急性肝损伤的保护作用[J].中国医院药学杂志,2013,33(23):4-8.
[5]徐任生,陈仲良.中草药有效成分提取与分离[M].2版.上海科学技术出版社:218-223.
[6]潘君汉.浅谈中药指纹图谱的意义[J].中国药业,2008,17(6):13-14.
[7]国家食品药品监督管理局.关于印发《中药注射剂指纹图谱研究的技术要求(暂行)》的通知[J].中国药品标准,2000,1(4):3.
Preliminary Study on HPLC Fingerprint of Triterpene acids Components from Ganoderma Lucidum
Wei Xiaoxia1,Li Peng2,Sun Hong1,Zhuang Jie1(1 Pharmacy Department of Fujian Provincial Hospital,Fujian Fuzhou 350001,China;2 Department of Natural Medicines of Pharmaceutical College of Medical University,350004)
Objective:To set up the fingerprint of triterpene acids components of ganoderma lucidum(GLA)and to provide a basis for its quality control. Methods:To extract the triterpene acids components of ganoderma lucidum by plant tissue crushing method and to establish the fingerprint of GLA by HPLC.Results:There were 8 characteristic peaks in HPLC fingerprint of GLA,their alpha values were 0.68,0.73,0.90,0.95,1.00,1.12,1.36 and 1.46 respectively.Conclusion: The established RP-HPLC fingerprint can provide a theoretical basis for the quality control of GLA.
Ganoderma lucidum;Triterpene acids;Fingerprint;HPLC
10.3969/j.issn.1672-5433.2014.04.006
2014-02-08)
国家自然科学青年基金(81202560);福建省教育厅科技计划项目(JA11107);2011年福建省高校产学合作科技重大项目(2011Y4003)
魏晓霞,女,硕士。研究方向:肿瘤药理。通讯作者E-mail:xxwei0321@163.com

