药品上市后临床试验远程数据管理模式的架构*
曹红波刘 智,李 楠,翟静波,王 辉,刘春香,商洪才
(1.天津中医药大学中医药研究院,天津 300193;2.天津中医药临床评价研究所,天津 300193)
药品上市后临床试验远程数据管理模式的架构*
曹红波1,2刘 智2,李 楠1,翟静波1,王 辉1,刘春香1,商洪才1,2
(1.天津中医药大学中医药研究院,天津 300193;2.天津中医药临床评价研究所,天津 300193)
药品上市后临床试验是生产药品临床证据的重要手段,而临床试验的质量控制是证据可靠性的关键。数据管理是药品上市后临床试验质量控制的重要内容,随着计算机技术的发展和应用,临床试验的远程数据管理模式逐渐成为趋势,文章对药品上市后临床试验当中传统数据管理与远程管理的区别和远程管理模式的架构作一介绍。
临床试验;远程数据管理;药品
临床数据管理是药物临床研究中的重要内容,数据的质量直接关系到能否对药物的安全性和有效性作出正确的评价[1]。药品上市后临床试验数据管理的最终目标是保证数据产生过程的真实、可靠,保证最终进入统计分析的数据规范、有效[2]。药品临床试验管理规范(GCP)是中国制定的确保药品临床试验质量的法律性文件,其中第五十三条对药品临床试验数据管理有明确规定:“数据管理的目的在于把得到的自受试者的数据迅速、完整、无误地纳入报告;所有涉及数据管理的各个步骤均需记录在案,以便对数据质量及试验实施进行检查。用适当的程序保证数据库的保密性,应具有计算机数据库的维护和支持程序”。
当前,中国药品上市后临床试验数据管理的模式主要分为两种:传统模式和远程模式。笔者对这两种模式的特点和远程数据管理模式的基本架构作一总结,希望能够为今后药品上市后临床试验数据管理者带来帮助[3]。
1 中国临床试验数据管理的现状
1.1传统数据管理模式
1.1.1定义 传统数据管理模式是基于纸质病历报告表(CRF)的一种单一的、静态的数据记录、核查和提交模式。见图1。
1.1.2特点 由于传统数据管理模式的局限性,导致其具有滞后性、不可靠性和低效率的缺点。
1.1.2.1滞后性 1)信息滞后:由于数据的采集过程采用纸质化的管理模式,质量监督部门、数据管理部门、试验组织部门不能实现信息的同步共享。2)决策滞后:信息的滞后导致了决策部门不能针对问题及时作出决策,有可能使问题扩大化或者产生连锁反应。3)进程滞后:由于纸质化管理客观条件的限制,导致数据处理和统计过程的繁琐和低效率,严重阻碍了药品临床试验的进程。
1.1.2.2不可靠性 1)数据记录:传统数据管理模式要求研究者采用纸张记录的方式进行数据的采集,这种方式常常由于人为因素的干扰且没有记录规则的约束而存在不可靠性隐患。2)数据迁移:传统数据管理模式经历了很多中间环节,包括纸质病历的填写、数据库的导入、最终的统计分析等过程,这些数据的迁移过程或多或少会影响数据的质量。3)数据管理:传统的数据管理规范常常因为人为因素和缺乏标准化的约束机制而难以落实,有时即使建立标准操作规程(SOP),也不能做到有效的管理。1.1.2.3低效率 时间成本和人力成本的严重消耗是传统数据管理模式的一大缺陷,往往即使耗费巨大的成本也无法达到理想的管理效率,常常表现为低水平的重复劳动。
1.2远程数据管理模式[4]
1.2.1定义 远程数据管理模式是指借助于计算机和网络技术,实现临床试验数据采集功能的电子化并在一定范围内共享,进而开展试验数据记录、核对和提交的动态、适时管理模式。见图2。
1.2.2特点 1)及时性:①信息及时:远程数据管理模式可以实现服药信息的及时共享、管理信息的及时传递、交流信息的及时反馈。②决策及时:基于远程数据管理系统的信息传递功能,试验组织者能够及时解决和协调试验中出现的问题,防微杜渐,为临床试验的顺利开展保驾护航。③管理及时:试验组织方、质量监查部门、数据管理部门可以基于远程数据管理平台同时开展工作,实现数据管理的同步。2)可靠性:①系统标准:基于智能的计算机管理模式,远程数据采集功能可以实现标准、可控的操作规程和规范,从而降低数据采集的失误率。②系统纠错:远程数据管理系统可以通过衍生的方法附加自动纠错功能,能够自动识别系统中不符合试验设计或系统要求的数据,从而降低了不规范数据的出现概率。③痕迹管理:根据美国食品药品监督管理局(FDA)“21CRF Part11”文件中对电子化临床试验系统痕迹管理的要求[5],用户在远程数据管理系统中进行的数据创建、修改或删除等任何活动都将被详细记录以备查验。因此,实现痕迹管理是远程数据系统的特色和优势,也为数据管理的可靠性提供了进一步的保障。3)高效率:远程数据管理模式享有共同的交流平台,数据采集、数据核查、质量控制、组织管理等均可在该平台实现同步化,从而减少了传统数据管理模式中繁琐的中间环节,提高了研究效率。远程数据管理一般采用电子化病例报告表(eCRFs)的数据记录方式。
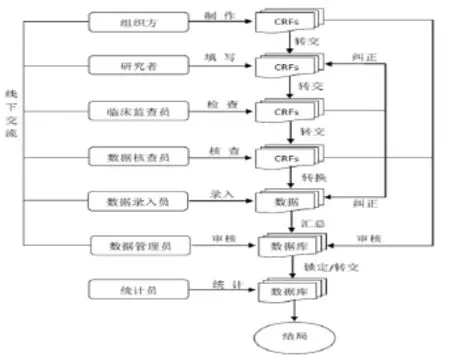
图1 传统数据管理模式Tab.1 Classical data management model
2 数据管理模式转型的必要性
2.1临床试验规模化和国际化的加快 随着国际医学界对证据质量要求的不断升级和药品临床试验的不断开展,规模化、国际化已成为普遍的趋势[6],而这种数量的增加和范围的扩大对临床试验的数据管理也提出了更高的要求,对数据信息采集、存储、使用与理解的技术落后,不足以支撑中医药学对信息量、信息处理利用效率与能力的要求,不利于中医药临床研究数据的交换与共享[7-8]。因此,传统的数据管理模式已远远不能满足现代药品临床试验的需要,向远程数据管理模式的转化迫在眉睫。
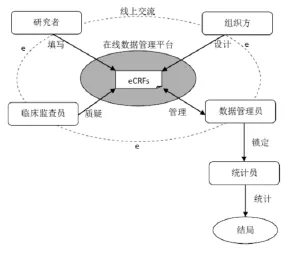
图2 远程数据管理模式Tab.2 Remote data management mode
2.2远程数据管理模式的普及和发展 目前,国外药品临床试验的远程化管理已经比较成熟,美国FDA实行了对电子化申报资料优先评审的制度,更加促进了临床试验远程数据管理模式的发展[9]。中国目前的临床试验仍然处于传统与远程模式混杂的局面,如何更快、更好的推进远程数据采集(RDC)在国内的普及,是当代临床研究人员所要面临的重要任务。
3 远程数据管理系统的基本架构
目前,临床试验数据管理系统架构模式主要分为C/S和B/S两种。
3.1C/S(Client/Server)模式 C/S以局域网为基础,是客户端/服务器的模式,属于小范围里的网络环境,局域网之间再通过专门服务器提供连接和数据交换服务。C/S功能强大,可以减轻服务器端压力,适用于用户需求特别复杂的情况。
3.2B/S(Browser/Server)模式 B/S以广域网为基础,是浏览器/服务器的模式,不必是专门的网络硬件环境。B/S的优势在于客户端免维护,适用于用户群庞大或客户需求经常变化的情况,只需要有操作系统和浏览器就行。
总体来说,B/S基于对访问安全以及速度的多重考虑,结构的程序架构更为成熟,比C/S有更高的要求和更强的适应范围,是数据远程管理发展的趋势。下面就B/S的架构模式作主要介绍:
B/S的架构模式基于HTTP传输协议,通过前台的各项操作来实现与网络服务器和后台数据库的互通、关联,共分为4个层面,即:客户端、数据层、功能层和安全层。见图3。
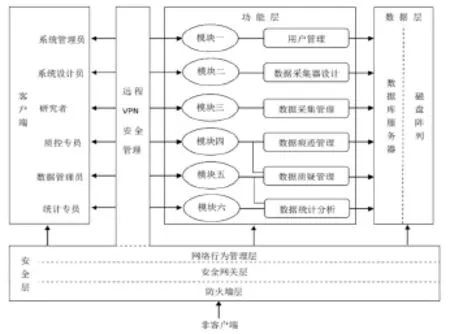
图3 远程数据管理系统的架构Tab.3 The structure of the remote data management system
3.2.1客户端 数据管理系统的客户端是系统用户与系统支持平台交互的主要界面。一方面,系统用户可以登录客户端,通过网络服务器向系统发出请求;另一方面,网络服务器可以通过HTTP协议将用户所需的文件资料反馈给用户。
3.2.2数据层 数据层是临床试验数据管理系统的重要组成部分,其主要功能是实现对临床试验数据的存储和备份,防止数据的丢失。
1)数据存储:试验数据的存储是数据层主要功能之一,其中数据库服务器担任了数据存储的主要任务。数据存储是数据文件在数据流动过程中集中存储便于查询信息的结构载体。数据以计算机语言的形式存储在磁盘介质内,保证数据的安全性。在临床信息数据应用中,数据存储平台模式的建立是未来临床信息发展的趋势。
2)数据备份:保证数据安全是数据层的另一重要功能,目前多采用磁盘阵列进行试验数据的备份,以有效防止因服务器损害等故障而导致的数据丢失。
数据备份可以分为热备份和冷备份两种,目前多采用两种结合的方式,以保障数据备份的稳定性:
①热备份(又叫线上备份):是指在不中止数据库正常操作的情况下进行的数据备份。
热备份的优点:备份时系统可以正常工作,不会耽误线上数据流的正常运行;数据可以恢复到备份的时间点,误差小;数据恢复的速度快,可对所有数据库进行完整性恢复。
热备份的缺点:备份过程中不能有任何失误,否则将会出现致命的后果;如果出现备份错误,将不可恢复到具体时间点;热备份需要高水平的技术人员进行,维护成本高。
②冷备份(又叫离线备份):是指数据库正常关闭或停止工作后人工进行的数据备份,即将关键数据集拷贝到另外的存储介质的方式。
冷备份的优点:非常快的保存方法,将数据文件拷贝到另外的磁盘上即可;容易恢复到某个时间点上,只需要拷贝回原来文件的位置替换即可;容易操作,维护成本低。
冷备份的缺点:只能恢复到备份时间的那个时间点上面;在实施备份的过程中,数据库必须处于关闭状态,不能进行任何操作;每次备份需要占用大量的磁盘空间,对于磁盘空间小的介质要求高。
3.2.3功能层 功能层介于客户端与数据层之间,是远程数据管理系统功能体系的主要结构,由几个功能模块共同组成,以满足不同客户的应用需求。功能层一般应分为六大模块:
1)系统管理模块:本模块主要为系统管理员服务。系统管理员通过该模块实现对系统中所有用户信息和机构信息的管理以及角色和权限的分配。
2)eCRF设计模块:本模块主要为eCRF设计人员服务。eCRF设计人员可以基于该模块提供的设计环境,实现纸质CRF或其他试验项目的电子化;通过对本模块中各种变量的规则设定,达到数据的衍生、关联、核查、统计等目的。
3)数据采集模块:本模块主要为临床研究人员提供服务。研究者通过本模块提供的主要功能实现对试验数据的录入、查询、修改、审批等智能化管理。
4)痕迹管理模块:本模块主要为质量监查部门提供服务。通过本模块的痕迹追踪功能,可以详细记录数据的创建、修改、删除等操作,实现对试验数据的质量评价。
5)质疑管理模块:本模块主要为数据管理员和质量监查员提供服务。数据管理员和质量监查员将借助于本模块实现对试验数据真实性和有效性的核查,并针对有疑问的数据向研究者提出质询。
6)统计分析模块:本模块为统计分析员、数据管理员的应用界面。数据管理员借助于本模块实现试验数据的导出和汇总;统计分析员应用本模块进行数据的统计和分析等。
3.2.4安全层 安全层是远程数据管理的重要组成部分,是临床试验数据安全的有力保障。根据用户登录系统方式的不同,可以分为非客户端登录和客户端登录两种:
1)非客户端登录:非客户端登录是指非系统指定用户的非正常登录,主要用于防止各种类型的网络入侵,保护数据安全。针对非客户端登录系统从外到内设有防火墙、安全网关、网络行为管理3层安全防护体系。
2)客户端登录:客户端登录是指系统指定用户的正常登录。系统通过远程登录VPN管理实现对客户端登录用户的安全管理。
4 数据远程管理的标准化
临床试验使用数据管理系统的最终目标在于使试验数据实现规范化与交换化。由于目前不同临床研究中的数据往往使用不同的变量名、代码或格式,使得研究的数据管理、数据分析、数据提交等过程变得异常复杂。因此,临床研究数据远程管理的标准化成为急需解决的共性问题。标准化是一个不断循环、螺旋式上升的动态过程,在标准修订过程中还需不断提高标准质量,使其更具适用性[10]。
临床数据交换标准协会(CDISC)是致力于开发医学和生物制药产品的行业标准的全球性组织,目前已经建立了收集数据、数据分析、数据交换、提交数据的一系列国际标准[11],其建立的CDISC-SDTM的研究数据格式已经被FDA接受作为标准的数据提交格式。伴随着CDISC标准的产生和被FDA接受,目前在研或在售的一些临床数据管理软件和电子数据采集系统大多开始遵循该标准。比较突出的如Oracle、Medidata等公司生产的数据管理系统软件,均可以导出符合CDISC标准的数据格式;而SAS统计软件也自9.1版本以后加入了CDISC数据标准软件包。
除了CDISC标准外,还有一些其他的标准,如:HL7,NCI,FDA等,这些标准正在努力共同创建BRIDG模型[12],这个模型整合了目前一些标准的共性,减少数据流从临床医生到研究人员过程中产生的潜在错误[13],保障了数据传递过程的安全、合理。
目前,中国在临床试验数据管理标准化方面尚处于探索阶段,很多内容需要继续完善,尤其是中医药临床研究领域的标准化,在西医作为主流医学的今天,中医学缺乏“现代语言”来进行很好的沟通和交流[14]。相关中医语义结构及术语标准研究基础薄弱,如中医证候、中医症状、疗效评价等尚属于空白,因此,中医要实现现代化,关键在于规范化、标准化,即进行话语系统的转换,建立起便于计算机统一处理的规范用语,进行编码[15-17]。随着临床研究远程数据管理的应用和普及,中医药临床研究相关标准的建立已迫在眉睫。
5 结语
计算机技术的普及和应用,使临床试验数据的电子化和远程管理将成为未来临床试验发展的趋势,医药领域尤其是上市后中成药应接受并积极拓展、应用这种技术,有利于临床试验数据管理的客观化和产生令人信服的中医药临床证据[18]。
[1] 孙亚林,贺 佳,曹 阳,等.临床数据管理的电子化趋势[J].中国新药杂志,2005,14(4):393-395.
[2] Rondel R,Varley S,Webb CC.Clinical data management[M]. London:UK Chichest,2000:1-19.
[3]谢 蓉,赵家骜.信息技术在新药临床试验数据管理中的应用[J].医药信息,2003,16(3):119-122.
[4]彭智才,尚政琴,王玉贵,等.药品临床试验数据管理的新探索[J].中国医学装备,2013,10(9):28-30.
[5] Department of Health and Human Services,Food and Drug Administration.21CFR Part 11,Electronic Records;Electronic Signatures;Final Rule[EB/OL].http://www.fda.gov/regulatoryinformation/ guidances/ucm125067.htm.2014-08-05.
[6]ICH-6.Good clinical practice[EB/OL].http://www.druggcp.net/regulation/detail.2014-03-20.
[7]黄宇虹,张伯礼.中风病发病时中医证候特点浅析[J].天津中医药大学学报,2007,26(2):59-60.
[8]李 庚,李晓彦,温泽淮.临床数据交换标准协会标准在中医药临床研究病历报告表设计中的应用[J].广州中医药大学学报,2014, 31(1):138-141.
[9] Miller E,Murphy J.Implementing and managing adaptive design for clinical trials[EB/OL].http://wenku.baidu.com/view/e29c3583e53a5 80216fcfe81.html.2006-01-17.
[10]赵 雪,陈泽林,郭 义.基于SWOT分析的中医药标准化战略思考[J].天津中医药大学学报,2011,30(4):196-199.
[11]CDISC.CDISC Vision&Mission[EB/OL].http://www.cdisc.org/CDISCVision-and-Mission.2014-06-23.
[12]BECKY A,JULIE E.BRIDG 3.0.3.Release USER′S GUIDE[EB/ OL].http://www.bridgemodel.com.2010-12-16.
[13]陆 芳,高 蕊,唐旭东,等.临床研究中的数据管理标准CDISC及其应用前景[J].中国新药杂志,2011,20(24):2400-2404.
[14]闫秀川,刘成海.可用于中医药系统研究的药物高内涵筛选分析[J].中草药,2008,39(8):1121-1124.
[15]张 玥,于铁成.关于中医现代化的思考[J].天津中医药,2007, 24(6):501.
[16]陈慧玲.DM在中药学中的应用分析[J].天津中医药大学学报,2009,28(2):96-97.
[17]胡广芹,陆小左,于春泉,等.基于云计算的中医健康管理系统[J].天津中医药,2011,28(6):475-477.
[18]胡莎莎,梁建凤,赵永根,等.OpenClinica在临床试验数据管理系统中的应用[J].医学信息学杂志,2012,33(9):36-39.
Remote mode of data management for a certain medicine in clinical trial after appearing on the market
CAO Hong-bo1,2,LIU Zhi2,LI Nan1,ZHAI Jing-bo1,WANG Hui1,LIU Chun-xiang1,SHANG Hong-cai1,2
(1.Institute of Traditional Chinese Medicine,Tianjin University of Traditional Chinese Medcine,Tianjin 300193,China; 2.Tianjin Institute of TCM Clinical Evaluation,Tianjin 300193,China)
Clinical trial is an important measure in providing some clinical evidences for production of a certain medicine.While the quality control of the clinical trial is the key for the evidence reliability.Data management is an important content in quality control of clinical trial after its appearing on the market and the remote data management mode of clinical trial has gradually become a trend along with the development and application of computer technology.In this paper,we will discuss the difference between the classical data management and remote data management.Meanwhile and the framework of remote data management will be introduced.
clinical trial;remote data management;medicine ···································
R954
A
1672-1519(2014)12-0730-05
2014-06-25)
(本文编辑:高 杉,马 英)
10.11656/j.issn.1672-1519.2014.12.08
国家自然科学基金青年科学基金项目(81202 849);天津市高等学校创新团队资助(TD12-5032);天津市高等学校科技发展基金计划(20110202)。
曹红波(1978-),男,医学博士,副研究员,主要从事中医药循证临床研究与评价的方法学研究。
商洪才,shanghongcai@foxmail.com。

