生物炭修复Cd,Pb污染土壤的研究进展
杨璋梅,方战强
(1. 华南师范大学 化学与环境学院,广东 广州 510006;2. 广东省水环境生态治理与修复工程技术研究中心,广东 广州 510006;3.广东高校城市水环境生态治理与修复工程技术研究中心,广东 广州 510006)
随着矿产开采、冶炼等工业活动以及污水灌溉、施用污泥和劣质化肥等农业活动的进行,Cd,Pb等有害重金属不断进入农业环境中,对农田、菜地等造成污染。目前,我国有Cd污染耕地约1.3×104hm2,涉及11个省市的25个地区;而粮食含Pb量大于1.0 mg/kg的粮食产地有11个[1-3]。作物受Cd,Pb污染后,不仅会严重影响其产量和品质,而且Cd,Pb会进一步通过食物链进入人体,危害人体健康。因此,对重金属污染土壤的有效修复成为国内外研究的热点。
生物炭是富含碳的生物质通过热裂解的方法,在缺氧或少氧的条件下制成的一种富有孔隙结构、含碳量高的炭化物质[4]。生物炭属于广义概念上的黑炭,其制备原材料来源广泛,农林业废弃物(如木材、秸秆、果壳)以及工业和城市生活中产生的有机废弃物(如垃圾、污泥)都可以作为原料。研究结果表明[5],生物炭能降低酸可提取态Cd,Pb的含量,从而降低重金属的生物有效性,作为改良剂修复重金属污染土壤具有可行性。
本文从生物炭的特性及制备、修复效果及其影响因素、修复机理等方面,对近年来国内外有关生物炭修复Cd,Pb污染土壤的研究成果和现状进行了总结,并对生物炭修复Cd,Pb污染土壤的发展前景和未来研究方向进行了展望。
1 生物炭的特性及制备
1.1 生物炭的特性
1)主要由C,H,O,N等元素组成,以高分子、高密度碳水化合物的形态存在。
2)较大的比表面积。炭化后的生物质具有微观孔隙结构,比表面积增大,大孔隙(宽度大于100 μm)的比表面积可达750~1 360 m2/g,小孔隙的为51~138 m2/g。
3)较高的pH。生物炭的pH一般都在8以上,如稻壳和油棕制成的生物炭pH分别为8.5和9.4,而芒草生物炭可达10.2。生物炭含有大量碱性物质,可与碱离子发生交换反应。
4)多种表面官能团,如羧基、羟基和羰基。这些基团能与重金属形成配合物,降低重金属的迁移率。
5)高芳香化结构,并因此呈现高稳定性及更强的抗微生物分解的能力。
生物炭的这些特性对土壤养分保持、水土利用、土壤结构、重金属和有机污染物的生物有效性均可产生重要影响[6-8]。
1.2 生物炭的制备
生物炭的制备主要分为炭化与活化两个过程。生物质的预处理可降低活化温度、缩短活化时间、提高生物炭产率。预处理方法主要包括脱灰、预氧化、浸渍等。根据加热方式的不同,生物炭的制备可分为热解法、微波法及水热法[9-10]。热解法是指在隔绝空气的条件下生物质进行高温裂解反应,其影响因素主要包括炭化与活化温度、炭化与活化时间、活化剂种类、活化剂浓度与用量等。该法存在加热速率缓慢、反应时间长、反应耗能大、传热效率低、反应原料加热不均等缺点。微波法是通过被加热体内部偶极分子的高频往复运动,使分子间相互碰撞产生大量摩擦热,继而使物料内外部同时快速均匀升温。微波加热具有操作简单、升温速率快、反应效率高、可选择性均匀加热等优点,不足之处在于物料的反应温度不能精确控制,且过量的微波辐射有损健康。水热法是在水热反应釜内通过在一定温度和压强下使生物质、催化剂和水相互反应,实现对生物质的炭化。水热法具有能效高、设备简单、操作简便且生物炭产率较高的特点。
当前生物炭的制备主要采用热解法,热解过程采用限氧升温方式。根据反应条件,热解可分为两种过程:一种是快速裂解,温度一般在700 ℃以上,生物燃料的制备通常采用这种方法;另一种是常规裂解,温度一般在300~500 ℃,生物炭的制备主要采用这种方法。Xu等[11]采用热解法,将风干的花生、油菜秸秆研磨后置于马弗炉中,升温至350℃,热解4 h,制得生物炭;Almaroai等[12]采用热解法,于400 ℃用橡木制成生物炭;Jiang等[13]采用热解法,将水稻秸秆在300 ℃下炭化4 h制成生物炭。
2 生物炭修复Cd,Pb污染土壤
2.1 修复效果的影响因素
制备生物炭的热解温度和原材料种类是影响生物炭性质的两个最主要的因素,这些性质包括结构、pH、官能团的种类和数量,以及元素组成等,将影响到生物炭对重金属污染土壤的修复效果。
2.1.1 热解温度
热解温度会显著影响生物炭的产率、灰分含量、元素含量、pH、表面官能团种类和数量、孔隙结构等理化性质[14-15]。一般,生物炭的热解温度越高,对重金属的固化效果越好。随热解温度的升高,生物炭中的碳含量增加,pH增大,表面极性官能团含量降低,芳构化程度加深,比表面积和孔隙率增大,吸附容量和最大不可逆吸附量也增大。Ding等[16]研究了不同热解温度下制成的甘蔗渣生物炭对Pb的吸附效果及机理的影响。实验结果表明,250 ℃和400 ℃下制成的生物炭对Pb的吸附效果优于500 ℃和600 ℃下制成的生物炭;低热解温度下制成的生物炭对Pb的吸附机理包括与官能团络合、阳离子交换和沉淀作用,而高热解温度下制成的生物炭则主要是沉淀作用和粒内扩散作用。
2.1.2 原材料种类
不同原材料在相同条件下制成的生物炭的理化性质具有一定的差异性,对土壤改良和污染物修复效果也不同。一方面,不同原材料制备的生物炭的比表面积、孔隙结构、表面官能团等性质有所差别,这些性质是影响生物炭吸附能力的重要因素;另一方面,不同原材料的化学组成影响了生物炭的元素组成和含量。Yuan等[17]分别采用菜籽秸秆、大豆秸秆、玉米秸秆和花生秸秆在低氧环境下热解得到了一系列的生物炭,发现不同原材料制成的生物炭的产率和性质差别较大,其中,花生秸秆生物炭比其余几种生物炭的碱金属离子和磷的含量都高。Lu等[18]对采用不同污泥材料于不同热解温度下制成的生物炭进行表征,研究了其用于重金属污染土壤修复的可行性。实验结果表明,不同原材料制成的生物炭其元素组成及官能团不同,对重金属的吸附效果也有一定差异。
2.2 修复效果
2.2.1 降低Cd,Pb的迁移率
生物炭可以提高土壤的pH。随pH的升高,土壤中的重金属离子形成金属氢氧化物、碳酸盐或磷酸盐沉淀,同时土壤表面的活性吸附位点也增多,使土壤对重金属离子的吸附能力增强。生物炭表面带有大量的负电荷,金属离子能与生物炭的表面电荷产生静电作用,从而影响其在土壤中的迁移转化。
生物炭的施用能降低污染土壤中Cd,Pb的迁移率,从而降低了Cd,Pb被植物吸收的风险。Zhang等[19]概括了近几年生物炭对土壤中重金属迁移率的影响的相关研究成果,见表1。Moon等[20]研究了大豆秸秆制成的生物炭对靶场污染土壤中Pb的固化,并采用毒性特性溶出程序对修复效果进行评估,结果表明20%(w)的生物炭对Pb的固化率可达90%以上。Park等[21]采用鸡粪或园林废物制成的生物炭以及活性炭、黑炭对Pb污染土壤进行修复,通过重金属吸附实验比较了4种改良剂对Pb的固化效果。研究结果表明:鸡粪制成的生物炭对Pb和Cd的固化效果最好,固化率可达93.5%和88.4%;生物炭对Pb的吸附效果优于Cd,因为Pb可与碳酸盐、磷酸盐等释放的离子络合而形成沉淀,导致迁移率降低。以上研究均表明生物炭能显著降低Cd,Pb的迁移率,从而降低其毒性,实现对污染土壤的修复。
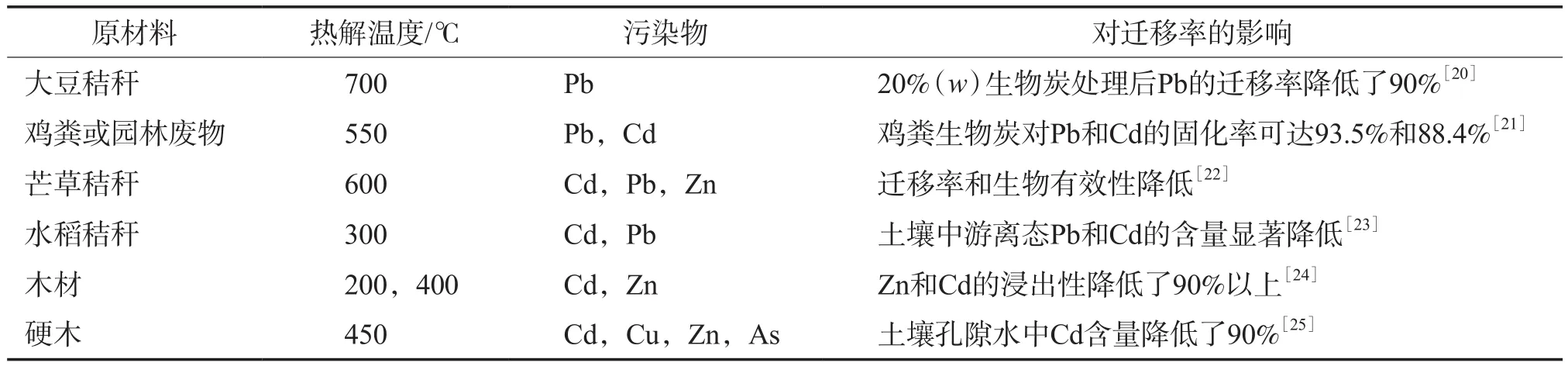
表1 生物炭对土壤中重金属迁移率的影响
2.2.2 降低Cd,Pb的生物有效性
生物有效性取决于土壤重金属在不同组分间的分配,即重金属形态。连续提取法被认为是评价重金属生物有效性的有效方法,它将土壤中重金属的形态分为酸可提取态、Fe-Mn氧化结合态、有机结合态和残渣态。酸可提取态迁移性强,可直接被生物利用;Fe-Mn氧化结合态和有机结合态在适当的环境条件下可转化为酸可提取态,即可间接被生物利用;残渣态不能被生物利用,迁移性最弱。
生物炭不仅可以直接吸附锁定土壤中的重金属离子,还可以通过影响土壤的pH、阳离子交换量(CEC)、持水量等理化性质,降低土壤中重金属的生物有效性。无论在单一污染还是复合污染土壤中,生物炭都能降低酸可提取态Cd,Pb的含量,从而降低Cd,Pb的生物有效性,具有良好的固定效果。生物炭对土壤中重金属离子的固持作用可降低重金属的生物有效性,减少重金属向植物根系的迁移,降低土壤中Cd,Pb污染物对植物的毒性,对于修复土壤重金属污染具有很大潜力。
Houben等[22]采用芒草秸秆制成生物炭,研究了质量分数分别为1%,5%,10%的生物炭对土壤中Cd,Pb,Zn的修复效果,并与石灰进行了修复效果的比较。实验结果表明,10%(w)的生物炭对重金属的固化效果与石灰相似,但生物炭修复土壤的油菜籽产量是石灰修复土壤的3倍,且Cd和Pb的生物利用率分别降低了71%和92%。Jiang等[23]采用水稻秸秆制成的生物炭修复模拟Cu,Pb,Cd污染老成土,比较了修复前后土壤中重金属各形态含量及生物利用率的变化,并对固化机制进行了探讨。实验研究表明,生物炭使土壤pH和CEC增大,使酸可提取态重金属含量降低,而氧化结合态和有机结合态含量增加,且生物炭对Cu和Pb的固化效果优于Cd。
据Park等[26]报道,鸡粪和园林废物制成的生物炭都能显著降低芥菜对土壤中Cd,Pb,Cu的吸收,且随生物炭施用量的增加,效果增强。Ahmad等[27]采用蚌壳、牛骨和生物炭降低射击场土壤中Pb的毒性,其中,生物炭使土壤中Pb的生物利用率降低了75.8%。
大量研究结果表明,生物炭的施用能影响土壤中重金属的形态和迁移转化,使易迁移态重金属转化为迁移性较弱的有机结合态或残渣态等,从而实现重金属的固化,使其生物有效性降低,减小对农作物和人类健康的危害。Zhang等[19]概括了近几年生物炭对土壤中重金属生物有效性的影响的相关研究成果,见表2。

表2 生物炭对土壤中重金属生物有效性的影响
由表2可见,不同条件、不同原料制成的生物炭均能降低重金属的生物利用率,减少植物对Cd,Pb的吸收,从而降低Cd,Pb的植物毒害作用。
2.3 修复机理
2.3.1 土壤pH的影响
pH是影响土壤中重金属生物有效性的重要因素,pH的改变导致重金属形态的变化。生物炭本身含有大量碱性物质,如碳酸盐类(碳酸钾、碳酸钠等)和氧化物(氧化钙、氧化镁等),可促进碱离子的交换反应,中和土壤酸度,使土壤pH升高,土壤中酸可提取态重金属的含量随pH的升高而减少,进而降低重金属的生物有效性。Yao等[31]研究发现,甜菜渣制成的生物炭含有大量的钙镁化合物,可在生物炭表面生成矿物结晶,能提高土壤的pH。Beesley等[25]的研究结果表明,生物炭能显著提高土壤的pH,使土壤孔隙水中的Cd含量降低90%。Xu等[32]研究发现,添加10%(w)的秸秆制成的生物炭后,土壤pH从3.83升至7.91。Jiang等[23]研究了水稻秸秆制成的生物炭对重金属化学形态及迁移率的影响。实验结果表明,经质量分数分别为3%和5%的生物炭修复后,土壤pH由5.38增至6.72和7.46,酸可提取态Pb,Cd的含量分别降低了18.8%,77.0%和5.6%,14.1%。
2.3.2 固化作用
2.3.2.1 表面吸附、络合作用
生物炭具有较大的比表面积,表面带有大量的负电荷,可通过离子交换和静电吸附作用降低土壤中Cd,Pb的活性。生物炭含有大量有机官能团,如OH,COOH,CO等,可与金属离子发生配位络合,形成金属配合物,降低迁移率,从而减小毒害作用[33]。Xu等[11]采用农作物秸秆制成生物炭,研究了生物炭对土壤中Cu,Cd,Pb的吸附作用,认为生物炭的吸附作用主要由非静电吸附作用贡献。Jiang等[13]用水稻秸秆制成的生物炭进行土培实验,分析了生物炭对土壤pH和CEC等性质的影响及吸附机制。实验结果表明,Pb(Ⅱ)主要通过与生物炭的含氧官能团(COOH和OH)形成表面络合物(见式(1)和式(2)),被吸附于生物炭表面,而使Pb固化。Lu等[34]也提出了类似的观点。
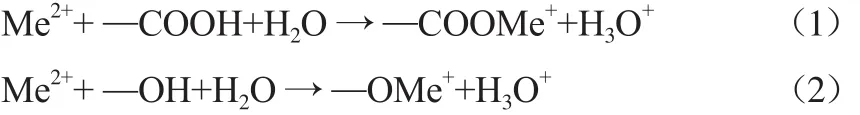
生物炭具有的大量负电荷和有机官能团,为其物理和化学吸附提供了基础。物理吸附一般是由生物炭与Cd,Pb分子间的作用力引起;而化学吸附是生物炭的盐基离子、含氧官能团与金属离子发生化学反应,生成稳定的化合物,实现重金属的固化。
2.3.2.2 沉淀作用
生物炭具有较高的阳离子交换能力,对土壤中重金属离子的亲和力较强,可促进Cd,Pb化合物水解,形成金属氢氧化物。Cd和Pb还能与碳酸盐、磷酸盐等结合,形成沉淀,使重金属固化。Lim等[35]的研究结果表明,Cd通过形成CdCO3,Cd3(PO4)2,Cd(OH)2沉淀而被固化,Pb主要通过形成磷氯铅矿(Pb1(0PO4)6(OH,Cl,F,…)2)沉淀实现固化。
2.3.2.3 小结
以生物炭对Pb污染土壤的修复为例,生物炭对Pb的固化机理见图1[16]。由图1可见,生物炭对Pb的固化可分为4个过程:1)Pb2+与官能团发生表面络合作用,与矿物氧化物的游离OH发生内层络合作用;2)Pb2+与生物炭表面的Ca2+和Mg2+等阳离子发生交换,促进金属与生物炭中的腐殖质、矿物氧化物的共沉淀和内层络合作用;3)物理吸附和表面沉淀也有助于Pb2+的稳定化;4)Pb2+在生物炭颗粒中的粒内扩散。

图1 生物炭对Pb的固化机理
生物炭对污染土壤中Cd和Pb的固化作用,是生物炭、土壤与Cd,Pb之间相互作用的结果。生物炭的施用改变了土壤的pH以及Cd,Pb的化学形态,使其固化,从而降低了土壤中Cd和Pb的生物有效性,减小对人体和生态环境的毒性,实现修复重金属污染土壤的目的。
3 展望
生物炭是近年来发展起来的热点研究领域,大量研究结果表明,生物炭在土壤养分保持、土壤理化性质改善和土壤的Cd,Pb等重金属污染修复中均表现出了积极的效果,有望发展成为可行的Cd,Pb污染土壤修复技术。目前,该领域的研究虽取得了一定成果,但要发展绿色可持续的土壤修复技术,仍需在以下几方面进行深入研究。
a)关于生物炭对Cd,Pb迁移转化的影响机理还缺乏系统的阐述,且未对各种机制的贡献率进行研究。因此,需进一步研究不同机制对生物炭固化Cd,Pb的贡献大小,以改善修复效果。
b)目前,生物炭修复Cd,Pb污染土壤的研究多数是在实验室或小规模的田间进行,在推广应用前,大规模的田间试验将成为研究的重点。
c)生物炭对Cd,Pb污染土壤的修复会使土壤pH升高,长期应用可能造成土壤碱化。目前的研究主要针对酸性土壤,而对碱性土壤的修复效果尚不清楚。
d)生物炭长期与土壤接触后可能出现老化问题,引起Cd,Pb的活化。应对生物炭及Cd,Pb的长期环境归趋进行研究,防止Cd,Pb再次活化,进入生态系统。
[1] 冉烈,李会合. 土壤镉污染现状及危害研究进展[J].重庆文理学院学报:自然科学版,2011,30(4):69-73.
[2] 黄震,黄占斌,孙朋成,等. 环境材料对作物吸收重金属Pb、Cd及土壤特性研究[J]. 环境科学学报,2012,32(10):2490-2499.
[3] 朱庆祥. 生物炭对Pb、Cd污染土壤的修复试验研究[D]. 重庆:重庆大学资源及环境科学学院,2011.
[4] Gaunt J L,Lehmann J. Energy balance and emissions associated with biochar sequestration and pyrolysis bioenergy production[J]. Environ Sci Technol,2008,42(11):4152-4158.
[5] Méndez A,Gómez A,Paz -Ferreiro J,et al. Effects of sewage sludge biochar on plant metal availability after application to a Mediterranean soil[J]. Chemosphere,2012,89(11):1354-1359.
[6] Beesley L,Moreno-Jiménez E,Gomez-Eyles J L,et al. A review of biochars’ potential role in the remediation, revegetation and restoration of contaminated soils[J]. Environ Pollut,2011,159(12):3269-3282.
[7] Wu Weixiang,Yang Min,Feng Qibo,et al. Chemical characterization of rice straw-derived biochar for soil amendment[J]. Biomass Bioenergy,2012,47:268-276.
[8] 张千丰,王光华. 生物炭理化性质及对土壤改良效果的研究进展[J]. 土壤与作物,2012,1(4):219 -226.
[9] 李保强,刘钧,李瑞阳,等. 生物质炭的制备及其在能源与环境领域中的应用[J]. 生物质化学工程,2012,46(1):34-38.
[10] 安增莉. 生物炭的制备及其对Pb(Ⅱ)的吸附特性研究[D]. 泉州:华侨大学化工学院,2011.
[11] Xu Renkou,Zhao Anzhen. Effect of biochars on adsorption of Cu(Ⅱ),Pb(Ⅱ) and Cd(Ⅱ) by three variable charge soils from southern China[J]. Environ Sci Pollut Res,2013,20(12):8491-8501.
[12] Almaroai Y A,Usman A R A,Ahmad M,et al.Effects of biochar,cow bone,and eggshell on Pb availability to maize in contaminated soil irrigated with saline water[J]. Environ Earth Sci,2014,71(3):1289-1296.
[13] Jiang Tianyu,Jiang Jun,Xu Renkou,et al. Adsorption of Pb(Ⅱ) on variable charge soils amended with rice-straw derived biochar[J]. Chemosphere,2012, 89(3):249-256.
[14] Yuan Haoran,Lu Tao,Zhao Dandan,et al. In fl uence of temperature on product distribution and biochar properties by municipal sludge pyrolysis[J]. J Mater Cycles Waste Manage,2013,15(3):357-361.
[15] Zhang Weihua,Mao Shengyao,Chen Hao,et al.Pb(Ⅱ) and Cr(Ⅵ) sorption by biochars pyrolyzed from the municipal wastewater sludge under different heating conditions[J]. Bioresour Technol,2013,147:545-552.
[16] Ding Wenchuan,Dong Xiaoling,Ime I M,et al.Pyrolytic temperatures impact lead sorption mechanisms by bagasse biochars[J]. Chemosphere,2014,105:68-74.
[17] Yuan Jinhua,Xu Renkou,Zhang Hong. The forms of alkalis in the biochar produced from crop residues at different temperatures[J]. Bioresour Technol,2011,102(3):3488-3497.
[18] Lu Huanliang,Zhang Weihua,Wang Shizhong,et al. Characterization of sewage sludge-derived biochars from different feedstocks and pyrolysis temperatures[J]. J Anal Appl Pyrolysis,2013,102:137-143.
[19] Zhang Xiaokai,Wang Hailong,He Lizhi,et al. Using biochar for remediation of soils contaminated with heavy metals and organic pollutants[J]. Environ Sci Pollut Res,2013,20(12):8472-8483.
[20] Moon Deok Hyun,Park Jae-Woo,Chang Yoon-Young,et al. Immobilization of lead in contaminatedfiring range soil using biochar[J]. Environ Sci Pollut Res,2013,20(12):8464-8471.
[21] Park J H,Choppala G,Lee Seul Ji,et al. Comparative sorption of Pb and Cd by biochars and its implication for metal immobilization in soils[J]. Water Air Soil Pollut,2013,224:1711-1722.
[22] Houben D,Evrard L,Sonnet P. Beneficial effects of biochar application to contaminated soils on the bioavailability of Cd,Pb and Zn and the biomass production of rapeseed (Brassica napus L.)[J]. Biomass Bioenergy,2013,57:196-204.
[23] Jiang Jun,Xu Renkou,Jiang Tianyu,et al. Immobilization of Cu(Ⅱ), Pb(Ⅱ) and Cd(Ⅱ) by the addition of rice straw derived biochar to a simulated polluted Ultisol[J]. J Hazard Mater,2012, 229/230:145-150.
[24] Debela F,Thring R W,Arocena J M. Immobilization of heavy metals by co-pyrolysis of contaminated soil with woody biomass[J]. Water Air Soil Pollut,2012,223(3):1161-1170.
[25] Beesley L,Moreno-Jiménez E,Gomez-Eyles J L. Effects of biochar and greenwaste compost amendments on mobility,bioavailabilityand toxicity of inorganic and organic contaminants in a multi-element polluted soil[J]. Environ Pollut,2010,158(6):2282 -2287.
[26] Park J H,Choppala G K,Bolan N S,et al. Biochar reduces the bioavailability and phytotoxicity of heavy metals[J]. Plant Soil,2011,348(1/2):439-451.
[27] Ahmad M,Lee Sang Soo,Yang J E,et al. Effects of soil dilution and amendments (mussel shell,cow bone, and biochar) on Pb availability and phytotoxicity in military shooting range soil[J]. Ecotoxicol Environ Saf,2012,79:225-231.
[28] Suppadit T,Kitikoon V,Phubphol A,et al. Effect of quail litter biochar on productivity of four new physic nut varieties planted in cadmium-contaminated soil[J].Chilean J Agric Res,2012,72(1):125-132.
[29] Fellet G,Marchiol L,Delle Vedove G,et al. Application of biochar on mine tailings:Effects and perspectives for land reclamation[J]. Chemosphere,2011,83(9):1262-1267.
[30] Namgay T,Singh B,Singh B P. In fl uence of biochar application to soil on the availability of As,Cd,Cu,Pb,and Zn to maize (Zea mays L.)[J]. Soil Res,2010,48(7):638-647.
[31] Yao Ying,Gao Bin,Inyang Mandu,et al. Biochar derived from anaerobically digested sugar beet tailings: Characterization and phosphate removal potential[J]. Bioresour Technol,2011,102(10):6273- 6278.
[32] Xu G,Wei L L,Sun J N,et al. What is more important for enhancing nutrient bioavailability with biochar application into a sandy soil:Direct or indirect mechanism?[J]. Ecol Eng, 2013,52:119-124.
[33] 王萌萌,周启星. 生物炭的土壤环境效应及其机制研究[J]. 环境化学,2013,32(5):768-780.
[34] Lu Huanliang,Zhang Weihua,Yang Yuxi,et al.Relative distribution of Pb2+sorption mechanisms by sludge-derived biochar[J]. Water Res,2012,46(3):854-862.
[35] Lim Jung Eun,Ahmad M,Usman A R A,et al. Effects of natural and calcined poultry waste on Cd,Pb and As mobility in contaminated soil[J]. Environ Earth Sci,2013,69(1):11-20.

