进行性核上性眼肌麻痹7例及文献复习
陈斐 聂志余 张天宇 管强 靳令经
进行性核上性眼肌麻痹(progressive supranuclear palsy,PSP)是一种发生于中老年人的中枢神经系统变性疾病,临床罕见,其患病率在美国约5.3/10万,英国(3.1~6.5)/10万,日本(2~17)/10万,国内尚无PSP患病率的报道。PSP主要临床特征为垂直性核上性眼肌麻痹、轴性肌张力障碍、帕金森综合征、假性延髓性麻痹、认知障碍和对左旋多巴反应差。本病诊断主要依靠临床表现,但其临床表现变异大,实验室检查缺乏特异性,临床上极易被误诊。此文结合文献,对7例PSP患者的临床资料进行回顾性分析,以期提高广大临床医生对PSP的认识。
1 对象和方法
1.1对象选择2000-01-2013-12在作者医院神经内科诊断的7例PSP患者,其中男6例,女1例。诊断参照1996年美国国立神经疾病和卒中研究所(the National Institute of Neurological Disorders,NINDS)及国际进行性核上性麻痹协会(the Society for Progressive Supranuclear Palsy,SPSP)联合推荐的诊断标准[1],其中2例符合拟诊标准,5例符合疑诊标准。一般临床资料见表1。
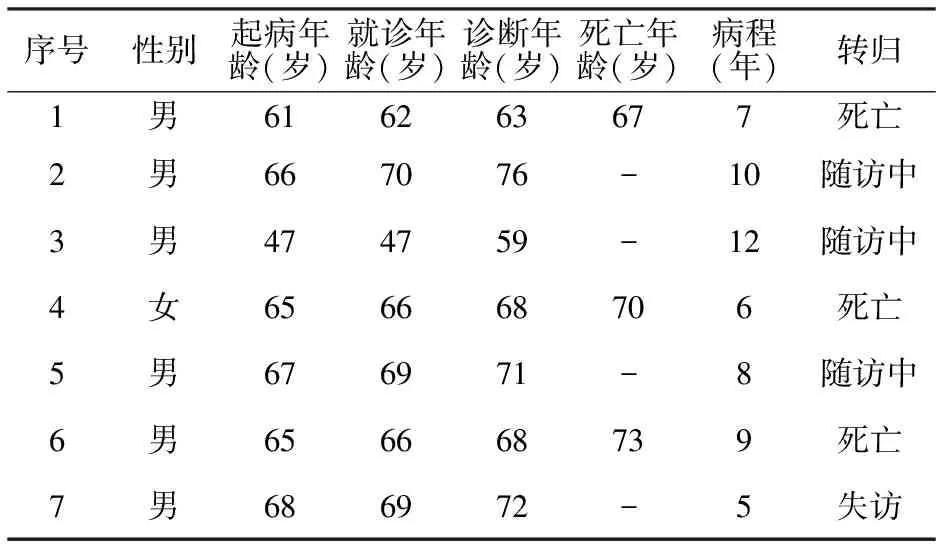
表 1 7例PSP患者一般临床资料
1.2方法回顾性分析所有患者的临床资料,包括详细询问病史、神经科体检。全部患者均行脑MRI平扫。
2 结果
2.1临床表现
2.1.1首发症状:4例以动作变慢、步态不稳为首发症状,其中1例伴工作能力下降;2例以眼部症状为首发症状,其中1例诉眼球干涩、视物不清,1例存在眼花、重影症状;1例以双手抖动为首发症状。
2.1.2临床表现:(1)垂直性核上性眼肌麻痹:7例均有垂直性核上性眼肌麻痹,1例以双眼扫视运动变慢起病,1例于病程第10年才出现垂直性核上性眼肌麻痹。5例先出现上视受限,2例先出现下视受限,最终均进展为上下视不能。(2)帕金森综合征症状:6例表现为表情呆滞,动作变慢,起步、转身困难,反复跌倒;4例出现上肢静止性震颤。7例均有轴性肌强直,4例表现为四肢及躯干肌肌张力增高并出现sitting en bloc征(图1~2)。2例仅表现为颈肌及上部躯干肌肌强直,以致颈后仰。(3)假性延髓性麻痹:6例于病程3~10年出现假性延髓性麻痹,其中先于凝视麻痹出现4例,后于凝视麻痹出现1例,与凝视麻痹同时出现1例。1例随访5年后失访,失访前尚未出现假性延髓性麻痹。(4)其他:2例出现认知功能障碍,1例病初即出现工作能力下降,另1例于病程第8年出现轻度认知功能障碍伴尿失禁。2例出现易怒、情绪波动等。
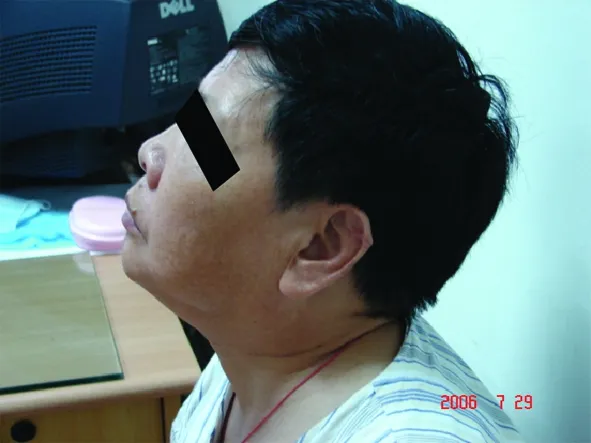
图1PSP患者出现面具脸,颈肌张力增高,呈颈部过伸位

图2PSP患者呈sitting en bloc现象:颈后伸,姿势僵直,坐在椅子上身体向后靠时双脚离地
2.2脑MRI表现7例脑MR平扫均见第三脑室和脚间池变宽、中脑萎缩,侧脑室扩大及外侧裂增宽等不同程度大脑皮质萎缩,以额叶明显(图3、4)。MR正中矢状位见中脑上端萎缩、上缘平坦或凹陷,T1加权像呈“蜂鸟征(humming bird sign)”(图5);轴位见中脑前后径变小,导水管扩张,四叠体池也增大,T2加权像中脑呈“鼠耳征(mouse ears sign)”(图6)。
2.3治疗全部患者均使用过抗帕金森病(Parkinson disease,PD)药物,如美多巴、息宁、司来吉兰、吡贝地尔缓释片、盐酸普拉克索、金刚烷胺等,均无明显疗效或疗效短暂。
3 讨论
PSP又称Steele-Richardson-Olszewski综合征,1904年由Posey首先描述,1964年由Steele等首先作为一个独立的疾病对其进行详细报道[2]。该病病因不明,目前普遍认为属一种tau蛋白病,位于17q21染色体上的tau基因编码突变是散发性PSP的主要危险因素。
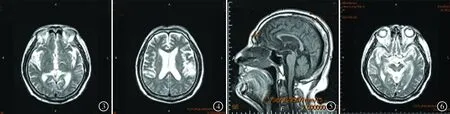
图3PSP患者头颅MRI平扫可见第三脑室增宽、扩大,外侧裂增宽、颞叶萎缩
图4PSP患者头颅MRI平扫可见侧脑室扩大,额叶皮质萎缩
图5PSP患者MRI正中矢状位T1加权像可见中脑上缘平坦或凹陷,呈“蜂鸟征”
图6PSP患者MRI轴位T2加权像中脑呈“鼠耳”状改变
PSP以散发为主。该组7例均为散发。PSP多在45岁后起病,平均发病年龄55~70岁,50岁前发病相对少见,60岁后为发病高峰。男性多于女性,男女之比文献报道不一,约(2~3)∶1到5∶3。本组患者发病年龄47~68岁,男女比为6∶1。
3.1临床表现PSP隐袭起病,进行性加重,早期易误诊,误诊时间可长达十余年。
3.1.1首发症状:文献报道[3]PSP最常见的首发症状依次是肢体强直-少动、姿势不稳、假性延髓性麻痹和认知损害。本组7例中4例以动作变慢、步态不稳为首发症状,另有2例以眼部症状为首发症状,表现为眼花、重影及视物模糊,易误诊为眼科疾病,1例以双手抖动为首发症状,易误诊为PD。该病早期诊断困难,应注意观察病程演变,以便及早诊断。
3.1.2临床表现:(1)核上性眼肌麻痹:是PSP最具诊断价值的临床表现,出现早晚差异很大,一般在出现核上性眼肌麻痹时才得以诊断。早期表现为两眼追随性下视麻痹、上视受限,逐渐发展成完全性垂直凝视麻痹,晚期侧视运动亦受累。自发性凝视较追踪性凝视更易受累[4],但核上性眼肌麻痹常在发病多年后才出现[5],给早期诊断造成困难。本组2例以此为首发症状,1例在病程第10年才出现该症状。因此临床上对运动迟缓和肌张力增高的患者应特别注意检查是否有核上性眼肌麻痹以排除PSP可能。(2)帕金森综合征症状:常对称起病,步态不稳是最常见的首发症状[4-5],尤易向后跌倒,系眼-前庭功能障碍、躯干强直、少动所致。轴性肌强直是本病的另一特征,即颈肌及上部躯干肌强直比四肢强直明显,表现为身体笔直伴颈后仰的特殊体姿[4]。本组7例均有轴性肌强直,4例伴四肢肌张力增高,2例颈肌及上部躯干肌肌强直显著,以致颈后伸,4例出现sitting en bloc征。(3) 假性延髓性麻痹:本组7例中6例出现假性延髓性麻痹症状,无以假性延髓性麻痹为首发症状者,可能与本组病例数较少有关;1例于病程第10年才出现假性延髓性麻痹症状,较罕见,文献中未见报道。(4)认知功能障碍与行为异常:认知功能障碍以皮质下痴呆为特征[4],表现为思维缓慢、健忘伴淡漠、抑郁及执行功能减退。晚期可出现睁闭眼失用症。本组仅2例出现认知功能障碍,1例出现于病初,1例于病程第8年出现,对诊断PSP不具特异性。
3.2MRI特征脑MR平扫可见第三脑室和脚间池变宽、中脑和四叠体萎缩、导水管周围FLAIR像高信号等改变,还可出现不同程度大脑皮质萎缩,以额叶明显[5-6]。Kato等[7]在MR正中矢状面T1加权像平扫研究中发现,PSP组以中脑顶盖萎缩为主,中脑嘴明显变尖,使中脑、脑桥和小脑整体上形似蜂鸟,称为“蜂鸟征”(humming bird sign), PD组和正常对照组未见此征象,认为“蜂鸟征”是PSP特征性MR表现,有助于PSP诊断,但其鉴别PSP与其他非典型帕金森综合征的敏感度和特异度尚存争议[6]。PSP患者MR轴位可见中脑前后径明显缩短,谓之“鼠耳征”(mouse ears sign);同时,由于中脑被盖部外侧缘凹陷,也可表现为“牵牛花征”[6]。本组7例头颅MRI均显示“蜂鸟征”和“鼠耳征”,可能与本组病例病程普遍较长有关。
3.3诊断和鉴别诊断神经病理学检查仍是目前确诊PSP的金标准[8]。迄今公开发表的PSP诊断标准有7种,多数基于不同作者自身的临床经验且内容互有重叠。目前公认的是1996年NINDS-SPSP推荐的诊断标准[1],该标准将PSP分为疑诊(possible)、拟诊(probable)和确诊(definite)。研究证实NINDS-SPSP诊断标准在敏感度、特异度及阳性预测值方面均优于另外几项诊断标准[9]。本组中2例为拟诊、5例为疑诊PSP。由于PSP缺乏特征性临床表现和实验室检查手段,易于误诊或漏诊。临床上需与PD、多系统萎缩(MSA)、弥漫性路易体病、Pick病等鉴别。本组7例均曾存在误诊情况,误诊最多的是PD,1例最初误诊为脑梗死,后误诊为MSA;另1例曾误诊为慢性酒精中毒性神经病。误诊时间最长者达12年,其中1例以眼部症状为首发症状者在眼科就诊5年后转入神经科就诊,在神经科又误诊为PD长达5年。
3.4治疗和预后目前,对PSP仍无有效治疗。文献报道,左旋多巴对PSP的近似有效率约26%,普拉克索未见明显疗效。5-羟色胺再摄取抑制剂、胆碱酯酶抑制剂、毒蕈碱受体拮抗剂、α2-肾上腺素能受体拮抗剂等也曾用于PSP治疗,但疗效均不确切。近期报道氨酪酸受体激动剂唑吡坦有助于改善PSP的运动障碍症状[10]。PSP平均存活时间为5~6.9年,首诊平均存活期约2.7年。病初4年内,75%的患者能独立完成日常活动,之后进展为完全性依赖[11]。本组7例中,1例随访5年后失访;3例分别于病程第6、7、9年死亡,死因为肺炎(2例)和泌尿系统感染(1例);4例仍在随访中,病程最长者已达12年,且生活尚能自理。文献报道[12]病程第1年即有跌倒者的存活期较无跌倒者短,早期出现尿失禁和肌张力障碍者存活期短,以震颤发病或以震颤为主要表现者存活期最长。发病年龄、性别、早期出现痴呆、垂直性核上性麻痹或躯干强直不影响预后。最常见死亡原因为吸入性肺炎,其次是心血管病及肾脏感染。
综上所述,PSP是一种病因未明的多发生于中老年人的少见的中枢神经系统变性疾病,隐袭起病,进行性加重。典型临床表现为垂直性眼肌麻痹、假性延髓性麻痹、轴性肌张力增高和认知障碍,但临床表现变化多端,与多种锥体外系统疾病的临床表现重叠,早期易误诊。临床上需与PD、MSA、弥漫性路易体病、Pick病等鉴别。脑部MR检查有助于上述疾病的鉴别。目前无有效治疗,预后较差。
[1]Litvan I, Agid Y, Calne D, et a1. Clinical research criteria for the diagnosis of progressive supranuclear palsy (Steele-Richardson-Olszewski syndrome): report of the NINDS-SPSP international workshop[J]. Neurology, 1996,47(1):1-9.
[2]Steele J, Richardson JC, Olszewski J. Progressive supranuclear palsy. A heterogeneous system degeneration involving brain stem, basal ganglia and cerebellum with vertical gaze and pseudobulbar palsy, nuchal dystonia and dementia[J]. Arch Neurol, 1964,10:353-359.
[3]Nath U, Ben-Shlomo Y, Thomson RG, et al. Clinical features and natural history of progressive supranuclear palsy: a clinical cohort study[J]. Neurol, 2003,60:910-916.
[4]Dickson DW, Ahmed Z, Algom AA, et a1. Neuropathology of variants of progressive supranuclear palsy[J]. Curt Opin Neurol, 2010,23(4):394-400.
[5]Barsottini OG, Felicio AC, Aquino CC, et a1. Progressive supranuclear palsy: new concepts[J]. Arq Neuropsiquiatr, 2010,68(6):938-946.
[6]Stamelou M, Knake S, Oertel WH, et a1. Magnetic resonance imaging in progressive supranuclear palsy[J]. J Neurol, 2011,258(4):549-558.
[7]Kato N, Arai KHattori T. Study of the rostral midbrain atrophy in progressive supranuclear palsy[J]. J Neurol Sci, 2003,210(1-2):57-60.
[8]Sakamoto R, Tsuchiya K, Mimura M. Clinical heterogeneity in progressive supranuclear palsy: problems of clinical diagnostic criteria of NINDS-SPSP in a retrospective study of seven Japanese autopsy cases[J]. Neuropathology, 2010,30(1):24-35.
[9]Williams DR, Lees AJ. Progressive supranuclear palsy: clinicopathological concepts and diagnostic challenges[J]. Lancet Neurol, 2009,8(3):270-279.
[10]Cotter C, Armytage T, Crimmins D. The use of zolpidem in the treatment of progressive supranuclear palsy[J]. J Clin Neurosci, 2010,17(3):385-386.
[11]Alvarez Gonzalez E, Maragoto Rizo C, Arteche Prior M, et al. A clinical and epidemiological description of a series of patients diagnosed as suffering from progressive supranuclear palsy[J]. Res Neurol, 2004,39(11):1006-1010.
[12]张莉,韩月珍,郭瑾洁.进行性核上性麻痹的发病机制及治疗[J].中国实用神经疾病杂志,2013,16(6):92-94.

