不同孔径介孔碳的合成及对药物的缓释性能研究
刘晓蒙, 高云鹏, 张 佳, 徐显峰, 郭 卓
(沈阳化工大学 材料科学与工程学院, 辽宁 沈阳 110142)
目前在医药工业和科技领域药物的缓/控释已成为一个重要的研究方向.缓释、控释药物制剂具有传统药物制剂所无法比拟的优越性,例如可以使血药浓度维持在一定水平、提高药物的利用率、药效时间延长、药物的毒副作用降低、降低抗药性.自从M41s[1-2]面世以来,由于其结构特性独特,具有较大的孔容、高比表面积、规则且可调的纳米尺度的孔道结构、表面亲水性及表面性质的可修饰性,对其应用研究已经拓展到药物载体领域[3-8].以不同的介孔硅为硬模板,合成一系列介孔碳[9-14].这些介孔碳具有规则的孔道结构,比较大的比表面积和较大的孔容,被广泛应用于催化、储氢、分离、吸附和药物载体等领域[15-17].现有报道中,大多以难溶性药物为模型,因其溶解度小,难以被吸收利用.
由于目前以介孔氧化硅为药物载体的研究比较多,而以介孔碳为药物载体的研究相对较少,本文以介孔硅分子筛为硬模板,合成不同孔径的介孔碳.以不同孔径的介孔碳作为药物载体,研究它们负载难溶性药物分子布洛芬的缓释性能,确定孔道结构和孔径对药物缓释性能的影响,为介孔材料作为药物缓/控释载体的实际应用提供实验依据.
1 实验部分
1.1 试剂及仪器
蔗糖,化学纯,北京化学试剂公司;SBA-15[18]与MCM-48[2]按照参考文献自制;布洛芬(Ibu),浙江车头制药有限公司;其他试剂均为分析纯,天津大茂试剂厂.
Siemens D5005粉末衍射仪;ASAP 2010 等温吸附仪;JEM-3010透射电子显微镜; JSM-6360-LW扫描电子显微镜;,UV-754紫外可见分光光度计.
1.2 CMK-3与CMK-1的合成
以六方孔道的SBA-15[18-19]和立方孔道的MCM-48[2]为硬模板,按照文献[11,19]分别合成CMK-3和CMK-1.详细实验步骤为:首先将1.25 g 蔗糖溶解于少量水中,然后加入H2SO4,一般保持蔗糖与H2SO4的质量比约为10/1,在80~100 ℃条件下使水分蒸发,然后160 ℃的烘箱中放置 6 h,完成初步碳化过程;将初步碳化的产物用研钵研细,加入0.75 g 蔗糖,0.08 g H2SO4和少量水,重复前一步骤的水分蒸发和初步碳化;最后将2次碳化的产物在氮气保护下,900 ℃保温4 h,完成整个碳化过程;使用质量分数5 %的HF溶液溶解碳化产物,以去除SBA-15和MCM-48模板,制备出介孔碳.以SBA-15为硬模板制得的介孔碳是CMK-3,以MCM-48为硬模板制得的介孔碳是CMK-1.
1.3 药物的组装及释放
分别将0.2 g CMK-3和CMK-1 置于100 mL、0.10 mol L-1的布洛芬正己烷溶液中,磁力搅拌到吸附平衡为止.紫外法测定滤液中药物的残留量,用差减法计算出组装体中布洛芬的含量,药物组装体分别标记为Ibu/CMK-3和 Ibu/CMK-1.
用负载药物后的介孔碳分子筛进行体外释放研究,在模拟人工肠液中进行(磷酸盐缓冲液,pH=7.4).取一定量的组装体压片(3 MPa),然后将样品片置于500 mL模拟人工肠液中,搅拌.定时吸取5 mL释放液,并且及时补充模拟人工肠液以保持释放液体积恒定,适当稀释,用紫外-可见分光光度计分析释放液中Ibu的浓度,测定药物的释放量.
2 结果与讨论
2.1 X射线衍射分析
图1是CMK-3,Ibu/CMK-3,CMK-1和 Ibu/CMK-1的XRD图.从图1可以看出:CMK-3的XRD图在2θ为0.9,1.6,1.9 处有3个衍射峰,分别为(100),(110) 和(200)晶面,说明CMK-3具有规则排列的六方有序孔道结构[19];CMK-1的XRD图在2θ为1.7,2.9 处有2个衍射峰,分别是(110) 和(211) 晶面,说明CMK-1规则排列的立方有序介孔孔道结构[11].当介孔碳CMK-3和CMK-1分别负载上药物布洛芬后,它们衍射峰的强度都有所降低,但衍射峰出现的位置不变,这说明它们负载药物后还具有规则排列的孔道结构,只是有序度稍稍降低.

图1 XRD 谱图Fig.1 Power XRD patterns
2.2 氮气吸附/脱附曲线
样品的氮气吸附/脱附等温线(77 K)和孔径分布如图2所示.所有样品的氮气吸附/脱附曲线都是典型的Ⅳ型等温线,都出现一个明显的滞后环,具有典型的介孔特征.介孔碳CMK-3的孔径分布集中在4.6 nm左右,CMK-1的孔径分布主要集中在2.7 nm.当CMK-3负载布洛芬后,孔径从4.6 nm减少到3.2 nm;CMK-1负载布洛芬后,孔径从2.7 nm减少到2.5 nm.负载布洛芬后,样品的比表面积、孔容和孔径均下降,说明药物成功负载介孔碳分子筛的孔道中.从氮气吸附/脱附曲线可以看出:对于CMK-3,组装药物分子后比表面积由1 508 m2·g-1降为1 324 m2·g-1,孔容由0.86 cm3·g-1降为0.78 cm3·g-1;对于CMK-1,组装药物分子后比表面积由1 018 m2·g-1降为 924 m2·g-1,孔容由0.51 cm3·g-1降为0.45 cm3·g-1.近一步说明药物分子已经载入到介孔的孔道中.

图2 样品氮气吸附/脱附等温线和孔径分布曲线Fig.2 Nitrogen adsorption/desorption isotherms and pore size distributions of samples
2.3 透射电镜分析
从图3可以看出:CMK-3具有明显的孔道结构,负载药物后依然保持很好的有序结构.CMK-1的有序结构不明显,这是因为CMK-1并不是MCM-48真正的复制品,在脱除MCM-48硬模板的过程中,其结晶学对称性下降[20],负载药物后有序度也降低.

图3 样品的透射电镜照片Fig.3 TEM of mesoporous carbon materials
2.4 扫描电镜分析
从图4可以看出:负载布洛芬的介孔碳CMK-3和介孔碳CMK-1,依旧是介孔碳各自原来的形貌,说明负载布洛芬后对原来分子筛的形貌不产生影响.

图4 样品的扫描电镜照片Fig.4 SEM of mesoporous carbon materials
2.5 红外光谱分析
图5是样品的红外光谱.从图5可以看出:CMK-3基本没有红外吸收,这是由于CMK-3基本没有官能团.在载药后样品的红外光谱图中可观察到药物分子季碳原子的伸缩振动峰(1 460 cm-1和 1 521 cm-1)以及烷基C—H的伸缩振动峰(2 920 cm-1和2 964 cm-1),在1 728 cm-1处可观察到羰基的伸缩振动峰,进一步说明药物分子已经负载到介孔碳孔道中.

图5 样品的红外图谱Fig.5 IR spectra of samples
2.6 组装量及释放性能
介孔碳最大载药量见图6.有研究表明,药物负载量的大小和载体的比表面积有关[7].比表面积大,载药量较大.本研究表明:载药量不仅与比表面积有关,与介孔的孔道结构及孔容也有关.由于CMK-3具有大的比表面积(1 508 m2·g-1)和孔容(0.86 cm3·g-1),因而具有较大的载药量(质量分数66.18 %).而CMK-1的比表面积(1 018 m2·g-1)和孔容(0.51 cm3·g-1)比CMK-3的比表面积和孔容要小,其载药量仅为48.57 %.
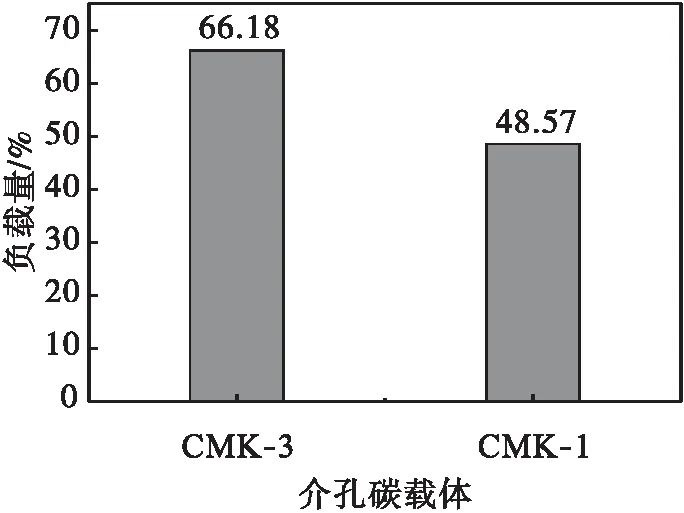
图6 介孔碳最大载药量Fig.6 Largest drug loading of mesoporous carbon materials
图7是负载药物的不同孔径的介孔碳分子筛,在模拟人工肠液中药物的释放曲线.
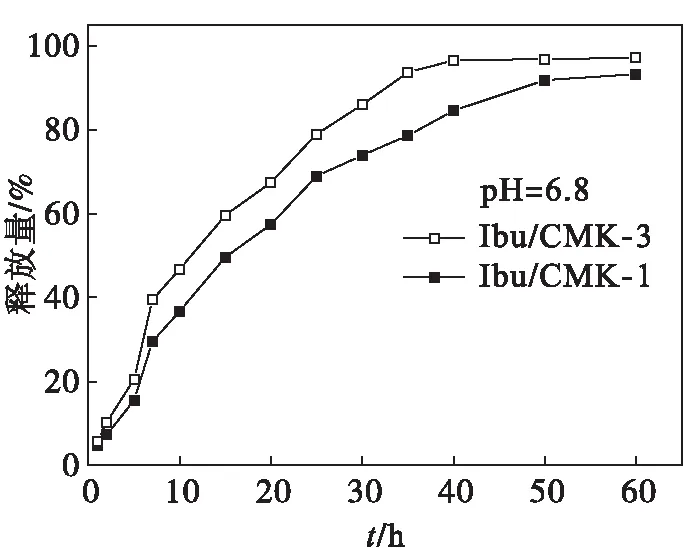
图7 布洛芬在模拟人工肠液中的释放曲线Fig.7 Release profiles of Ibu from simulated intestinal fluid
从图7可以看出:取定布洛芬在模拟肠液中释放过程的几个时间点:5、10、15、30、40 h,可观测到Ibu/CMK-3和Ibu/CMK-1释放量分别为20.5 %、46.7 %、59.6 %、85.9 % 、96.5 % 以及15.5 %、36.7 %、49.6 %、73.9 %、84.5 %.Ibu/CMK-3 和Ibu/CMK-1载药体系完全药物释放所需时间分别是36 h和50 h.释放速率的差异可归因于孔道结构和孔径影响,Ibu/CMK-1具有立方相的孔道结构,药物分子不容易在立方相的孔道中传输,不利于药物释放,同时,其还具有相对小的孔径(2.5 nm),该介孔碳载体对药物分子的扩散阻力较大,药物释放缓慢.
3 结 论
采用硬模板法制备了2种不同孔径不同结构的介孔碳分子筛,用介孔碳分子筛分别负载难溶性药物布洛芬,通过各种表征手段,表明布洛芬成功负载到介孔碳的孔道中.研究了负载布洛芬的介孔碳分子筛的缓释性质,研究结果表明:CMK-1具有立方相的孔道结构,药物分子不容易在立方相的孔道中传输,不利于药物的释放,同时,其还具有相对小的孔径,该介孔碳载体对药物分子的扩散阻力较大,药物释放缓慢.
参考文献:
[1] Kresge C T,Leonowicz M E,Roth W J,et al.Ordered Mesoporous Molecular Sieves Synthesized by a Liquid-crystal Template Mechanism[J].Nature,1992,359(6397):710-712.
[2] Beck J S,Vartuli J C,Roth W J,et al.A New Family of Mesoporous Molecular Sieves Prepared with Liquid Crystal Templates[J].J Am Chem Soc,1992,114(27):10834-10843.
[3] Horcajada P,Rámila A,Pérez-Parient J,et al.Influence of Pore Size of MCM-41 Matrices on Drug Delivery Rate[J].Microporous and Mesoporous Materials,2004,68(1/3):105-109.
[4] Horcajada P,Rámila A,Ferey G,et al.Influence of Superficial Organic Modification of MCM-41 Matrices on Drug Delivery Rate[J].Solid State Sciences,2006,8(10):1243-1249.
[5] Szegedi A,Popova M,Goshev I,et al.Controlled Drug Release on Amine Functionalized Spherical MCM-41[J].Journal of Solid State Chemistry,2012,194:257-263.
[6] Mortera R,Fiorilli S,Garrone E,et al.Structural changes of MCM-41 Spheres During Ibuprofen Release to SBF[J].Studies in Surface Science and Catalysis,2008,174(Part B):1001-1004.
[7] Szegedi A,Popova M,Goshev I,et al.Effect of Amine Functionalization of Spherical MCM-41 and SBA-15 on Controlled Drug Release[J].Journal of Solid State Chemistry,2011,184(5):1201-1207.
[8] Ghedini E,Signoretto M,Pinna F,et al.Ibuprofen Delivery Behaviour on MCM-41:Influence of Organic Groups Amount[J].Studies in Surface Science and Catalysis,2008,174(Part A):429-432.
[9] Karandikar P,Patil K R,Mitra A,et al.Synthesis and Characterization of Mesoporous Carbon Through Inexpensive Mesoporus Silica as Template[J].Microporous and Mesoporous Materials,2007,98(1/3):189-199.
[10] Kruk M,Jaroniec M,Ryoo R,et al.Characterization of Ordered Mesoporous Carbons Synthesized Using MCM-48 Silicas as Templates[J].J Phys Chem B,2000,104(33):7960-7968.
[11] Joo S H,Jun S,Ryoo R.Synthesis of Ordered Mesoporous Carbon Molecular Sieves CMK-1[J].Microporous Mesoporous Mater,2001,44/45:153-158.
[12] Li H C,Yasuhiro S,Li Y S,et al.Synthesis of Carbon Replicas of SBA-1 and SBA-7 Mesoporous Silicas[J].Microporous and Mesoporous Materials,2006,95(1/3):193-199.
[13] Jun S,Joo S H,Ryoo R,et al.Synthesis of New Nanoporous Carbon with Hexagonally Ordered Mesostructure[J].J Am Chem Soc,2000,122(43):10712-10713.
[14] Enterría M,Suárez-García F,Martínez-Alonso A,et al.Synthesis of Ordered Micro-mesoporous Carbons by Activation of SBA-15 Carbon Replicas[J].Microporous and Mesoporous Materials,2012,151(15):390-396.
[15] Liu Z,Mi J H,Yang Y,et al.Synthesis of Pt-containing Ordered Mesoporous Carbons and Their Catalysis for Toluene Hydrogenation[J].Materials Letters,2011,65(23/24):3548-3551.
[16] Thomas J L,Dai M Z,Wei Y,et al.Rapid Adsorption of Alcohol Biofuels by High Surface Areamesoporous Carbon[J].Microporous and Mesoporous Materials,2012,148(1):107-114.
[17] Wang X F,Liu P,Tian Y.Ordered Mesoporous Carbons for Ibuprofen Drug Loading and Release Behavior Original Research Article[J].Microporous and Mesoporous Materials,2011,142(1):334-340.
[18] Zhao D Y,Feng J L,Huo Q S,et al.Triblock Copolymer Syntheses of Mesoporous Silica with Periodic 50 to 300 Angstrom Pores[J].Science, 1998, 279 (5350):548-552.
[19] He J G,Ma K,Jin J,et al.Preparation and Characterization of Octyl-modified Ordered Mesoporous Carbon CMK-3 for Phenol Adsorption[J].Microporous and Mesoporous Materials,2009,121(1/3):173-177.
[20] Ryoo R,Joo S H,Jun S.Synthesis of Highly Ordered Carbon Molecular Sieves via Template-mediated Structural Transformation[J].J Phys Chem B 1999,103(37):7743-7746.

