葛根黄酮自微乳化滴丸的制备及体外评价
樊红波,王玉,刘昕,孙士淋,张广远,管清香
(吉林大学药学院,长春130021)
葛根为临床常用中药,具有解肌退热、升阳透疹、生津止泻的功效,葛根黄酮为其主要有效成分,临床上主要用于治疗心血管疾病[1],但其难溶于水,口服吸收程度较差,生物利用度小,体内消除快且不易蓄积[2]。因此,提高葛根黄酮溶解度及生物利用度成为其制剂研究中的主要问题。研究表明,自微乳化给药系统(Self-microemulsifying drug delivery system,SMEDDS)可提高水难溶性药物生物利用度[3],但自乳化制剂都是液体形式,通常是封装在软胶囊或硬胶囊中,易造成囊壁软化。本试验将自微乳技术与固体分散技术结合,制备葛根黄酮自微乳化滴丸,拟在提高葛根黄酮的口服生物利用度的同时,避免自微乳制成胶囊时囊壁软化导致的药物漏泄[4],简化其制备工艺,提高生产率,降低成本,有利于劳动保护[5]。
1 仪器与试药
AB204-N电子分析天平(梅特勒-托利多仪器上海有限公司);THZ-82水浴恒温振荡器(金坛市精达仪器制造厂);DW-1型滴丸机(江苏泰州市制药机械二厂);RCZ-8A智能药物溶出仪(天津大学精密仪器厂)。
Crodamol GTCC(Croda公司),Maisine 35-1(法国Gattefosse公司),Cremophor RH 40(德国BASF公司),葛根黄酮(纯度66.7%,西安赛邦医药科技有限公司),葛根素标准品(中国药品生物制品检验所),甲基硅油、液体石蜡均为化学纯,其他试剂均为分析纯。
2 方法
2.1标准曲线的绘制
取葛根素储备液适量,用蒸馏水稀释适当倍数配制成浓度分别为2.036μg/mL、4.072μg/mL、6.108μg/mL、8.144μg/mL、10.180μg/mL、12.220μg/mL的系列葛根素标准品溶液。分别在250nm波长处测定吸光度,用吸光度(Y)对浓度(X)作线性回归,得回归方程为:Y=0.0672X+0.004 76(R2=0.9998)。
2.2葛根黄酮自微乳的制备
取处方量Crodamol GTCC、Maisine 35-1﹑Cremophor RH 40和1,2-丙二醇,混匀,加入处方量葛根黄酮,超声溶解,搅拌均匀,得葛根黄酮自微乳。
2.3葛根黄酮自微乳化滴丸的制备
根据预实验确定SMEDDS与滴丸基质比例、温度和滴距对自乳化滴丸有较大的影响,每个因素选择3个水平,采用L9(34)正交法优选滴丸制备工艺,因素水平见表1。以滴丸硬度、圆整度、丸重差异为指标进行综合评价,具体评分标准如表2所示。
表1L9(34)实验因素水平表
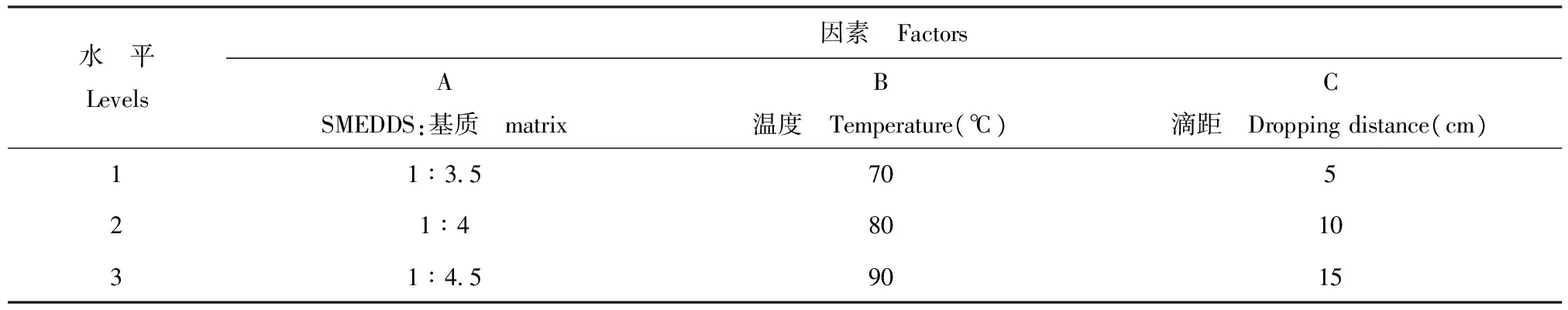
Table 1Factors and levels of L9(34) orthogonal test
表2L9(34)应变量评价标准
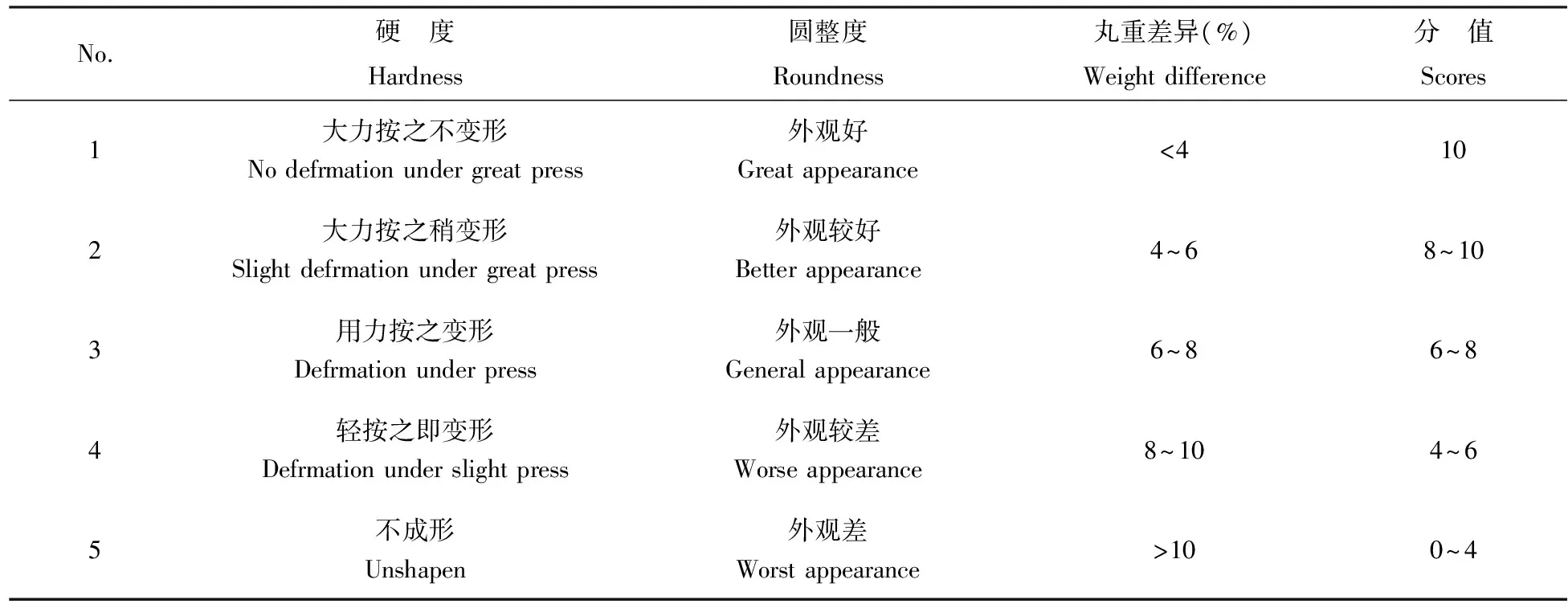
Table 2Evaluation criterion of depend variables for L9(34) orthogonal test
2.4体外释放度研究
对比葛根黄酮自微乳化滴丸与市售愈风宁心滴丸体外释放行为。取2种滴丸各6粒,以(37±0.5)℃脱气蒸馏水900mL为释放介质,转速为75r/min,分别于2min、5min、10min、20min、40min、60min取样5mL,补充同体积同温度的蒸馏水,样品经0.45μm微孔滤膜过滤后,稀释后测定含量。
3 结果与讨论
3.1精密度实验
取葛根素储备液适量,用蒸馏水稀释配制低浓度(2.036μg/mL)、中浓度(6.108μg/mL)、高浓度(12.220μg/mL)葛根素溶液,测定日内及日间精密度。结果表明,本方法精密度的RSD均小于2%,该方法精密度良好。
3.2回收率实验
按处方称取一定比例的空白辅料,分别加入不同体积葛根素储备液,配制低浓度(2.036μg/mL)、中浓度(6.108μg/mL)、高浓度(12.220μg/mL)样品溶液,0.45μm微孔滤膜,取续滤液测定吸收度。结果表明,平均回收率大于95%,RSD小于2%,该方法回收率良好。
3.3葛根黄酮自微乳化滴丸工艺优选
预实验表明,冷凝剂温度小于2℃时,滴丸不圆整、丸重差异大;冷凝剂温度大于10℃时,滴丸形状变扁、丸重差异大。本试验分别用甲基硅油和液体石蜡作冷凝剂,结果发现,甲基硅油做冷凝基质得到的滴丸丸形圆整度、硬度、表面光滑度等均较液体石蜡好。在混合自微乳与滴丸基质时发现,自微乳比例较高时,滴丸硬度差,容易黏连;基质比例高,硬度好,圆整度好,但载药量小,服用量大,且成本高。考虑到载药量,确定自微乳与滴丸基质的质量混合范围在1∶3.5~1∶4.5、固定滴速50滴/min、冷凝剂温度2℃~10℃制备滴丸。
由极差分析结果,影响滴丸成型工艺的因素依次排列为B>C>A,其中A因素的水平1、水平2与水平3之间相差不大。为提高载药量,A因素选择A1;B因素水平2明显优于水平1和水平3,确定采用B2;C因素水平2明显优于水平1和水平3,确定采用C2。故确定各因素采用A1B2C2,即SMEDDS与基质比例为1∶3.5、物料温度80℃、滴距为10cm(表3)。
表3L9(34)实验及结果

Table 3L9(34) Experiment s and results
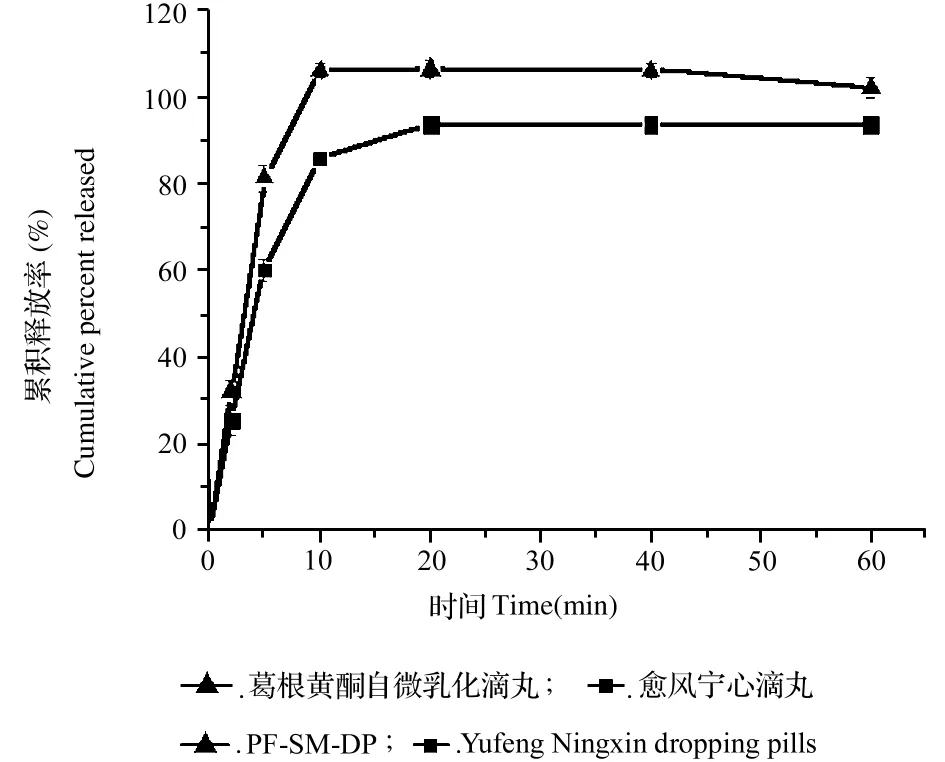
3.4葛根黄酮自微乳化滴丸体外释放度
制成自微乳的药物滴丸释放速率明显高于仅制成滴丸的药物,自微乳化滴丸10min的溶出度可达105.10%,而愈风宁心滴丸10min的释放度仅达到82.03%(图1)。自微乳滴丸释放速率明显高于仅制成滴丸的药物,可能是因自微乳加入溶液形成载药小乳滴,增加了药物表面积和溶解度,提高了溶出度。
由此可见,自微乳技术与固体分散体技术结合可更好地提高葛根黄酮的体外溶出速率和葛根黄酮口服生物利用度。葛根黄酮自微乳化滴丸大鼠体内研究将另文报道。
[1]陈江林,江丽霞,曾靖.葛根异黄酮对运动训练大鼠血液生化指标及抗氧化的影响[J].中国当代医药,2014,21(1):6-8.
[2]徐轶尔,李秋红,杨菲菲,等.中药葛根的药理药效研究[J].吉林中医药,2010,30(11):993-994.
[3]Larsen AT,Ohlsson AG,Polentarutti B,et al.Oral bioavailability of cinnarizine in dogs:Relation to SNEDDS droplet size,drug solubility and in vitro precipitation[J].European Journal of Pharmaceutical Sciences,2013,48:335-339.
[4]Mei XH,Etzler FM,Wang ZR,et al.Use of texture analyzer to study hydrophilic solvent effects on the mechanical properties of hard gelatin capsules[J].International Journal of Pharmaceutics,2006,324:128-135.
[5]周雅琴,陈燕军,冯青然.中药滴丸剂的研究进展[J].中国中药杂志,2006,31(2):101-105.

