改良FOLFOX6新辅助化疗与术后化疗治疗进展期胃癌的临床效果比较
贺新伟 薛迪新
浙江省瑞安市人民医院,浙江瑞安325200
改良FOLFOX6新辅助化疗与术后化疗治疗进展期胃癌的临床效果比较
贺新伟 薛迪新▲
浙江省瑞安市人民医院,浙江瑞安325200
目的比较改良FOLFOX6新辅助化疗与术后化疗治疗进展期胃癌的临床效果及不良反应。方法选择2009年3月~2010年6月瑞安市人民医院60例经组织学证实的局部进展期或转移性胃癌患者,分为改良FOLFOX6新辅助化疗组(术前组)、改良FOLFOX6术后辅助化疗组(术后组),化疗4周后进行疗效评价,观察两组临床效果、疾病进展时间、生存时间和不良反应。结果术前组总有效率及肿瘤控制率(50.0%、76.7%)均高于术后组(43.3%、70.0%),差异有统计学意义(χ2=5.90,5.88,均P<0.05)。术前组Ⅲ~Ⅳ度不良反应发生为8例,术后组Ⅲ~Ⅳ度不良反应发生为13例,差异有统计学意义(χ2=10.76,P<0.05)。术前组肿瘤进展时间少于术后组[(10.4±2.4)个月比(16.9±1.7)个月],2年生存率高于术后组(86.67%比66.67%),差异有统计学意义(t=7.71,χ2= 8.02,均P<0.05)。结论改良FOLFOX6新辅助化疗相对于改良FOLFOX6术后辅助化疗而言,其疗效和肿瘤进展时间、生存时间比较更佳,预期将为临床进展期胃癌的治疗提供新的高效安全的化疗方案,能有效提高进展期胃癌患者生存时间和生活质量,减少患者经济负担。
改良FOLFOX6曰新辅助化疗曰术后化疗曰进展期胃癌
胃癌是消化系统最常见的恶性肿瘤,致死率居各类肿瘤的第2位。当前,外科手术切除依然是唯一可能根治胃癌的手段,但根治术后仍有较高局部区域复发率(22%~94%)和远处转移率[1],且早期胃癌患者临床症状往往不典型甚至缺乏症状,导致大多数患者确诊时多为进展期胃癌,而对于大多数胃癌患者来说,外科手术难以达到生物学意义上的根治[2]。近年来,新辅助化疗因其可有效降低胃癌临床分期和提高根治性切除率,因此受到外科医师重视[3]。然而由于传统的进展期胃癌新辅助化疗方案基本沿用了胃癌根治术后辅助化疗的基本方案,存在治疗总有效率低、根治性切除率低和毒副作用大等缺点,致使该方法不能在临床治疗中进行推广应用。改良FOLFOX6方案是目前应用较为成熟且可信度较高的改良型新辅助化疗法,该方法首先在治疗结肠癌中成效显著,同时对胃癌Ⅱ期及进展期胃癌的治疗也有一定的效果。但关于全面比较及研究改良FOLFOX6方案在进展期胃癌中的报道相对匮乏,不能够系统地解释改良FOLFOX6在应用中的疗效及注意事项。鉴于此,为了明确改良FOLFOX6在治疗进展期胃癌中的效果及引起的不良反应,本研究拟设计将浙江省瑞安市人民医院(以下简称“我院”)肿瘤外科收治的进展期胃癌患者随机分为改良FOLFOX6新辅助化疗组和术后化疗组,观察、比较和分析两组化疗前后临床疗效、不良反应、肿瘤进展时间、生存时间差异,探讨改良FOLFOX6新辅助化疗的临床应用的价值,以期为改良FOLFOX6在治疗NAC中的应用提供临床数据支持。现将研究报道如下:
1 资料与方法
1.1 一般资料
选择我院肿瘤外科2009年3月~2010年6月收治住院的进展期胃癌患者60例,将其分为改良FOLFOX6新辅助化疗组(术前组)和改良FOLFOX6术后辅助化疗组(术后组)。术前组30例,其中男18例,女12例;年龄42~78岁,中位年龄58.33岁;中分化腺癌12例,低分化腺癌9例,印戒细胞癌9例;临床分期:Ⅱ期8例,Ⅲ期13例,Ⅳ期9例;KPS评分均>70分。术后组30例,其中男20例,女10例;年龄41~79岁中位年龄56.18岁;中分化腺癌12例,低分化腺癌10例,印戒细胞癌8例;临床分期:Ⅱ期患者10例,Ⅲ期患者9例,Ⅳ期患者11例,KPS评分均>70分。两组患者在年龄、性别、病程分期、病理类型指标等方面差异无统计学意义(P>0.05),具有可比性。
1.2 纳入标准
①所有病例均经胃镜活检,病理学证实为胃腺癌;②cTNM分期为T3~4NanyM(依据2009年UICC TNM分期标准:主要依据腹部CT,并结合胃镜、B超等,必要时超声内镜,MRI、PET/CT、上消化道造影等);③患者年龄18~80岁;④Karnofsky评分≥70分;⑤预计生存时间≥3个月;⑥既往无根治或姑息手术、放化疗史等的初治患者;⑦主要器官功能正常,无化疗禁忌证;⑧患者签署化疗知情同意书。
1.3 治疗方法
1.3.1 术前组采用改良FOLFOX6方案新辅助化疗组。改良FOLFOX6化疗方案如下:奥沙利铂130 mg/m2,静脉滴入>2 h,第1天;亚叶酸钙400 mg/m2静脉滴入,第1天;5-氟尿嘧啶400 mg/m2,静脉滴入<2 h,第1天;随后予5-氟尿嘧啶2.4 g/m2,持续静脉滴入46 h。21 d为1个化疗周期,共3个周期。化疗过程中常规使用升白安片及利血生片各2片,3次/d,预防及控制白细胞降低;止吐药昂丹司琼针8 mg化疗前30 min静推1次;制酸剂洛赛克针40 mg,1次/d,静推。
1.3.2 术后组手术方式同上,术后4~6周开始行改良FOLFOX6方案术后辅助化疗,化疗前及3个周期后4周进行全面检查。
1.4 观察指标及评价标准
临床疗效:所有病例均在化疗4周后行疗效确认。参考2000年由美国和加拿大国立癌症研究所,欧洲癌症研究和治疗组织提出的实体瘤疗效反应评价标准来进行疗效评估[4]。总有效:完全缓解+部分缓解;肿瘤控制=完全缓解+部分缓解+稳定。
不良反应:化疗毒性的评定依据WHO毒性反应评价标准判定[5],通常分为0~Ⅳ度,严重不良反应指Ⅲ度以上。
其他:肿瘤进展时间及2年生存率。
1.5 统计学方法
采用SPSS 14.0软件进行统计分析,正态分布计量资料以均数±标准差(±s)表示,两组间比较采用t检验计数资料以率表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组疗效比较
结果显示,术前组总有效率及肿瘤控制率均高于术后组,差异有统计学意义(χ2=5.90、5.88,均P<0.05)。见表1。
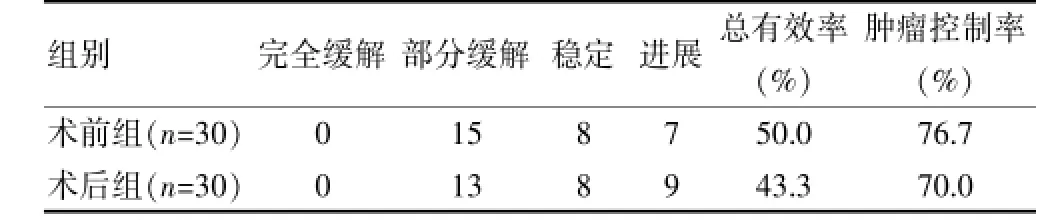
表1 两组疗效比较(例)
2.2 两组不良反应比较
结果显示,两组均无化疗相关死亡。其中术前组发生Ⅲ~Ⅳ度不良反应为8例,术后组发生Ⅲ~Ⅳ度不良反应为13例,两组比较,差异有统计学意义(χ2=10.76,P<0.05)。见表2。
2.3 两组肿瘤进展时间尧2年生存率比较
结果显示,术前组肿瘤进展时间少于术后组,2年生存率高于术后组,差异有统计学意义(t=7.71,χ2= 8.02,均P<0.05)。见表3。
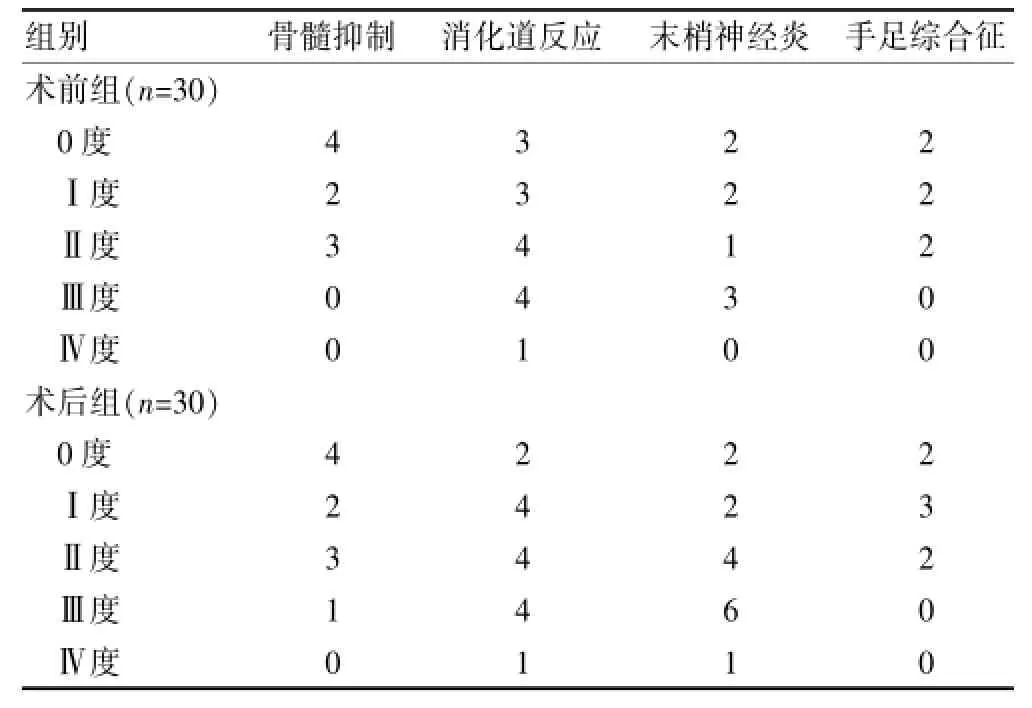
表2 不良反应比较(例)

表3 两组肿瘤进展时间、2年生存率比较
3 讨论
胃癌是人类最常见的恶性肿瘤之一,也是世界第二大癌症死亡原因[6]。迄今为止,手术切除仍然是治疗胃癌的最重要手段,且唯有根治性切除方可治愈。但研究表明,超过七成的胃癌患者就诊时已属进展期[7],因此,进展期胃癌应当采用综合化疗、放疗、分子生物等多种模式进行治疗。化疗是胃癌综合治疗的主要组成部分之一,在胃癌的治疗中起重要的作用。目前,临床上研究及应用较多的是术后辅助化疗,理论上术后辅助化疗可通过杀灭体内残存的微小转移灶以延长生存期,但临床实验显示其在胃癌中的收效甚微,结果不令人满意。
近年来,新铺助化疗受到国内外相关领域的重点关注。它可早期治疗微小转移灶;清除手术可能残留的肿瘤细胞,使肿瘤细胞活力降低,不易播散入血;确定患者对化疗的敏感性;避免抗药性;肿瘤缩小有利于肿瘤切除,对患者术后治疗计划的制订和判定预后具有重要意义。目前,进展期胃癌新辅助化疗国内外尚无一个公认的标准方案。因此,如何选择高效低毒的化疗方案成为目前NAC治疗进展期胃癌的探索目标和迫切需要。
当前,以铂类和氟尿嘧啶为基础的化疗方案仍然被公认为是胃癌的基础化疗方案。近年来,新药如紫杉类、奥沙利铂、伊立替康以及卡培他滨、替吉奥胶囊等的出现促进了胃癌化疗的发展。奥沙利铂是第3代铂类抗癌药,与顺铂有着相似的作用机制,但相对顺铂而言,抑制DNA的能力更强,结合速度更快,细胞毒作用更强,而不良反应更少。5-氟尿嘧啶(5-Fu)为作用于S期的周期性特异性药物,与OXA联合应用具有协同作用[8]。甲酰四氢叶酸钙是5-Fu的生化调节剂,与5-Fu合用能促进氟尿嘧啶脱氧核甘酸与胸甘酸合成酶(TS)的稳定结合,增加5-Fu的细胞库容,从而大大提高5-Fu的疗效[9]。由法国De-Gramont教授牵头从1984年起创立的草酸铂与亚叶酸钙/5-Fu组成的联合方案称为FOLFOX方案,因使用剂量和时间形式多样而形成了FOLFOX1~7系列方案[10]。FOLFOX6的治疗方案是在FOLFOX4的基础上,将5-FU推注的次数从2次减到1次,并将连续静脉滴注的总量提高到2400 mg/m2,持续46 h。取消5-FU推注可以减少中性粒细胞降低的发生,且更简单易行。
研究发现FOLFOX6方案用于进展期胃癌的新辅助化疗,结果显示其能有效提高疗效和获得较好的根治性切除率,在治疗晚期胃癌发生时候也具有较高的疗效,且初治患者的有效率高于复治者,其引起的毒副作用也可以耐受,在治疗进展期胃癌时有效率可达50%左右,但会引起不同程度的骨髓抑制、胃肠道反应及神经毒性反应,一般患者较耐受[11-14]。近年来国内外研究发现FOLFOX6方案对胃癌也颇具疗效,但主要应用于术后辅助化疗,但临床疗效报道存在差异[15-18]。鉴于此,有研究者尝试将FOLFOX6方案用于进展期胃癌的新辅助化疗,结果显示其能有效提高疗效[19-21]。然而,FOLFOX6新辅助化疗在进展期胃癌中的应用研究仍相对较少,有待进一步研究。
鉴于此,笔者对改良FOLFOX6新辅助化疗法进行了研究。结果显示,术前组在总有效率、肿瘤控制率、不良反应、肿瘤进展时间、生存率方面均优于对照组,说明获得改良FOLFOX6方案相在治疗进展期胃癌的临床疗效相对于改良FOLFOX6术后辅助化疗组具有更佳的疗效,且不良反应更少,研究结果显示改良FOLFOX6方案能有效延长进展期胃癌患者生存时间,提高进展期胃癌患者生活质量,同时改良FOLFOX6方案的相对经济性将为患者减少经济负担,将为改良FOLFOX6方案中的相关药物的相关产业带来巨大的经济效益。
[1]殷蔚伯,余子豪,徐国镇,等.肿瘤放射治疗学[M].4版.北京:中国协和医科大学出版社,2008:808.
[2]傅国平,王薇,裘哲君,等.替吉奥联合奥沙利铂或顺铂治疗进展期胃癌的临床观察[J].中国癌症杂志,2012,22(4):291-294.
[3]金懋林.新辅助化疗在胃癌化疗中的作用[J].外科理论与实践,2005,5(3):140-142.
[4]DuffaudF,TherasseE.Newguidelinestoevaluatetheresponse to treatment in solid tumors[J].Bull Cance L,2000,87:881-886.
[5]孙燕,周际昌.临床肿瘤内科手册[M].2版.北京:人民卫生出版社,1996:18-26.
[6]RiveraFC,Vega-VillegasME,Lopez-BreaMF.Chemothempy of advanced gastric cancer[J].Cancer Treat Rev,2007,33(4):315.
[7]Hundahl SA,Phillips JL,Menck HR.The national cancer data base report on poor survival of U.S.gastric carcinoma patients treated with gastrectomy:fifth edition american joint committee on cancer staging,proximal disease,and the"different disease"hypothesis[J].Cancer,2000,88(4):921-932.
[8]Kline CL,Schiccitano A,Zhu J,et al.personalized dosing via pharmacokinetic monitoring of 5-fluorouracil might reduce toxicity in early-or late-stage colorectal cancer patients treated with infusional 5-fluorouracil-based chemo therapy regimens[J].Clinical Colorectal Cancer,2014,13(2):119-126.
[9]许德明,陈国权,李声谊,等.大剂量醛氢叶酸联合氟尿嘧啶为主的化疗方案治疗头颈与消化道癌56例[J].中华肿瘤杂志,2002,24(1):93-95.
[10]王浩,刘超,周少飞.改良FOLFOX7方案对Ⅲ期胃癌新辅助化疗的临床观察[J].疑难病杂志,2012,11(3):186-188.
[11]王晓云,赵玉亮.FOLFOX6方案治疗晚期胃癌临床观察[J].中国肿瘤临床与康复,2009,16(4):340-341.
[12]于洪波,冼海兵,邓燕明,等.FOLFOX6方案和TLF方案一线治疗晚期胃癌的疗效分析[J].南方医科大学学报,2010,30(10):2373-2376.
[13]郁兰芳,褚斌斌,方维佳,等.FOLFOX6方案治疗局部晚期或转移性胃癌的临床研究[J].现代实用医学,2006,18(6):393-394.
[14]Bekaii-Saab T,Wu C.Seeing the forest through the trees:A systematic review of the safety and efficacy of combination chemotherapies used in the treatment of metastatic colorectal cancer[J].Critical Reviews in Oncology/Hematology,2014,91(1):9-34.
[15]Tatsushima Y,Egashira N,Narishige Y,et al.Calcium channel blockers reduce oxaliplatin-induced acute neuropathy:a retrospective study of 69 male patients receiving modified FOLFOX6 therapy[J].Biomedicine&Pharmacotherapy,2013,67(1):39-42.
[16]Wainberg ZA,Messersmith WA,Peddi PF,et al.A phase 1B study of dulanermin in combination with modified FOLFOX6 plus bevacizumab in patients with metastatic colorectal cancer[J].Clinical Colorectal Cancer,2013,12(4):248-254.
[17]孙宝信,白璐,李青山,等.替吉奥联合奥沙利铂与FOLFOX6方案治疗晚期胃癌的疗效对比[J].中国老年学杂志,2013,33(14):3306-3308.
[18]冯丽丽,卢雨霖,赵楚英,等.FOLFOX6方案与FOLFIRI方案交替治疗晚期结肠癌的疗效观察[J].中国医药导刊,2014,(3):456,460.
[19]罗永忠,欧阳周.XELOX与FOLFOX6方案一线治疗晚期结直肠癌的近期疗效及不良反应比较[J].现代肿瘤医学,2010,18(1):125-127.
[20]包佳琪,赵兴胜,乌云高娃,等.替吉奥联合奥沙利铂方案与FOLFOX6方案辅助化疗在可切除Ⅱ/Ⅲ期胃癌围术期患者中的比较研究[J].癌症进展,2014,(1):70-74,92.
[21]邬麟,卢放根,殷先利,等.OFL方案时辰化疗与常规FOLFOX6方案一线治疗晚期结直肠癌效果比较[J].中国医药导报,2013,10(33):20-24.
Comparative study of the clinical efficacy in the treatment of advanced gastric cancer chemotherapy between improved FOLFOX6 neoadjuvant chemotherapy and postoperative chemotherpy
HE XinweiXUE Dixin▲The People's Hospital of Rui'an City,Zhejiang Province,Rui'an325200,China
Objective To observe the clinical effect and adverse reaction of modified FOLFOX6 neoadjuvant chemotherapy and postoperative chemotherapy in advanced gastric cancer.Methods 60 patients with histologically proven locally advanced or metastatic gastric cancerin March 2009 to June 2010 in the People's Hospital of Rui'an City were randomly divided into modified FOLFOX6 neoadjuvant chemotherapy group(preoperation group),chemotherapy group modified FOLFOX6 operation(postoperation group),the therapeutic effect was evaluated after 4 weeks,the clinical curative effect,disease progression and survival time,adverse reaction were observed.Results The total effectiveness and tumor control rate of preoperation group were 50.0%,76.7%,which were higher than those of postoperation group(43.3%, 70.0%),with statistical significance between the two groups(χ2=5.90,5.88,all P<0.05).The preoperation group forⅢ-Ⅳdegree of adverse reactions were 8 cases,and the postoperation group were 13 cases,there was significant difference(χ2=10.76,P<0.05).The tumor progression time was shorter in preoperation group than that in postoperation group[(10.4±2.4)months vs(16.9±1.7)months],and survival rate in 2 years was higher in preoperation group than that in postoperation group(86.67%vs 66.67%),there were significant differences between two groups(t=7.71,χ2=8.02, all P<0.05).Conclusion The curative effect and tumor progression,time survival time in modified FOLFOX6 neoadjuvant chemotherapy is better than the improved FOLFOX6 postoperative adjuvant,That is expected to provide efficient and safe new chemotherapy for the treatment of advanced gastric cancer,and can effectively improve survival time and quality of life and reduce the economic burden of the patients with advanced gastric cancer.
Modified FOLFOX6;Neoadjuvant chemotherapy;Postoperative chemotherapy;Advanced gastric cancer
R735.2
A
1673-7210(2014)11(b)-0017-04
2014-07-18本文编辑:苏畅)
浙江省瑞安市科技计划项目(编号YY2014024)。
▲通讯作者

