HPLC 法测定生脉饮(人参方)中五味子醇甲的含量
李 斌
(黑龙江省黑河市药品检验所,黑龙江黑河164300)
生脉饮(人参方)为《中国药典2010年版一部》收录的品种,由红参、五味子、麦冬组成,有益气复脉、养阴生津的功效,其质量标准只有鉴别、检查项,无含量测定项[1]。为确保生脉饮药品质量,我们对生脉饮(人参方)的质量标准控制进行摸索,采用高效液相色谱法(HPLC)测定制剂中五味子醇甲的含量,方法如下。
1 仪器与试药
日本LC-2010AHT高效液相色谱仪,甲醇为色谱纯,五味子醇甲对照品由中国药品生物制品检定所提供(批号:110857-200709),五批生脉饮(人参方)分别由北京同仁堂药厂提供批号为:20120322、20120324、20120326、20120921、20120923,生脉饮(人参方)五味子阴性由黑河三精药厂制备(除五味子不加,处方其他药按工艺生产)。
2 方法与结果
2.1 波长选择:取五味子醇甲对照品溶液,在紫外区200~400 nm进行扫描,确定最大吸收波长为250.1 nm。
2.2 色谱条件及专属性:色谱柱为AgilentC18(250 mm×4.6 nm);流动相为甲醇 - 水(58:42);流速 1.0 mL/min;柱温 30 ℃;检测波长 250 nm[2]。
2.3 五味子醇甲对照品溶液制备:精密称取五味子醇甲对照品12.18 mg,置50 mL量瓶中,加甲醇使溶解并稀释至刻度,精密吸取3.0 mL,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得作为对照品溶液。(制成每1 mL含0.073 mg的溶液),即得。见图1。
2.4 供试品溶液制备:精密量取装量差异项下的本品25 mL,用乙酸乙酯振摇提取5次,30 mL/次,合并乙酸乙酯液,蒸干,残渣加甲醇适量使溶解,转移至10 mL量瓶中,加甲醇至刻度,摇匀,用微孔滤膜(0.45 μm)滤过,作为供试品溶液。见图2。
2.5 五味子阴性溶液制备:以相同的处方比例,按生脉饮(人参方)制备工艺制备不含五味子药材的阴性样品,精密吸取此样品25 mL,按供试品溶液的制备方法制备不含五味子的阴性溶液。见图3。
2.6 线性关系考察:精密吸取五味子醇甲对照品溶液1、5、10、15、20、25 μL 在上述色谱条件下重复进样 2 次,测定峰面积值,以峰面积平均值和浓度进行回归处理,得回归方程为:Y=1948084X+5295.66,r=1.0000。线性范围在 0.073 ~1.825 μg 呈良好的线性关系。专属性:
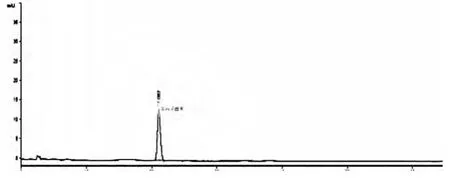
图1 五味子醇甲对照品溶液色谱图
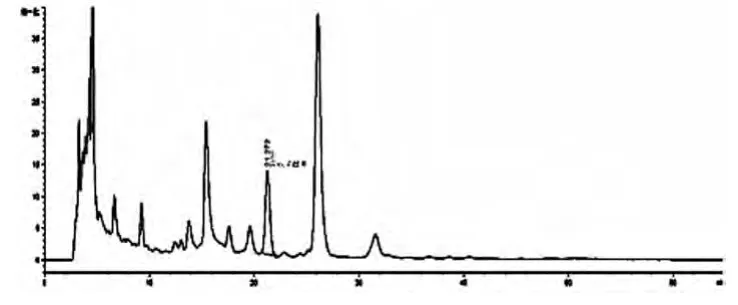
图2 供试品溶液色谱图
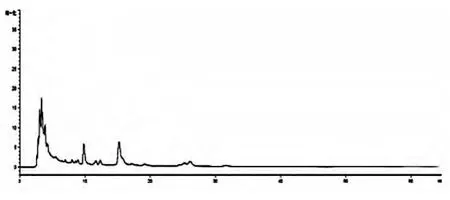
图3 五味子阴性溶液色
2.7 系统适应性:精密吸取五味子醇甲对照品溶液10 μL,重复进样5次,测定结果RSD为0.8%。
2.8 稳定性试验:取批号为20120322供试品溶液,每隔4 h进样10 μL,测定五味子醇甲峰面积值,共测定6次,测定结果 RSD 为0.9%
2.9 精密度(重复性)试验:取批号为20120322供试品溶液进行6次平行试验,测定五味子醇甲的含量,每次进样量10 μL,测定结果平均值每毫升含五味子醇甲为0.022 mg(RSD 为 0.9%)。
2.10 准确度试验:采用加样回收法,精密称取进行重复性试验的生脉饮(人参方)批号为20120322样品10 mL,精密量取3 mL五味子醇甲对照品溶液加入,按供试品制备法制备,按五味子醇甲含量测定方法进行测定,计算加样回收率,结果见表1。
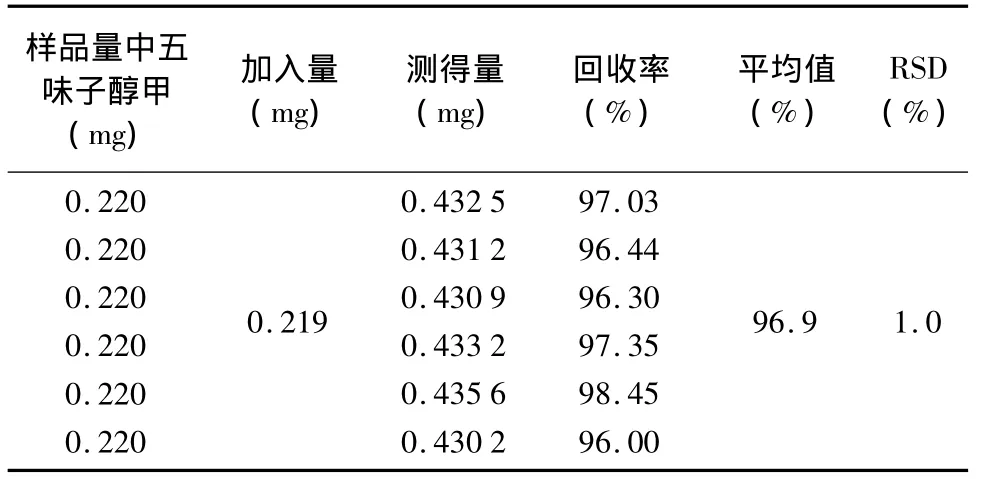
表1 回收率试验结果
2.11 样品含量测定:取各供试品溶液,按上述色谱分离条件,进样10 μL,测定五味子醇甲峰面积,计算含量,结果见表2。
3 小结与讨论
生脉饮(人参方)中五味子为处方中臣药,有收敛固色、益气生津、补肾宁心的功效,临床多用于抗肝损伤、抗氧化、增强代谢、中枢镇静等,主要成分为五味子中木脂素(五味子醇甲、五味子乙素等)[3],选择五味子醇甲进行对处方中五味子含量评价,是因为南五味子中五味子醇甲含量非常低,所以选择五味子醇甲作为含量评价,可以防止投料时南北五味子混用。对五味子中五味子醇甲进行了含量测定,可以控制生脉饮(人参方)的质量。
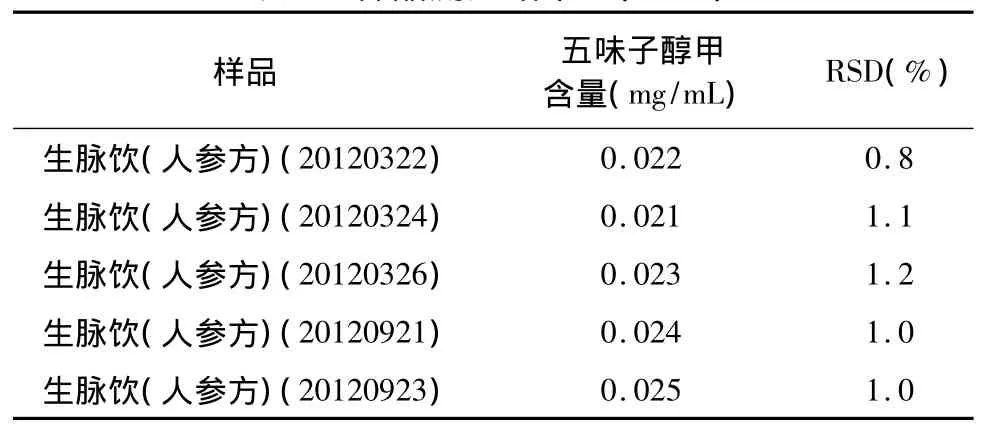
表2 样品测定结果 (n=2)
本实验采用高效液相色谱法测定有效成分五味子醇甲的含量,本法能达到有效分离各组分的目的,具有灵敏度高、操作简单、分离效果好、阴性无干扰等优点,试验证明五个批号生脉饮(人参方)中五味子醇甲含量均值为0.023 mg/mL,根据制剂含量方法学验证中范围规定为平均值的80%,推算生脉饮(人参方)中五味子醇甲含量应不低于0.018 mg/mL。
[1] 国家药典委员会.中华人民共和国药典一部[S].北京:中国科技出版社,2010:653.
[2] 国家药典委员会.中华人民共和国药典一部[S].北京:中国科技出版社,2010:760.
[3] 肖培根.新编中药志第二卷[M].北京:化学工业出版社,2002:123.

