α-干扰素联合恩替卡韦治疗慢性乙型肝炎患者疗效Meta分析
李媚,唐保东,杨琛,徐雅,谭妙莲,钟碧慧
·病毒性肝炎·
α-干扰素联合恩替卡韦治疗慢性乙型肝炎患者疗效Meta分析
李媚,唐保东,杨琛,徐雅,谭妙莲,钟碧慧
目的比较干扰素-α联合恩替卡韦及干扰素单药治疗慢性乙型肝炎的疗效。方法查阅在PubMed、EMbase和Cochrane Library以及中国科技期刊全文数据库、万方、中国生物医学文献数据库2013年2月10日之前发表的文献,纳入所有符合条件的随机对照试验,应用Review Manager.5.1.0统计学软件进行分析。结果纳入合格文献4篇,包括259例慢性乙型肝炎患者,其中115例接受干扰素-α联合恩替卡韦治疗,144例为干扰素-α单药治疗。纳入文献漏斗图分析表明,研究以真值为中心呈对称性分布;在24 w时,联合治疗患者HBV DNA阴转率为78.3%(90/115),显著高于单药治疗组[42.4%(61/144),RR=1.89,95%CI 1.52~2.36,P<0.00001];在48 w时,联合治疗组HBV DNA阴转率为92.6%(88/95),显著高于单药治疗组[63.7%(79/124),RR=1.46,95%CI 1.26~1.70,P<0.00001];在24 w时,联合治疗组HBeAg血清转换率为37.4%(43/115),显著高于单药治疗组[27.1%(39/144),RR=1.46,95%CI 1.03~2.08,P=0.03];在48 w时,联合冶疗组HBeAg血清转换率为64.2%(61/95),显著高于INF-α单药治疗组[39.5%(49/124),RR=1.55,95%CI 1.19~2.01,P=0.001];在24 w时,联合冶疗组ALT复常率为75.7%(87/115),显著高于单药治疗组[45.8%(66/144),RR=1.71,95%CI 1.39~2.11,P<0.00001)];在48 w时,联合冶疗组ALT复常率为93.7%(89/95),显著高于单药治疗组[66.1%(82/124),RR=1.41,95%CI 1.23~1.61,P<0.00001]。结论干扰素-α联合恩替卡韦治疗慢性乙型肝炎的疗效优于干扰素-α单药治疗。
慢性乙型肝炎;干扰素-α;恩替卡韦;治疗;Meta分析
慢性乙型肝炎(Chronic hepatitis B,CHB)是一个严重的全球性公共卫生问题。随着医学的发展,慢性乙型肝炎的治疗取得了巨大的进展。到目前为止,抗乙型肝炎病毒的药物在我国上市的有6种,分别是普通干扰素-α(interferon,INF-α)、聚乙二醇干扰素(Peginterferon,Peg-IFN)、拉米夫定、阿德福韦、替比夫定、恩替卡韦,但是无论是前两种干扰素还是后4种核苷/核苷酸类似物(Nucleotide analogue,NUC)均未能取得满意的疗效。NUC通过干扰HBV DNA多聚酶的活性,直接抑制病毒的复制,但长期用药易发生病毒变异,产生耐药,造成病毒学反弹[1];干扰素则是通过免疫调节作用提高细胞毒性T淋巴细胞活性,从而清除病毒感染的肝细胞,但任何一种药物的单药治疗往往应答率较低[2]。我们查阅了INF-α联合恩替卡韦(entecavir,ETV)治疗CHB的临床试验,发现各家报道的疗效和安全性评价不一。为此,本研究检索了有关IFN-α联合ETV治疗CHB患者的随机对照试验[3~6],系统评价疗效,以期为临床用药提供参考。
1 资料与方法
1.1 检索策略应用计算机检索PubMed、EMbase和Cochrane Library,以及中国科技期刊全文数据库、万方、中国生物医学文献数据库。检索不限语种,年限均从建库至2014年2月10日。采用主题词与自由词相结合的方式,其中英文检索词为“hepatitisB、chronic、CHB、interferon-α(alpha)、entecavir、random、blind、control、meta analysis”,中文检索词为“慢性乙型肝炎、慢乙肝、干扰素-α、恩替卡韦、随机、对照、双盲”。另外,应用Google、百度、ISI web of science等搜索引擎在互联网上查找相关的文献。追查已纳入文献的参考文献,与本领域的专家、通讯作者等联系,以获取以上检索未发现的相关信息。对纳入的文献数据描述不够详尽者则联系作者,以获取所需要的数据。
1.2 纳入和排除标准纳入标准:①研究设计为随机对照试验(RCT);②研究对象为HBeAg阳性或HBeAg阴性的慢性乙型肝炎患者,CHB的诊断符合2005年或2010年制定的慢性乙型肝炎防治指南[7,8];③干预措施为试验组应用干扰素-α联合恩替卡韦治疗,对照组为单用干扰素-α(Peg-IFN或普通干扰素),治疗时间至少是6个月;④试验组和对照组在年龄、性别、生化、乙型肝炎病毒定量等方面具
有均衡的可比性;⑤国内外公开发表的论文。排除标准:①合并感染甲、丙、丁、戊型肝炎病毒、EB病毒、巨细胞病毒、人类免疫缺陷病毒(HIV)等感染;②合并有药物性肝损害、自身免疫性肝病、酒精性肝病、遗传代谢性肝病、肝移植、恶性肿瘤等;③有干扰素治疗禁忌证(如总胆红素>42 μmol/L,治疗前中性粒细胞计数<1.0×109/L,血小板计数<50× 109/L,严重的心、肝、肺、肾功能障碍者,未控制的甲状腺功能亢进症,既往有精神性疾病或严重抑郁症史的患者及妊娠期女性等;④6个月内接受过抗病毒治疗。
1.3 纳入文献的质量评价及资料提取由两名作者独立筛选文献、提取资料。对有不同意见者,通过讨论达成一致或与第三名研究者协商解决;对原文叙述不清,与原文作者联系后取得详细的数据;对同一研究组人群发表的多篇文献,只选其中质量最好的或样本量最大的。采用Jadad[9]评分系统进行文献质量评价。资料提取包括:一般信息如文题、来源、作者、发表时间等;研究特征如研究对象的年龄范围、性别比例、例数、各组患者的基线情况、干预措施;结局指标如HBV DNA阴转率及HBV DNA的检测下限、HBeAg阴转率或血清学转换率、HBsAg阴转率或血清转换率、ALT复常率、安全性等。
1.4 统计分析采用Review Manager 5.1.0 for Windows统计学软件,计数资料用RR及其95%可信限区间(CI)表示,采用x2检验和I2检验来检测各个研究间的异质性。对研究间存在异质性(P<0.10,I2>50%)者,采用随机效应模型,反之则采用固定效应模型分析。总体效应检测使用Z评分,采用“倒漏斗图”分析潜在的发表偏倚,P<0.05为有统计学差异。
2 结果
2.1 纳入研究的一般情况初检相关文献821篇,根据论文题目及摘要,排除了810篇重复性或非临床试验或研究目的与本系统评价不符的文献,在剩下的11篇文献中,有5篇是回顾性研究,2篇无对照组,最后纳入4篇文献(3篇中文,1篇英文),共有259例慢性乙型肝炎患者,其中115例接受干扰素-α联合恩替卡韦治疗,144例为干扰素-α单药治疗。纳入文献基本特征以及Jadad评分见表1。
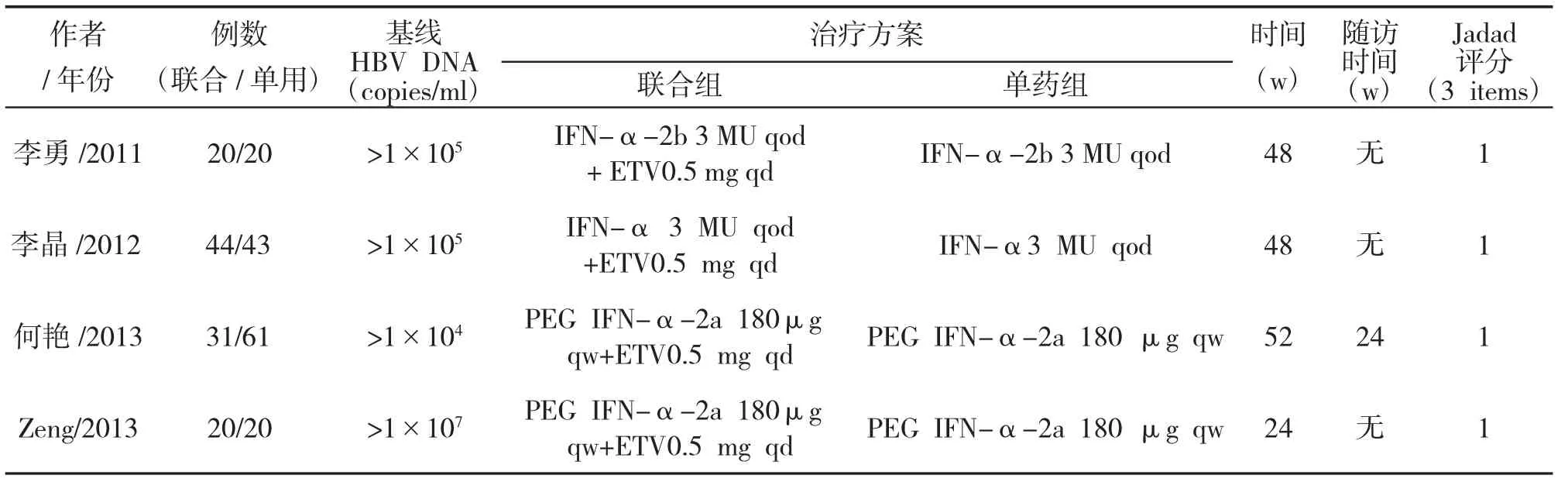
表1 纳入文献的基本特征
2.2 纳入研究方法 的质量学评价4篇纳入文献均为单中心、非双盲的随机对照试验,均未注明随机分配方法。纳入的文献均有纳入和排除标准,其中3篇是参照2005年制定的慢性乙型肝炎防治指南,1篇是参照2010年中国慢性乙型肝炎防治指南。4篇文章对疗效的判断均有明确的定义。纳入的4个研究均声明两组基线资料具有可比性,但只有1篇文章详细报道了观察组和对照组的基线情况,其余3篇仅注明两组患者在性别、年龄、病程、病情程度方面的差异无统计学意义。纳入的文献均没有进行乙型肝炎病毒基因型检测,只有1篇文章描述了治疗前后肝组织学的改变[5],但未行统计学分析。只有1篇文章进行HBsAg和HBeAg定量检测及比较[6]。有2篇文章观察了HBeAg阴转率[4,6]。4篇均观察了HBeAg血清转换率。纳入文献均没有注明失访的病例数。我们对纳入文献绘制漏斗图分析,结果表明研究以真值为中心呈对称性分布,提示纳入文献的发表偏倚较小。
2.3 HBV DNA阴转率INF-α联合ETV组与INF-α单药治疗组HBV DNA阴转率比较见图1。

图1 IFN-α联合ETV与IFN-α治疗CHB患者HBV DNA转阴率比较
在治疗24 w,研究间无统计学异质性(P=0.33,I2=13%),采用固定效应模型分析。合并分析结果显示,INF-α+ETV治疗患者HBV DNA阴转率高于INF-α单药治疗组,差异有统计学意义[78.3%(90/115)对42.4%(61/144),RR=1.89,95%CI 1.52~2.36,P<0.00001];3个研究[3~5]有治疗48 w的结果,研究间无统计学异质性(P=0.95,I2=0%),采用固定效应模型分析,合并分析结果显示,INF-α+ETV组HBV DNA阴转率高于INF-α单药治疗组,差异有统计学意义[92.6%(88/95)对63.7%(79/124),RR=1.46,95%CI 1.26~1.70,P<0.00001]。
2.4 HBeAg血清转换率INF-α联合ETV组与INF-α单药治疗组HBeAg血清转换率比较见图2。在治疗24 w,研究间无统计学异质性(P=0.78,I2=0%),采用固定效应模型分析,合并分析结果显示,INF-α+ETV组HBeAg血清转换率高于INF-α单药治疗组,差异有统计学意义[37.4%(43/115)对27.1%(39/144),RR=1.46,95%CI 1.03~2.08,P=0.03]。3个研究[3~5]有治疗48 w的结果,研究间无统计学异质性(P=0.58,I2=0%),采用固定效应模型分析,合并分析结果显示,同样是INF-α+ETV组HBeAg血清转换率高于INF-α单药治疗组,差异有统计学意义[64.2%(61/95)对39.5%(49/124),RR=1.55,95%CI 1.19~2.01,P=0.001]。
2.5 ALT复常率INF-α联合ETV组与INF-α单药治疗组ALT复常率比较见图3。在治疗24 w,研究间无统计学异质性(P=0.78,I2=0%),采用固定效应模型分析,合并分析结果显示,INF-α+ETV组ALT复常率高于INF-α单药治疗组,差异有统计学意义[75.7%(87/115)对45.8%(66/144),RR= 1.71,95%CI 1.39~2.11,P<0.00001)]。3个研究[3~5]有治疗48 w的结果,研究间无统计学异质性(P= 0.81,I2=0%),采用固定效应模型分析,合并分析结果显示,同样是INF-α+ETV组ALT复常率高于INF-α单药治疗组,差异有统计学意义[93.7%(89/ 95)对66.1%(82/124),RR=1.41,95%CI 1.23~1.61,P<0.00001]。
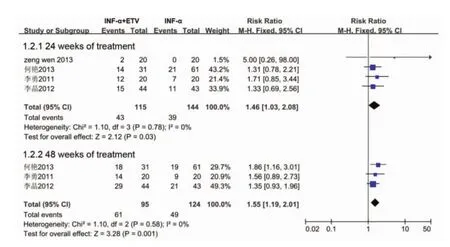
图2 IFN-α联合ETV与IFN-α治疗CHB患者HBeAg血清转换率比较
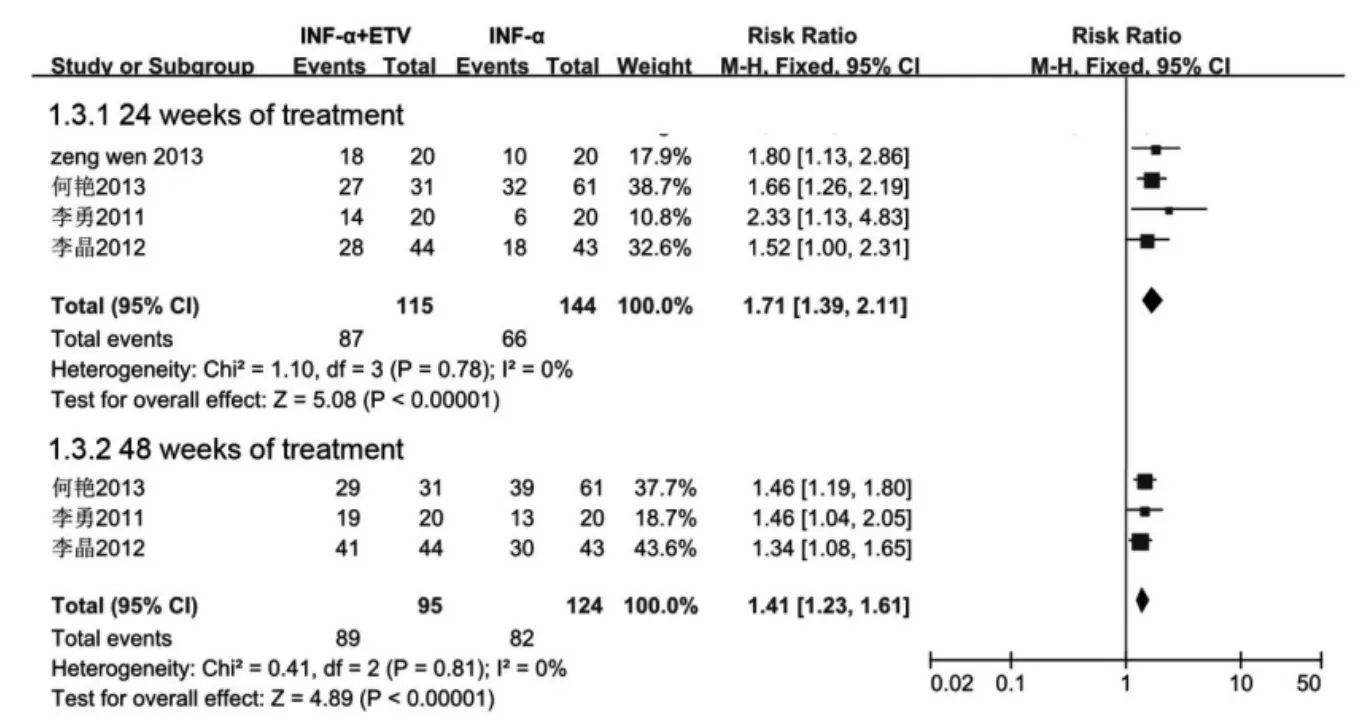
图3 IFN-α联合ETV与IFN-α治疗CHB患者ALT复常率比较
3 讨论
有报导发现高HBV DNA载量会损伤T细胞对乙型肝炎病毒相关抗原反应的能力,而NUC能降低HBV DNA载量,恢复T细胞的免疫功能,使干扰素发挥最佳的抗病毒效果[10]。因此,理论上NUC与干扰素这两种抗病毒机制不同的药物合用能达到更好的疗效。既往,人们对拉米夫定与干扰素合用的疗效进行了大量的临床试验,发现治疗结束时联合组疗效好,但停药观察6个月甚至更长的时间后两者合用与单用干扰素的疗效无显著性差异[11]。尽管如此,联合用药可降低拉米夫定的耐药率[12]。替比夫定与干扰素合用被证实可引起多种神经病变[13]。最近,大量的关于阿德福韦与干扰素合用的文献表明,无论是在治疗结束以及治疗后随访,合用组比单用干扰素组有更高的疗效[14]。恩替卡韦是一个强效低耐药的核苷类似物,是目前欧洲肝病指南推荐的一线用药[11]。因此,人们期待恩替卡韦与干扰素联用能取得更好的疗效。日本的Satoru Hagiwara对17例基因C型的CHB患者联合使用PEG-IFN-α-2b和EV、ETV48 w,治疗结束时发现肝内HBV cccDNA水平平均下降1.4 log copies/mg,随访24 w时HBeAg血清转换率达73%[15],但这个研究没有设置对照组。最近,有若干联合使用INF-α和ETV的随机对照研究,其疗效及安全性等评价不一。本研究采用荟萃分析,对收集到的2014年2月10日以前的应用干扰素-α联合ETV治疗CHB的临床随机对照试验进行meta分析,为临床实践和决策提供了比单个研究更为可靠的证据。本研究纳入了4个随机对照试验,进行meta分析结果显示在治疗24 w和48 w,联合用药组比单用干扰素组有更高的HBV DNA阴转率、HBeAg血清转换率及ALT复常率。
本研究的不足之处在于纳入文献数量相对较少,部分文献样本量较少,缺乏多中心、大规模的随机对照试验。纳入的文献均未具体描述随机化方法,未报道是否使用盲法,未检索到除中文、英语外其他语种的随机对照研究。因此,可能出现选择性偏倚、测量偏倚以及分布偏倚。在所纳入的文献中,只有1个研究[5]随访了24 w,表明随访24 w联合治疗组HBV DNA阴转率明显高于单药治疗组。只有1个研究[5]在治疗前后行肝穿刺检查,但因样本量少而未行统计分析。有两个研究观察了治疗前后HBsAg变化,其中一篇[5]结果提示治疗52 w联合组与单药组HBsAg阴转率分别为25.8%和16.4%,有统计学差异。另一篇[6]示治疗24 w联合组与单药组HBsAg定量无统计学差异。只有两个研究报导了不良反应。一篇[6]简单描述了治疗期间两组均未出现严重的不良反应,另一篇[4]认为联合用药组不良反应少于单药组,差异有统计学意义。显然,HBeAg的状态(阳性或阴性)、HBV的基因型及干扰素的种类(普通/聚乙二醇化)对疗效均有影响。所纳入的文献均未检测HBV基因型。有一篇入选的都是HBeAg阳性患者[6],另一篇描述了试验组和对照组HBeAg阳性例数,且两组比较无明显差异[5],其余两个研究[3,4]并未描述患者的HBeAg状态。因纳入的研究少,亦无法按照干扰素种类进行亚组分析。
总而言之,本研究发现干扰素-α联合ETV治疗CHB对改善病毒学应答及生化学应答均优于单用干扰素-α,可作为慢性乙型肝炎的治疗选择之一。今后,需要更严格设计的RCT、更长期的随访以及多中心的研究来进一步验证干扰素-α联合ETV治疗CHB的疗效。
[1]陈成伟,陈从新,陈士俊等.核苷和核苷酸类药物治疗慢性乙型肝炎的耐药及其管理.实用肝脏病杂志,2013,16(1):1-8.
[2]Enomoto M,Tamori A,Nishiguchi S,et al.Combination therapy with a nucleos(t)ide analogue and interferon for chronic hepatitis B:simultaneous or sequential.J Gastroenterol,2013,48:999-1005.
[3]李勇.干扰素α-2b与恩替卡韦联合治疗慢性乙型肝炎患者疗效观察.中国实用医药,2011,6(35):136-138.
[4]李晶.α-干扰素联合恩替卡韦治疗慢性乙型肝炎早期疗效.肝脏,2012,17(10):714-716.
[5]何艳,唐晓鹏,郑萱鹤,等.干扰素联合核苷(酸)类似物治疗慢性乙型肝炎的疗效观察.临床肝胆病杂志,2013,29(2): 114-119.
[6]Zeng W,Yuan J,Liu YX,et al.Efficacy of peg-interferon alpha-2a combinated with entecavir on HBeAg positive chronic hepatitis B patients with high serum hepatitis B viral loads. Zhonghua Shi Yan He Lin Chuang Bing Du Xue Za Zhi,2013,27(2):115-8.
[7]中华医学会肝病学分会,感染病学分会.慢性乙型肝炎防治指南.实用肝脏病杂志,2006,9(1):8-18.
[8]中华医学会感染病学分会,中华医学会肝病学分会.慢性乙型肝炎防治指南(2010年版).实用肝脏病杂志,2011,13(2):81-89.
[9]Jadad AR,Moore RA,Carroll D,et al.Assessing the quality of reports of randomized clinical trials:is blinding necessary.Control Clin Trials,1996,17:1-12.
[10]Dandri M,Locarnini S.New insight in the pathobiology of hepatitis B virus infection.Gut,2012,61(1):6-17.
[11] European Association For The Study Of The Liver. EASL clinical practice guidelines: Management of chronic hepatitis B virus infection. J Hepatol,2012,57(1):167-85.
[12] Shi Y,Wu YH,Shu ZY,et al. Interferon and lamivudine combination therapy versus lamivudine monotherapy for hepatitis Be antigen-negative hepatitis B treatment:a meta-analysis of randomized controlled trials. Hepatobiliary Pancreat Dis Int, 2010,9:462-72.
[13]Marcellin P,Avila C,Wursthorn K,et al.Telbivudine(LDT)plus peg-interferon(PEGIFN)in HBeAg-positive chronic hepatitis B-very potent antiviral efficacy but risk of peripheral neuropathy(PN).J Hepatol,2010,52:6-7.
[14] Huang R,Hao Y,Zhang J,et al. Interferon-αl plus adefovircombination therapy versus interferon-αl monotherapy for chronic hepatitis B treatment:A meta-analysis. Hepatol Res,2013,43(10):1040-1051
[15]Hagiwara S,Kudo M,Osaki Y,et al.Impact of peginterferon alpha-2b and entecavir hydrate combination therapy on persistent viral suppression in patients with chronic hepatitis B.J Med Virol,2013,85(6):987-95.
(收稿:2014-04-08)
(校对:陈从新)
Efficacy of Interferon- α and entecavir in the treatment of patients with chronic hepatitis B:ameta- analysis
Li Mei,Tang Baodong,Yang Chen,et al. Department of Gastroenterology,First Affiliated Hospital,Sun Yat-Sen University,Guangzhou 510700,Guangdong Province,China
ObjectiveTo investigate the efficacy of combination therapy of interferon-α(IFN-α)plus entecavir(ETV)or IFN-α monotherapy in the treatment of patients with chronic hepatitis B(CHB).Methods Articles published before February 10,2013 in database of PubMed,EMbase,Cochrane Library,China Biology Medicine disc,CNKI and WANFANG were searched.All eligible randomized controlled trials were included. Review Manager.5.1.0 for Windows was used for Meta-analysis.ResultsFour articles that met the inclusion criteriawereobtained,includingatotalof259patientswithchronichepatitisB,ofwhich115received combination therapy and 144 received interferon-α alone.The funnel plot analysis showed that the research was distributed symmetrically with the true value as the center.HBV DNA negative rate in patients in combination therapy was higher than patients receiving monotherapy at 24 w and 48 w,and the differences were statistically significant[78.3%(90/115)vs.42.4%(61/144),RR=1.89,95%CI 1.52~2.36,P<0.00001,and 92.6%(88/95)vs. 63.7%(79/124),RR=1.46,95%CI 1.26~1.70,P<0.00001];serum HBeAg conversion rate in patients in combination therapy group was significantly higher than patients receiving monotherapy at 24 w and 48 w[37.4%(43/115)vs. 27.1%(39/144),RR=1.46,95%CI 1.03~2.08,P=0.03,and 64.2%(61/95)vs.39.5%(49/124),RR=1.55,95%CI 1.19~2.01,P=0.001];ALT normalization rate in patients receiving combination therapy was also significantly higher than in patients with monotherapy at 24 w and 48 w[75.7%(87/115)vs.45.8%(66/144),RR=1.71,95%CI 1.39~2.11,P<0.00001,and 93.7%(89/95)vs.66.1%(82/124),RR=1.41,95%CI 1.23~1.61,P<0.00001].Conclusions Efficacy of interferon-α plus entecavir in the treatment of patients with CHB is superior to IFN-α monotherapy.
Chronic hepatitis B;Interferon-α;Entecavir;Combination therapy;Meta-analysis
510700广州市中山大学附属第一医院东院消化内科(李媚,唐保东,徐雅,钟碧慧);体检中心(杨琛);预防保健科(谭妙莲)
李媚,女,38岁,医学博士,主治医师。主要从事消化及肝病的诊断与治疗学研究。E-mail:digoxin@126.com
钟碧慧,E-mail:digoxin@126.com
10.3969/j.issn.1672-5069.2014.06.007

