大黄酸金属配合物的抑菌活性研究
向晖,潘晓丽,谭玉柱,吴兵,陆小华,董小萍
·药理毒理·
大黄酸金属配合物的抑菌活性研究
向晖,潘晓丽,谭玉柱,吴兵,陆小华,董小萍
目的:合成大黄酸的三种金属配合物并对其结构进行表征,对比研究配体和配合物对三种细菌的体外抑菌活性大小。方法:在无水乙醇中合成了大黄酸的三种金属配合物,采用紫外光谱法,红外光谱法,核磁共振氢谱法对产物结构进行表征,确定了配合物的组成及结构。采用二倍稀释法测定了配合物的最小抑菌浓度(MIC),采用滤纸片法测定了配体及配合物对金黄色葡萄球菌、肺炎链球菌、大肠杆菌的抑菌活性大小。结果:合成的配合物经结构表征后,初步确定了其可能结构式为2分子大黄酸和1分子金属离子配位,抑菌活性测试结果表明,配合物的抑菌活性强于配体,其中大黄酸锰对于金黄色葡萄球菌以及大肠杆菌抑制作用都最强,抑菌圈大小分别达到了23.3、20.5 mm;而大黄酸钴对肺炎链球菌抑菌活性最强,抑菌圈达22.5 mm。二倍稀释法得出了配合物和配体的MIC值(最小抑菌浓度),根据该值大小可知,配合物抑菌活性总体上强于配体,但也有少部分与配体相当。结论:大黄酸和金属离子形成配合物后,抑菌活性增强。
大黄酸;滤纸片法;二倍稀释法;金属配合物;抑菌
大黄酸(Rhein,见图1),来源于蓼科植物大黄、何首乌、虎杖等中药中,属于单蒽核类1,8—二羟基蒽醌衍生物[1]。来源丰富,易于提纯。大黄酸药理作用广泛,具有抗炎、抗肿瘤、抗菌[2]以及保肝[3]等活性,具有临床药用价值。大黄酸对于金黄色葡萄球菌、链球菌、枯草杆菌、伤寒杆菌、大肠杆菌等均有较强的抑制作用。其抑制细菌繁殖的机制可能是:抑制细菌糖代谢,以及糖代谢中间产物的氧化,脱氢以及抑制蛋白质与核酸的合成[4]。中药配位学说认为:可能是有机成分与微量元素组成的配位化物 ,天然药物以其中的有机物分子与微量元素间形成的配合物在动植物及人体的生命活动中发挥作用[5]。而许多实验证实,中药的有效成分在形成配合物后,生物活性增强。例如木犀草素与锌离子配位后,抗DPPH自由基活性增强[6],白花丹素与金属离子配位后,抗癌活性增加[7]。大黄酸是一种含有α-酚羟基的蒽醌化合物,其中1,8 位羟基和9位羰基适于各种金属离子配位。本文选择锰[8]、钴、锌[9]等人体所必须的微量元素作为中心原子,合成大黄酸金属配合物;采用紫外光谱法、红外光谱法、核磁共振氢谱法等对配合物进行结构表征;选用金黄色葡萄球菌、肺炎链球菌、大肠杆菌等对配合物和配体进行抑菌活性测试,对比了配体和配合物的抑菌活性,筛选出抑菌活性最高的配合物。

图1 大黄酸结构
1 实验部分
1.1 实验试剂与仪器
菌种由成都中医药大学基础医学院提供。
BRUKER AM-400型超导核磁共振仪; BRUKER Tensor-27型傅立叶变换中红外光谱仪;UV-1700型紫外分光光度计;PHB-8型pH计;二氧化碳培养箱(MCO-15AC,三洋电机株式会社);双人单面垂直送风净化工作台(SW-SJ-2D,中国苏州智净净化设备有限公司);优普超纯水制造系统(UPH-Ⅱ-10T,成都超纯科技有限公司);BP211D型电子分析天平(十万分之一,德国Sartorius公司)。平板计数琼脂PCA(生产批号:20120809,青岛高科园海生物技术有限公司);酵母粉(LP0021,LOT:1185342,生产厂家:o x o i d);蛋白胨(L P O O 4 2,LOT:1094936,生产厂家:oxoid)。
1.2 配合物的合成
在装有搅拌器和冷凝管的150 mL三口瓶中,加入1 mmol大黄酸的60 mL无水乙醇,搅拌,至大黄酸溶解后,加入0.5 mmol C4H6O4Zn.2H2O(醋酸锌)的10 mL 无水乙醇醇溶液,逐滴加入氨水的乙醇溶液(1∶1,V∶V),调节配体溶液的pH 值为8~10,继续以反应温度为40℃搅拌反应12 h, 将溶液静置后真空抽滤, 依次用无水乙醇及乙醚将沉淀洗涤数次,真空干燥72 h,得粉末状固体。以醋酸锰Mn(CH3COO)2.4H2O,醋酸钴CH3COOCo.4H2O,替代醋酸锌合成了大黄酸-钴,大黄酸-锰配合物。
1.3 抑菌实验
1.3.1 菌液制备 分别取试验菌种(大肠杆菌,金黄色葡萄球菌,肺炎链球菌)适量,以液体培养基15 mL(含蛋白胨10 g.L-1、酵母粉5 g.L-1、氯化钠10 g.L-1,以0.1 mol.L-1氢氧化钠调节pH为7-7.4)在培养皿中以37°C,5.0% CO2条件下培养24 h,得细菌混悬液,以无菌生理盐水调整菌液浓度为10-7CFU.mL-1,备用。
1.3.2 药液制备 称取一定量固体药物,1 mg.mL-1溶于灭菌的二甲基亚砜溶剂中,以紫外照射灭菌8 h,并且以0.22 μm微孔滤膜过滤。临用前将灭菌后的,直径5 mm圆形滤纸片泡入药液内2 h,备用。
1.3.3 平皿实验法 趁热吸取灭菌后的平板计数琼脂PCA液体在培养皿内,每碟15 mL,待其凝固后,吸取50 μL制备好的菌液均匀涂布于琼脂表面,将含菌琼脂培养基放入孵箱培养0.5 h后取出,再将含药纸片平整地贴在含菌培养基上,在37°C,5%CO2条件下培养24 h,测量抑菌圈直径。平行测定3次,取平均值[10]。
1.3.4 二倍稀释法 称取2 mg固体药物,溶解于0.02 mol.L-1的氢氧化钠溶液中,以稀盐酸调整pH值为7~7.4,最后以ph7~7.4的超纯水定容至10 mL。取灭菌小试管数支,在第一支试管中加入2 mL药液和2 mL培养基,混匀后从第一支试管中取出2 mL混合液加入到第二支试管中,同时第二支试管中加入培养基2 mL,以此类推,每个化合物稀释5个浓度,第6支试管中不加菌液作为空白对照组。各试管中分别加入菌液50 μL,在37°C,5%二氧化碳条件下孵化24 h观察结果。以不生长细菌(即试管内液体不浑浊)的最小浓度为MIC。平行测定3次,以2次以上结果相同为准。
2 实验结果
2.1 配合物基本性质
配合物与配体相比较,外观颜色发生较大变化(大黄酸-钴和大黄酸锰为紫红色,大黄酸-锌为桔黄色),三种金属配合物均难溶于乙醚,氯仿,丙酮等有机试剂,但易溶解在dmso,dmf等碱性试剂中。配合物熔点较高,在400°C条件下仍然不分解。在900℃马弗炉中灼烧数小时后可以得到金属氧化物粉末。
2.2 配合物的紫外光谱
将大黄酸和大黄酸金属配合物配制成5×10-5mol.L-1的无水甲醇溶液,在200~600 nm范围内进行UV全波长扫描得配体和配合物的紫外吸收光谱数据(见表1)。大黄酸在229 nm的吸收带属于笨样结构,257 nm则属于醌结构,431 nm处吸收则属于C=O键。而形成配合物后金属离子和配体之间的电子发生转移,π共轭离域体系增大,电子跃迁需要的能量下降,故配合物吸收峰发生红移,但基本保持配体峰形。此外配合物均在517nm左右均出现一个新峰,可能原因是由于蒽醌结构中C=O参与配位,该键上电子云密度变化造成。
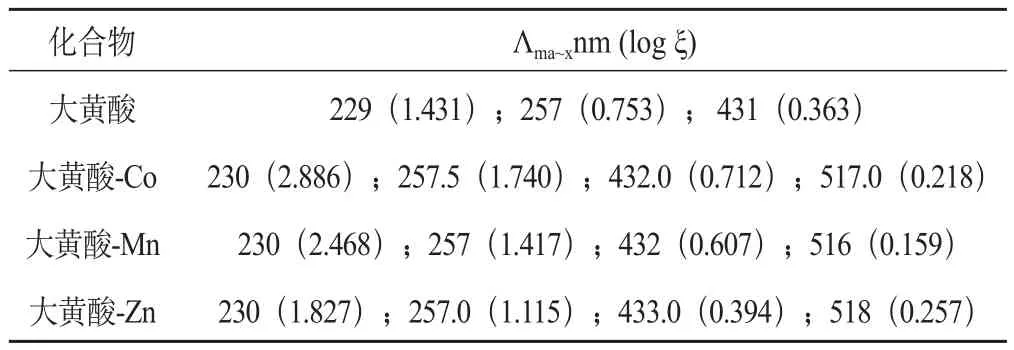
表1 大黄酸及大黄酸金属配合物的UV(nm)数据
2.3 配合物红外光谱
配体以及配合物的红外光谱数据见表2,与大黄酸在3060 cm-1有较宽的羟基吸收带,而配合物中此吸收减弱,说明α-羟基参与了配位,配合物在3250~3430 cm-1处出现宽的吸收峰,表明配合物中可能有结晶水存在。配体大黄酸1629 cm-1的吸收来自于可以和α-羟基形成氢键的羰基,即9位羰基;1692 cm-1属于10位羰基[11]。相比配体,配合物9位C=O吸收峰均发生红移,原因是金属离子通过9位羰基与α-羟基配位,羰基的双键的伸缩力常数减小,电子云密度降低,从而使峰带移向低波数区域。而参与配位的α-OH的碳氧键上,由于配位作用使金属离子,羰基氧,羟基氧,蒽醌环上碳原子成环,引起共轭效应,C-O键上电子云密度增加,故C-O的吸收峰紫移,进一步说明羰基和羟基参与配位。同时配合物均在510~520 cm-1之间产生了M-O,即金属离子的伸缩振动吸收峰。
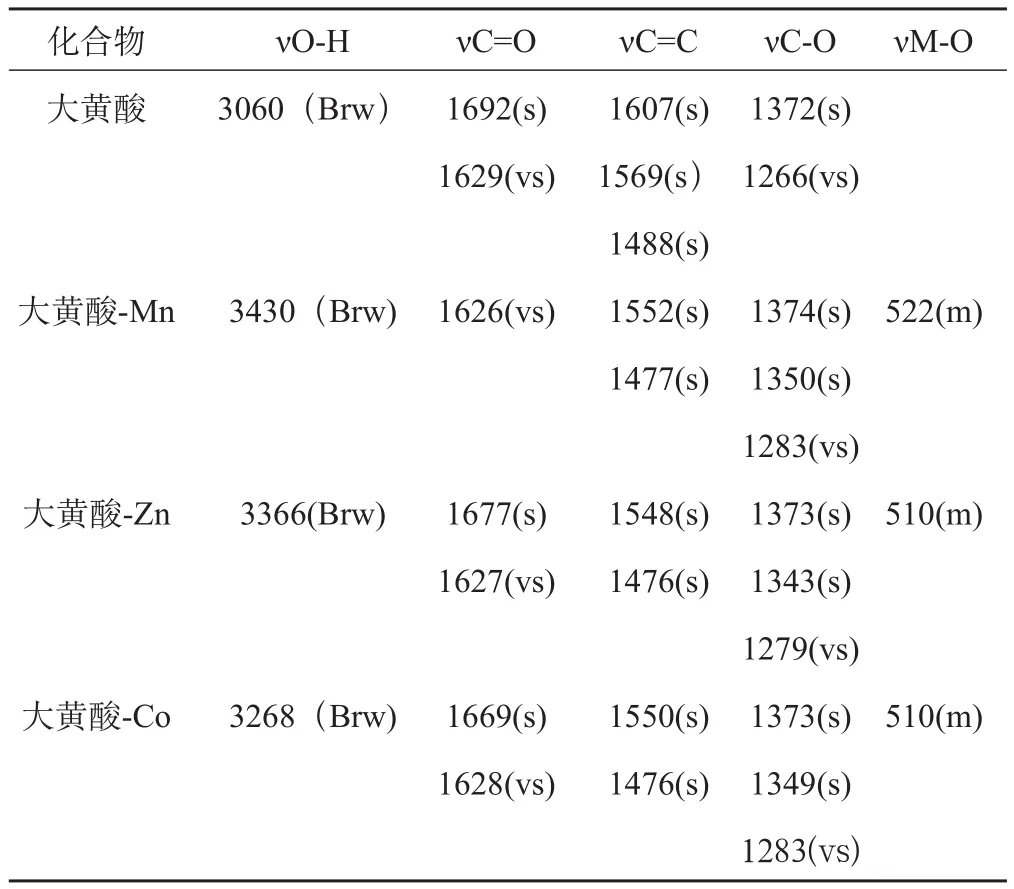
表2 大黄酸及大黄酸金属配合物的IR(cm-1)数据
2.4 配合物的核磁共振氢谱
在氘代二甲基亚砜溶剂中测定了配体和配合物的核磁共振氢谱,配体和配合物峰形差别较大,结果见表3。大黄酸的羧基峰是δ13.73的一个钝峰,δ11.89则属于大黄酸的两个羟基。蒽环上的氢则位于δ7~9之间。大黄酸钴配合物在δ10.15~13.78(m,4H)出现一弱多重峰,此峰为羟基和羧基峰重合后形成。在δ7.29~8.07范围内出现单峰、重峰及多重峰,为蒽环上的氢;大黄酸锰配合物在δ12.18(m,4H)出现一弱多重峰,在7.00~8.50(m,10H)出现宽三重峰;大黄酸锌在δ12.56(m,2H)出现弱多重峰,在δ6.3~8.8(m,10H)出现宽多重峰。3位羧基具有强的吸电子诱导效应,因此1位羟基更容易解离,通过9位羰基与金属离子形成配合物。
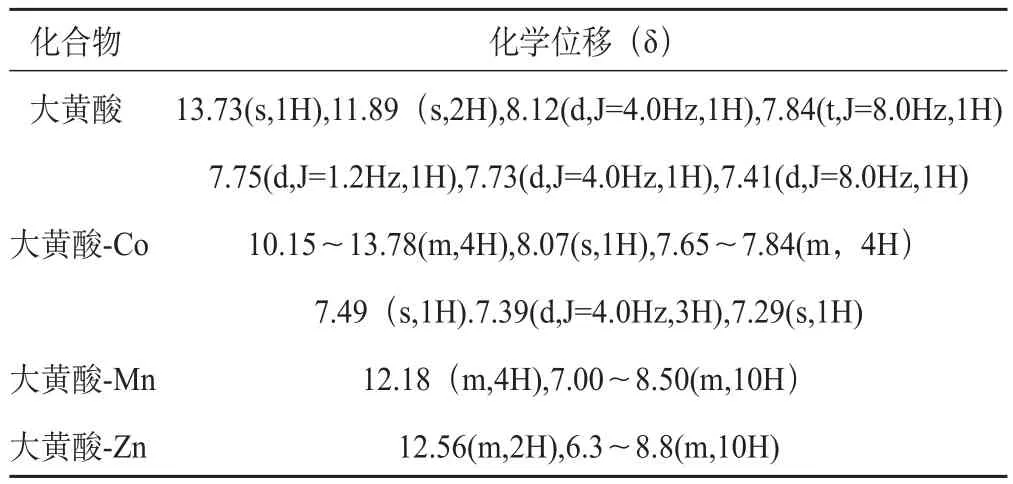
表3 大黄酸及大黄酸配合物的1H NMR的数据(DMSO)
综合上述分析结果,大黄酸金属配合物的可能组成为:两分子大黄酸与一分子金属离子通过基与1位羟基形成配合(见图2)。
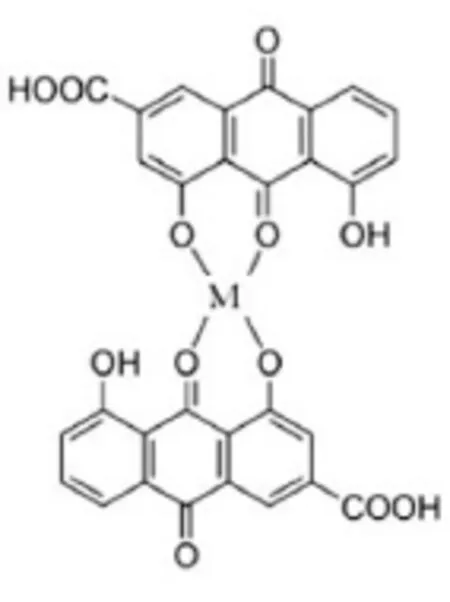
图2 大黄酸金属配合物可能结构
2.5 滤纸片法实验结果
大黄酸及大黄酸的配合物的dmso溶液均可以产生抑菌圈,结果见表4,大多数配合物的抑菌活性大于配体。抑菌圈大于20 mm为强抑菌作用,10-20 mm为中等抑菌强度,抑菌圈小于10 mm为弱抑菌作用[12]。由抑菌圈大小来看,大黄酸锰对于金黄色葡萄球菌(SA)以及大肠杆菌(E.coli)抑制作用最强,大黄酸钴对于肺炎链球菌(s.pneumoniae)抑菌活性最强。空白的dmso对于三种细菌均未产生明显的抑菌圈。
表4 抑菌实验结果(抑菌圈直径/mm,,n=3 )

表4 抑菌实验结果(抑菌圈直径/mm,,n=3 )
菌种 dmso 大黄酸 大黄酸-Mn 大黄酸-Co 大黄酸-Zn金黄色葡萄球菌 — 19.0±0.91 23.3±0.74 21.6±0.82 18.4±0.35大肠杆菌 — 16.5±0.50 20.5±0.66 19.5±0.48 16.5±0.69肺炎链球菌 — 18.2±0.85 20.7±0.92 22.5±0.33 19.0±0.70
2.6 二倍稀释法测定结果
结果表明大黄酸和大黄酸金属配合物对三种细菌均具有抑菌活性,其中大黄酸-锰和大黄酸-钴对金黄色葡萄球菌的抑菌活性强于配体大黄酸,MIC均达到12.5 μg.mL-1,小于大黄酸(25 μg.mL-1);大黄酸金属配合物对于大肠杆菌抑菌作用稍差,但MIC高于配体。大黄酸-锰对于肺炎链球菌抑菌活性最强,其MIC值达到6.025 μg.mL-1。
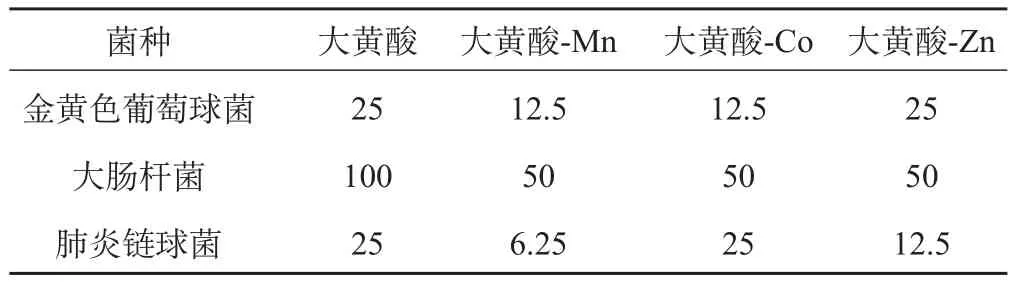
表5 二倍稀释法实验结果(MIC/μg.mL-1,n=3)
3 讨论
本文以大黄中活性成分大黄酸为原料,合成了大黄酸-锰,大黄酸-锌,大黄酸-钴三种金属配合物,采用紫外光谱法,红外光谱法,核磁共振氢谱法等三种方法对配合物结构进行了表征,确定了配合物可能的结构组成。滤纸片法测试结果和二倍稀释法测试结果大致吻合。抑菌活性测试结果说明,大多数配合物抑菌活性强于配体,初步证实了大黄酸与金属离子具有协同抗菌作用。
[1] 张元发,王勇强,董双林.大黄酸在刺参体内的药代动力学研究[J].渔业科学进展,2010,12,31(6):78.
[2] 郭美姿,徐海荣.大黄酸药理作用的研究进展[J].国外医学(中医中药分册),2002,24(3):139.
[3] 孙向红,孙玉维,李红,等.何首乌主要成分大黄索,大黄酸及二苯乙烯苷对肝细胞,肝癌细胞的影响[J].现代中西医结合杂志,2010,19 (11):1315.
[4] 庄江能.大黄的主要成分及其临床药理研究进展[J].西南军医,2009,9,11(5):931.
[5] 曹治权,王秀萍,曹广智,等.中药中微量元素的存在状态与生物活性关系的研究[J].广东微量元素科学,1995,2(10):181.
[6] 侯巍,楚婧,侯丽然.木犀草素与锌配合物的合成及其DPPH自由基清除活性的研究[J].黑龙江医科药学,2012,8,35(4):16.
[7] 谭明雄.中药白花丹活性成分白花丹素金属配合物的合成,抗肿瘤活性及与DNA作用研究[D].湖南:中南大学,2008.[J].武汉化工学院学报,2001,26(1):11.
[8] 刘波,潘志权.锰酶及其模拟物研究进展[J].武汉化工学院学报,2001,26(1):11.
[9] 徐强,宋仲容.微量元素与心脑血管疾病[J].黔西南民族师范高等专科学校学报,2005, 9(3):75.
[10] 陈志民.稀土芳香羧酸配合物的合成、晶体结构及抑菌活性研究[D].河北:河北师范大学,2009.
[11] 张庆梅,贡雪东,肖鹤鸣,等.蒽醌及其羟基衍生物的密度泛函理论研究[J].化学学报,2006,65(5):383.
[12] 消毒防范技术规范2002[M].北京:中华人民共和国卫生部,2002.
(责任编辑:陈思敏)
The study on inhibiting capacity of Rhein metal complex on bacteria
XIANG Hui, PAN Xiao-li, TAN Yu-zhu, WU Bing, LU Xiao-hua, DONG Xiao-ping//(Pharmacy College, Chengdu University of Traditional Chinese Medicine; The Ministry of Education Key Laboratory of Standardization of Chinese Herbal Medicine; State Key Laboratory Breeding Base of Systematic Research, Development and Utilization of Chinese Medicine Resources Co-founded by Sichuan Province and MOST, Chengdu 611137, China)
Objective:Synthesize three Rhein metal complex and represent the structure,then compare the in vitro inhibition of three bacteria.Method:The metal complexes were synthesized in absolute alcohol and UV spectrum,IR spectrum,NMR were used to represent the structure to identify the composition and construction. The MIC of complexes were detected using double dilution method, and the inhibiting capacity of metal complexes on Staphylococcus aureus, Streptococcus pneumonia and colibacillary were tested by flter paper method.Result:Through the structural representation, the metal complex structure was confrmed to be consisted of two Rhein molecule and one metallic ion. By the method of flter paper,the inhibiting capacity on bacteria of the metal complex were better than ligand. Rhein-Mn showed the strongest inhibiting capacity on Staphylococcus aureus and Bacterium coli with inhibition zone of 23.3 mm and 20.5 mm respectively. The strongest inhibiting capacity on Streptococcus pneumoniae was found in Rhein-Co with inhibition zone of22.5 mm. The MIC of complexes detected using double dilution method showed that the inhibiting capacity of metal complexes were mostly stronger than the ligand.Conclusion:After Rhein and metallic ion formed metal complex,the inhibiting capacity are enhanced.
Rhein; flter paper method; double dilution method; metal complex;inhibiting capacity on bacteria
R 285.5
A
1674-926X(2014)04-007-04
四川省教育厅资助项目(13ZB0302)
成都中医药大学药学院 中药材标准化教育部重点实验室 中药资源系统研究与开发利用省部共建国家重点实验室培育基地,四川 成都 611137
向晖,在读研究生 Email:xianghui12688@126.com
董小萍,教授,主要从事中药质量标准化研究Email:dongxiaoping11@126.com
2014-05-06

