基于核酸适配体与金纳米粒子检测水中Hg2+的研究
宇 佳,孙 璐,迟德富
(东北林业大学林学院,黑龙江哈尔滨 150040)
基于核酸适配体与金纳米粒子检测水中Hg2+的研究
宇 佳,孙 璐,迟德富*
(东北林业大学林学院,黑龙江哈尔滨 150040)
基于Hg2+与胸腺嘧啶(T)的T-T错配结合的特性,构建出一种快速便捷的可在高盐溶液中诱导金纳米粒子可控聚集的比色检测Hg2+的方法。采用硼氢化钠还原法制备金纳米粒子,并应用透射电子显微镜和紫外分光光度计对其进行表征。设计核酸适配体并修饰金纳米粒子表面,增强金纳米粒子的稳定性,使其能够拮抗高盐诱导下的团聚行为,当存在Hg2+时,核酸适配体与Hg2+结合,使得金粒子去保护而聚集,产生了颜色的变化,从而通过比色法定量分析Hg2+的浓度。结果表明,以硼氢化钠为还原剂可以得到稳定性好且分布均匀的平均粒径约为27nm的金纳米粒子;伴随Hg2+浓度的提高,体系颜色由红色向蓝色发生转变;荧光光谱结果表明,伴随Hg2+浓度的提高,荧光强度逐渐增强;说明金纳米粒子逐步发生团聚;检测体系对8种常见离子具有明显的选择检测性能。
金纳米粒子,汞离子,比色探针,饮用水安全
随着工业的高速发展,水中重金属的污染问题也随之日益严重。在众多重金属离子污染中,汞离子(Hg2+)的危害最为严重[1]。Hg2+能够进入人体内并与体内的各种酶蛋白上的S-H和S-S键牢固结合,使蛋白质发生变性,严重影响人类的生命安全,因此,在饮用水中Hg2+的定性检测和定量分析的研究具有重要的意义[2]。目前,测定重金属离子的方法主要有原子光谱法[3]、紫外-可见分光光度法[4]、电化学分析法[5]等。这些方法大多需经过复杂的预处理过程和昂贵的仪器设备,难以满足快速分析的需求,因此急需研发一种高效便捷的检测方法[6]。金纳米粒子自身具有优良的光学性且其溶液的颜色与个体粒径及颗粒的间距有关。当颗粒间距明显小于粒径,金纳米粒子就容易发生团聚,宏观上溶液颜色由酒红色变为紫色或蓝色,利用这一性质,在控制其粒径大小的同时,结合表面修饰与改性等方法,就可以设计出针对于快速检测金属离子的金纳米比色探针[7-10]。1997年,Science上报到了Mirkin研究组应用金颗粒标记寡核苷酸并对靶标寡核苷酸进行检测,开创了利用金纳米颗粒比色检测的新纪元[11]。2002年,Obare等在金粒子表面修饰上1,10-邻二氮杂菲基团,从而实现了对溶液中Li+的特异性响应。金粒子表面的配体通过与Li+发生配位作用形成复合物,进而导致金纳米粒子的大规模聚集。通过分析共振峰位置移动与Li+浓度的关系,实现了对Li+的定量测量,其精度达到10~ 100mmol/L[12]。Lee等用寡聚双链DNA修饰金纳米粒子,利用DNA双链随温度升高而变性的性质,诱导金纳米粒子的聚集,通过金纳米粒子溶胶颜色的变化(变为紫红色)指示体系中的Hg2+,从而实现对Hg2+的特异性和选择性的响应[13]。2008年,刘晓刚课题组利用的胸腺嘧啶与汞离子发生配位的原理,采用DNA功能化纳米金颗粒,并设计增加功能化DNA双链中错配胸腺嘧啶的数目,DNA链中错配碱基的数目增多,使DNA链的链解温度下降,通过系统的实验,设计增加错配胸腺嘧啶的数目达到8对时,该检测方法可在常温下进行,通过金纳米溶胶颜色的变化,可视的检测限为3μmol/L[14]。
本研究针对Hg2+与胸腺嘧啶(T)T-T错配的结合特异性[15],设计出特异性螯合Hg2+的核酸适配体,用以修饰金纳米粒子。当体系中出现Hg2+时,会与粒子表面核苷酸结合,使得金纳米粒子迅速聚集,从而引起体系颜色发生变化,进而判断样品中Hg2+的浓度。本研究将为水环境污染中重金属离子的检测与治理提供基础资料。
1 材料与方法
1.1 材料与仪器
氯金酸、氯化汞、碳酸钾、氯化钠、硫酸铜、醋酸锌和氯化铁 均为分析纯,购自于国药集团化学试剂有限公司;硼氢化钠 购自于上海振兴化工一厂;其余化学试剂 均为分析纯;水 为Millipore二次去离子水。
Tecnai G220 透 射 电 子 显 微 镜 Royal Dutch Philips Electronics Ltd;激光粒度仪(BT-9300H) 成都贝斯达仪器仪表厂;紫外-可见光分光光度计(UV2250) 北京桑翌科技发展有限公司。
1.2 核酸适配体的设计
根据Hg2+可与富含胸腺嘧啶的单链DNA特异性结合形成发卡结构这一特点,设计核酸适配体。由上海生工生物工程技术服务有限公司合成设计序列为5’-CGGTTGCACTTGTTTGTT-3’的核苷酸片段。用去离子水溶解稀释到100μmol/L。实验操作时的工作浓度为5μmol/L。
1.3 金纳米粒子的制备与表征
参考Marie等[16]方法改进。在4℃预冷的20mL的双蒸水中,加入0.5mL质量分数为1%的氯金酸;再加入0.2mol/L的碳酸钾溶液0.1mL;在搅拌的条件下,迅速分批次加入新鲜配制的硼氢化钠水溶液(质量浓度为0.5mg/mL)0.5mL,直至溶液出现酒红色为止,磁力搅拌10min,4℃静置保存。紫外-可见光吸收光谱:采用紫外-可见光分光光度计扫描金纳米粒子的吸收光谱,最大波长应在520nm左右。粒径分布:置于超声波清洗器上超声振荡使其分散成单个颗粒,然后用激光粒度分布仪检测粒径的大小及分布情况。透射电镜:采用透射电子显微镜观察金纳米粒子探针的表观形貌和粒度分布情况。
1.4 不同浓度Hg2+的快速比色检测[17]
向离心管中分别加入10μL的5μmol/L核酸适配体和终浓度的为0、0.1、1.0、5、10、50、100、200、300μmol/L汞离子溶液,加灭菌水至整个体系为60μL,混匀,于20℃水浴中孵育30min。再依次加入100μL金胶,100μL的磷酸盐缓冲溶液(pH7.3)。室温反应15min,观察记录颜色的变化,取各检测体系约3mL于光程为1cm的荧光比色皿中,以432nm作为激发波长,扫描波长范围400~480nm,测定不同汞离子浓度检测体系的荧光强度的变化范围。
1.5 比色探针的检测选择性研究
实验设计A、B两组进行,A组:向离心管中加入10μL的5μmol/L的DNA和0.5μmol/L的汞液,再向体系中分别添加浓度为汞离子浓度50倍的Fe3+、Cu2+、Na+、K+、Ca2+、Zn2+、Mg2+和Mn2+,加去离子水至总体积为60μL,B组:不加入汞液,其他与A组相同。对照组为不加其他金属离子的反应体系。混匀,于20℃水浴中孵育30min。再依次加入100μL金胶和100μL的磷酸盐缓冲溶液(pH7.3),室温反应15min,观察记录颜色变化。
2 结果与分析
2.1 金纳米粒子的性能表征
紫外-可见光光谱能与金纳米粒子大小、形状与分散状态等信息呈现出完全不同的响应,通过分析其谱图,可以得到有关颗粒粒度和结构等重要信息。根据理论,纳米金颗粒的特征等离子体吸收峰在510~550nm处,并且随着粒子尺寸的增加吸收峰的位置发生红移,此吸收峰的位置和形状与颗粒高分散和缔合态的存在有关[18-19]。
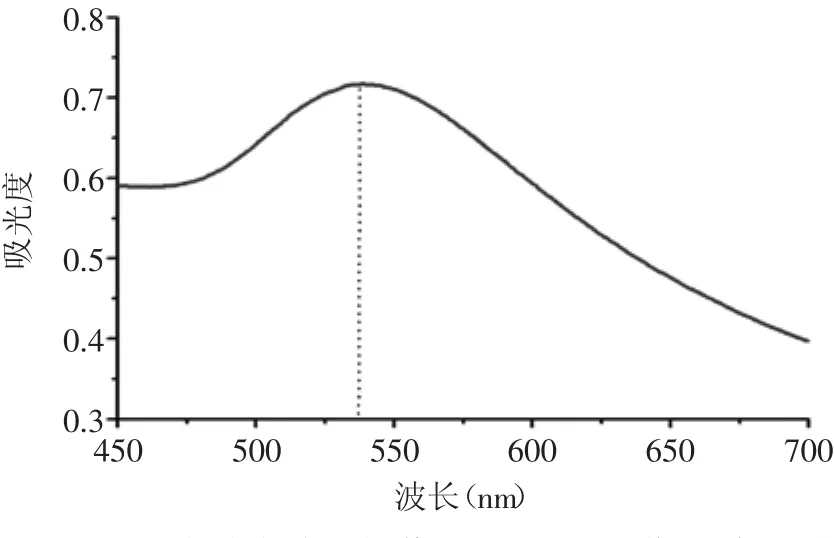
图1 金纳米粒子的紫外-可见光吸收光谱Fig.1 UV-vis absorption spectra of AuNPs
由图1可知,采用硼氢化钠还原法所制备的金纳米粒子在约527nm处具有明显的吸收峰,且所制备的金溶胶颜色为酒红色。采用透射电子扫描电镜对所制备的金纳米粒子的表观形貌进行表征,结果见图2。硼氢化钠还原法制得的金纳米粒子粒径分布均匀,具有良好的单分散性能,整体呈规则的球型,没有发现团聚的现象,利用激光粒度仪测定粒径分布,得出金纳米粒子平均粒径大小约为27nm。

图2 金纳米粒子的透射电镜图片(200,000×)Fig.2 TEM image of chitosan-stabilized AuNPs with the scale bar(200,000×)
2.2 Hg2+的比色检测研究
基于金纳米粒子的汞离子快速检测原理为胸腺嘧啶(T)与Hg2+形成“T-Hg2+-T”结构诱导单链DNA折叠或两个单链形成双链,进而使金纳米失去保护在盐诱导下聚集,通过纳米金溶液的颜色变化检测Hg2+。但是金纳米粒子在检测的过程中容易被样品中其他种类离子所影响,造成不必要的颗粒聚集,从而影响检测体系的灵敏度和准确度[20]。针对此类问题,本研究设计了含T-T错配的镊子型核酸适配体并用其修饰金纳米粒子,使得金纳米粒子能在高盐中稳定存在,实现了对Hg2+的快速光度法检测。采用金纳米粒子与核酸适配体复合构建的金纳米比色探针,快速比色检测不同浓度的汞离子,结果见表1。

表1 基于金纳米粒子和核酸适配体的汞离子比色检测Table 1 Colorimetric detection of mercury ions based on gold particles and aptamers
由表1可知,伴随着样品中Hg2+的浓度的提高,颜色逐渐变化,由酒红色向蓝灰色转变;当汞离子浓度达到300μmol/L时,颜色变化最为显著;当汞离子浓度为0.1μmol/L时,与对照的颜色基本没有区别;当汞离子浓度大于50μmol/L时,颜色变化开始明显。由结果可知,此体系可以用于比色测定,通过目测就能判断汞离子的残留,本研究可用于饮用水或者其他食品中痕量的汞离子的快速检测。
为了能够准确的确定不同浓度汞离子与金纳米粒子的反应程度,用以构建实时精确的检测模型,采用荧光光谱法对检测体系进测定,结果见图3。
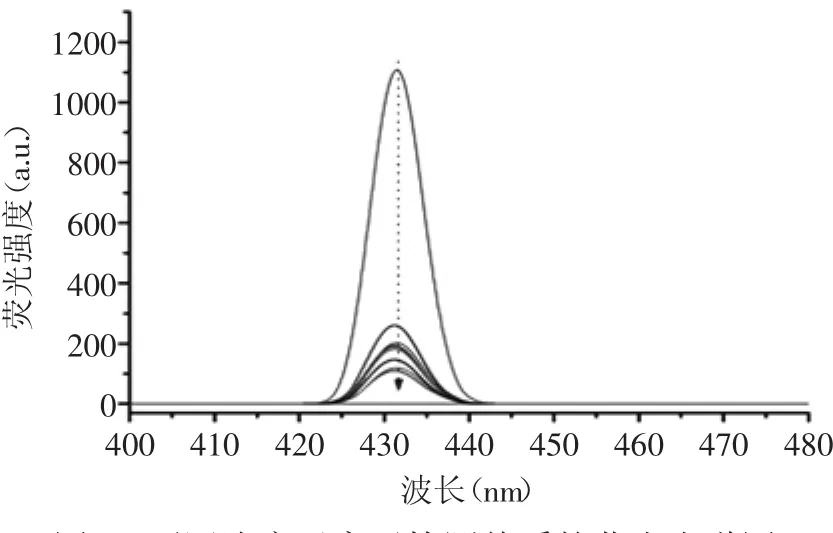
图3 不同浓度汞离子检测体系的荧光光谱图Fig.3 Fluorescence spectra of the solution at the different concentrations of Hg2+
采用荧光光谱法精确测定不同浓度汞离子与金纳米比色探针的反应过程。由图3可知,反应体系中汞离子的浓度与荧光强度具有相关性,伴随着汞离子浓度的增加,荧光强度也逐渐提高。说明汞离子的在体系中诱导了金纳米粒子的聚集,出现了荧光增强效应。其中,当汞离子浓度为0.1μmol/L时,荧光强度与对照样品的荧光强度基本一致,当汞离子浓度大于50μmol/L时,荧光强度增加明显,由200μmol/L增加到300μmol/L时,荧光强度达到最大。此结果与表1中颜色变化规律基本一致。
2.3 选择性研究
比色检测体系的一个重要指标就是检测选择性,现实样品中往往存在有其他种类的金属离子,此类离子会在一定程度上干扰检测体系。本研究选择300μmol/L汞离子浓度作为参照标准,选择8种样品中常见的金属离子用作干扰研究,常见金属离子为Fe3+、Cu2+、Na+、K+、Ca2+、Zn2+、Mg2+、Mn2+,每种金属离子的浓度为汞离子浓度的50倍,即1.5mmol/L。
由表2A组结果可知,当相同的反应体系中加入不同的金属离子后,只有汞离子的反应体系的颜色发生了变化,变为蓝灰色,此结果与表1基本一致,而其余离子的反应体系颜色没有发生明显的改变,初步说明基于特异性核酸适配体的金纳米比色探针具有较强的检测选择性。由表2B组可知,当汞离子与8种不同金属离子分别同时出现在检测体系中时,反应颜色基本一致,没有发生明显变化,说明本研究所设计的检测体系具有选择性。

表2 汞离子比色检测选择性能Table 2 Selectivity of colorimetric detection of mercury ion
3 结论
本文将纳米金和DNA相结合,设计了一种基于盐诱导纳米金聚集的比色检测Hg2+的方法。设计的镊子型dsDNA能够有效地保护金纳米粒子,且其结构非常有利于“T-Hg2+-T”的形成。将这种镊子型DNA与纳米金相结合对Hg2+进行检测,可实现对Hg2+的快速检测。本方法具有良好的灵敏性和特异性,为对重金属离子的检测及环境污染分析技术的改进提供理论参考依据。
[1]Milaeva E R.The role of radical reactions in organomercurials impact on lipid peroxidation[J].Journal of Inorganic Biochemistry,2006,100(5):905-915.
[2]Li T,Dong S J,Wang E K.Label-free colorimetric detection of aqueous mercuryion(Hg2+) using Hg2+-modulated G-quadruplex-based DNAzymes[J].Analytical Chemistry,2009,81(6):2144-2149.
[3] 汪尔康.分析化学新进展[M].北京:科学出版社,2002.
[4]刘兴奋,武海萍,李玉兰.一种高灵敏度、高特异性检测重金属Hg2+的比色生物传感方法[J]. 核技术,2007,30(5):23-27.
[5]Wang S,Forzani E S,Tao N.Detection of heavy metal ions in water by high-resolution surface plasmon resonance spectroscopy combined with anodic stripping voltammetry[J]. Analytical Chemistry,2007,79(12):4427-4432.
[6]Wang Q,Kim D,Dionysiou DD,et al.Sources and remediation for mercury contamination in aquatic systems-a literature review [J].Environmental Pollution,2004,131(2):323-336.
[7]Hu B,Pan CL,Sun Y,et al.Optimization of fabrication parameters to produce chitosan-tripolyphosphate nanoparticles for delivery of tea catechins[J].Journal of Agricultural and Food Chemistry,2008,56(16):7451-7458.
[8]Junga C,Chung JW,Kim UO,et al.Real-time colorimetric detection of target DNA using isothermal target and signaling probe amplification and gold nanoparticle cross-linking assay[J]. Biosensors and Bioelectronics,2011,26(5):1953-1958.
[9]Kim T,Lee CH,Joo SW,et al.Kinetics of gold nanoparticle aggregation:Experiments and modeling[J].Journal of Colloid and Interface Science,2008,318(8):238-243.
[10]Wu ZJ,Zhao H,Xue Y,et al.Colorimetric detection of melamine during the formation of gold nanoparticles[J].Biosensors and Bioelectronics,2011,26(5):2574-2578.
[11]Elghanian R,Storhoff J J,Mucic R C,et al.Selective Colorimetric Detection of Polynucleotides Based on the Distance-Dependent Optical Properties of Gold Nanoparticles[J].Science 1997,277:1078-1081.
[12]Obare S O,Hollowell R E,Murphy C J.Sensing Strategy for Lithium Ion Based on Gold Nanoparticles[J].Langmuir,2002,18(26):10407-10410.
[13]Lee J S,Han M S,Mirkin C A.Colorimetric Detection of Mercuric Ion(Hg2+)in Aqueous Media using DNA-Functionalized Gold Nanoparticles[J].Angewandte Chemie,2007,46(22):4093-4096.
[14]Xue X J,Wang F,Liu X G.One-setp,room temperature,colorimetric detection of mercury(Hg2+) using DNA/nanopartilce conjugates[J].Journal of The American Chemical Society,2008,130(11):3244-3245.
[15]Marc R.Knecht,Manish Sethi.Bio-inspired colorimetric detection of Hg2+and Pb2+heavy metal ions using Au nanoparticles [J].Analytical and Bioanalytical Chemistry,2009,394(1):33-46.
[16]Daniel M C , Astruc D.Gold Nanoparticles:Assembly ,Supramolecular Chemistry ,Quantum-Size-Related Properties and Applications toward Biology,Catalysis,and Nanotechnology [J].Chemical Reviews,2004,104(1):293-346.
[17] 裴智明.金纳米材料制备及其金属离子检测应用[D].重庆:重庆大学,2012.
[18]Daniel W L,Han M S,Lee J S,et al.Colorimetric nitrite and nitrate detection with gold nanoparticle probes and kinetic end points[J].Journal of the American Chemical Society,2009,131(18):6362-6363.
[19]Murphy C J,Gole A M,Hunyadi S E,et al.Chemical sensing and imaging withmetallic nanorods[J].Chemical Communications,2008,5(4):544-557.
[20] 凌绍明,范燕燕,蒋治良,等.镊子型dsDNA稳定的纳米金光度法快速检测Hg2+的研究[J]. 分析测试学报,2011,30(7):804-812.
Colorimetric biosensing of Mercury(II) ion using the novel aptamer modified gold nanoparticles as a probe
YU Jia,SUN Lu,CHI De-fu*
(College of Forestry,Northeast Forestry University,Harbin 150040,China)
A simple and rapid colorimetric method was developed for the detection of Hg2+based on the specific thymine T-Hg2+-T structure and gold nanoparticles (AuNPs) in the presence of a given high concentration of salt.The gold nanoparticles were prepared by the NaBH4reduction method.Transmission electron microscopy,laser particles size analyzer,and UV-vis spectroscopy were used to characterize the samples.The aptamer was designed to attach to AuNPs and effectively prevent AuNPs from salt induced aggregation.While the presence of Hg2+ions,the AuNPs were less well-protected thus aggregated at the salt concentration ,resulting into a color change.It could be colorimetric quantitative analysis of the concentration of Hg2+.The results showed that the product with good stability and good distribution could be obtained with taking sodium borohydride as reductant AuNPs had a mean diameter of 27nm.It was observed that the aptamer-stabilized AuNPs solution showed a color change from red-to-blue when Hg2+was added into the solution.The aptamer-AuNPs exhibited strong fluorescence emission , while upon addition Hg2+, the solution showed a dramatic increase of the fluorescence intensity as a result of the aggregation behavior of the AuNPs.The paper based sensor showed high selectivity for 8 kinds of metal ions.
gold nanoparticles;mercury(II);colorimetric probe;drinking water safety
O561.3
A
1002-0306(2014)22-0053-04
10.13386/j.issn1002-0306.2014.22.002
2014-01-15
宇佳(1978-),女,助理研究员,主要从事生物分析方面的研究。
* 通 讯 作 者 :迟德 富(1962-),男,教授 ,主要 从事 保护 生物 学 方面 的研究。
国家科技支撑计划课题(2012BAD19B07)。

