紫外键联马来酸酐表面改性聚丙烯腈超滤膜
魏秀珍,李光胜,聂井姣,吕伯昇,项海,陈金媛
(浙江工业大学生物与环境工程学院,浙江 杭州 310014)
聚丙烯腈(PAN)是目前应用广泛的膜材料之一,其制备的超滤膜具有许多优异的性能,如耐溶剂、不易水解、抗氧化、化学稳定性好,耐细菌腐蚀等[1]。然而在实际工业应用中,PAN膜容易被污染,限制了PAN超滤膜更广泛的运用。近年来,越来越多的研究者致力于减小膜污染方面的研究,发现提高膜的亲水性是改善膜抗污染性的重要途径[2]。聚合物膜亲水改性的方法主要有共混改性[3]、表面涂覆[4]和表面接枝改性[5]。紫外光(UV)接枝是利用紫外光照射,在膜表面产生自由基,进而引发单体在膜表面聚合[6]。相较于其他改性方法,该方法因操作简单,反应不触及膜本体,并且成本较低等优点在近几年得到广泛的研究与应用[7-8]。除了改性方法,改性剂的选择也是接枝改性的重要方面。马来酸酐(MAH)分子内含有双键,是很好的UV改性单体,且马来酸酐不易均聚,在膜表面不会形成交联结构。水解后的MAH含有羧酸基团,可以提高膜表面的亲水性。尤为重要的是,膜表面键联MAH后,MAH分子的带有酸酐基团使膜表面进一步功能化,可以通过简单功能团之间的化学反应在膜表面继续键联其他功能单体,优化膜的性能[9]。
本文采用UV引发表面改性技术将MAH单体键联到PAN超滤膜表面,考察了辐照强度、辐照时间、光敏剂浓度、单体浓度等对膜表面MAH反应率的影响,从而确定了优化反应条件。最后从膜的结构和性能上分析了表面键联MAH单体对PAN超滤膜的影响。
1 实 验
1.1 主要试剂与仪器
聚丙烯腈超滤膜(MWCO,5万),购自蓝景技术工程有限公司;马来酸酐,分析纯,购自上海凌峰化学试剂有限公司;二苯甲酮,分析纯,购自中国上海双香助剂厂;牛血清蛋白(BSA,Mw= 67000),购自中国医药上海化学试剂医药公司,N,N-二甲基乙酰胺(DMAc),购自上海三爱思试剂有限公司。
1.2 PAN超滤膜紫外键联马来酸酐
以二苯甲酮(BP)为光敏剂、丙酮为溶剂,首先将清洗干净并干燥的PAN膜放入40m L光敏剂溶液中浸泡1h,然后取出晾干,再将膜浸入30m L单体溶液中用紫外灯辐照一定时间,得到MAH键联改性PAN膜。UV光辐照键联MAH过程如图1所示。
MAH的反应率测定采用分光光度法[10]。取适量键联MAH的PAN膜,加入3m L N,N-二甲基乙酰胺(DMAc),静置1h,然后加入显色剂2m L[取4m L磷酸缓冲溶液(pH=12),向其中加入4mg若丹明染料溶解,随后加入100m L甲苯,充分振荡混合,静置分层,取上层甲苯萃取液作为显色剂],静置 1h使其充分显色。用分光光度计(北京瑞利,VIS-7220)测513nm处吸光度,根据式(1)计算反应率(RY)。
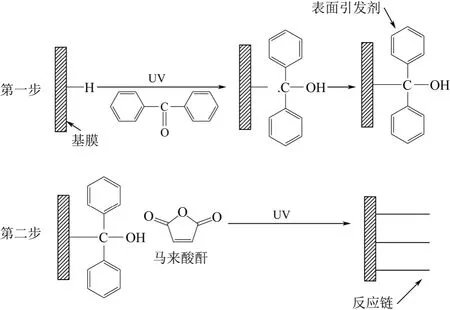
图1 PAN膜表面紫外键联马来酸酐单体流程

式中,M为键联MAH量(标准曲线计算得到);S为键联膜的面积。
1.3 膜性能表征
利用衰减全反射-傅里叶变换红外光谱仪(美国FEI,Vector 22,ATR/FT-IR)表征膜表面的化学组成;利用场发射扫描电子显微镜(荷兰 FEI,JSM-5510LV,SEM)表征膜的表面结构;通过接触角测定仪(德国Dataphysics,OCA20)测定膜表面的接触角。
1.4 膜水通量及抗污染性能的测试
采用死端过滤法测定膜通量随时间的变化趋势。其中膜的有效过滤面积为 3.14cm2,压力为0.1MPa。利用 BSA溶液表征膜的抗污染性,将膜放入1g/L BSA溶液中浸泡12h,使BSA吸附到膜表面或进入膜孔内,造成膜的污染,随后测试污染膜的水通量。然后将被污染膜清洗30m in后,重新测试其水通量 Jw2,计算通量恢复率。通量恢复率是反应膜抗污染性能较常见且实用的一个指标[11],计算公式如式(2)。

2 实验结果与讨论
2.1 PAN膜表面UV键联MAH影响因素
本实验考察了辐照时间、紫外光强度、光敏剂浓度和单体MAH浓度等对MAH反应率的影响。若非特别说明,紫外辐照时间为 25m in, 单体浓度为20g/L, 光敏剂浓度为20mmol/L。
2.1.1 紫外光强度对MAH反应率的影响
紫外光强度随着紫外灯功率变化而变化,选用100W、150W、200W、250W 4种不同功率的紫外灯对 PAN膜进行辐照键联改性,紫外光强度对MAH反应率的影响结果如图2所示。从图2中可以看出,随着紫外灯功率增强,MAH在PAN膜上的反应率仅呈现出较小的变化,基本维持在 10~15μg/cm2,在150W时反应率达到最大值。这可能是因为当功率为100W辐照25m in后,膜表面的活性位点已大部分被光敏剂引发,随后光照强度增加到 150W,活性位点增加量较少,所以反应率仅有少许增加。然而当功率继续增大时,已激发的部分活性位点受到强烈光照的影响被破坏,反而导致反应率下降。因此后续试验均采用150 W的紫外灯辐照。
2.1.2 辐照时间对MAH反应率的影响
紫外光辐照时间对PAN膜表面MAH反应率的影响如图3所示。随着辐照时间延长,MAH在PAN膜表面的反应率先线性增大然后趋于稳定,MAH在膜上的反应率最大值为15μg/cm2。这是由于在初始阶段(0~10min)活性位点随着辐照时间的增加呈线性增长,所以反应率持续升高。随着键联反应进行,键联单体被持续消耗,活性位点增加也变得缓慢,反应率增长变得缓慢,最终逐步稳定。后续实验选取辐照时间为25m in。
2.1.3 光敏剂浓度对MAH反应率的影响

图2 紫外光强度对表面反应率的影响
光敏剂BP在UV光照射下能引发PAN膜上的氢原子产生活性位点,这些活性位点引发MAH分子中的双键打开,使MAH分子键联到PAN膜表面,BP浓度对MAH反应率影响如图4所示。MAH反应率随着BP浓度的增加呈现出先增加后减小最后趋于稳定的现象。在初始阶段(0~10mmol/L),反应率随BP浓度的增加迅速增加,这是由于光敏剂的作用就是引发膜表面产生活性位点,随着光敏剂浓度的增加,膜表面的活性位点显著增多,反应率明显升高。在中间阶段(10~15mmol/L),膜表面反应率增加开始减缓并稳定。这是因为当光敏剂增加到一定浓度时,固定面积膜表面的活性位点大部分都已被激发,增大光敏剂BP的浓度对活性位点的增加影响不明显,最后导致膜表面反应率仅小幅度增加。在最后阶段(15~30mmol/L),随着光敏剂浓度的持续增大,膜表面的反应率反而稍有下降。这是因为一方面光敏剂浓度的增加将阻碍键联单体与膜表面的接触,影响反应率;另一方面,光敏剂浓度的增加导致MAH反式异构体的形成,不利于键联反应的进行。
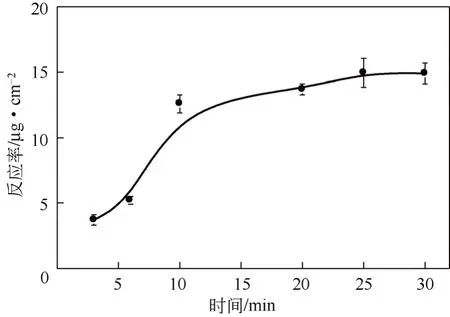
图3 紫外辐射时间对表面反应率的影响
2.1.4 单体浓度对反应率的影响

图4 光敏剂BP浓度对表面反应率的影响
理论上来说,MAH浓度越高,扩散到PAN膜表面的MAH分子就越多,反应率越高。MAH浓度对反应率影响结果如图5所示。随着MAH浓度升高,MAH在PAN膜表面的反应率迅速升高,反应率在MAH浓度达到20g/L后趋于稳定,此时膜表面反应率为20μg/cm2左右。在起始阶段,MAH浓度的增加能够有效增加PAN与MAH接触的概率,引起反应率增加。随着MAH浓度的进一步增加,MAH分子间的相互缔结使改性溶液黏度增大,阻碍了MAH分子向膜表面的迁移,使PAN膜表面MAH反应率基本保持不变。
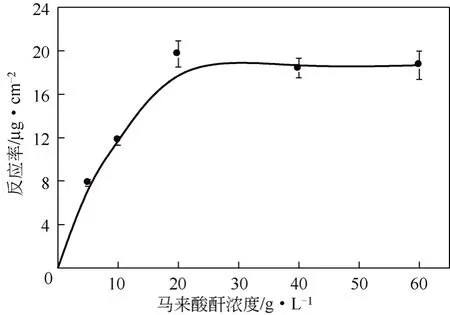
图5 马来酸酐单体浓度对表面反应率的影响
通过上述系列实验得到膜表面键联MAH的最优条件,即紫外光强度为150W、辐射时间为25min、光敏剂BP浓度为15mmol/L和单体MAH浓度为20g/L。在此优化条件下,膜表面 MAH反应率为20μg/cm2。尽管得到了MAH在PAN膜表面UV键联的优化条件,然而从整个实验过程来看,无论改变什么参数,单体MAH在膜上的反应率均不高。这主要是由于马来酸酐的分子结构造成的,无论从电子效应和立体位阻效应而言,它都不利于聚合,首先这一单体的双键是和两个羰基共轭,电子云密度太低,这也是它活性低的原因之一,对其部分中和后,MAH的顺势构型不稳定,容易变成反式异构体,这样就带来了位阻效应的问题,因此键联也变得比较困难。然而,MAH键联至PAN膜表面不仅可以提高膜表面的亲水性能,还能使膜表面功能化。因为膜表面酸酐基团可以进一步键联其他亲水性聚合物,如含有多个羟基基团的超支化聚酯(HBP)、聚酰胺等,这样即使在MAH反应率较低的情况下也可以大大提高膜的亲水性。
2.2 膜表面ATR/FT-IR分析
ATR/FT-IR可以探测到膜表面几微米深度的化学组成。PAN超滤膜和键联MAH膜的ATR/FT-IR谱图如图6所示。 其中,2250cm-1属于氰基(C≡N)的伸缩振动吸收峰;1739cm-1是羧酸羰基C=O伸缩振动特征吸收峰,而在PAN膜中出现此峰是因为原膜制备时添加剂的加入以及部分 CN水解导致的;1420cm-1属于烯烃的变角振动吸收峰;1390cm-1属于羧酸跟 COO—对称伸缩的特征吸收峰;2940cm-1是C—H的特征吸收峰。1739cm-1(C=O)处特征吸收峰的增强和 1390cm-1特征吸收峰的出现说明MAH成功键联到PAN超滤膜上。
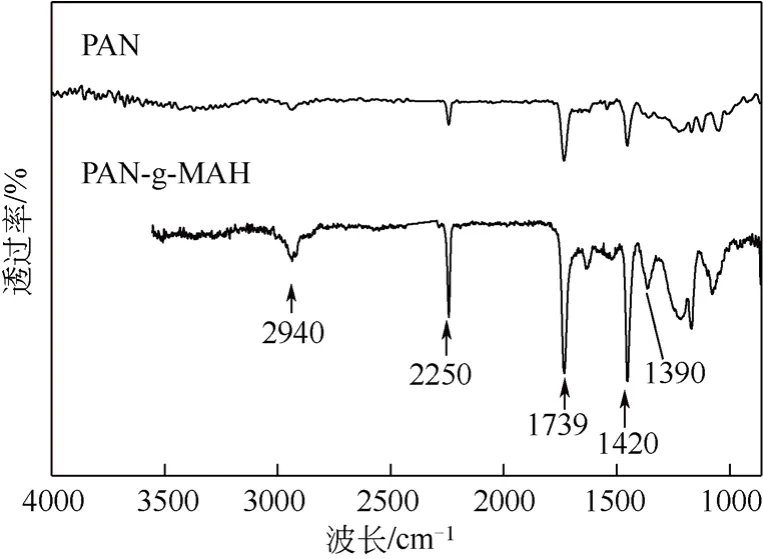
图6 原PAN膜与键联改性膜的 ATR/FT-IR 图
2.3 表面改性对膜表面和断面形貌的影响
PAN原膜与改性膜的表面和断面形貌如图7所示。如图7所示,PAN超滤原膜表面致密且较光滑,断面结构呈现出典型的超滤膜非对称结构:存在微孔表面皮层和指状大孔结构亚层。PAN膜表面键联MAH后,膜的断面结构并没有发生变化,只是膜的表面变得更加粗糙,同时呈现小粒子团聚的形态,这是由于MAH已经键联到膜表面的结果。从SEM形貌结构可以看出,MAH键联改性只发生在膜表面,对膜内部的结构不产生影响。
2.4 键联改性对PAN膜亲水性的影响

图7 原PAN膜与改性膜的扫描电镜图
通过测定膜表面水接触角随时间的变化考察了表面键联改性对PAN膜亲水性的影响,结果如图8所示。研究表明,膜的亲水性越好,其起始水接触角会越低,且随时间的延长,水接触角下降的速率也越快[12]。从图8中可以看出,PAN原膜的起始接触角为70.6°,而MAH键联改性膜的起始接触角为62.4°。并且经过250s后,PAN原膜的起始接触角仅下降10%左右,而PAN-MAH膜起始接触角则下降超过 13%,这表明经过 MAH键联改性的PAN膜的亲水性得到改善。膜亲水性的提高有助于膜通量的增加和膜抗污染性的增强。

图8 原PAN膜与改性膜的动态接触角
2.5 膜水通量与抗污染性
膜的超滤过程设计为3个阶段:第一阶段为原膜与改性膜未经任何污染的纯水过滤阶段(Jw1);第二个阶段为膜经牛血清蛋白(BSA)静态污染后过滤阶段;第三阶段为纯水清洗污染膜后过滤阶段(Jw2)。PAN原膜和MAH改性膜的水通量随时间变化情况如图9所示。从图9中可以看出,在前15min纯水过滤过程,两种膜的通量都有一个明显的下降,之后趋于稳定。这是由于新膜在起始过滤压力下都存在一个压实过程以及溶液的浓差极化作用。稳定时PAN原膜通量为150L/(m2·h), MAH键联改性膜的通量为170L/(m2·h)。尽管MAH膜的亲水性更好,但结果显示表面键联MAH的膜仅比PAN原膜通量稍高。这是由于PAN膜表面键联后,表面的孔径减小和部分孔道堵塞减小了膜通量。MAH键联改性膜表面亲水性增加与表面孔径减小从两个相反的方面综合影响了膜的水通量,最终导致了膜水通量稍有增加。膜经BSA污染后通量再一次明显减少,稳定运行时PAN原膜和MAH键联改性膜通量分别为25L/(m2·h)和55L/(m2·h),通量损失率分别为83.3%与67.6%。这说明与PAN原膜相比,改性膜抗污染性增强。最后将膜放入清水中清洗,清洗后PAN原膜和 MAH 改性膜通量分别为 50L/(m2·h)和125L/(m2·h),通量恢复率分别为 33.3%和 73.5%,说明改性膜的抗污染性能明显优于原膜。MAH键联改性膜表现出较低的通量损失和较高的通量恢复率,这主要是因为经过UV辐照键联MAH后使PAN膜表面存在酸酐基团,酸酐基团接触水溶液后一部分水解成羧酸基团,羧酸基团具有良好的亲水性,在运行过程中更容易吸附溶液中的水分子在膜表面形成水分子层,这层水合分子层能有效抵挡蛋白质污染物的黏附与沉积,使膜难以污染而易于清洗,所以MAH键联改性膜的抗污染性能得到提高。

图9 膜通量随时间变化趋势图
3 结 论
(1)PAN膜表面紫外键联MAH的最佳条件为:在紫外灯功率150W,辐照时间为25min,光敏剂浓度15mmol/L,单体浓度20g/L时,MAH在PAN膜表面反应率最高,为20μg/cm2。
(2)ATR /FT-IR、SEM结果表明单体MAH成功键联到PAN膜表面。PAN膜表面键联MAH后,纯水通量仅稍有提高,但是抗污染性显著增强,改性前后的通量损失率分别为83.3%与 67.6%;通量恢复率为33.3%和73.5%。
(3)PAN膜表面键联MAH后表面产生的可反应性酸酐基团可使膜进一步功能化,通过简单的基团反应即可使聚丙烯酸、聚丙烯酰胺、聚乙烯醇等亲水性大分子或其他温敏性以及pH值响应性聚合物等键联到经MAH改性的膜表面,以此制备出具有特异功能性的膜,拓展高分子膜的应用范围。
[1] 万灵书,黄小军,徐志康,等.聚丙烯腈分离膜改性研究进展及其应用[J].功能高分子报,2004,17(3):527-534.
[2] 唐广军,孙本惠.聚偏氟乙烯膜的亲水性改性研究进展[J].化工进展,2004,23(5):480-485.
[3] Pezeshk N,Rana D,Narbaitz R M,et al.Novel modified PVDF ultrafiltration flat-sheet membranes[J].J.Membr.Sci,2012,389:280-286.
[4] Frahn J,Malsch G,Schwarz F H.Generation of a selective layer on polyacrylonitrile membrane supports for separation of aromatic/non-aromatic hydrocarbon m ixtures by pervaporation[J].Macromol.Symp,2001,164:269-276.
[5] Qiu G M,Zhu L P,Zhu B K,et al.Grafting of styrene/maleic anhydride copolymer onto PVDF membrane by supercritical carbon dioxide:Preparation, characterization and biocompatibility[J].J.Supercrit.Fluid,2008,45(3):374-383.
[6] Rahimpour A.UV photo-grafting of hydrophilic monomers onto the surface of nano-porous PES membranes for improving surface properties[J].Desalination,2011,265(1-3):93-101.
[7] Hua H L,Li N,Wu L L,et al.Anti-fouling ultrafiltration membrane prepared from polysulfone-graft-methyl acrylate copolymers by UV-induced grafting method[J].J.Environ.Sci-China,2008,20(5):565-570.
[8] Song L J,Zhao J,Yang H W,et al.Biocompatibility of polypropylene non-woven fabric membrane via UV-induced graft polymerization of 2-acrylam ido-2-methylpropane sulfonic acid[J].Appl.Surf.Sci,2011,258(1):425-430.
[9] Zhang W,Du Z P,Wang W X,et al.Synthesis and aggregation behavior of grafted maleic acid copolymers[J].J.Colloid.Interf.Sci,2012,374:187-196.
[10] Nie F Q,Xu Z K,Huang X J,et al.Acrylonitrile-based copolymer membranes containing reactive groups:Surface modification by the immobilization of poly(ethylene glycol) for improving antifouling property and biocompatibility[J].Langmuir,2003,19(23):9889-9895.
[11] Peng J,Su Y,Shi Q,et al.Protein fouling resistant membrane prepared by amphiphilic pegylated polyethersulfone[J].Bioresour.Technol.,2011,102(3):2289-2295.
[12] Yi Z,Zhu L P,Zhao Y F,et al.An extending of candidate for the hydrophilic modification of polysulfone membranes from the compatibility consideration:The polyethersulfone-based amphiphilic copolymer as an example[J].J.Membr.Sci.,2012,390-391:48-57.

