基于萘酰亚胺的Turn-on型Fe3+荧光探针
殷丽艳,陈甜甜,朱维平
(华东理工大学 药学院,上海 200237)
过渡金属及重金属元素在自然界中含量丰富,其中一些金属元素在生命过程中起着非常重要的作用[1]。在大脑中,铁元素是含量最为丰富的过渡金属元素,脑组织可充分利用它并将它转化为某些酶的重要组成部分,共同参与氧气的运输与代谢;而且铁元素在许多金属蛋白酶中也是不可或缺的组成部分;同时,在生命体的有氧代谢与电子转移等过程中,铁元素扮演着酶的催化剂等重要角色,因而铁离子的转运与传递、储存与利用,以及平衡与代谢等过程都与有机体的生理功能密切相关,铁离子的缺乏或过量都会导致严重的机体功能紊乱[2]。因此,准确检测人体内铁离子的含量以及跟踪其代谢过程对于疾病诊断与病情控制具有重要的作用。
目前检测铁离子的方法有很多种,其中荧光分析法具有快速响应与高灵敏度的特点,因此利用荧光探针来定性与定量检测铁离子已成为研究的热点。近年来,关于铁离子荧光探针的研究已有一些报道[3-6],但是由于 Fe(Ⅲ)的顺磁性,通常会使荧光猝灭[7-10],因此荧光增强型的 Fe3+探针很少见报道。
随着生命科学、有机化学、分析化学和材料化学等多学科多领域的研究不断交叉深入,以及荧光检测技术的不断提高,化学传感越来越依赖于新颖的传感材料来实现其价值。在小分子荧光化合物出现后,通常利用固载技术将小分子荧光化合物引入到固相载体中,制造出荧光传感材料[11]。其中应用较广泛和成熟的一类材料是硅胶纳米颗粒材料,它是一类良好的荧光传感材载体,尺寸处于料纳米级,对细胞没有明显的毒性,其骨架对热、pH以及机械应力稳定,同时其比表面积大、负载量高等优点使其可利用范围广。通过将小分子荧光探针进行硅烷化修饰后,将其共价键合到硅胶颗粒上,可以制得能够检测各种目标分子的荧光传感材料。
在小分子荧光团中,萘酰亚胺类荧光团因具有高荧光量子产率、光稳定性和化学稳定性以及较大的Stokes位移等特点而得到广泛应用[12-15]。本文选择萘酰亚胺作为荧光团,通过哌嗪与N-2-氯乙酰氨基喹啉反应得到目标探针NPAP,其作用机理是:当体系中没有Fe3+离子存在时,哌嗪的氮原子上的孤对电子对萘酰亚胺荧光团产生PET(photo induced electron transfer,光诱导电子转移)过程,因而荧光比较弱;当体系中有Fe3+存在时,探针与Fe3+结合后抑制其PET过程,荧光团的荧光发射出来。同时,本文将Fe3+离子小分子荧光探针NPAP通过硅烷化修饰后得到了化合物B4,然后共价键合到硅胶颗粒表面,得到了Fe3+离子荧光传感器FS。
1 实验部分
1.1 仪器和试剂
Avance 400MHz(Bruker)核磁共振仪(TMS为内标),MicroMass GCT CA055质谱仪(ESI源),Varian Cary Bio 100紫外光谱仪,Varian Cary Eclipse Bio荧光光谱仪,SZ-98自动双重纯水蒸馏器(上海本波仪器),Sartorius PB-10精密数显酸度计。
实验制备过程中所用试剂均为市售分析纯试剂;二甘醇胺、无水哌嗪购于阿拉丁试剂公司;N,N-二 异 丙 基 乙 基 胺 (N,N-Diisopropylethylamine,DIPEA)购于邦成化工公司;柱色谱硅胶为青岛海洋化工厂产品(300~400目)。
1.2 Fe3+离子小分子荧光探针NPAP和荧光传感器FS的合成
探针NPAP的合成路线如图1所示,由原料8-氨基喹啉与2-氯乙酰氯反应得到化合物B1,然后由原料4-溴-1,8萘酐B0与二甘醇胺反应得到N-取代萘酰亚胺B2,再与无水哌嗪反应得到化合物B3,最后与化合物B1反应得到探针NPAP。
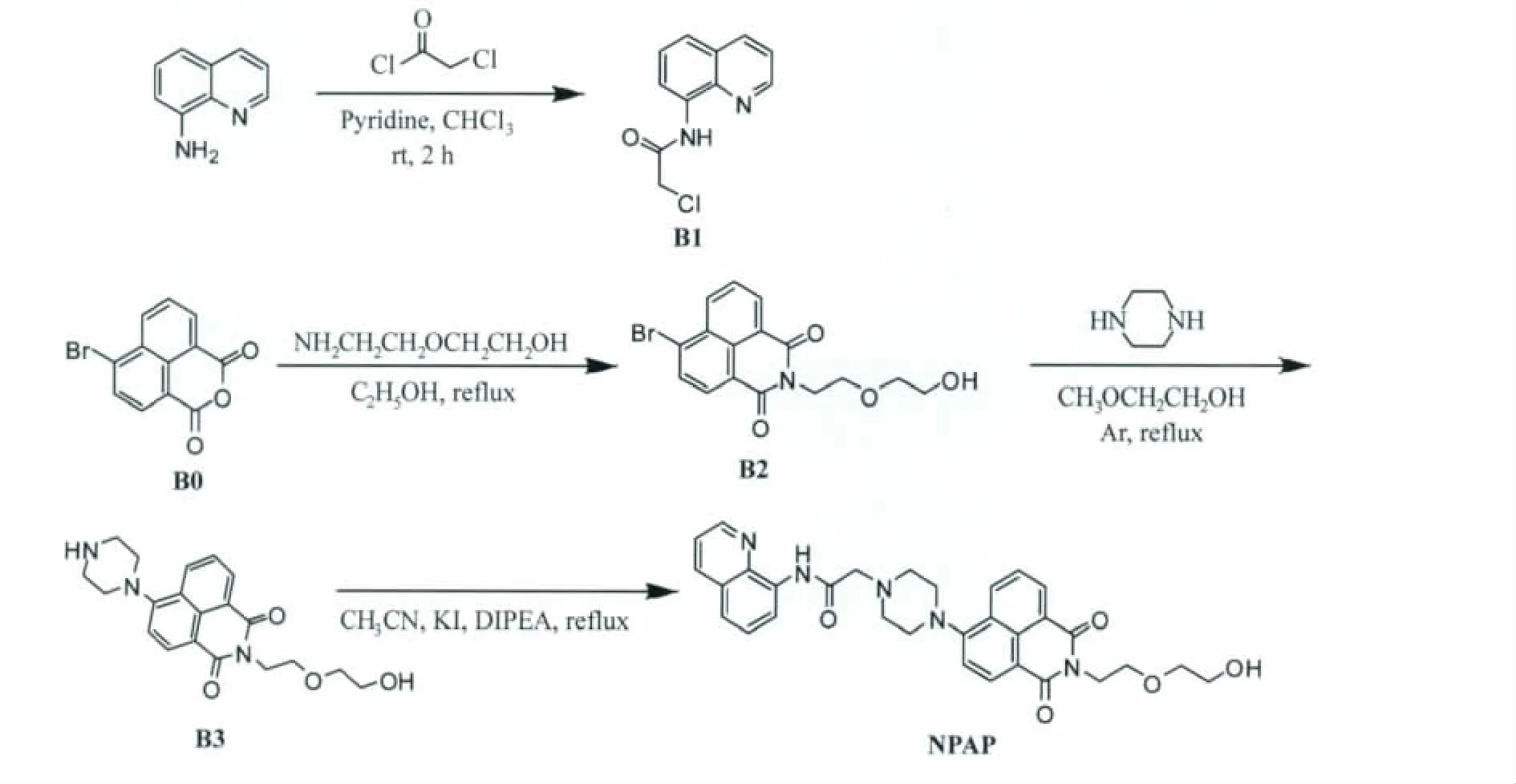
图1 荧光探针NPAP的合成路线Synthesis of the fluorescent sensor NPAP
荧光传感器FS的合成路线如图2所示,将化合物NPAP进行硅烷化修饰得到化合物B4,然后与事先预处理好的二氧化硅硅胶纳米颗粒共价键合,得到荧光传感器FS。
1.2.1 化合物B1的合成[16]
将576.0mg(4.0mmol)8-氨基喹啉和0.5 mL吡啶溶于20mL重蒸过的氯仿中,再将542.0 mg(4.8mmol)氯乙酰氯在冰浴下缓慢滴加到上述反应液中,滴加完毕撤去冰浴,室温反应2h,TLC跟踪反应结束后,停止反应,减压蒸去溶剂,硅胶柱层析(石油醚/乙酸乙酯,5∶1,V/V)得白色针状晶体B1,760.0mg,收率为86.6%。
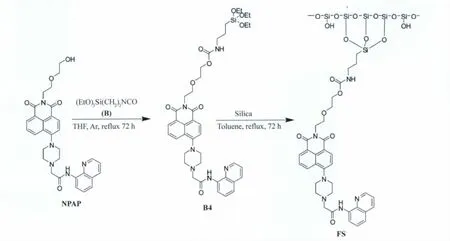
图2 荧光传感器FS的合成路线Synthesis of the fluorescent sensor FS
1.2.2 化合物B2的合成
将500.0mg(1.8mmol)4-溴-1,8-萘酐(B0)、190.0mg 2-(2-氨基乙氧基)乙醇溶于10mL无水乙醇中,加热回流1h,冷却至室温,放置过夜,析出晶体,抽滤取滤饼,红外烘干得 N-(2-(2-羟乙氧基)乙基)-4-溴-1,8-萘酰亚胺黄色晶体(B2),515.0 mg,收率为78.6%,熔点:132.0~133.6℃。
1.2.3 化合物B3的合成
将500.0mg(1.3mmol)N-(2-(2-羟乙氧基)乙基)-4-溴-1,8-萘酰亚胺(B2)和454.5mg(5.3 mmol)无水哌嗪溶于15.0mL乙二醇单甲醚中,加热回流,氩气保护下反应10h,停止反应,旋干溶剂,硅胶柱色谱分离(二氯甲烷/甲醇,15∶1,V/V),得到化合物B3,450.0mg,收率为92.3%,熔 点:198.0~200.0℃。1HNMR (400MHz,CDCl3):2.0(br,1H),3.20(d,J=4.4Hz,4H),3.24 (d,J=4.8Hz,4H,),3.66 (br,2H),3.67 (br,2H),3.84 (t,J=5.6Hz,2H),4.43(t,J=5.6Hz,2H),7.20(d,J=8.0Hz,1H),7.69(t,J=7.8Hz,1H),8.42(d,J=8.4Hz,1H),8.53 (d,J=6.8Hz,1H),8.58(d,J=6.8Hz,1H)。
1.2.4 化合物NPAP的合成
将200.0mg(0.9mmol)N-2-氯乙酰氨基喹啉(B1),365.6mg(1.0mmol)化合物B3,60.0mg碘化钾,2mL N,N-二异丙基乙基胺(DIPEA)溶于60.0mL乙腈中,在氩气保护下加热回流反应10h,停止反应后,旋干溶剂,硅胶柱色谱分离(二氯甲烷/甲醇,70∶1,V/V),得黄色晶体 NPAP,260.0mg,收率为54.2%。1HNMR (400MHz,CDCl3):3.03(br,4H),3.45(br,6H),3.67(d,J=12.4Hz,4H),3.84 (br,2H),4.41(br,2H),7.25(d,J=8.0Hz,1H),7.43(t,J=3.6Hz,1H),7.51 (d,J=7.2Hz,2H),7.66(t,J=7.2Hz,1H),8.38(d,J=8.0Hz,1H),8.52(t,J=7.2Hz,2H),8.76(d,J=6.0Hz,1H),8.83 (s,1H),11.44 (s,1H)。13CNMR (100MHz,CDCl3):39.3,53.3,53.4,61.8,62.4,68.5,72.3,115.0,116.6,121.6,121.9,123.0,125.8,126.1,127.3,128.0,129.9,130.4,131.3,132.7,134.1,136.2,138.9,148.6,155.9,164.2,164.6,168.6。HRMS(ESI)calcd.For C31H31N5O5[M+H+]554.2325,found 554.2404。
1.2.5 化合物B4的合成
将50.0mg(90.0μmol)NPAP和178.0mg(72.0μmol)化合物B溶于10.0mL重蒸过的甲苯中,然后滴加4滴二异丙基乙基胺,在氩气保护下加热、回流反应72h。停止反应后,旋干溶剂,TLC大板分离(二氯甲烷/甲醇,40∶1,V/V),得黄色固体50.0mg,收率为69.4%。1HNMR (400 MHz,CDCl3):0.63(t,J=9.2Hz,2H),1.27(s,9H),1.62(t,J=8.4Hz,2H),3.07(br,4H),3.15 (t,J=6.4Hz,2H),3.49 (br,4H),3.52 (br,4H),3.76 (br,4H),3.80~3.87(m,8H),4.20(br,2H),4.46(t,J=6.0 Hz,2H),7.33(d,J=8.0Hz,1H),7.48(q,J=8.0Hz,1H),7.56(d,J=8.0Hz,1H),7.60(d,J=8.0Hz,1H),7.74(t,J=8.0Hz,1H),8.19(d,J=7.6Hz,1H),8.47 (d,J=8.4 Hz,1H),8.59(d,J=8.4Hz,1H),8.61(d,J=7.6Hz,1H),8.81(dd,J1=6.8Hz,J2=1.6Hz,1H),8.88(d,J=2.8Hz,1H),11.50(s,1H)。HRMS(ESI)calcd.For C41H52N6O9[M+Na+]823.3463,found 823.3465。
1.2.6 荧光传感器FS的合成
将10.0mg化合物B4和1.5g经过活化的硅胶于15.0mL无水甲苯中混合,氩气保护下加热回流反应72h,停止反应后,过滤,取滤饼,滤饼用无水乙醇洗涤至没有颜色,所得到的固体在甲醇中回流24h,然后过滤,所得固体在120℃烘箱干燥24h,得到荧光传感器FS。
2 结果与讨论
2.1 探针NPAP对Fe3+离子的滴定曲线
我们在0.01mol/L Tris-HCl(乙腈/水,80∶20,V/V),pH=6.46,探针 NPAP (0.5μmol/L)的测试条件下,检测其探针随着Fe3+的加入的荧光发射光谱。如图3所示,随着Fe3+不断加入,探针NPAP的荧光强度不断增强,最后当Fe3+离子加到320当量时,荧光强度不再增强,其荧光增强10倍,且伴随着波长20nm的蓝移(从540nm到520nm)。
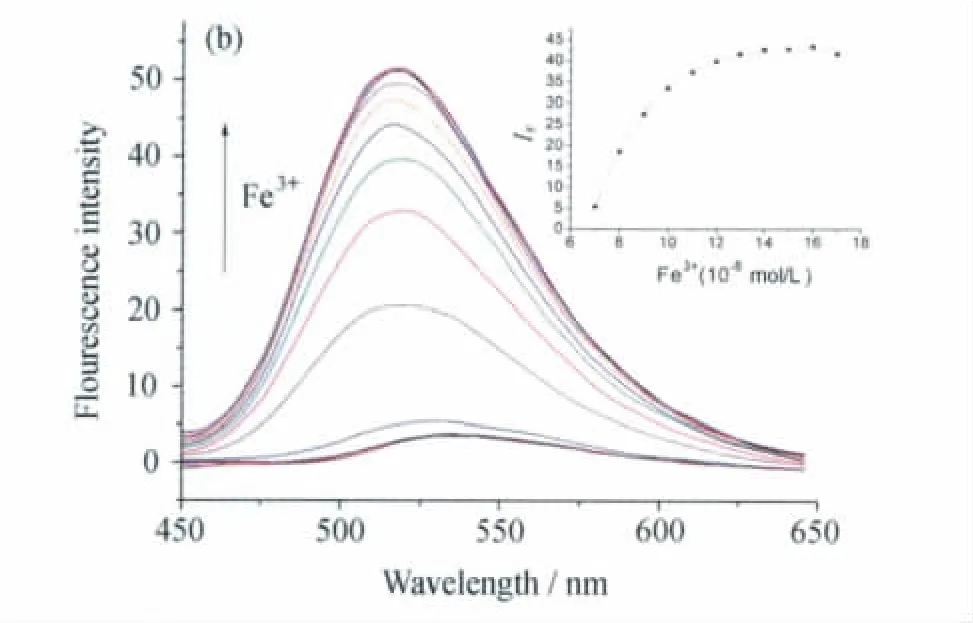
图3 探针NPAP(0.5μmol/L)在不同Fe3+的荧光光谱图插图是探针NPAP在520nm处的荧光强度与Fe3+浓度的关系Fluorescence spectra of NPAP(0.5μmol/L)in the presence of increasing concentrations of Fe3+ ,inset:integrate fluorescence intensity as a function of Fe3+ion concentrations
进一步研究了pH值对体系的影响。pH滴定实验是在0.01mol/L Tris-HCl(乙腈/水,80∶20,V/V)中测定。图4表明,探针NPAP在波长为520nm处的荧光强度随着pH值的增加而降低,且伴随着20nm的红移(从520nm到540 nm)。这是因为在酸性条件下,哌嗪上氮原子被质子化,抑制其PET过程,导致荧光增强;另外,哌嗪上氮原子弱的ICT(Intramolecular Charge transfer)过程导致其波长稍微红移。然而,在pH 6.0~12.0的范围内,探针NPAP荧光强度几乎保持不变,如图5所示,即此探针能在宽pH范围内稳定,不受pH影响。
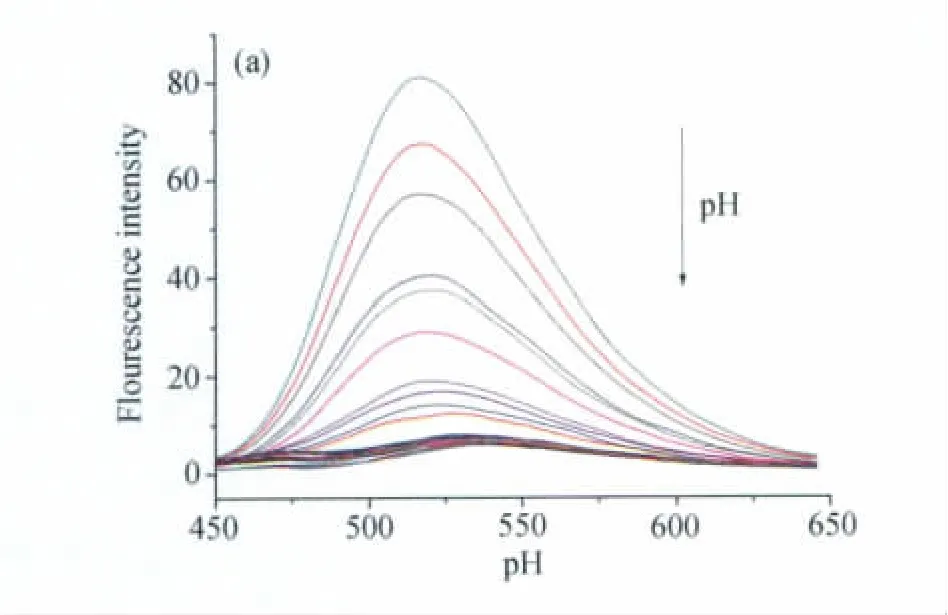
图4 探针NPAP(0.5μmol/L)在不同pH下发射光谱的变化Fluorescence spectra of NPAP(0.5μmol/L)at different pH values
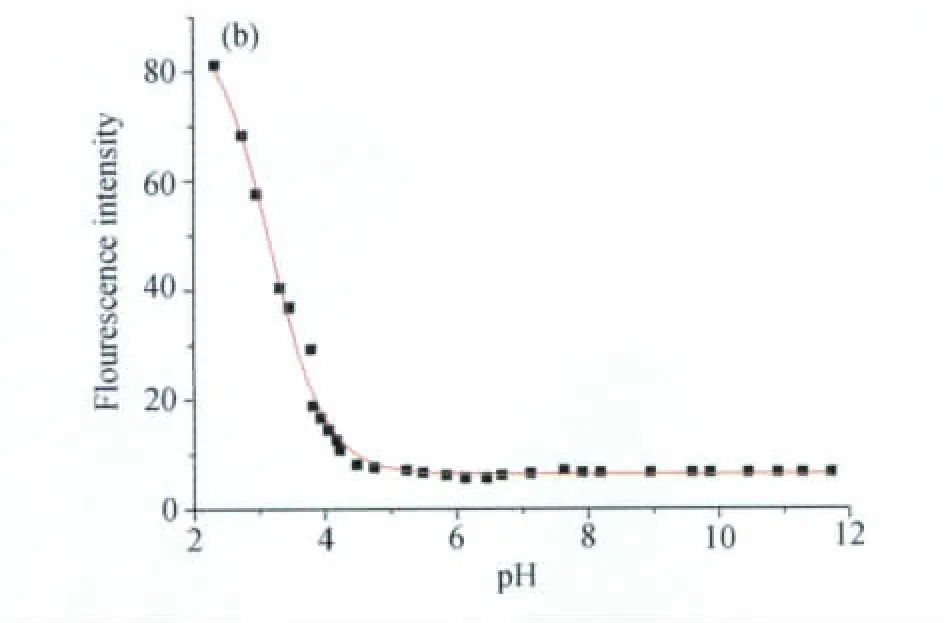
图5 探针NPAP(0.5μmol/L)的荧光强度对pH的变化曲线Fluorescence response of NPAP(0.5μmol/L)at different pH values
2.2 探针NPAP的选择性和竞争性的研究
前面我们已经探讨了探针NPAP在不同pH下光谱性能和对Fe3+的识别性能,但是考察探针的另一个指标是选择性。如图6和图7所示,探针对 Fe3+有较高的选择性,其中 Fe2+、Zn2+、Hg2+、Pb2+、Co2+、Cd2+等离子都没有响应,其中Cu2+离子是荧光猝灭的,Cr3+离子是荧光增强的,且荧光增强1倍。实验结果表明探针NPAP对Fe3+离子是一个荧光增强型(turn-on)探针。
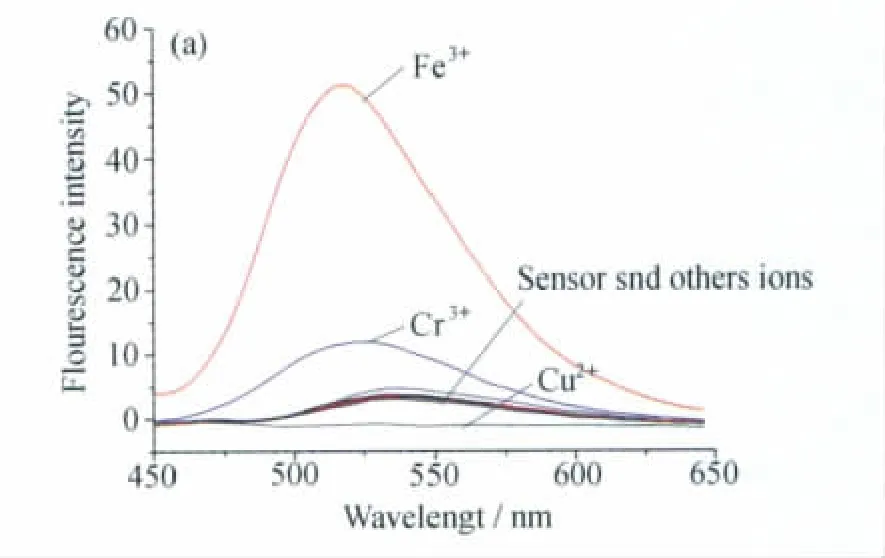
图6 探针NPAP对不同离子的荧光光谱图Fluorescence spectra of NPAP(0.5μmol/L)to different metal ions(1.6μmol/L)
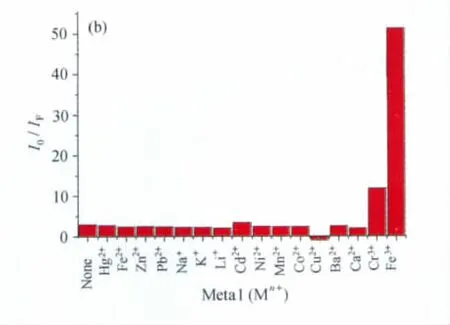
图7 探针NPAP对不同离子的荧光响应曲线Fluorescence response of NPAP(0.5μmol/L)to different metal ions(1.6μmol/L)
探针NPAP的竞争性如图8所示,可以看出,除Cr3+离子有一定的干扰外,探针NPAP不受其他离子的干扰。选择性和竞争性实验结果表明,NPAP是一个选择性识别Fe3+的turn-on探针。
2.3 荧光传感器FS对Fe3+的滴定曲线
FS对 Fe3+的滴定在0.01mol/L Tris-HCl(乙腈/水,80∶20,V/V),pH=6.46中测试,如图9所示,随着Fe3+离子浓度的增加,FS的荧光逐渐增强,且伴随着波长稍微的蓝移(约5nm),且在20~140μmol/L Fe3+离子含量范围内,FS的荧光强度与Fe3+离子浓度呈良好的线性关系(R2=0.9023)。
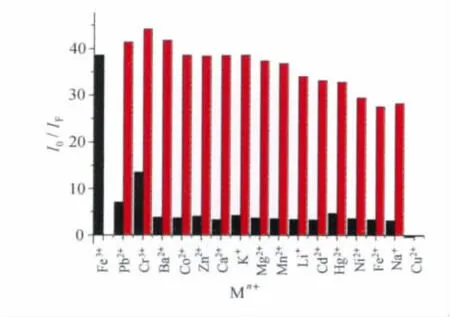
图8 探针NPAP(0.5μmol/L)的竞争性实验:在存在其他离子3.2当量的溶液中,加入3.2当量的Fe3+后的荧光响应The florescence intensity of NPAP(0.5μmol/L)with 3.2equiv of Fe3+ and other metal ions
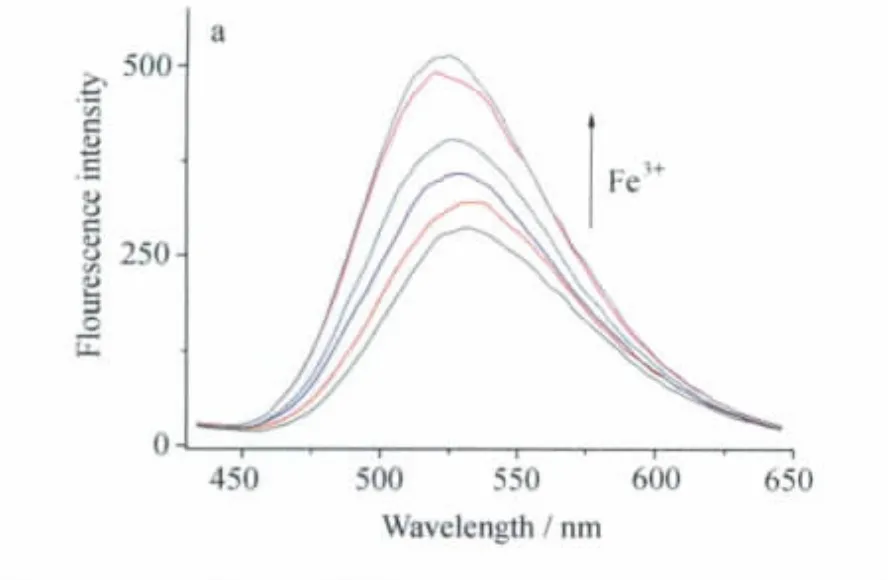
图9 FS对不同浓度的Fe3+滴定曲线Fluorescence spectra of FSin the presence of increasing concentrations of Fe3+
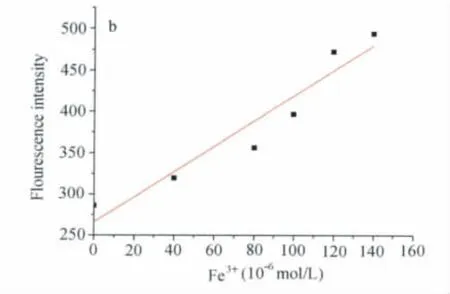
图10 FS荧光强度与Fe3+浓度的曲线The integrate fluorescence intensity of FS as a function of Fe3+ion concentration
3 结论
以萘酰亚胺作为荧光团,通过哌嗪与N-2-氯乙酰氨基喹啉(受体)反应得到基于PET原理的荧光增强型 (turn-on)Fe3+探针,此 探针能在pH6.0~12.0范围内保持荧光强度不变,而且能选择性识别溶液中的Fe3+,具有良好的选择性和灵敏性。同时将NPAP硅烷化修饰后,共价键联到硅胶颗粒上得到荧光增强型Fe3+传感材料FS,且在20~140μmol/L Fe3+离子含量范围内,FS的荧光强度与Fe3+离子浓度呈良好的线性关系(R2= 0.9023)。
[1] Que E L,Domaille D W,Chang C J.Metals in neurobiology:probing their chemistry and biology with molecular imaging[J].Chemical Reviews,2008,108(5):1517-1549.
[2] Singh N,Kaur N,Callan J.Incorporation of siderophore binding sites in a dipodal fluorescent sensor for Fe(Ⅲ)[J].Journal of Fluorescence,2009,19(4):649-654.
[3] Fakih S,Podinovskaia M,Kong X,Schaible U E,Collins H L,Hider R C.Monitoring intracellular labile iron pools:a novel fluorescent iron(Ⅲ)sensor as a potential non-invasive diagnosis tool[J].Journal of Pharmaceutical Sciences,2009,98(6):2212-2226.
[4] Liu S D,Zhang L W,Liu X.A highly sensitive and selective fluorescent probe for Fe3+based on 2-(2-hydroxyphenyl)benzothiazole[J].New Journal of Chemistry,2013,37(3):821-826.
[5] Ghosh K,Rathi S,Kushwaha R.Sensing of Fe(Ⅲ)ion via turn-on fluorescence by fluorescence probes derived from 1-naphthylamine[J].Tetrahedron Letters,2013,54(48):6460-6463.
[6] Chung P,Liu S R,Wang H F,Wu S P.A pyrene-based highly selective turn-on fluorescent chemosensor for iron(Ⅲ)ions and its application in living cell imaging[J].Journal of Fluorescence,2013,23(6):1139-1145.
[7] Wolf C,Mei X,Rokadia H K.Selective detection of Fe(Ⅲ)ions in aqueous solution with a 1,8-diac ridylnaphthalenederived fluorosensor[J].Tetrahedron Letters,2004,45(42):7867-7871.
[8] Xiang Y,Tong A.A New Rhodamine-based chemosensor exhibiting selective Fe(Ⅲ)-amplified fluorescence[J].Organic Letters,2006,8(8):1549-1552.
[9] Mao J,Wang L,Dou W,Tang X,Yan Y,Liu W.Tuning the selectivity of two chemosensors to Fe(Ⅲ)and Cr(Ⅲ)[J].Organic Letters,2007,9(22):4567-4570.
[10] 时丽丽 孙欢鹤,尚卓镔,王 煜.1,8-二(2-羟乙基)亚氨基蒽醌荧光探针用于Fe(Ⅲ)的高选择性测定[J].影像科学与光化学,2013,31(2):132-139.
Shi L L,Sun H H,Shang Z B,Wang Y.Highly selective fluorescent sensing of Fe3+by a new anthraquinone derivative 1,8-bis(2-hydroxyethylimino)anthraquinone [J].Imaging Science and Photochemistry,2013,31(2):132-139.
[11] He C,Zhu W,Xu Y,Chen T,Qian X.Trace mercury(Ⅱ)detection and separation in serum and water samples using a reusable bifunctional fluorescent sensor[J].Analytica Chimica Acta,2009,651(2):227-233.
[12] Jia L,Zhang Y,Guo X,Qian X.A novel chromatism switcher with double receptors selectively for Ag+in neutral aqueous solution:4,5-diaminoalkeneamino-N-alkyl-l,8-naphthalimides[J].Tetrahedron Letters,2004,45(20):3969-3973.
[13] Guo X,Qian X,Jia L.A highly selective and sensitive fluorescent chemosensor for Hg2+in neutral buffer aqueous solution[J].Journal of the American Chemical Society,2004,126(8):2272-2273.
[14] Greenfield S R,Svec W A,Gosztola D,Wasielewski M R.Multistep photochemical charge separation in rod-like molecules based on aromatic imides and diimides[J].Journal of the A-merican Chemical Society,1996,118(28):6767-6777.
[15] de Silva A P,Gunaratne H Q N,Habib-Jiwan J-L,McCoy C P,Rice T E,Soumillion J-P.New fluorescent model compounds for the study of photoinduced electron transfer:the influence of a molecular electric field in the excited state[J].Angewandte Chemie International Edition,1995,34(16):1728-1731.
[16] Zhang Y,Guo X,Si W,Jia L,Qian X.Ratiometric and water-soluble fluorescent zinc sensor of carboxamidoquinoline with an alkoxyethylamino chain as receptor[J].Organic Letters,2008,10(3):473-476.

