多孔磷酸三钙修复腔隙性骨缺损 38 例随访研究
许宋锋 徐明 于秀淳 孙玉玺 杨阳 苏情 胡睿 翟永飞 卢建熙
多孔磷酸三钙修复腔隙性骨缺损 38 例随访研究
许宋锋 徐明 于秀淳 孙玉玺 杨阳 苏情 胡睿 翟永飞 卢建熙
目的报告多孔磷酸三钙 ( tricalcium phosphate,TCP ) 治疗 38 例腔隙性骨缺损患者至少随访 2 年的临床效果。方法2008 年 3 月至 2011 年 9 月,对 38 例腔隙性骨缺损患者采用多孔磷酸三钙填充修复,男 22 例,女 16 例。年龄 3~58 岁,平均 23 岁。缺损范围最小 0.72 cm3,最大 151.88 cm3,平均35.62 cm3。随访 25~65 个月,平均 41 个月。采用在体 TCP 人工骨降解的 X 线片并图像分析软件分析植骨区灰度变化,计算材料降解率,动态观察多孔磷酸三钙人工骨降解情况。结果所有患者术后未见任何过敏或毒性反应。随时间延长,人工骨材料逐渐降解,新骨逐渐形成,以术后 1 年内降解速度最快。患者年龄越小( <16 岁 )、肿瘤体积越小 ( <10 cm3),新骨成骨、材料降解速度越快。结论多孔磷酸三钙人工骨可以用作良性或侵袭性骨肿瘤骨缺损的修复,平均随访 41 个月,疗效满意。
磷酸钙类;骨疾病;修复外科手术;生物医学研究
随着 β-磷酸三钙 ( β-TCP ) 生物陶瓷研究的深入,它的成骨及降解效应被得到肯定,近年来临床应用愈来愈广泛[1-2],可是缺少植入人体后的大样本长期临床研究。我们以往研究表明,多孔磷酸三钙人工骨可以用作骨肿瘤骨缺损的修复并取得满意早期临床疗效[3-4]。那么,其对于腔隙性骨缺损修复的长期疗效如何?2008 年以来,我科对 38 例腔隙性骨缺损采用多孔磷酸三钙填充修复,至少随访2 年,疗效满意。
资料与方法
一、一般资料
2008 年 3 月至 2011 年 9 月,我们对 38 例腔隙性骨缺损患者采用多孔磷酸三钙填充修复,其中男 22 例,女 16 例。年龄 3~58 岁,平均 23 岁。病变原因:内生软骨瘤 9 例,骨囊肿 6 例,死骨及炎性组织 6 例,骨纤维结构不良 5 例,非骨化性纤维瘤 3 例,嗜酸性肉芽肿 2 例,骨巨细胞瘤2 例,增生性纤维瘤 1 例,软骨母细胞瘤 1 例。病变部位:股骨 13 例,胫骨 11 例,指骨 4 例,肱骨 4 例,掌骨、腓骨、胸骨、桡骨、距骨、跟骨各1 例。缺损范围最小 0.72 cm3,最大 151.88 cm3,平均 35.62 cm3。随访 25~65 个月,平均 41 个月。术后观察患者全身及切口局部反应,复查随访时常规摄患部 DR-X 线平片,部分患者行 CT 扫描。术后常规抗生素治疗 24 h,个别延长至 48 h。引流液 24 h后<50 ml / 日即拔除引流管 ( 条 )。
二、手术方法
采用硬膜外或臂丛麻醉,1 例胸骨采用全麻。常规显露病变,开骨槽并彻底刮除肿瘤组织。瘤壁以电刀或苯酚彻底、广泛烧灼,注意避免苯酚外溢灼伤正常组织。生理盐水反复冲洗,纱布填塞瘤腔并彻底止血。以颗粒状多孔磷酸三钙填充,松散放置,不挤压。38 例中 2 例负重部位骨缺损范围较大的采用异体松质骨条+多孔 TCP 人工骨,1 例为右股骨骨巨细胞瘤术后复发 ( 缺损范围21 cm2),1 例为左股骨颈骨纤维结构不良 ( 缺损范围15 cm2)。其余均为单纯 TCP 人工骨填充。
多孔磷酸三钙生物陶瓷颗粒由上海贝奥路生物材料有限公司研制和生产[5-6],成分为 β-TCP,纯度>95%,直径 3~5 mm,孔隙率 ( 70±15 ) %,均匀分布球形孔径 500~600 μm,孔壁光滑,连接径110~120 μm,孔隙连通率>99% ( 图1 )。
三、疗效判定标准
通过 X 线进行磷酸钙人工骨的图像分析,半定量反映材料降解情况,间接反映新骨生成情况。分别于术前 1 周内、术后 l 个月、3 个月、6 个月、1 年、2 年、3 年行正位 X 线摄片,16 格区分法[7]并使用图像分析软件 Imagetool V3.0 ( UTHSCSA,USA ) 分析植骨区灰度变化,计算材料降解率,动态观察多孔磷酸三钙人工骨降解情况。半定量评定标准 ( 5 分法 )[7]具体为:“一”材料边界和内部结构清晰易辨;“+”材料边界模糊,但内部结构易辨;“++”材料边界和内部结构模糊,结构较难辨认;“+++”材料内部结构无法辨认,但材料痕迹存在;“++++”材料痕迹消失,与周围结构融合。
28 例序列影像资料完整的患者进行图像半定量分析,其中 3 例超过 2 年但是不足 3 年。按年龄分为<16 岁组 ( 10 例 ) 和>16 岁组 ( 18 例 ),按肿瘤体积分为<10 cm3组 ( 16 例 ) 和>10 cm3组( 12 例 )。
结 果
所有患者术后未见任何过敏或毒性反应,无皮疹或高热,无瘙痒或红肿,术前和术后 1~2 周内的血钙、磷水平未见明显升高,伤口均 I 期愈合。X 线片显示人工骨与宿主骨贴合紧密无间隙,随时间推移,骨缺损处材料逐渐降解,骨小梁形态逐渐形成,解剖形状大部分或全部恢复。
总体观察 ( 表1 ) ( 图2 ),术后 3 个月约一半人工骨降解 ( 51.89% ),同时新骨形成;术后 6 个月,人工骨残余约 1 / 4,新骨小梁形成 ( 图3~6 );术后1 年骨小梁塑形满意,仍有人工骨存在 ( 87.78% ),多数出现硬化骨 ( 图3~6 );术后 2~3 年甚至5 年,人工骨未完全降解 ( 96.48%~99.04% ),但患者功能正常 ( 图3~4 )。说明随时间延长,人工骨材料逐渐降解,新骨逐渐形成,以术后 1 年新骨成骨、材料降解速度最快。
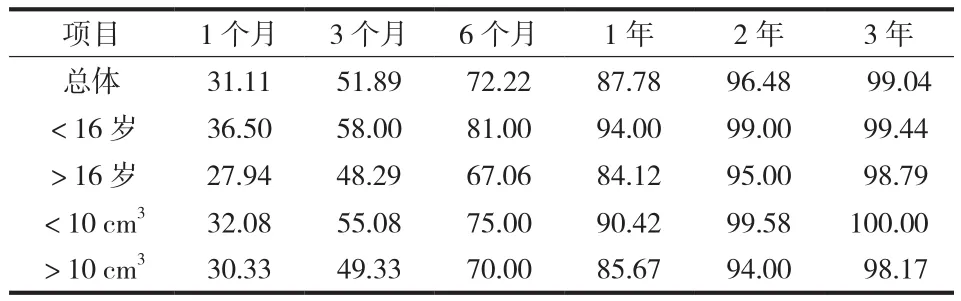
表1 不同随访时间各组影像学评分“++++”所占百分比 ( % )Tab.1 The percentage of “++++” in different groups at various follow-up points ( % )
年龄<16 岁组新骨成骨、材料降解速度明显高于>16 岁组,差异有统计学意义 ( P<0.05 ),术后1 个月至 12 个月最明显 ( P<0.01 )。说明年龄越小,新骨成骨、材料降解速度越快,新骨塑形时间越短,功能恢复越快。
体积<10 cm3组新骨成骨、材料降解速度明显高于>10 cm3组,差异有统计学意义 ( P<0.05 ),术后 3 个月至 12 个月最明显 ( P<0.01 )。说明肿瘤体积越小,新骨成骨、材料降解速度越快,新骨塑形时间越短,功能恢复越快。
术后 1 年部分病例随访出现骨硬化现象 ( 图3~5 ),可能由于人工骨材料没有完全降解,而新骨形成满意,导致局部密度增高。随时间进一步延续,人工骨材料进一步降解 ( 速度慢于术后 1 年内 ),新骨进一步塑形,恢复原有骨小梁结构及髓腔再通。
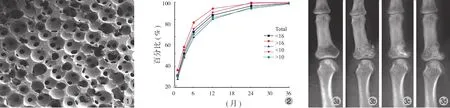
图 1 扫描电子显微镜观察 β-TCP 多孔生物陶瓷微结构 ( ×400 )图 2 总体及分年龄组 ( 16 岁 )、体积 ( 10 cm3) 半定量分析曲线图图 3 患者,男,43 岁,左小指指骨内生软骨瘤,肿瘤体积 0.72 cm33a:术前 X 线片见左小指植骨低密度病变;3b:术后 1 个月 X 线片见材料填充满意;3c:术后 1 年材料完全降解,局部硬化骨形成;3d:术后 5 年新骨骨小梁形成,硬化骨消失Fig.1 The microstructure of porous β-TCP bioactive ceramic was observed with scanning electronic microscope ( ×400 )Fig.2 The diagram of semi-quantitive radiographic analyzing in total, in different age groups ( 16 years ) and in different volume groups ( 10 cm3)Fig.3 A 43-year-old male patient was diagnosed as phalanx enchondroma in the left little fnger, and the tumor volume was 0.72 cm3 3a: The preoperative X-ray showed low density lesion in the phalange of the left little fnger; 3b: The X-ray at 1 month after the operation showed TCP was flled into the defect; 3c: At 1 year after the operation, TCP was fully degraded with local sclerotic bone formation; 3d: At 5 years after the operation, trabecular bone formation was observed with the disappearance of sclerotic bone
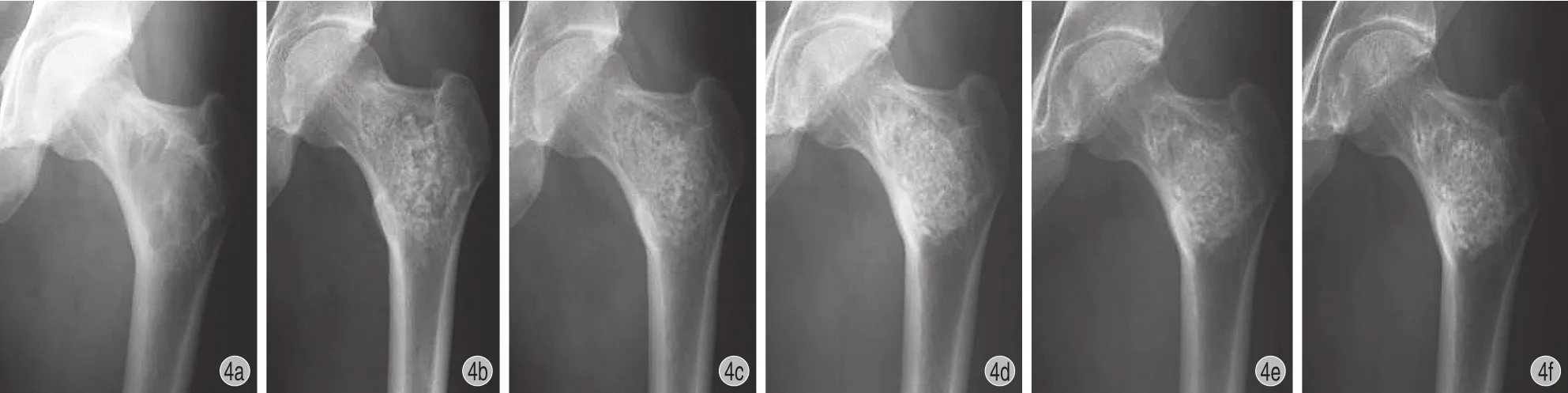
图 4 患者,男,37 岁,左股骨近端骨囊肿,肿瘤体积 49.35 cm34a:术前 X 线片见左股骨粗隆间边界清楚的溶骨性病变;4b~4c:术后 5 天及术后 3 个月 X 线片见材料填充满意;4d:术后 1 年新骨骨小梁塑形,出现硬化骨,TCP 仍存在;4e~4f:术后 2 年、3 年,股骨颈、粗隆部骨小梁力线结构清晰正常,TCP 未完全降解Fig.4 A 37-year-old male patient was diagnosed as bone cyst in the left proximal femur, and the tumor volume was 49.35 cm3 4a: The preoperative X-ray showed osteolytic lesion with a clear border in the left femoral trochanter; 4b-4c: The X-rays at 5 days and 3 months after the operation showed TCP was flled into the defect; 4d: At 1 year after the operation, the new trabecular bone remodeling and local sclerotic bone formation were observed, with the existence of TCP; 4e-4f: At 2 and 3 years after the operation, the normal bone trabecula was observed in the femoral neck and trochanter. TCP had not been fully degradedtrabecular bone formation was observed with the disappearance of sclerotic bone
讨 论
骨肿瘤病灶清除术后形成的骨缺损是骨科治疗的一个难题。理想的人工骨修复材料应具有良好的生物相容性,能有效充当新骨形成的支架,在体内逐渐生物降解并被新生骨组织替代。植骨一般分为结构植骨和填充植骨。对于无机陶瓷材料,弹性模量高,力学强度较差,更适合于结构植骨,即为骨髓干细胞提供暂时性支架结构,利于细胞贴附,随新生骨组织逐渐形成,支架结构逐渐降解。同以往研究类似,多孔 TCP 主要充当新骨形成的支架,发挥骨传导作用完成骨缺损修复[8]。我们发现,术后X 线片多孔 TCP 颗粒间有间隙,部分材料甚至远离缺损部位。但是,术后随访发现仍然取得良好骨修复效果,游离的 TCP 逐渐降解消失 ( 图3 ),进一步提示本研究所采用多孔 TCP 人工骨具有良好生物降解性。Lu 等[5]的研究指出,TCP 降解性优于 CPC,因为其降解主要依靠生理溶液溶解而不是 CPC 依赖的细胞介导降解。我们认为手术中应当将多孔 TCP人工骨松散放置,不要施加任何挤压力,更不能像对待自体骨和异体骨那样打压植骨,因为 β-TCP 生物陶瓷的带有内连接的多孔微结构是其成骨及降解的必备微环境条件,而打压植骨则破坏了人工骨的微结构,使其成骨及降解过程完成缓慢。因此,结构比材料本身更重要。
对于骨缺损的修复,要在对骨组织形成和再生过程充分认识的基础上,不仅仅是植入新的空间结构,更重要的是骨缺损部位形成新的功能性骨组织[9]。近年来,除了传统自体骨和异体骨,生物陶瓷材料逐渐应用于临床骨缺损修复,主要包括磷酸三钙 ( tricalcium phosphate,TCP )、羟基磷灰石 ( hydroxyapatite,HA ) 和自固化磷酸钙 ( calciun phosphate cement,CPC )。CPC 已作为骨替代物用于骨肿瘤骨缺损的修复,取得了优于 HA 的临床效果[10-11]。Lu 等[5]的研究指出,TCP 较 CPC、HA 具有更好的降解性和成骨效果。本组研究表明,随时间延长,TCP 人工骨材料逐渐降解,新骨逐渐形成,以术后 1 年内降解速度最快。患者年龄越小(<16 岁 )、肿瘤体积越小 (<10 cm3),新骨成骨、材料降解速度越快。
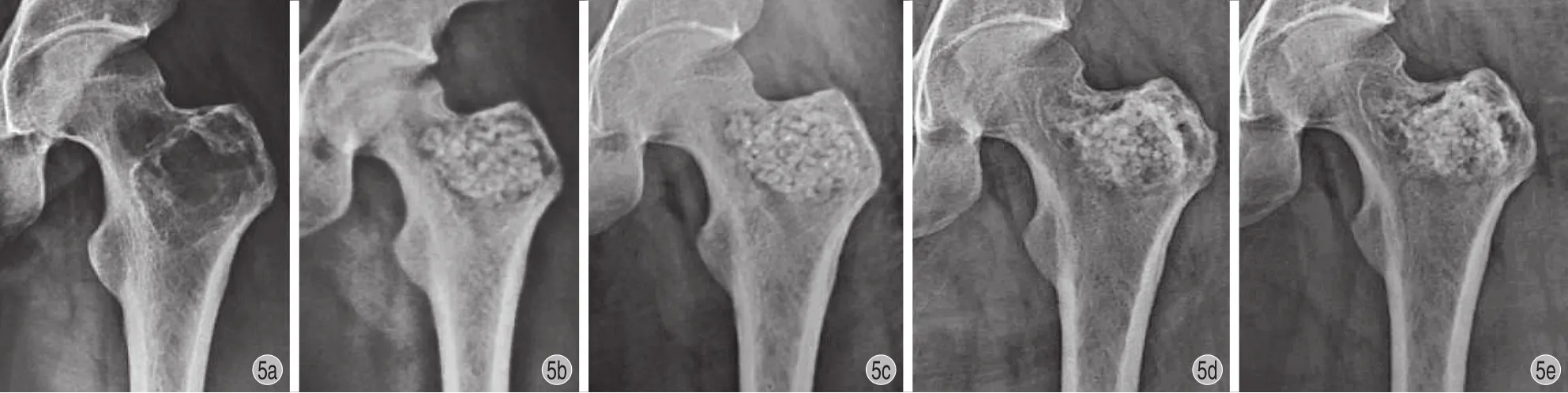
图 5 患者,男,22 岁,右股骨粗隆软骨母细胞瘤,肿瘤体积 47.73 cm35a:术前 X 线片见右股骨粗隆间边界清楚的溶骨性病变;5b~5c:术后 4 天及术后 1 个月 X 线片见材料填充满意;5d:TCP 长期存在,但患者功能在术后 6 个月恢复正常;5e:术后 1 年仍可观察到 TCP 存在,但功能无异常Fig.5 A 22-year-old male patient was diagnosed as chondroblastoma in the right femoral trochanter, and the tumor volume was 47.73 cm3 5a: The preoperative X-ray showed osteolytic lesion with a clear border in the right femoral trochanter; 5b-5c: The X-rays at 4 days and 1 month after the operation showed TCP was flled into the defect; 5d: The limb function of the patient was restored normally at 6 months after the operation, with the long-term existence of TCP; 5e: At 1 year after the operation, the limb function of the patient was still in normal condition, and TCP could still be observed
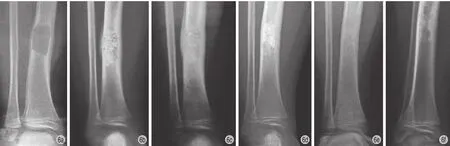
图 6 患者,男,4 岁,右胫骨下段骨囊肿,肿瘤体积 10.08 cm36a:术前 X 线片见右胫骨下段边界清楚的溶骨性病变;6b~6c:术后3 天及术后 1 个月 X 线片见材料填充满意;6d:术后 3 个月观察到骨性愈合;6e:术后 1 年出现硬化骨,髓腔开始再通;6f:术后 3 年材料完全消失,髓腔再通满意Fig.6 A 4-year-old male patient was diagnosed as bone cyst in the right distal tibia, and the tumor volume was 10.08 cm3 6a: The preoperative X-ray showed osteolytic lesion with a clear border in the right distal tibia; 6b-6c: The X-rays at 3 days and 1 month after the operation showed TCP was flled into the defect; 6d: At 3 months after the operation, bony healing was observed; 6e: At 1 year after the operation, the medullar cavity was reformed, with local sclerotic bone formation; 6f: At 3 years after the operation, good medullar cavity reformation was observed, with fully disappearance of the TCP
我们认为,对于上肢 ( 如肱骨、指骨等 ) 及不负重部位 ( 如胸骨等 ) 的骨缺损,可以采用单纯多孔 TCP 填充修复 ( 图3 )。对于脊柱、下肢等负重部位,应当使用内固定钢板或适当选用自体骨、异体骨做辅助支撑。以往临床研究也采用多孔 TCP 人工骨与自体骨、异体骨混合用于大范围骨缺损的修复[8]。Jiang 等[12]采用本研究使用的多孔 TCP+内固定钢板治疗跟骨骨折,优良率 91.9%。Dai 等[13]将本研究使用的多孔 TCP+融合笼用于颈前路椎体间融合,随访 2 年,影像融合率 100%。同样用于腰椎后外侧融合,随访 3 年,影像融合率 100%[14],而自体骨组均出现取骨处疼痛现象。因此,本研究采用的多孔 TCP 在脊柱、下肢等负重部位骨肿瘤骨缺损修复中也应当具有良好的骨缺损修复效果。
多孔 β-TCP 人工骨颗粒作为一种新型的生物可控性微结构的骨植入修复材料,具有良好的生物相容性、可降解性、骨传导性等优点,可以取代同种异体骨作为修复骨腔隙性缺损的植骨材料。我们临床长期随访表明,虽然存在生物力学强度差、支撑力不够等不足,多孔磷酸三钙修复腔隙性骨缺损的成骨能力确切、降解速度可靠。本研究仅为单中心临床回顾性研究,尚需进行前瞻性多中心、随机对照临床研究,更客观的评价此材料的临床应用价值。
[1] 桑宏勋. 多孔TCP人工骨修复肿瘤性骨缺损的临床效果与骨愈合机制探讨. 中国修复重建外科杂志, 2008, 22(4): 463-467.
[2] 史定伟. β-TCP 植入人体骨缺损后的组织学观察. 生物骨科材料与临床研究, 2008, 5(3):8-10.
[3] 许宋锋, 于秀淳, 徐明. 多孔磷酸三钙修复良性骨肿瘤骨缺损的临床研究. 生物骨科材料与临床研究, 2011, 8(03):10-13.
[4] 翟永飞. 胸骨内生软骨瘤一例报告. 中国骨肿瘤骨病, 2011, 10(2):209-210.
[5] Lu J, Descamps M, Dejou J, et al. The biodegradation mechanism of calcium phosphate biomaterials in bone. Journal of Biomedical Materials Research, 2002, 63(4):408-412.
[6] Lu JX, Flautre B, Anselme K, et al. Role of interconnections in porous bioceramics on bone recolonization in vitro and in vivo. Journal of Materials Science, 1999, 10(2):111-120.
[7] Sang H, Wang Z, Guo Z, et al. Clinical results and the mechanism of bone healing for the repair of bone defects due to tumor resection with novel interporous TCP. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi, 2008, 22(4):463-467.
[8] 郑启新, 杜靖远. 多孔磷酸三钙陶瓷人工骨修复儿童骨缺损.中华小儿外科杂志, 1996, 17(2):70-72.
[9] Kneser U, Schaefer DJ, Polykandriotis E, et al. Tissue engineering of bone: the reconstructive surgeon’s point of view. J Cell Mol Med, 2006, 10(1):7-19.
[10] Yajima H, Murata K, Kawamura K, et al. Treatment of intraosseous ganglia and bone cysts of the carpal bones with injectable calcium phosphate bone cement. Hand Surg, 2008, 13(3):167-173.
[11] Matsumine A, Kusuzaki K, Matsubara T, et al. Calcium phosphate cement in musculoskeletal tumor surgery. Journal of Surgical Oncology, 2006, 93(3):212-220.
[12] Jiang SD, Jiang LS, Dai LY. Surgical treatment of calcaneal fractures with use of β-tricalcium phosphate ceramic grafting. Foot & Ankle International, 2008, 29(10):1015-1019.
[13] Dai LY, Jiang LS. Anterior cervical fusion with interbody cage containing beta-tricalcium phosphate augmented with plate fxation: a prospective randomized study with 2-year follow-up. Eur Spine J, 2008, 17(5):698-705.
[14] Dai LY, Jiang LS. Single-level instrumented posterolateral fusion of lumbar spine with beta-tricalcium phosphate versus autograft: a prospective, randomized study with 3-year followup. Spine, 2008, 33(12):1299-1304.
( 本文编辑:王永刚 )
2014 Spinendos 国际经皮脊柱内镜学术研讨会通知
由中国康复医学会脊柱脊髓损伤专业委员会微创脊柱外科学组、《中国骨与关节杂志》编辑部、卫计委内镜与微创医师定期考核培训学校与中国人民解放军总医院第一附属医院全军骨科研究所联合主办的“2014 Spinendos国际经皮脊柱内镜学术研讨会”,定于 2014 年 5 月 9~11 日在北京举行。侯树勋医师作为本次研讨会的主席,诚挚地邀请各位同仁前来参加本次研讨会。
此次研讨会将邀请德国著名的经皮脊柱内镜专家Stefan Hellinger 医师出席会议,同时也邀请到众多国内著名的经皮脊柱内镜专家出席本次研讨会并作精彩的发言。本次研讨会将以尸体操作培训、手术演示和病例讨论的方式来介绍当前经皮脊柱内镜技术的手术方法、适应证和并发症。从临床实用角度,结合临床疑难病例,现场互动讨论,欢迎大家提供病例,进行讨论。
联系人及方式:连伟 13581626681
http: //www.spinendos.com.cn
Email: spinendos@163.com
Porous tricalcium phosphate for the repair of lacunar bone defects: a follow-up report of 38 cases
XU Songfeng, XU Ming, YU Xiu-chun, SUN Yu-xi, YANG Yang, SU Qing, HU Rui, ZHAI Yong-fei, LU Jian-xi. Department of Orthopedics, General Hospital of Jinan Military Region, Jinan, Shandong, 250031, PRC
ObjectiveTo assess the over-2-year clinical outcomes of porous tricalcium phosphate ( TCP ) for the repair of lacunar bone defects.MethodsA total of 38 patients with lacunar bone defects underwent the repair with porous TCP from March 2008 to September 2011, including 22 males and 16 females, whose average age was 23 years old ( range; 3-58 years ). Tumor sizes varied from 0.72 cm3to 151.88 cm3, with the average size of 35.62 cm3. All patients were followed up for a mean period of 41 months ( range; 25-65 months ). The in vivo biodegradation rate of the implanted TCP was evaluated based on the radiographic analyzing method. The gray scale change of the grafting area in plain X-ray images was used to assess the degradation of porous TCP.ResultsThere was neither signifcant reverse reaction to the transplanted material nor locally infammatory reaction in all of the cases. Bone defects were repaired gradually, in company with the degradation of TCP materials and the formation of new bone. The rates of TCP degradation and new bone formation were fastest in the frst year postoperatively. The younger the patients were ( <16 years old ) and the smaller the tumor size was ( <10 cm3), the faster the rates were.ConclusionsThe porous TCP is an ideal material for the repair of lacunar bone defects caused by benign or invasive tumors, and the over-2-year follow-up results are satisfactory .
Calcium phosphates; Bone diseases; Reconstructive surgical procedures; Biomedical research
10.3969/j.issn.2095-252X.2014.04.010
R738.1
250031 济南军区总医院骨病科 ( 许宋锋,徐明,于秀淳,孙玉玺,杨阳,苏情,胡睿,翟永飞 );200335 上海贝奥路生物材料有限公司 ( 卢建熙 )
于秀淳,Email: yxch48@vip.sina.com
2013-10-27 )

