坐珠达西组分的定性鉴别研究
董红娇, 曾锐
(西南民族大学民族医药研究院, 四川 成都 610041)
坐珠达西组分的定性鉴别研究
董红娇, 曾锐
(西南民族大学民族医药研究院, 四川 成都 610041)
目的: 提高坐珠达西品种的质量标准.方法: 采用薄层色谱法, 以对照品、对照药材为对照, 对藏药坐珠达西中诃子、余甘子、石榴子、安息香、木香、丁香、藏木香、藏红花、牛黄、熊胆、甘青青兰及荜茇共12味药材进行了定性鉴别, 并采用HPLC法对坐珠达西味药中的西红花苷Ⅰ、西红花苷Ⅱ、绿原酸以及山奈酚, 以Kromasil C18色谱柱(4.6mm×250mm, 5µm)流动相甲醇-0.05%磷酸溶液, 梯度洗脱, 流速1mL·min-1, 西红花苷Ⅰ和西红花苷Ⅱ检测波长为455nm, 绿原酸检测波长为352nm, 山奈酚检测波长为225nm, 进行定性鉴别.结果: 在与对照品或对照药材相应的位置上, 供试品显现相同斑点, 且在HPLC中西红花苷Ⅱ对坐珠达西的质量贡献尤为明显.结论: 该鉴别方法分离度良好,准确可靠, 可用于藏药坐珠达西的质量标准研究.
坐珠达西; 西红花苷Ⅰ;西红花苷Ⅱ; 绿原酸; 山奈酚
藏药坐珠达西由诃子、余甘子、石榴子、安息香、红花等35味药物组成, 具有疏肝、健胃、清热、愈溃疡、消肿等功效, 主要用于治疗“木布”病迁延不愈、胃脘嘈杂、消化不良、浮肿、水肿等症, 为藏药治疗慢性胃炎的常用药物.薄层色谱鉴别法是一种通过供试品与对照品或对照药材在相应位置显示相同斑点, 来定性鉴别某种药物有无的一种检验方法, 具有操作简便、准确快捷等特点, 广泛用于药物的区分鉴别.为保证药物疗效, 本课题通过查阅相关资料, 最终对坐珠达西方中具有明显抗胃炎的木香、安息香等, 及贵重药物牛黄、熊胆等共12味药物进行了系统的定性鉴别, 并对藏红花中的西红花苷Ⅰ、西红花苷Ⅱ、绿原酸以及山奈酚采用高效液相方法进行了定性鉴别.
1 仪器与试药
1.1 仪器
ZF1-Ⅱ紫外分析仪(上海嘉腾科技有限公司); 硅胶G、GF254、H(青岛海洋化工厂分厂), 聚酰胺薄膜(浙江省台州市路桥四甲生化塑料厂出品); Waters 2695/2996型高效液相色谱仪, 2996PDA检测器, Empower化学工作站.
1.2 试药
没食子酸(批号:111109, 四川省维克奇生物科技有限, HPLC≥98%), 苯甲酸(批号:120807, 四川省维克奇生物科技有限, HPLC≥98%), 木香烃内酯(批号:120322, 四川省维克奇生物科技有限, HPLC≥98%), 去氢木香烃内酯(批号:120321, 四川省维克奇生物科技有限, HPLC≥98%), 齐墩果酸(批号:MUST-13041606, 成都曼思特生物科技有限公司/中国科学院成都生物研究所, HPLC≥98%), 胡椒碱(批号:130829, 成都普菲德生物技术有限公司, HPLC≥98%)对照品; 坐珠达西供试品(批号:20120618, 四川阿坝州藏医院藏医药研究所制); 西红花苷Ⅰ(批号:120714, 纯度≥98.0%), 西红花苷Ⅱ(批号:110925, 纯度≥98.0%)对照品(四川省维克奇生物科技有限);绿原酸(批号:121125, 纯度≥98.0%), 山奈酚(批号:120718, 纯度≥98.0%).
2.1 诃子、余甘子、石榴子的薄层鉴别
2.1.1 供试品溶液制备
取坐珠达西丸剂, 研磨成分, 取粉末0.5g, 加甲醇10mL, 超声20min, 滤过, 水浴挥杆溶剂, 加1mL乙醇溶解, 为供试品溶液.
2.1.2 对照品溶液制备
取没食子酸对照品0.5mg, 加乙醇制成1mg·mL-1的溶液, 作为对照品溶液.
2.1.3 对照药材溶液制备
取诃子、余甘子、石榴子药材粉末2g, 按2.1.1项下方法制得对照药材溶液.
2.1.4 阴性样品溶液
按样品处方配比, 称取不含诃子、余甘子、石榴子的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂,按2.1.1项下方法制成阴性样品溶液.
2.1.5 薄层鉴别及结果
参照文献[1-5], 将上述供试品溶液, 对照品溶液, 对照药材溶液, 阴性样品溶液各约吸取5µL, 分别点于同一聚酰胺薄层板上, 以乙酸乙酯-甲酸(3:1)为展开剂, 上行展开一次, 取出, 晾干, 喷以2%三氯化铁乙醇溶液, 日光下检视, 斑点呈蓝色; 在与对照品, 对照药材相应的位置上, 供试品色谱均显示相同颜色的斑点, 结果见图1.
2.2 安息香的薄层鉴别
2.2.1 供试品溶液制备
取坐珠达西丸剂, 研磨成分, 取粉末0.5g, 加甲醇4mL, 超声5min, 滤过, 取滤液作为供试品溶液.
2.2.2 对照品溶液制备
称取苯甲酸对照品, 加甲醇制成4mg·mL-1的溶液, 作为对照品溶液.
2.2.3 对照药材溶液制备
取安息香药材粉末0.5g, 按2.2.1项下方法制得对照药材溶液.
2.2.4 阴性样品溶液
按样品处方配比, 称取不含安息香的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂, 按2.2.1项下方法制成阴性样品溶液.
2.2.5 薄层鉴别及结果
依照药典中薄层色谱法[6], 将以上供试品溶液、对照品溶液、对照药材溶液、阴性样品溶液各约吸取5µL, 分别点于同一硅胶GF254薄层板上, 以石油醚(60-90℃)-正己烷-乙酸乙酯-冰醋酸(6:4:3:0.5)为展开剂, 取出, 晾干,以紫外灯(254nm)下检视;在与对照品, 对照药材相应的位置上, 供试品色谱均显示相同颜色的斑点, 结果见图2.
2.3 木香的薄层鉴别
2.3.1 供试品溶液制备
取坐珠达西丸剂, 研磨成分, 取粉末0.5g, 加氯仿10mL, 超声30min, 取上清液为供试品溶液.
2.3.2 对照品溶液制备
取木香烃内酯和去氢木香烃内酯对照品, 分别加氯仿制成0.5mg·mL-1的溶液, 作为对照品溶液.
2.3.3 阴性样品溶液
按样品处方配比, 称取不含木香的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂, 按2.5.1项下方法制成阴性样品溶液.
2.3.4 对照药材溶液制备
取木香药材粉末0.5g, 按2.3.1项下方法制得对照药材溶液.
2.3.5 薄层鉴别及结果
参照文献[7-8], 将上述供试品溶液, 对照品溶液, 对照药材溶液, 阴性样品溶液各约吸取5µL, 分别点于同一硅胶G薄层板上, 以氯仿-环己烷(9:1)为展开剂, 展开, 取出, 晾干, 喷以1%香草醛硫酸溶液, 105℃加热至斑点显色清晰; 木香普通薄层鉴别在与对照品相应的位置上, 供试品色谱显示相同颜色的斑点, 结果见图3.

图1 诃子、余甘子、石榴子薄层图谱Fig.1 TLC chromatogram of myroblan, emblic leafflowerfruit, pomegranate seed

图2 安息香薄层图谱Fig.2 TLC chromatogram of benzoin
2.4 丁香的薄层鉴别
2.4.1 供试品溶液制备 取坐珠达西丸剂, 研磨成分, 取粉末0.5g, 加无乙醚5mL, 振摇数分钟, 过滤, 滤液作为供试品溶液.
2.4.2 阴性样品溶液 按样品处方配比, 称取不含丁香的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂,按2.9.1项下方法制成阴性样品溶液.
2.4.3 薄层鉴别及结果 依照药典中薄层色谱法, 将上述供试品溶液, 对照药材溶液, 阴性样品溶液各约吸取5µL, 分别点于同一硅胶G薄层板上, 以石油醚-乙酸乙酯(9:1)为展开剂, 展开, 取出, 晾干, 喷以5%香草醛硫酸溶液,105℃加热至斑点显色清晰; 在与对照药材相应的位置上, 供试品色谱中均显相同颜色的斑点, 结果见图4.
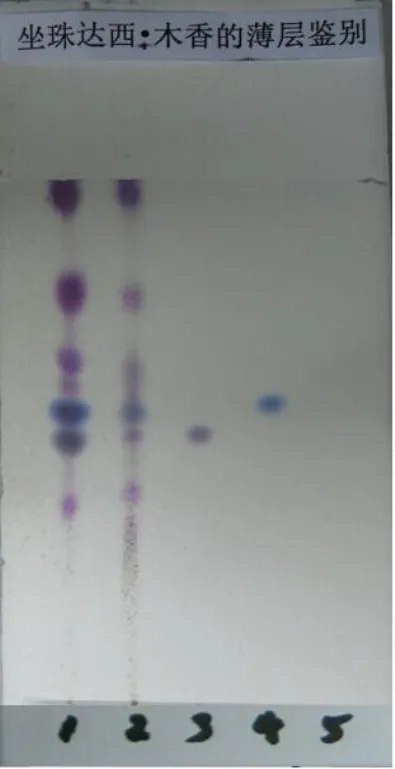
图3 木香薄层图谱Fig.3 TLC chromatogram of elecampane

图4 丁香薄层图谱Fig.4 TLC chromatogram of dove
2.5 藏木香的薄层鉴别
2.5.1 供试品溶液制备
取坐珠达西丸剂, 研磨成分, 取粉末0.5g, 加氯仿25mL, 超声30min, 过滤, 滤液浓缩至2mL,作为供试品溶液.
2.5.2 对照品溶液制备
取土木香内酯和异土木香内酯对照品, 分别加氯仿制成1mg·mL-1的溶液, 作为对照品溶液.
2.5.3 阴性样品溶液
按样品处方配比, 称取不含藏木香的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂, 按2.6.1项下方法制成阴性样品溶液.
2.5.4 薄层鉴别及结果
参照文献[9], 将上述供试品溶液, 对照品溶液, 对照药材溶液, 阴性样品溶液各约吸取5µL, 分别点于同一硅胶G薄层板上, 以石油醚(60-90℃)-乙酸乙酯(5:2)为展开剂, 展开, 取出, 晾干, 喷以5%香草醛硫酸溶液, 105℃加热至斑点显色清晰, 结果见图5.
2.6 藏红花的薄层鉴别
2.6.1 供试品溶液制备
取坐珠达西丸剂, 研磨成分, 取粉末0.5g, 加80%丙酮溶液5mL, 密塞, 振摇15min, 静置, 取上清液作为供试品溶液.
2.6.2 对照药材溶液制备
取藏红花对照药材0.5g, 按2.3.1项下方法配制, 吸取上清液1mL定容至10mL作为对照药材溶液.
2.6.3 阴性样品溶液制备
按样品处方配比, 称取不含藏红花的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂, 按2.3.1项下方法制成阴性样品溶液.
2.6.4 薄层鉴别及结果
依照药典中红花薄层色谱法, 将以上供试品溶液、对照药材溶液、阴性样品溶液各约吸取5µL, 分别点于同一硅胶H薄层板上, 以乙酸乙酯-甲酸-水-甲醇(7:2:3:0.4)为展开剂, 展开, 取出, 晾干.在与对照药材相应的位置上, 供试品中显相同颜色的斑点, 结果见图6.

图5 藏木香薄层鉴别图谱Fig.5 TLC chromatogram of Tibet inula root

图6 藏红花薄层鉴别图谱Fig.6 TLC chromatogram of saffron crocus
2.7 牛黄、熊胆的薄层鉴别
2.7.1 供试品溶液制备
取坐珠达西丸剂, 研磨成分, 取粉末2g, 加乙醇20mL, 超声10min, 滤过, 滤液蒸干, 残渣加10%氢氧化钠溶液20mL,置水浴上加热回流水解6h, 冷却, 滴加盐酸调节pH至2-3, 用乙酸乙酯萃取2次, 每次15mL, 合并乙酸乙酯溶液, 蒸干, 残渣加乙醇5mL使溶液, 静置, 取上清液作为供试品溶液.
2.7.2 对照品溶液制备
称取胆酸和去氧胆酸对照品, 各加乙醇制成1mg·mL-1的溶液, 作为对照品溶液.
2.7.3 阴性样品溶液
按样品处方配比, 称取不含牛黄、熊胆的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂, 按2.4.1项下方法制成阴性样品溶液.
2.7.4 薄层鉴别及结果
参照文献[10-11], 将上述供试品溶液、对照品溶液、阴性样品溶液各约吸取5µL, 分别点于同一硅胶G薄层板上, 以氯仿-甲醇-水(15:9:2)为展开剂, 上行展开, 取出, 晾干, 喷以10%硫酸乙醇溶液, 吹干, 日光下检视, 结果见图7、8.

图7 牛黄薄层鉴别图谱Fig.7 TLC chromatogram of bezoar

图8 熊胆薄层鉴别图谱 Fig.8 TLC chromatogram of felurs
2.8 甘青青兰的薄层鉴别
2.8.1 供试品溶液制备
取坐珠达西丸剂, 研磨成分, 取粉末1g, 加甲醇25mL, 超声30min, 过滤, 滤液浓缩至2mL,作为供试品溶液.
2.8.2 对照品溶液制备
取齐墩果酸对照品, 分别加甲醇制成1mg·mL-1的溶液, 作为对照品溶液.
2.8.3 阴性样品溶液
按样品处方配比, 称取不含甘青青兰的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂, 按2.7.1项下方法制成阴性样品溶液.
2.8.4 薄层鉴别及结果
参照文献[12], 将上述供试品溶液, 对照品溶液, 对照药材溶液, 阴性样品溶液各约吸取5µL, 分别点于同一硅胶G薄层板上, 以甲苯-乙酸乙酯-冰醋酸(14:4:0.5)为展开剂, 展开, 取出, 晾干, 喷以10%硫酸乙醇溶液, 105℃加热至斑点显色清晰, 结果见图9.
2.9 荜茇的薄层鉴别
2.9.1 供试品溶液制备
取坐珠达西丸剂, 研磨成分, 取粉末1g, 加无水乙醇25mL, 超声30min, 过滤, 滤液浓缩至2mL,作为供试品溶液.
2.9.2 对照品溶液制备
取胡椒碱对照品, 分别加无水乙醇制成1mg·mL-1的溶液, 作为对照品溶液.
2.9.3 阴性样品溶液
按样品处方配比, 称取不含荜茇的其他药材, 模拟生产工艺制成坐珠达西阴性对照丸剂, 按2.8.1项下方法制成阴性样品溶液.
2.9.4 薄层鉴别及结果
参照文献[13], 将上述供试品溶液, 对照品溶液, 对照药材溶液, 阴性样品溶液各约吸取5µL, 分别点于同一硅胶G薄层板上, 以甲苯-乙酸乙酯-丙酮(7:2:1)为展开剂, 展开, 取出, 晾干, 喷以10%硫酸乙醇溶液, 加热至斑点显色清晰, 结果见图10.

图9 甘青青兰薄层鉴别图谱Fig.9 TLC chromatogram of dracocephalum tanguticum maxim

图10 荜茇兰薄层鉴别图谱Fig.10 TLC chromatogram of fructus piperis longi
2.10 西红花苷Ⅰ、西红花苷Ⅱ绿原酸以及山奈酚的液相色谱鉴别[15]
2.10.1 色谱条件
Kromasil C18色谱柱(4.6×250mm,5µm); 流动相甲醇(A)-0.05%磷酸溶液(B),梯度洗脱, 0~8min, 13%~20%A; 8~20min, 20%~38%; 20~30min, 38%A~50%A; 30~45min, 50%A~70%A; 45~65min, 70%A~80%A; 流速为1mL·min-1; 柱温30℃; 进样量10µL; 西红花苷Ⅰ和西红花苷Ⅱ检测波长为455nm, 绿原酸检测波长为352nm,山奈酚检测波长为225nm.
2.10.2 对照品溶液的制备
取绿原酸、山萘酚适量, 精密称定, 加甲醇制成每1mL含1.102, 1.080 mg的溶液; 再取西红花苷I 、西红花苷II 适量, 精密称定, 加稀乙醇制成每1mL含1.070, 1.064mg的溶液, 即得各对照品溶液.分别精密吸取上述对照品溶液各1.3, 1.7, 0.5, 0.2mL于25mL量瓶中, 加甲醇定容至刻度, 即得混合对照品溶液.
2.10.3 供试品溶液的制备
取坐珠达西粉末1.0g, 精密称定, 置具塞锥形瓶中, 精密加入甲醇25mL, 密封, 称重, 超声提取30min.冷却至室温后称重, 用甲醇补足重量, 摇匀, 滤过, 取续滤液即得.
2.10.4 测定结果
取上述对照品溶液及供试品溶液, 按“2.10.1”项下色谱条件, 分别精密吸取对照品溶液、供试品溶液各10 μL,注入液相色谱仪, 测得液相色谱图, 结果见图11.结果表明, 西红花苷Ⅰ、西红花苷Ⅱ、绿原酸以及山奈酚的色谱峰分离良好.

图11 西红花苷Ⅰ、西红花苷Ⅱ、绿原酸以及山奈酚HPLC图谱Fig.11 HPLC chromatogram of Crocin Ⅰ, Crocin Ⅱ, Chlorogenic and Kaempferol
3 讨论
1) 坐珠达西收载于卫生部藏药部颁标准, 由于历史条件等限制, 原标准薄层鉴别只收录1味药物的鉴别.该药由32味药物组成, 其中诃子在藏药中被视为“药中之王”, 具有很好的解毒功效, 余甘子、石榴子、荜茇、甘青青兰、木香、藏木香、丁香、安息香等都对胃病具有很好的治疗效果或协同作用, 红花用来治疗肝、血病, 且与牛黄、熊胆同为贵重药物, 选取该12个药物作为检测对象, 从多方面考虑入手, 具有一定的科学意义.本实验首次对坐珠达西这一藏医临床常用特色治疗慢性胃病的仁青类药物进行了较系统的薄层鉴别方法研究, 检测指标多, 总药物数量的1/3, 可有效的控制坐珠达西的质量标准, 同时为质量标准中的含量测定, 成分鉴别等提供一定的参考依据.
2) 薄层色谱方法简便快捷, 成本低, 尤其便于在基层藏医院和研究所推广使用. 坐珠达西处方中多数药物的的薄层鉴别方法藏药部颁标准中并没有收载, 同时考虑诃子等药物在药典中的处理方法较为复杂, 故本次试验中在参考文献报道的基础上进行了优化研究, 进一步简化实验操作过程, 本方法具有在基层医疗和生产单位实际推广使用价值.
3) 本实验还对诃子、余甘子、石榴子、安息香、木香、丁香进行了薄层色谱的抗氧化鉴别, 但由于方法不成熟, 暂不列入标准正文.坐珠达西处方中西红花具有活血化瘀, 清热解毒, 解郁安神的作用, 为方中的主药且为贵重药材, 故本试验以西红花的主要有效成分西红花苷Ⅰ、西红花苷Ⅱ、绿原酸以及山奈酚为指标, 进行了定性鉴别.
[1]丁岗, 陆蕴如, 冀春茹, 等.诃子的薄层鉴别[J].北京中医药大学学报, 2001, 24(1): 45-46.
[2]卢平华, 严玉贞.诃子质量标准研究[J].中药新药与临床药理, 2002, 13(6): 385-388.
[3]李先瑞, 顾雪竹, 肖碧英, 等.绒毛诃子与诃子质量评价与比较[J].中国实验方剂学杂志, 2010, 16(17): 48-52.
[4]刘圆, 白志川, 于杰.藏药复方中余甘子和甘草及木香的薄层定性鉴别[J].西北农业大学学报: 自然科学版, 2004, 26(5): 625-628.
[5]杨成, 熊延靖, 刘辉.薄层色谱-自显影技术检测石榴皮清除自由基活性成分[J].皖南医学院学报, 2011, 30(4): 270-271.
[6]国家药典委员会.中国药典,Ⅰ部[S].北京: 化学工业出版社, 2010.
[7]王青山, 齐双虎, 包巴特尔, 等.蒙药中木香的薄层色谱鉴别研究[J].时珍国医国药杂志, 2001, 12(5): 430-431.
[8]李湘平, 袁檖樑, 李汶.薄层色谱法定性鉴别胃可舒片中的陈皮、甘草、木香[J].中国医药指南, 2014, 12(10): 51-52.
[9] 贡布东智, 交巴杰布.藏药制剂-西周卡策尔质量标准研究[J].中国社区医师·医学专业, 2012, 14(22): 39-42.
[10] 鞠建明, 孔铭, 钱大玮, 等.六神软膏质量控制标准研究[J].药物分析杂志, 2010, 30(6): 1060-1063
[11] 杨洪武, 王峥, 辛敏通, 等.薄层扫描法测定人工牛黄及其制剂中胆酸的含量[J].中成药, 2003, 25(4): 290-292.
[12] 王二云, 卢玉梁.细叶铁线莲药材中齐墩果酸薄层色谱鉴别的研究[J].北方药学, 2012, 9(3): 13-17.
[13] 刘淑贞, 赵俊萍.槟榔十三味丸中荜茇薄层色谱鉴别的研究[J].北方药学2012, 9(1):8-12.
[14] 马肖, 王兰霞, 赵建邦, 等.提高坐珠达西质量标准的研究[J].中国现代应用药学,2012, 3: 29 (3):121-125.
Preliminary study for Tibetan medicine Zuozhudaxi
Dong Hong-jiao ,Zeng Rui
(Ethnic Medicine Instiute of Southwest University for Nationalities,Chengdu 610041,P.R.C)
Objective: To enhance the quality standard of Zuozhudaxi.Method: The study makes a qualitative identification for 12 crud drugs(myroblan, emblic leafflower fruit, pomegranate seed, benzoin, elecampane, dove, Tibet inula root, saffron crocus, bezoar, felursi, dracocephalum tanguticum maxim, fructus piperis longi) in “Zuozhudaxi” by TLC with reference substance and the HPLC analysis was performed on an Kromasil C18 (4.6mm×250mm, 5µm)column. The column temperatrue was set at 30 ℃. A mixture of methyl alcohol -0.05% phosphoric acid aqueous solution was used as the mobile phase gradient elute with the flow rate at 1mL·min-1, and detected by different UV wave length, i.e 445nm for Crocin Ⅰ, CrocinⅡ, 352nm for Chlorogenic acid, 225nm for Kaempferol. Result: The TLC indicated that 12 identified herbs could show the same colorpot as the control herbs or contrast in the same position, CrocinⅡcontributions to the quality of Zuozhudaxi particularly.Conclusion: This identification method is good separating degree, accurate and stable.It can be used for quality specification study for“Zuozhudaxi”.
Zuozhudaxi; crocinⅠ; crocinⅡ; chlorogenic acid; kaempferol.
R28, R29
A
1003-4271(2014)06-0853-08
10.3969/j.issn.1003-4271.2014.06.10
2014-09-24
曾锐(1976-), 男, 汉族, 四川人, 副教授, 从事药物制剂及民族药的研究, E-mail: Mackzeng@gmail.com
课题得到国家“十二五”科技支撑计划(No.2012BAI27B07)的资助

