经皮冠状动脉介入术对急性心肌梗死碎裂QRS波的影响及预后分析
李国草,刘艳军,夏云龙,高连君,张树龙,杨延宗,董颖雪,尹晓盟,常 栋
随着急诊溶栓及早期经皮冠状动脉介入术(PCI)等方法对急性冠脉综合征(ACS)的治疗,临床上Q波型心肌梗死的发生率明显下降,即从原来的66.9%下降到37.5 %,心肌梗死后Q波消失率从过去的6.0%上升到25.0%[1]。这种急性期治疗手段的改进使非Q波型心肌梗死和非ST段抬高型心肌梗死(NSTEMI)的发生率均有所增加,使得体表心电图病理性Q波在心肌梗死诊断中的敏感性明显下降。因此,临床上需要寻找诊断心肌梗死更为敏感特异的心电图指标。碎裂QRS波(fragmented QRS complex,fQRS)是一种新的等位性Q波样改变的心电图表现,其对心肌梗死的诊断价值,预测心源性猝死、再发心肌梗死、心力衰竭、脑血管事件、持续性室性心动过速或心室纤颤等主要心脏不良事件及其特殊的临床意义和应用价值越来越受到重视。本研究旨在进一步探讨PCI治疗急性心肌梗死(AMI)后对fQRS的影响及预后分析。
1 资料与方法
1.1 一般资料 选择2010年7月—2011年6月我院收治并确诊的AMI患者137例,其中男109例,女28例;平均年龄(60.5±12.5)岁。患者均符合2007年10月ESC/ACC /AHA/WHF联合颁布的AMI诊断标准,即心肌生化标志物升高超过参考范围上限的99百分位值,同时伴有下述心肌缺血证据之一:(1)缺血导致的临床症状;(2)心电图提示新发ST- T段改变;(3)心电图出现病理性Q波;(4)影像学证实存在新发局部室壁运动异常或存活心肌丢失。
1.2 心电图检查 2006年Das等[2]将fQRS列为一个新的无创心电学指标,并将其定义为:常规12导联心电图〔滤波范围(filter range)为(0.15,100.00) Hz;交流滤波器(AC filter):60 Hz,25 mm/s,10 mm/mV〕上,相邻的两个或两个以上导联QRS波群呈多相的RSR′波,包括≥1个R波或者R、S波存在单个或多个顿挫或切迹,S波顿挫或切迹多发生在S波底部(见图1),这种fQRS常出现在冠状动脉供血区域对应的两个或两个以上的导联。
典型fQRS心电图特征包括:(1)QRS波时限<120 ms;(2)有或没有Q波,若出现Q波,Q波可能存在单个或多个顿挫或切迹,可形成Qr或QR型QRS波;(3)除外完全或不完全束支阻滞。对于时限> 120 ms的宽QRS波群(如束支传导阻滞、室性期前收缩或起搏心电图等)中的fQRS则另有规定[3]:两个或两个以上相邻导联的R波或S波出现两个以上的切迹,如在宽的室性期前收缩图形中只有两个切迹,那么这两个切迹的距离应>40 ms方能称为fQRS(见图2)。

图1 不同类型的fQRS心电图

图2 宽QRS波群的fQRS形态
1.3 研究方法 将陆续入院的AMI患者按病情不同分成3组:急诊PCI组31例、择期PCI组61例、未行PCI(拒绝或无法行PCI治疗)组45例。每组患者术前、术后当天、术后1周、术后2周、术后随访6个月时分别行心电图检查,分析心电图上的fQRS,统计每组患者fQRS发生率,分析各个时期3组fQRS发生率的变化。根据体表心电图有无fQRS将其分成fQRS组(70例)和无fQRS组(67例),并比较两组室性心律失常发生率。同时各组患者术后均行超声心动图检查,评价左心室射血分数(LVEF)及室壁节段性运动异常率。

2 结果
2.1 一般资料比较 3组患者的年龄、性别比较,差异无统计学意义(P>0.05);3组的高血压、糖尿病、陈旧性心肌梗死、脑梗死、心房纤颤患病率及心肌梗死部位分布比较,差异无统计学意义(P>0.05,见表1)。
2.2 3组患者超声心动图指标比较 3组LVEF及室壁节段性运动异常率比较,差异均无统计学意义(P>0.05,见表2)。
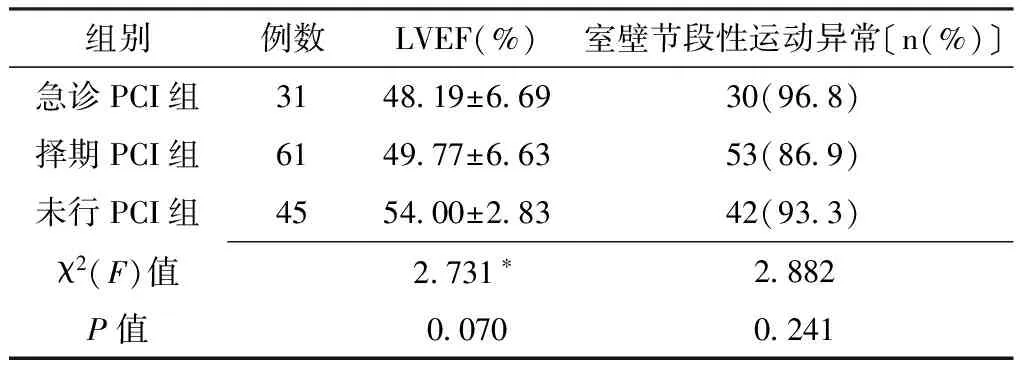
表2 3组患者术后超声心动图指标比较Table 2 Comparison of ECG index after surgery among the three groups
注:*为F值;LVEF=左心室射血分数
2.3 3组患不同时间心电图fQRS发生率比较 术前、术后当天、术后1周3组fQRS发生率比较,差异无统计学意义(P>0.05);而在术后2周和随访6个月时3组fQRS发生率比较,差异有统计学意义(P<0.05,见表3)。
2.4 3组患者室性心律失常发生率及病死率比较 3组患者住院期间室性心律失常发生率比较,差异有统计学意义(P<0.05);3组患者住院期间病死率比较,差异无统计学意义(P>0.05,见表4)。
2.5 fQRS组和无fQRS组室性心律失常发生率比较 经Fisher确切概率法显示,fQRS组患者室性心律失常发生率高于无fQRS组〔8.6%(6/70)与0%(0/67)〕,差异有统计学意义(P=0.028)。
3 讨论
目前,关于fQRS的形成机制有多种学说,如局部心肌瘢痕理论、梗死区内阻滞、梗死区周围阻滞、多灶性梗死、细胞间阻抗的变化及其他电生理与解剖学的观点等。在ACS时,fQRS出现在超急性期冠状T波及损伤性ST段改变之后,大多数患者在心肌缺血发生后的几小时或十几小时出现(Q波出现的时间6~14 h,平均9 h),与胚胎性r波颇为相似;fQRS还可能在急性心肌缺血发生后的几天内出现,其演变过程存在以下3种情况:(1)从无到有,并稳定存在,即当fQRS长期稳定存在时,提示该部位的心肌存在陈旧性梗死;(2)从无到有,然后进展为病理性Q波,即fQRS出现后,随着心肌缺血的进一步加重而进展为病理性Q波;(3)从无到有,再消失,即fQRS在AMI发展过程中呈一过性出现,并随心肌缺血的改善或病程的进展而消失[1]。本研究通过对AMI患者心电图fQRS的发生率进行分析发现,137例患者中急诊PCI组、择期PCI组及未行PCI组患者术前心电图梗死部位对应导联可见fQRS者分别为14例(45.2%)、35例(57.4% )、21例(46.7%)。
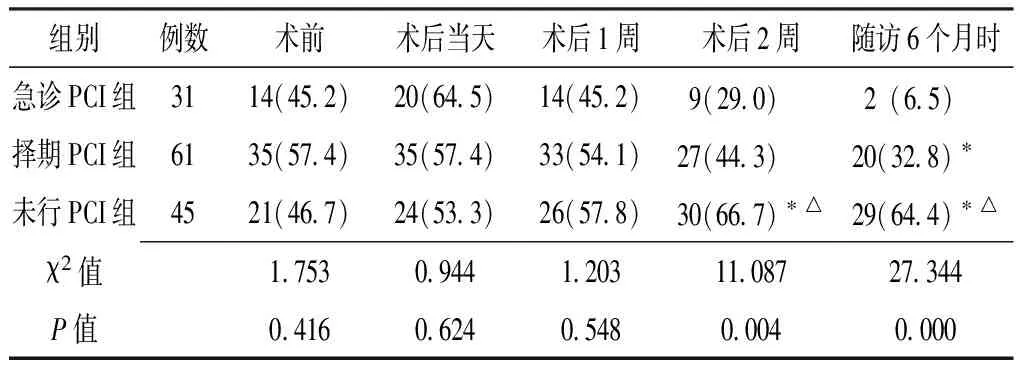
表3 3组患者不同时间心电图fQRS发生率比较〔n(%)〕Table 3 Comparison of ECG fQRS incidence among the three groups
注:与急诊PCI组比较,*P<0.01;与择期PCI组比较,△P<0.01
表4 3组患者室性心律失常发生率及病死率比较〔n(%)〕
Table4 Comparison of ventricular arrhythmias and mortality among the three groups

组别例数室性心律失常发生率病死率急诊PCI组314(12 9) 1(3 2)择期PCI组611(1 6)∗0 未行PCI组451(2 2) 1(2 2)χ2值6 9722 173P值0 0310 306
注:与急诊PCI组比较,*P<0.01

表1 3组患者一般资料比较Table 1 Comparison of general information among the three groups
注:*为F值
心肌梗死患者的主要不良心血管事件(MACE)包括心源性猝死、再发心肌梗死、心力衰竭、脑血管事件、持续性室性心动过速或心室纤颤。近些年,多位学者通过对冠心病心肌梗死PCI治疗或冠状动脉旁路移植术研究发现心电图有fQRS者比无fQRS者的全因死亡率更高、更具危险性;MACE的发生率明显增高,通过Kaplan-Meier 生存曲线的分析,fQRS组全因死亡率明显高于无fQRS组。多变量因素的分析结果也表明,fQRS阳性是MACE较强的独立预测因子,并且证明fQRS是冠心病和扩张型心肌病(DCM)患者发生室性心律失常的独立预测因子。无论心电图是否存在ST段抬高,fQRS对AMI的预测具有中度敏感度和高度特异度,是ACS患者病死率高的独立预测因子[4-10]。最近,有学者发现fQRS可预测致心律失常性右室心肌病(ARVC/D)及Brugada综合征等的早期诊断以及早期的猝死预警、恶性室性心律失常等的发生[11-12]。
本研究通过比较AMI患者入院后经过不同的治疗方法(急诊PCI、择期PCI及未行PCI)挽救缺血心肌后体表心电图fQRS的变化情况及观察心电图fQRS发生率的变化发现,随访6个月后心电图fQRS发生率在急诊PCI组较择期PCI组及未行PCI组降低,择期PCI组较未行PCI组降低,说明早期开通心肌再灌注可挽救缺血心肌。本研究还发现,根据患者体表心电图是否有fQRS将患者分成fQRS组和无fQRS组,fQRS组患者室性心律失常发生率高于无fQRS组,进一步说明心肌梗死患者(尤其是心电图存在fQRS者),心肌存在瘢痕组织,更容易发生室性心律失常,而心肌梗死后出现恶性室性心律失常是患者死亡的主要原因,fQRS可能对远期预测心肌梗死患者的病死率有一定价值。本研究发现住院期间急诊PCI组室性心律失常发生率较择期PCI组高,择期PCI组及未行PCI组间室性心律失常发生率无差异,且各组病死率间无差异,一方面可能由于研究样本数量小、患者平均住院时间及随访时间均较短;另一方面可能由于急诊PCI组患者相对症状均较重,梗死面积较大,而未行PCI组患者症状及梗死面积相对较轻,且急诊再灌注时容易出现室性心律失常所致。
综上所述,针对AMI患者早期开通冠状动脉血管可以挽救缺血心肌而减少心肌瘢痕的形成,进而降低心电图fQRS的发生率,减少室性心律失常的发生率;而通过分析不同时期的心肌再灌注治疗对fQRS发生率的影响,进一步提示急诊PCI的价值优于择期PCI,为临床治疗提供了一定的参考价值。
1 郭继鸿.碎裂QRS波[J].临床心电学杂志,2008,17(1):60-68.
2 Das MK,Khan B,Jacob S,et al.Significance of a fragmented QRS complex versus a Q wave in patients with coronary artery disease[J].Circulation,2006,113(21):2495-2501.
3 Das MK,Suradi H,Maskoun W,et al.Fragmented wide QRS on a 12-lead ECG:a sign of myocardial scar and poor prognosis[J].Circ Arrhythm Electrophysiol,2008,1(4):258-268.
4 Sha J,Zhang S,Tang M,et al.Fragmented QRS is associated with all-cause mortality and ventricular arrhythmias in patient with idiopathic dilated cardiomyopathy[J].Ann Noninvasive Electrocardiol,2011,16(3):270-275.
5 Das MK,Saha C,El Masry H,et al.Fragmented QRS on a 12-lead ECG:a predictor of mortality and cardiac events in patients with coronary artery disease[J].Heart Rhythm,2007,4(11):1385-1392.
7 Ari H,Cetinkaya S,Ari S,et al.The prognostic significance of a fragmented QRS complex after primary percutaneous coronary intervention[J].Heart Vessels,2012,27(1):20-28.
8 Das MK,Michael MA,Suradi H,et al.Usefulness of fragmented QRS on a 12-lead electrocardiogram in acute coronary syndrome for predicting mortality[J].Am J Cardiol,2009,104(12):1631-1637.
9 Torigoe K,Tamura A,Kawano Y,et al.The number of leads with fragmented QRS is independently associated with cardiac death or hospitalization for heart failure in patients with prior myocardial infarction[J].J Cardiol,2012,59(1):36-41.
10 Peters S,Trümmel M,Koehler B.QRS fragmentation in standard ECG as a diagnostic marker of arrhythmogenic right ventricular dysplasia-cardiomyopathy[J].Heart Rhythm,2008,5(10):1417-1421.
11 Morita H,Kusano KF,Miura D,et al.Fragmented QRS as a marker of conduction abnormality and a predictor of prognosis of Brugada syndrome[J].Circulation,2008,118(17):1697-1704.
12 Das MK,El Masry H.Fragmented QRS and other depolarization abnormalities as a predictor of mortality and sudden cardiac death[J].Curr Opin Cardiol,2010,25(1):59-64.

