基于“温补脾阳”功效的附子“效—毒—证”关联研究
栾永福孙 蓉
(1山东省中医药研究院,济南,250014;2天津中医药大学,天津,300073)
基于“温补脾阳”功效的附子“效—毒—证”关联研究
栾永福1,2孙 蓉1
(1山东省中医药研究院,济南,250014;2天津中医药大学,天津,300073)
目的:分别研究附子水提物预防或治疗给药对脾肾阳虚证大鼠发挥温补脾阳功效时的药效及其伴随毒副作用。方法:按15%大黄粉悬液每天给药剂量为8.9 g·kg-1·d-1,连续给药9 d,且附加冰水游泳致力竭的方法,制备大鼠脾肾阳虚证模型。预防实验组给药与造模同时进行,治疗实验组造模成功后给药,两个实验药物组均给药9 d。实验期间进行证候积分和体重称量,并检测血中TSH、IgG、C3等药效指标和LDH、CTn-I等心毒性指标的水平。结果:附子水提物能改善脾肾阳虚证大鼠的证候积分,增大脾体比值、肾体比值、肾上腺体比值和胸腺体比值,同时能升高血清中TSH、IgG、C3水平,且升高血LDH、CTn-I的水平,降低心体比值。结论:附子水提物对大黄致脾肾阳虚证大鼠具有一定的预防和治疗作用,同时均伴有一定的心脏毒性作用。
附子;脾肾阳虚;功效;毒性
附子为毛茛科植物乌头Aconitum carmichaelliDebx.的子根的加工品,习称“泥附子”[1]。其性辛、甘,大热;有毒。归心、肾、脾经。具有回阳救逆,补火助阳,散寒止痛的功效。用于亡阳虚脱,肢冷脉微,心阳不足,胸痹心痛,虚寒吐泻,脱腹冷痛,肾阳虚衰,阳痿宫冷,阴寒水肿,阳虚外感,寒湿痹痛。附子是一味临床常用中药,然而其固有毒性影响了该药的进一步开发应用。其毒性物质基础主要是双酯型二萜类生物碱,主要为乌头碱、新乌头碱、次乌头碱等乌头属类生物碱。
“是药三分毒”,中药毒性是“药物”的一种基本属性和客观表现,中药毒性与功效和证候密切相关,是在中医辨证用药和中药发挥功效的过程中被逐渐认知和发现的,因此,中药毒性应当放在功效(适应证)和中医的“证候”中间进行综合评价和认知,不能孤立地就毒性论毒性。
附子作为有毒中药在不同证候模型上体现的功效与毒性有一定的差异性,因此附子的功效与毒性应当放在证候的背景下进行合理评价和科学认知。只有在其主治证候的基础上进行功效与毒性研究,才符合中医药的研究特点,才能科学合理地进行有毒中药的毒性-功效-证候关联性评价。脾肾阳虚证是指脾肾阳气虚衰、阴寒内生所表现的虚寒证候,临床表现为畏寒喜温、形寒肢冷、乏力、消瘦、便溏及腹泻等[2],为附子的主治证候之一。鉴于此,本实验制备了脾肾阳虚证大鼠模型,并对附子水提物对脾肾阳虚证大鼠的功效与毒性进行了观察和评价,将附子的功效与毒性放在证候的基础上综合评价,平衡利弊,以期为附子在临床实践中可以更加安全、更加合理、更具疗效的应用提供实验依据,进而合理阐释中医理论中“药以治病,因毒为能”的合理性与科学性。
1 实验材料
1.1 实验药物 附子(Aconitum carmichaeliDebx.),购自北京同仁堂饮片有限责任公司,批号:201232732 -S。经山东省中医药研究院林慧彬研究员鉴定为毛茛科植物乌头的子根,按2010年版《中华人民共和国药典》(以下简称《中国药典》)附子项下检查,符合各项规定。取附子药材1000 g用10倍量水浸泡,加热回流提取2次,每次1.5 h,16层纱布过滤,取药液浓缩至含生药量1.2 g·mL-1,批号:20130419。实验前分别用蒸馏水稀释至1.080 g·m L-1、0.540 g·m L-1、0.270 g·mL-1、0.191 g·mL-1、0.135 g·m L-1、0.096 g·mL-1、0.068 g·mL-1,备用。
附子理中丸(北京同仁堂科技发展股份有限公司制药厂),由附子(制)100 g、党参200 g、白术(炒)150 g、干姜100 g、甘草100 g制成,产品批号:12011329。附子理中丸具有温中健脾之功效,用于脾胃虚寒,脘腹冷痛,呕吐泄泻,手足不温。故用其作为大黄所致脾肾阳虚证的阳性药。实验前用蒸馏水制成0.243 g· mL-1水悬液,备用。
大黄(山东百味堂中药饮片有限公司),批号:121101。经山东省中医药研究院林慧彬研究员鉴定为药用大黄Rheum officinaleBaill.的干燥根及根茎,且符合各项标准,可用于实验研究。实验前用蒸馏水制成15%大黄粉悬液,备用。
1.2 实验动物 Wistar大鼠,雄性,体重140~200 g,共100只,购自山东省鲁抗医药股份有限公司,动物合格证号:SCXK(鲁)20130001。
1.3 仪器与试剂 YP20001电子天平(上海上天精密仪器有限公司);AL104电子天平(梅特勒-托利多仪器(上海)有限公司);KDM型调温电热套,购于山东鄄城华鲁电热仪器有限公司;DZKM-S-6电热恒温水浴锅(北京市永光明医疗仪器厂)。UV-2102 PC型紫外可见分光光度仪(中美合资尤尼柯有限公司),常规病理检测仪器等。
TSH(促甲状腺素)(201307)、IgG(免疫球蛋白)(201307)、C3(C3补体)(201307)、LDH(乳酸脱氢酶)(20130722)、CTn-I(心肌肌钙蛋白)(201307)试剂盒均购自由南京建成生物工程研究所。
1.4 剂量设置依据 按照2010版《中国药典》规定,附子人临床日用量为3~15 g,按最大剂量换算至大鼠则为1.35 g·kg-1,所以设置相当于人日用量的1、2、4、8倍剂量组,于1、2倍剂量之间设置1个剂量组,于1倍剂量之下设置2个剂量组。因此本实验设置7个剂量组:10.80、5.40、2.70、1.91、1.35、0.96、0.68 g· kg-1。
附子理中丸,人日用量3粒,每粒9 g,所以人日用量为27 g/d,换算至大鼠则为2.43 g·kg-1·d-1。因此本实验将其浓度配置为0.243 g·mL-1,按10 mL· kg-1灌胃给药。
2 实验方法
2.1 脾肾阳虚证大鼠模型的制备 大鼠每天上午灌胃15%大黄粉悬液,用药量为8.9 g·kg-1·d-1,连服9 d,下午冰水游泳致力竭(力竭标准为全身下沉至没颈,不能坚持游泳)。有萎靡、倦卧、毛枯槁、畏寒、消瘦、四肢不收、便溏脱肛、纳呆、活动频度下降、肛门红肿等表现者为造模成功[3]。
2.2 实验分组与给药
2.2.1 附子水提物预防给药对脾肾阳虚证大鼠的效毒关联评价 取大鼠100只,雌性各半,按体重分为正常对照组、脾肾阳虚证模型组、附子水提物10.80、5.40、2.70、1.91、1.35、0.96、0.68 g·kg-1剂量组和中药阳性药组。
对照组每天按10 mL·kg-1灌胃蒸馏水;模型组每天进行造模;附子各剂量组每天造模后按10mL·kg-1分别灌胃10.80、5.40、2.70、1.91、1.35、0.96、0.68 g ·kg-1生药量的附子水提物;中药阳性药组每天造模后按10 mL·kg-1灌胃2.43 g·kg-1的附子理中丸水悬液。
2.2.2 附子水提物治疗给药对脾肾阳虚证大鼠的效毒关联评价 取成模大鼠90只,雌雄各半,按体重分为脾肾阳虚证模型组、附子水提物10.80、5.40、2.70、1.91、1.35、0.96、0.68 g·kg-1剂量组和中药阳性药组,另取10只雌雄各半正常大鼠作为对照组。
对照组和模型组每天按10 m L/kg灌胃蒸馏水;附子各剂量组每天按10 mL·kg-1分别灌胃10.80、5.40、2.70、1.91、1.35、0.96、0.68 g·kg-1生药量的附子水提物;中药阳性药组每天按10 mL·kg-1灌胃2.43 g·kg-1的附子理中丸水悬液。
2.3 观察与记录 每天称量体重并进行证候积分,积分标准[4]如表1。

表1 脾肾阳虚证大鼠证候积分表
2.4 标本采集与检测 末次给药24 h后,大鼠摘眼球法取血后脱颈椎处死,取心、肝、脾、肾、脑、肾上腺、胸腺称重,然后用将血浆进行3500 r/min离心10 min,取上清液检测TSH、IgG、C3、LDH、CTn-I的含量。
2.5 数据的统计与处理 数据用(¯x±s)表示,采用SPSS 13.0统计软件对各组数据进行统计处理和组间比较,P<0.05为数据统计有统计学意义。
3 实验结果
3.1 对体重变化的影响
3.1.1 预防实验 附子水提物预防给药对脾肾阳虚证大鼠体重的影响,详见表2。
表2 附子水提物预防给药对脾肾阳虚证大鼠体重的影响(±s,n=10)
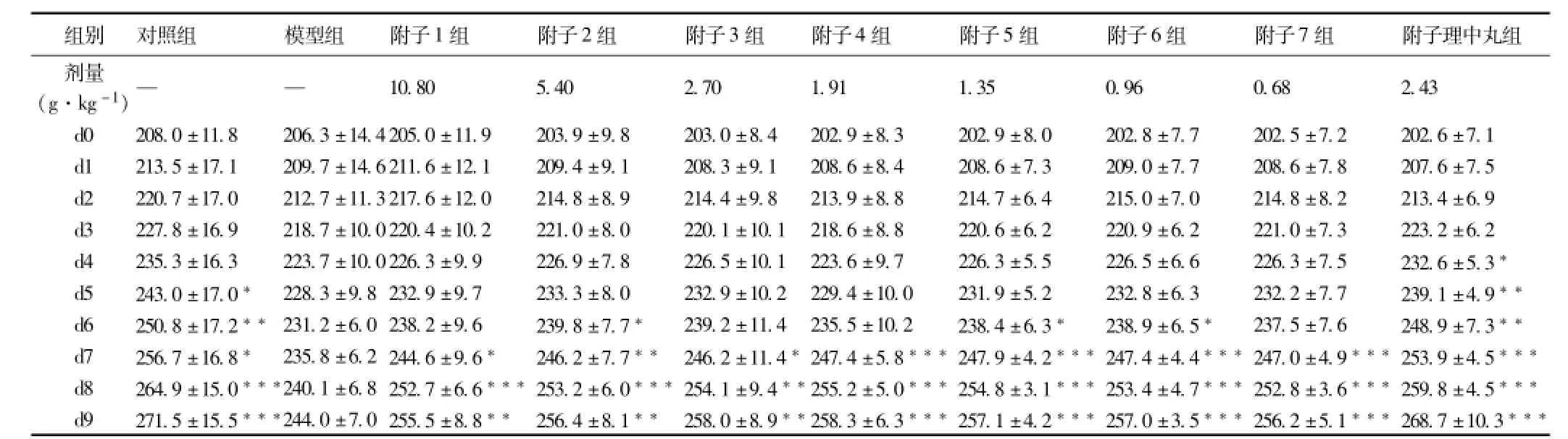
表2 附子水提物预防给药对脾肾阳虚证大鼠体重的影响(±s,n=10)
注:与模型组相比,*表示P<0.05,**表示P<0.01,***表示P<0.001。(下同)
组附子理中丸组剂量(g·kg-1)——组别对照组模型组附子1组附子2组附子3组附子4组附子5组附子6组附子7 10.80 5.40 2.70 1.91 1.35 0.96 0.68 2.43 d0 208.0±11.8 206.3±14.4205.0±11.9 203.9±9.8 203.0±8.4 202.9±8.3 202.9±8.0 202.8±7.7 202.5±7.2 202.6±7.1 d1 213.5±17.1 209.7±14.6211.6±12.1 209.4±9.1 208.3±9.1 208.6±8.4 208.6±7.3 209.0±7.7 208.6±7.8 207.6±7.5 d2 220.7±17.0 212.7±11.3217.6±12.0 214.8±8.9 214.4±9.8 213.9±8.8 214.7±6.4 215.0±7.0 214.8±8.2 213.4±6.9 d3 227.8±16.9 218.7±10.0220.4±10.2 221.0±8.0 220.1±10.1 218.6±8.8 220.6±6.2 220.9±6.2 221.0±7.3 223.2±6.2 d4 235.3±16.3 223.7±10.0226.3±9.9 226.9±7.8 226.5±10.1 223.6±9.7 226.3±5.5 226.5±6.6 226.3±7.5 232.6±5.3*d5 243.0±17.0*228.3±9.8 232.9±9.7 233.3±8.0 232.9±10.2 229.4±10.0 231.9±5.2 232.8±6.3 232.2±7.7 239.1±4.9**d6 250.8±17.2**231.2±6.0 238.2±9.6 239.8±7.7*239.2±11.4 235.5±10.2 238.4±6.3*238.9±6.5*237.5±7.6 248.9±7.3**d7 256.7±16.8*235.8±6.2 244.6±9.6*246.2±7.7**246.2±11.4*247.4±5.8***247.9±4.2***247.4±4.4***247.0±4.9***253.9±4.5***d8 264.9±15.0***240.1±6.8 252.7±6.6***253.2±6.0***254.1±9.4**255.2±5.0***254.8±3.1***253.4±4.7***252.8±3.6***259.8±4.5***d9 271.5±15.5***244.0±7.0 255.5±8.8**256.4±8.1**258.0±8.9**258.3±6.3***257.1±4.2***257.0±3.5***256.2±5.1***268.7±10.3***
由表2可知,与正常组相比,脾肾阳虚模型组大鼠体重增长明显缓慢;预防给药附子水提物后,大鼠体重增长加快,在一定的范围内随着剂量的增大体重增长幅度升高。
3.1.2 治疗实验 附子水提物治疗给药对脾肾阳虚证大鼠体重的影响,详见表3。由表3可知,与正常组相比,脾肾阳虚模型组大鼠体重增长明显缓慢;治疗给药附子水提物后,大鼠体重增长加快,在一定的范围内随着剂量的增大体重增长幅度升高。
表3 附子水提物治疗给药对脾肾阳虚证大鼠体重的影响(±s,n=10)

表3 附子水提物治疗给药对脾肾阳虚证大鼠体重的影响(±s,n=10)
组附子理中丸组剂量(g·kg-1)——组别对照组模型组附子1组附子2组附子3组附子4组附子5组附子6组附子7 10.80 5.40 2.70 1.91 1.35 0.96 0.68 2.43 d0 174.3±11.8 174.4±11.7174.5±11.7 174.4±11.7 174.4±11.5 174.9±11.5 175.0±11.4 174.9±11.4 174.9±11.4 174.9±11.4 d1 180.1±12.7 178.8±11.7180.3±11.8 179.5±12.2 181.0±11.5 180.6±12.2 181.0±12.4 182.2±11.6 182.1±12.0 180.9±11.8 d2 185.8±13.4 183.9±12.0185.6±12.2 184.7±12.3 186.2±11.8 184.9±11.9 185.4±12.4 185.2±12.2 187.2±12.6 185.8±11.6 d3 192.0±14.3 188.7±12.2190.7±12.1 190.4±12.1 190.5±12.4 189.8±13.3 191.3±12.3 187.2±13.4 192.1±12.6 190.8±11.8 d4 197.5±14.0 193.0±12.7193.7±12.8 192.7±12.4 193.5±13.0 193.7±13.5 194.3±12.4 191.7±12.7 194.8±12.8 193.6±12.0 d5 202.2±14.8 194.2±13.5196.7±13.1 194.8±12.1 195.5±13.1 196.8±12.7 195.1±12.9 194.3±12.2 197.8±12.8 197.6±13.0 d6 206.8±16.6 198.0±13.4199.8±12.8 197.2±12.3 198.9±12.1 199.9±13.0 197.1±12.7 197.2±11.9 199.2±13.3 199.1±13.3 d7 211.6±15.7 201.4±12.7203.4±13.3 201.7±12.8 202.2±12.8 203.6±13.1 199.6±12.7 200.7±12.3 202.0±13.5 202.8±13.9 d8 216.1±16.6 203.2±12.2205.5±14.0 204.2±13.1 204.3±13.2 205.7±12.6 201.4±12.7 204.3±12.6 205.9±13.5 204.5±13.8 d9 219.8±17.2 205.7±12.5209.2±14.4 207.6±13.6 206.2±13.1 207.5±13.0 204.5±13.1 207.7±12.7 208.8±13.8 207.5±14.1 d10 225.2±17.6*210.4±13.5210.7±14.6 210.0±13.6 209.7±13.0 211.4±14.3 207.5±12.2 210.7±13.4 212.4±14.6 214.1±14.2 d11 233.0±16.7**212.6±14.4215.8±14.9 214.4±13.8 215.6±13.1 214.8±14.4 213.0±12.2 213.0±12.5 213.4±11.0 218.9±14.8 d12 239.4±16.7**214.2±15.5222.5±15.5 220.5±13.5 220.6±13.4 220.6±14.4 220.5±9.1 219.6±14.1 219.4±11.8 222.8±15.2 d13 246.0±16.3***216.9±14.8227.4±15.8 225.7±11.8 225.4±11.2 225.4±14.9 224.8±9.7 224.7±12.7 224.3±12.9 231.5±16.4 d14 252.1±16.6***221.2±15.3234.9±16.0 233.9±9.32*233.6±10.9 234.5±10.7*231.0±8.2 230.4±12.9 230.4±13.7 239.6±16.5*d15 258.0±17.6***226.0±13.2240.1±16.3*240.3±8.0**241.0±7.8**242.0±8.5**242.1±4.8**240.9±8.0**241.0±10.0*246.6±15.4**d16 264.4±17.4***228.2±15.4245.5±18.0*245.3±10.5**246.8±8.2**252.4±7.0***250.0±3.3***248.9±5.5***248.9±7.7**251.1±14.9**d17 272.3±17.9***230.8±15.1250.9±19.0*251.1±15.5**253.4±15.1**259.1±9.0***257.0±6.4***255.2±8.5***254.8±17.3**259.2±15.7***d18 280.5±18.4***234.9±15.1258.9±14.6**261.1±12.7***264.7±11.7***267.0±8.5***267.4±14.2***267.0±15.5***267.4±17.6***271.0±12.0***
3.2 改善脾肾阳虚证候药效ED50值
3.2.1 预防实验 附子水提物对脾肾阳虚模型大鼠的预防作用药效ED50计算数据见表4(证候积分小于3为有效),附子水提物预防给药对脾肾阳虚模型大鼠证候积分的影响见图1。

表4 附子水提物对脾肾阳虚模型大鼠的预防作用药效ED50计算数据表
由Bliss法计算得回归方程y=4.8830+ 4.1912Log(D),半数有效量ED50=1.0664 g·kg-1,ED5095%的可信限为0.7740~1.3406 g·kg-1,ED5=0.4320 g·kg-1,ED95=2.6326 g·kg-1。

图1 附子水提物预防给药对脾肾阳虚证大鼠证候积分的影响
由图1可知,预防给药附子水提物后,脾肾阳虚大鼠证候积分明显减小,且随着剂量的增大,效果越显著。
3.2.2 治疗实验 附子水提物对脾肾阳虚模型大鼠的预防作用药效ED50计算数据表见表5(证候积分小于3为有效),附子水提物对预防给药对脾肾阳虚模型大鼠证候积分的影响见图2。
由Bliss法计算得回归方程y=4.9146+ 3.8587Log(D),半数有效量ED50=1.0523 g·kg-1,ED5095%的可信限=0.7306~1.3416 g·kg-1,ED5=0.3943 g·kg-1,ED95=2.8081 g·kg-1。
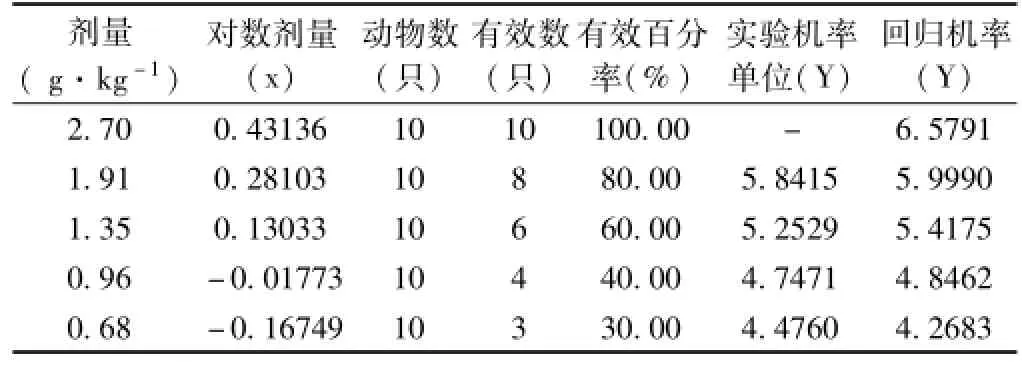
表5 附子水提物对脾肾阳虚模型大鼠的治疗作用药效ED50计算数据表
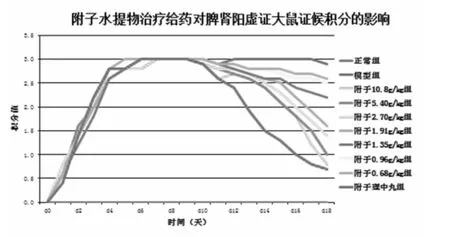
图2 附子水提物治疗给药对脾肾阳虚证大鼠证候积分的影响
由图2可知,治疗给药附子水提物后,脾肾阳虚证大鼠证候积分明显降低,且随着剂量的增大,效果更加显著。
3.3 对脾肾阳虚证大鼠药效生化指标的影响 附子水提物对预防给药和治疗给药对脾肾阳虚模型大鼠血
TSH、IgG、C3指标的影响分别见表6和表7。
表6 附子水提物预防给药对脾肾阳虚证大鼠血清TSH、IgG、C3的影响(±s,n=10)

表6 附子水提物预防给药对脾肾阳虚证大鼠血清TSH、IgG、C3的影响(±s,n=10)
TSH IgG C3对照组28.2±3.5***12.5±1.3***486.5±20.8组别***模型组18.4±2.2 9.3±1.0 398.8±10.6附子10.8 g·kg-1组25.0±2.5***11.3±1.1***457.9±11.9***附子5.4 g·kg-1组24.1±2.4***11.2±0.9***449.9±9.3***附子2.7 g·kg-1组22.9±1.4***11.0±1.4**441.4±5.9***附子1.91 g·kg-1组22.4±1.0***10.9±1.6*429.3±9.9***附子1.35 g·kg-1组21.3±0.9**10.4±0.8*416.8±20.6*附子0.96 g·kg-1组20.4±0.7*10.4±0.9*412.2±15.9*附子0.68 g·kg-1组19.5±1.0 9.5±1.0 401.3±28.9附子理中丸组26.9±1.8***12.0±1.5***469.0±13.0***
表7 附子水提物治疗给药对脾肾阳虚证大鼠血清TSH、IgG、C3的影响(±s,n=10)

表7 附子水提物治疗给药对脾肾阳虚证大鼠血清TSH、IgG、C3的影响(±s,n=10)
TSH IgG C3对照组28.6±3.3***12.7±1.3***490.8±24.1组别***模型组18.8±2.2 9.4±1.0 403.1±9.3附子10.8 g·kg-1组25.5±2.4***11.5±1.1***462.5±12.0***附子5.4 g·kg-1组24.6±2.4***11.4±0.9***454.4±9.5***附子2.7 g·kg-1组23.3±1.2***11.2±1.4**445.7±6.0***附子1.91 g·kg-1组22.8±1.0***11.1±1.6*433.4±10.1***附子1.35 g·kg-1组21.7±0.9**10.6±0.9*420.6±21.0*附子0.96 g·kg-1组20.8±0.7***10.6±0.9*415.9±16.2*附子0.68 g·kg-1组19.9±1.0 9.7±1.0 404.8±29.4附子理中丸组27.4±1.8***12.2±1.5***473.2±14.2***
由表6可知,预防给药附子水提物后,各组脾肾阳虚大鼠TSH、IgG和C3水平显著升高,且随着剂量的增大,其效果越显著。
由表7可知,治疗给药附子后,各组脾肾阳虚证大鼠TSH、IgG和C3水平显著升高,且随着剂量的增大,其效果越显著。
3.4 对脏体比值的影响
3.4.1 预防实验 附子预防给药对脾肾阳虚证大鼠脏体比值的影响见表8、表9。
由表8可知,与模型组相比,预防给药后,附子各剂量组均可引起脾肾阳虚大鼠心体比值降低,但只有附子1组有统计学意义;附子各剂量组均未引起脾肾阳虚证大鼠肝体比值和脑体比值的显著变化。
表8 附子预防给药对脾肾阳虚证大鼠心、肝和脑体比值(g/100 g)的影响(±s,n=10)

表8 附子预防给药对脾肾阳虚证大鼠心、肝和脑体比值(g/100 g)的影响(±s,n=10)
脑体比值对照组组别心体比值 肝体比值0.411±0.017 4.013±0.136 0.558±0.018模型组0.400±0.017 4.025±0.244 0.542±0.019附子10.8 g·kg-1组0.360±0.027**4.036±0.168 0.549±0.018附子5.4 g·kg-1组0.386±0.021 4.073±0.118 0.549±0.018附子2.7 g·kg-1组0.389±0.020 4.030±0.151 0.548±0.018附子1.91 g·kg-1组0.398±0.024 4.036±0.199 0.546±0.023附子1.35 g·kg-1组0.399±0.022 4.007±0.302 0.548±0.022附子0.96 g·kg-1组0.400±0.031 4.015±0.137 0.544±0.019附子0.68 g·kg-1组0.403±0.016 4.022±0.148 0.547±0.019附子理中丸组0.410±0.016 4.030±0.162 0.553±0.021
表9 附子预防给药对脾肾阳虚证大鼠脾、肾、肾上腺和胸腺体比值(g/100 g)的影响(±s,n=10)

表9 附子预防给药对脾肾阳虚证大鼠脾、肾、肾上腺和胸腺体比值(g/100 g)的影响(±s,n=10)
组别脾体比值 肾体比值 肾上腺体比值 胸腺体比值对照组0.321±0.017***0.714±0.023***0.019±0.001***0.191±0.002***模型组0.223±0.009 0.637±0.026 0.015±0.000 0.158±0.004附子10.8 g·kg-1组0.289±0.032***0.694±0.043**0.018±0.001***0.190±0.005***附子5.4 g·kg-1组0.266±0.011***0.689±0.028***0.018±0.000***0.189±0.005***附子2.7 g·kg-1组0.252±0.020***0.681±0.037**0.018±0.000***0.186±0.006***附子1.91 g·kg-1组0.243±0.010***0.672±0.035*0.018±0.000***0.187±0.005***附子1.35 g·kg-1组0.240±0.017**0.679±0.045*0.018±0.001***0.180±0.006***附子0.96 g·kg-1组0.238±0.006***0.675±0.044*0.018±0.000***0.179±0.007***附子0.68 g·kg-1组0.235±0.003***0.672±0.030*0.017±0.001***0.177±0.006***附子理中丸组0.314±0.028***0.687±0.022***0.019±0.001***0.189±0.005***
表10 附子治疗给药对脾肾阳虚证大鼠心、肝和脑体比值(g/100g)的影响(±s,n=10)
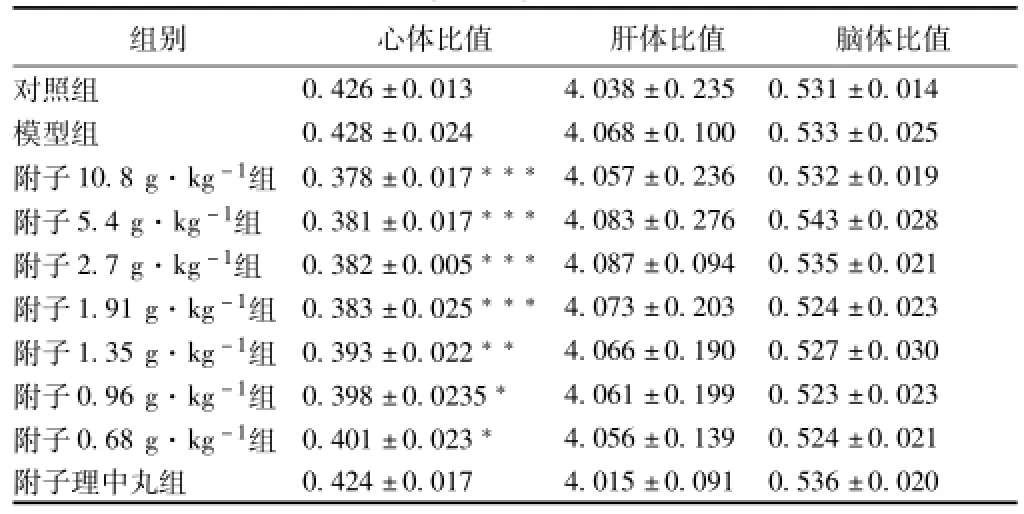
表10 附子治疗给药对脾肾阳虚证大鼠心、肝和脑体比值(g/100g)的影响(±s,n=10)
组别心体比值肝体比值脑体比值对照组0.426±0.013 4.038±0.235 0.531±0.014模型组0.428±0.024 4.068±0.100 0.533±0.025附子10.8 g·kg-1组0.378±0.017***4.057±0.236 0.532±0.019附子5.4 g·kg-1组0.381±0.017***4.083±0.276 0.543±0.028附子2.7 g·kg-1组0.382±0.005***4.087±0.094 0.535±0.021附子1.91 g·kg-1组0.383±0.025***4.073±0.203 0.524±0.023附子1.35 g·kg-1组0.393±0.022**4.066±0.190 0.527±0.030附子0.96 g·kg-1组0.398±0.0235*4.061±0.199 0.523±0.023附子0.68 g·kg-1组0.401±0.023*4.056±0.139 0.524±0.021附子理中丸组0.424±0.017 4.015±0.091 0.536±0.020
由表9可知,与模型组相比,预防给药后,附子各剂量组均可引起脾肾阳虚大鼠脾体比值显著性升高,且随着剂量的增大,其作用越显著;附子各剂量组均可引起脾肾阳虚大鼠肾体比值显著性升高,且随着剂量的增大,其作用越显著;附子各剂量组均可引起脾肾阳虚大鼠肾上腺体比值显著性升高,且随着剂量的增大,其作用越显著;附子各剂量组均可引起脾肾阳虚大鼠胸腺体比值显著性升高,且随着剂量的增大,其作用越显著。
3.4.2 治疗实验 附子治疗给药对脾肾阳虚证大鼠脏体比值的影响见表10、表11。
表11 附子治疗给药对脾肾阳虚证大鼠脾、肾、肾上腺和胸腺体比值(g/100g)的影响(±s,n=10)

表11 附子治疗给药对脾肾阳虚证大鼠脾、肾、肾上腺和胸腺体比值(g/100g)的影响(±s,n=10)
组别脾体比值肾体比值肾上腺体比值胸腺体比值对照组0.329±0.007***0.749±0.012***0.019±0.001***0.191±0.008***模型组0.281±0.025 0.711±0.008 0.017±0.001 0.163±0.006附子10.8 g·kg-1组0.311±0.019**0.732±0.010***0.018±0.001*0.184±0.009***附子5.4 g·kg-1组0.304±0.015*0.727±0.018*0.018±0.001*0.181±0.009***附子2.7 g·kg-1组0.300±0.005*0.724±0.014*0.018±0.001 0.180±0.008***附子1.91 g·kg-1组0.297±0.008 0.722±0.006**0.018±0.001*0.179±0.005***附子1.35 g·kg-1组0.290±0.006 0.722±0.008**0.018±0.001*0.178±0.007***附子0.96 g·kg-1组0.286±0.0034 0.716±0.011 0.018±0.000*0.177±0.004***附子0.68 g·kg-1组0.284±0.009 0.712±0.026 0.018±0.001*0.173±0.008**附子理中丸组0.323±0.009***0.743±0.012***0.018±0.001*0.188±0.009***
由表10可知,与模型组相比,治疗给药后,附子各剂量组均可引起脾肾阳虚大鼠心体比值显著性降低,且随着剂量的增大,其作用越显著;附子各剂量组均未引起脾肾阳虚证大鼠肝体比值和脑体比值的显著变化。
由表11可知,与模型组相比,治疗给药后,附子各剂量组均可引起脾肾阳虚大鼠脾体比值显著性升高,且随着剂量的增大,其作用越显著;附子各剂量组均可引起脾肾阳虚大鼠肾体比值显著性升高,且随着剂量的增大,其作用越显著;附子各剂量组均可引起脾肾阳虚大鼠肾上腺体比值显著性升高,且随着剂量的增大,其作用越显著;附子各剂量组均可引起脾肾阳虚大鼠胸腺体比值显著性升高,且随着剂量的增大,其作用越显著。
3.5 对药效伴随毒性指标LDH、CTN-I的影响
3.5.1 预防实验 附子水提物预防给药对脾肾阳虚大鼠血生化指标LDH、CTN-I的影响见表12。
表12 附子水提物预防脾肾阳虚实验对大鼠LDH、CTN-I的影响(±s,n=10)
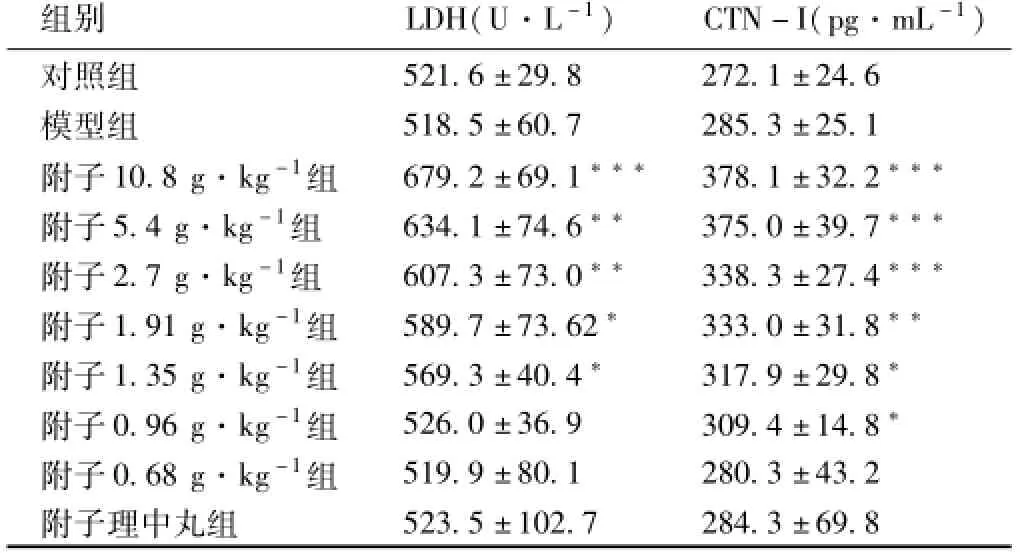
表12 附子水提物预防脾肾阳虚实验对大鼠LDH、CTN-I的影响(±s,n=10)
组别LDH(U·L-1)CTN-I(pg·mL-1)对照组521.6±29.8 272.1±24.6模型组518.5±60.7 285.3±25.1附子10.8 g·kg-1组679.2±69.1***378.1±32.2***附子5.4 g·kg-1组634.1±74.6**375.0±39.7***附子2.7 g·kg-1组607.3±73.0**338.3±27.4***附子1.91 g·kg-1组589.7±73.62*333.0±31.8**附子1.35 g·kg-1组569.3±40.4*317.9±29.8*附子0.96 g·kg-1组526.0±36.9 309.4±14.8*附子0.68 g·kg-1组519.9±80.1 280.3±43.2附子理中丸组523.5±102.7 284.3±69.8
由表12可知,预防给药后,附子各剂量组均可引起脾肾阳虚大鼠血LDH、CTN-I显著性升高,且随着剂量的增大,其作用越显著。
表13 附子水提物治疗脾肾阳虚实验对大鼠LDH、CTN-I的影响(±s,n=10)

表13 附子水提物治疗脾肾阳虚实验对大鼠LDH、CTN-I的影响(±s,n=10)
组别LDH(U·L-1)CTN-I(pg·m L-1)对照组526.4±30.3 276.1±24.8模型组523.9±61.5 289.4±25.3附子10.8 g·kg-1组686.0±69.8***383.0±32.5***附子5.4 g·kg-1组640.4±75.3**380.0±40.1***附子2.7 g·kg-1组613.5±73.7**342.9±27.6***附子1.91 g·kg-1组595.9±74.5*337.5±32.2**附子1.35 g·kg-1组574.9±41.0*322.3±30.2*附子0.96 g·kg-1组531.3±37.3 313.8±15.0*附子0.68 g·kg-1组525.0±80.9 284.3±43.7附子理中丸组528.5±103.6 288.2±70.4
3.5.2 治疗实验 附子水提物治疗给药对脾肾阳虚大鼠血生化指标LDH、CTN-I的影响见表13。
由表13可知,治疗给药后,附子各剂量组均可引起脾肾阳虚大鼠血LDH、CTN-I显著性升高,且随着剂量的增大,其作用越显著。
4 结论与讨论
本实验研究发现预防给药和治疗给药附子水提物后,脾肾阳虚证大鼠的体重增长状况较模型组显著加快,症状亦得到显著改善,其脾体比值、肾体比值、肾上腺体比值和胸腺体比值均有所升高,同时血清TSH、IgG和C3的水平亦有所升高,且均呈现一定的剂量依赖性。体重增长加快说明模型组大鼠脾脏的运化水谷功能得到改善,IgG和C3的水平升高则从免疫力方面反映了脾阳虚症状的改善,脾体比值的升高和证候积分的降低则进一步说明了模型大鼠的脾阳虚证得到一定的改善;同理,模型大鼠TSH水平的升高提示其甲状腺功能得到恢复,其肾脏和肾上腺的重量指数的升高亦说明其性腺轴和肾上腺轴水平得到改善,证候积分的降低同样说明模型大鼠的肾阳虚证得到缓解[5-7]。但是,比较预防给药和治疗给药的药效,二者的半数有效量相接近,但预防给药的ED95则小于治疗给药,说明附子水提物能对大黄致脾肾阳虚证大鼠的预防药效强于治疗药效。LDH和CTN-I是心脏受到损伤的指标,附子水提物能显著升高血中LDH和CTN-I的水平,并降低大鼠心体比值,且存在一定的剂量依赖性,说明其发挥药效的同时伴有一定的心脏毒性,这与附子的临床不良反应报道相符合[8-9]。综上所述,附子水提物具有一定温补脾阳的功效,且预防给药效果较治疗给药显著,这可能与药物发挥药效时机体的状态有一定的关系。同时附子水提物对脾肾阳虚大鼠具有一定的心脏毒性,但预防给药与治疗给药尚未发现统计学意义。
附子上助心阳、中温脾阳、下补肾阳,为“回阳救逆第一品药”。由于附子具有回阳救逆、补火助阳之功,故若服用过量或阴虚阳亢者若服用,则会造成阳气过盛或亡阴证。鉴于此,“辨证论治”思想显得尤为可贵,“辩证”是为了取得更好的疗效,同时也是为了避免毒副作用。“辨证论治”也是确保临床用药“安全有效”的基本保障,强调的认识中药时不能孤立地去研究药物本身的毒性,而是要着眼于药物与机体的相互关系。《黄帝内经》“有故无殒”思想为我们提供了相关的理论依据。
“有故无殒,亦无殒也”强调的即为辨证施治:“有是故用是药”即“有是证用是药”,实为对中药药性与毒性的认识,强调的是中药“毒-效-证”之间的密切关系,对临床合理用药具有一定的指导作用。“人参杀人无过,大黄救人无功”则是割裂了“毒-效-证”之间的关系,忽略辨证而孤立地评价药物。附子在不同证候模型上体现的功效与毒性有一定的差异,附子毒性的研究不能离开机体病“证”去孤立地研究药物的毒性,而应该充分考虑药物和机体之间的关系,因此附子的功效与毒性应当以中医理论为指导的前提下放在证候的背景下进行合理评价和科学认知,正确理解毒性、功效和证候及三者之间的关系,合理辨证用药才能达到减毒增效的效果。
本实验只考察了附子水提物对脾肾阳虚证大鼠的功效以及心脏毒性作用,其毒性作用机制、作用特点以及附子其他组分的相关作用则尚需进一步研究。
[1]中华人民共和国药典委员会.中华人民共和国药典[S].北京:化学工业出版社,2010:315-316.
[2]邵峰,李赛雷,刘荣华,等.附子对脾阳虚小鼠的抗寒泻作用[J].中国实验方剂学杂志,2011,17(14):176-178.
[3]孙锋,叶柏川,陈辉,等.肾气丸治疗脾肾阳虚型胃溃疡动物模型的实验研究[J].新中医,2012,44(8):168-170.
[4]张永华,姚念宏,王春银,等.脾肾阳虚证动物模型造型初步家验观察[J].山东医药科学实验临床报道,1982(2):1-4.
[5]Hayashi T,stetler-stevenson WG,fleming MV.etal.Immuno-hischem-icalstudy of metalloproteinases and their tissue inhibitors in the lungs of patients with diffuse alveolar damage and idiopathic pulmonary fibrosis[J].Am J Pathol,1996,149(4):1241.
[6]罗慰慈.现代呼吸病学[M].北京:人民卫生出版杜,1997:119.
[7]姜莉,陈佰义,侯显明.肺纤维化大鼠细胞外基质蛋白的变[J].中国医科大学学报,1998,27(1):26.
[8]谢晓芳.附子心脏毒性作用机制研究[D].成都:成都中医药大学,2012.
[9]吕圭源,陈素红,李立文,等.黄芪生脉饮有效部位对心肌缺血大鼠血清CK、LDH、AST的影响[J].浙江中医药大学学报,2006,30(2):208-210.
(2014-01-06收稿 责任编辑:洪志强)
Efficacy-Toxicity-Syndrome Relevancy of Fuzi regarding Its Effect of Warming and Tonifying Spleen Yang
Luan Yongfu1,2,Sun Rong1
(1 Shandong Research Academy of TCM,Shandong Jinan 250014,China;2 Tianjin University of Traditional Chinese Medicine,Tianjin 300073,China)
Objective:To investigate efficacy and toxicity of Fuzi water extract for control and treatment of yang deficiency of spleen and kidney in rats.Methods:Establish rat model of syndrome of yang deficiency of spleen and kidney by administering15%rhubarb powder suspension to rat for 9 days,8.9g·kg-1·d-1everyday and then making it swim in cold water until stressed out.The prevention group was establishing the syndrome model and simultaneously treated with Fuzi.The treatment group was treated after the disease model was established successfully.Treatment duration was 9 days.Syndrome scores and weight were collected,and determined content level of TSH,IgG and cardiac toxicity index C3,LDH,CTn-I.Results:Fuzi water extract could improve the rat model of yang deficiency of spleen and kidney,increase spleen weight,kidney weight,adrenal gland weight and thymus weight to body weight,increase the level of serum TSH,IgG,C3 and LDH,CTn-I,and decrease heart to body weight ratio.Conclusion:Fuzi water extract has preventing and curing effect on syndrome of yang deficiency of spleen and kidney and has certain cardiac toxicity.
Fuzi;Yang deficiency of Spleen and Kidney;Efficacy;Toxicity
R285.5
A
10.3969/j.issn.1673-7202.2014.02.008
国家重点基础研究发展计划(973计划)中医基础理论专项资助项目课题2(编号:2009CB522802)
栾永福,男,在读硕士研究生,中药药理学,E-mail:luanyongfu668@126.com
孙蓉,女,研究员,博士生导师。济南市燕子山西路7号,250014,电话:(0531)82949843,E-mail:sunrong107@163.com

