松杉暗孔菌发酵液的化学成分研究
郭 华,冯 涛,李正辉,刘吉开*
1鞍山师范学院化学与生命科学学院,鞍山 114005;2 中国科学院昆明植物研究所 植物化学与西部植物资源持续利用国家重点实验室,昆明 650201
松杉暗孔菌(Phaeolus schweinitzii),属于多孔菌科(Polyporaceae)暗孔菌属(Phaeolus)的一种木栖寄生高等真菌,菌盖直径一般在8~24 cm 之间,厚度约为2 cm。在我国主要分布于黑龙江、吉林、河北、新疆、四川、云南、广东、台湾等低中海拔的林区,可作药用,煮后可食用,但生吃有毒[1]。文献报道从该菌子实体中已分离得到具有β-分泌酶抑制活性的化合物hispidin[2]。为了进一步从松杉暗孔菌中寻找具有生物活性的次生代谢产物,我们对该菌发酵液进行了系统的化学成分研究,从其乙酸乙酯提取物中分离得到11 个已知化合物,其中1 为新的链状化合物。
1 仪器与材料
比旋光度值由Horbia SEPA-300 旋光仪测定;UV 由UV-210A 型分光光度计测定;IR 由Bruker Tensor27 型红外光谱仪测定(KBr 压片);ESI+-MS由VG AutoSpec-3000 质谱仪测定,高分辨质谱HRTOF-MS 由API QSTAR 飞行时间质谱仪测定;1H NMR 和13C NMR 由Bruker AM-400 和DRX 500 测定,内标为TMS;柱层析硅胶(80~100 目和200~300 目)和薄层层析材料均为青岛海洋化工厂生产;分析型和制备型HPLC 为Agilent 1100 HPLC,色谱柱为Agilent Zorbax SB-C18(4.6 mm × 150 mm,5 μm)和YMC(9.4 mm × 150 mm,5 μm)柱;Sephadex LH-20 为Amersham Biosciences 公司产品;RP-18(40~63 μm)为德国Merck 公司产品。显色方法为254、365 nm 荧光,10%硫酸乙醇溶液和硫酸香草醛处理后加热及碘蒸气显色。
松杉暗孔菌(Phaeolus schweinitzii)于2010年采自于昆明植物园,由中国科学院昆明植物研究所杨祝良研究员鉴定。
2 培养与发酵
由昆明植物研究所李正辉工程师采用斜面转摇瓶液体培养的方法对该菌种进行发酵培养[3]。培养基:葡萄糖5%,猪肉蛋白胨0.15%,酵母粉0.5%,KH2PO4和MgSO4各0.05%,150 rpm,24 ℃摇床发酵25 d,发酵液总量为20 L。
3 提取与分离
松杉暗孔菌发酵液(20 L)除去菌丝体后,用乙酸乙酯萃取三次,提取液合并,减压蒸干得浸膏10.0 g,上硅胶柱色谱粗分,石油醚-丙酮(100∶0→0∶100)梯度洗脱给出组分A~H。组分C(石油醚-丙酮,30∶1)先上正相硅胶柱,用石油醚-丙酮20∶1 分离,后经RP-18 反相硅胶柱色谱,用甲醇-水(90%甲醇)系统洗脱,再用Sephadex LH-20(氯仿-甲醇,1∶1)柱层析,得到化合物3 (5.0 mg)、5 (8.5 mg)、8 (4.0 mg)、9 (3.0 mg)。组分E(石油醚-丙酮,10∶1)组分经正相硅胶柱色谱,用石油醚-乙酸乙酯8∶1 溶剂系统分离,后用Sephadex LH-20(氯仿-甲醇,1∶1)柱层析,再经制备型HPLC,用乙腈/水20∶80→50∶50 梯度洗脱,纯化得到化合物1(3.0 mg)、2(5.5 mg)、7(6.5 mg)。组分F(石油醚-丙酮,5∶1)经正相硅胶柱色谱,以氯仿-甲醇溶剂系统梯度洗脱(100∶1→20∶1)和Sephadex LH-20(氯仿-甲醇,1∶1)柱层析分离,再经制备型HPLC,用乙腈/水40 ∶60梯度洗脱,纯化得到化合物4(3.0 mg)、6(5.5 mg)、10(12.0 mg)、11(15.0 mg)。
4 结构鉴定
化合物1 白色粉末;[α]15D-9.8 (c 0.23,MeOH);UV (MeOH)λmax(log ε)270 (1.8),231(1.7)nm;IR (KBr)νmax3436,2974,2939,1715 cm-1;1H NMR (CDCl3,400 MHz)及13C NMR(CDCl3,125 MHz)数据见表1;ESI-MS (positive)m/z 235[M+Na]+;HR-TOF-MS m/z 235.1314[M+Na]+(calcd for C12H20O3Na,235.1310)。
化合物1 的分子式由其HR-TOF-MS (m/z 235.1314[M+Na]+)确定为C12H20O3,有3 个不饱和度。其IR 谱在3436 cm-1与1715 cm-1处的吸收峰暗示该化合物的结构中应该含有羟基和双键或羰基。在其13C NMR(DEPT)中,该化合物显示1 个双键,1 个含氧CH,2 个CO,2 个CH3和5 个CH2信号。由以上数据可认为化合物1 为链状烯烃,同时包含两个羰基和一个羟基,这些官能团的位置可由HMBC 谱确定:由H-1 (δH2.15,3H,s)与C-2 (δC208.0,s)、C-3 (δC42.9,t)和H-12 (δH1.06,3H,t,J=4.0 Hz)与C-11 (δC35.9,t)、C-10 (δC210.7,s)的HMBC 相关表明两个羰基在2、10 位;由H-6(δH5.47,1H,dd,J=6.4,6.0 Hz)与C-7 (δC130.0,d)、C-8 (δC26.2,t)及C-9 (δC41.5,t)的HMBC 相关表明化合物1 为6-dodecene;另H-3 (δH2.53,2H,m)、H-6 和C-5 (δC71.8,d)的HMBC 相关说明C-5 位为羟基取代。此外,从H-6 的耦合常数(6.4,6.0 Hz)判定该化合物为顺式烯烃,而C-5位的绝对构型由于化合物量较少没有确定。由此化合物1 被确定为(6Z)-5-hydroxy-6-dodecene-2,10-dione。
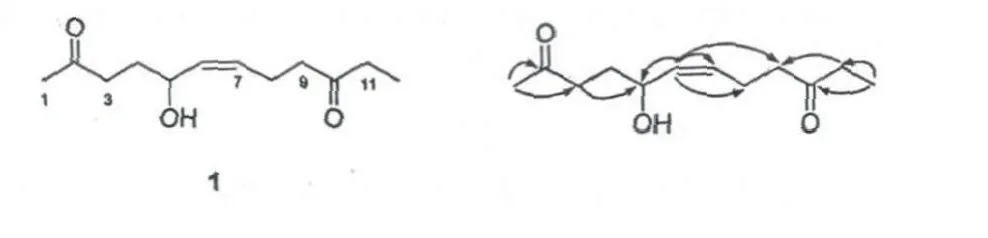
图1 化合物1 的结构和主要HMBC 相关Fig.1 Chemical structure and key HMBC correlations of 1
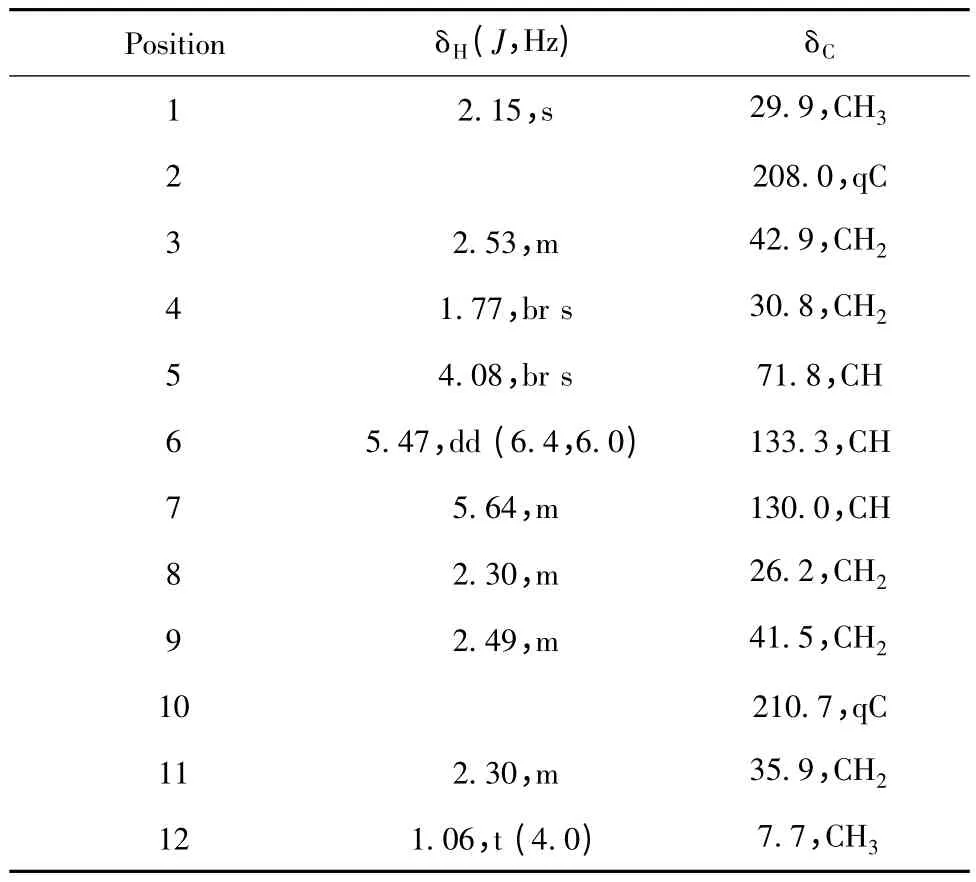
表1 化合物1 的1H and 13C 数据(400/125 MHz,CDCl3)Table 1 1H NMR and 13C NMR data of 1 at 400/125 MHz,respectively,in CDCl3
化合物2C11H12O2,黄色粉末;1H NMR(CDCl3,400 MHz)δ:6.64 (1H,d,J=8.5 Hz,H-8),6.57 (1H,dd,J=8.5,2.9 Hz,H-7),6.47(1H,d,J=2.9 Hz,H-5),6.24 (1H,d,J=9.7 Hz,H-4),5.62 (1H,d,J=9.7 Hz,H-3),1.38(6H,s,2 ×CH3-2);13C NMR (CDCl3,150 MHz)δ:149.5 (s,C-6),146.9 (s,C-8a),132.2 (d,C-3),122.3 (d,C-4),122.0 (s,C-4a),117.0 (d,C-8),115.6 (d,C-7),112.9 (d,C-5),75.9 (s,C-2),27.7 (q,2 ×CH3-2)。上述数据与文献值[4]报道一致,确定该化合物为2,2-二甲基-1-苯并吡喃-6-醇。
化合物3 C18H32O2,无色油状物;1H NMR(CDCl3,400 MHz)δ:5.35 (4H,m,H-9,H-10,H-12,H-13),2.75 (2H,m,H-11),2.34 (2H,t,J=7.6 Hz,H-2),2.04 (4H,m,H-8,H-14),1.63 (2H,m,H-3),1.31 (14H,m,H-4 to H-7 and H-15 to H-17),0.87 (3H,t,J=7.2 Hz,H-18)。上述数据与文献值[5]报道一致,与亚油酸对照品共薄层,Rf值相同,确定该化合物为亚油酸。
化合物4 C10H10O4,无色油状物;1H NMR(C5D5N,500 MHz)δ:7.79 (2H,m,H-3,H-6),7.47(2H,m,H-4,H-5),3.83 (6H,s,2 × OCH3);13C NMR (C5D5N,100 MHz)δ:168.1 (s,C-7,C-8),132.6 (s,C-1,C-2),131.6 (d,C-3,C-6),129.3 (d,C-4,C-5),52.6 (q,2 × OCH3)。上述数据与文献值[6]报道一致,确定该化合物为邻苯二甲酸二甲酯。
化合物5 C28H44O,白色晶体;mp.152~154℃;EI-MS m/z (%):396[M]+(55),363(61),337(40),271(17),253(48),211(37),197(28),185(23),171(30),157(55),143(57),131(27),119(30),91(28),81(27),69(100),55(56);1H NMR(CDCl3,400 MHz)δ:5.56(1H,m,H-6),5.41(1H,m,H-7),5.12~5.28(2H,m,H-22,H-23),3.59(1H,m,H-3),1.02(3H,d,J=6.9 Hz,H-21),0.94(3H,s,H-19),0.91(3H,d,J=6.8 Hz,H-28),0.83(3H,d,J=6.8 Hz,H-27),0.81(3H,d,J=6.8Hz,H-26),0.60(3H,s,H-18);13C NMR(CDCl3,100 MHz)δ:141.1(s,C-8),139.6(s,C-5),135.7(d,C-22),132.2(d,C-23),119.5(d,C-6),116.2(d,C-7),70.4(d,C-3),56.0(d,C-17),54.8(d,C-14),46.2(d,C-9),43.1(s,C-13),40.7(d,C-24),40.7(t,C-4),40.6(d,C-20),39.1(t,C-12),38.5(t,C-1),37.2(s,C-10),33.2(d,C-25),32.3(t,C-2),28.2(t,C-16),23.3(t,C-15),21.1(t,C-11),21.3(q,C-21),19.8(q,C-26),19.5(q,C-27),17.4(q,C-28),16.1(q,C-19),11.9(q,C-18)。以上波谱数据与文献[7]数据报道一致,确定该化合物为麦角甾-5,7,22-三烯-3β-醇。
化合物6 C12H12O2,无色油状物;1H NMR(CDCl3,400 MHz)δ:6.89 (1H,dd,J=2.4,0.8 Hz,H-3),6.77 (1H,dd,J=8.8,2.4 Hz,H-5),6.74 (1H,dd,J=8.8,0.8 Hz,H-6),5.41 (1H,m,H-4'),5.29 (1H,m,H-4'),3.83 (3H,s,OCH3),1.94 (3H,dd,J=1.6,1.2 Hz,CH3-3');13C NMR(CDCl3,125 MHz)δ:154.5 (s,C-1),149.2 (s,C-4),126.9 (s,C-3'),122.1 (t,C-4'),120.1 (d,C-3),116.5 (d,C-5),113.3 (s,C-2),112.4 (d,C-6),94.9 (s,C-2'),84.3 (s,C-1'),56.7 (q,OCH3),23.5 (q,CH3-3').上述数据与文献值[8]报道一致,确定该化合物为Eulatinol。
化合物7 C8H10O2,无色结晶;EI-MS m/z(%):138[M]+(28),107(100),77(14);1H NMR(CDCl3,500 MHz)δ:6.94(2H,d,J=8.5 Hz,H-2,H-6),6.66(2H,d,J=8.5 Hz,H-3,H-5),3.61(2H,t,J=6.8 Hz,H-8),2.63(2H,t,J=6.8 Hz,H-7);13C NMR (CDCl3,125 MHz)δ:154.8(s,C-4),129.6(d,C-2,C-6),129.4(s,C-1),115.0(d,C-3,C-5),64.2(t,C-8),37.8(t,C-7)。以上波谱数据与文献[9]报道一致,确定该化合物为对羟基苯乙醇。
化合物8 C11H10O2,无色油状物;1H NMR(CDCl3,400 MHz)δ:6.82 (1H,dd,J=8.8,0.4 Hz,H-6),6.81 (1H,d,J=3.2 Hz,H-3),6.74(1H,dd,J=8.8,3.2 Hz,H-5),5.43 (1H,m,H-4'),5.36 (1H,m,H-4'),2.01 (3H,dd,J=1.6,1.2 Hz,CH3-3');13C NMR (CDCl3,125 MHz)δ:150.9 (s,C-1),148.7 (s,C-4),126.1 (s,C-3'),123.1 (t,C-4'),117.6 (d,C-3),117.5 (d,C-5),115.5 (d,C-6),109.9 (s,C-2),97.6 (s,C-2'),81.9 (s,C-1'),23.5 (q,CH3-3')。上述数据与文献值[8]报道一致,确定该化合物为Siccayne。
化合物9 C6H6O4,无色片晶;mp.174~175℃;1H NMR (CDCl3,500 MHz)δ:7.14 (1H,d,J=3.4 Hz,H-3),6.45 (1H,d,J=3.4 Hz,H-4),4.56(2H,s,CH2);13C NMR (CDCl3,125 MHz)δ:160.8(s,C-1),159.7 (s,C-2),144.6 (s,C-5),118.6 (d,C-3),109.2 (d,C-4),56.5 (t,C-6)。上述数据与文献值[10]报道一致,确定该化合物为5-羟甲基糠酸。
化合物10 C6H6O2,白色针晶;mp.170~171℃;1H NMR (CDCl3,500 MHz)δ:6.51 (4H,s,H-2,H-3,H-5,H-6)。上述数据与文献值[11]报道一致,与对苯二酚对照品共薄层,Rf值相同,确定该化合物为对苯二酚。
化合物11 C6H6O3,黄色油状物;EI-MS m/z(%):126[M]+(13),125(13),109(100),97(27),81(14),69(6),53(5);1H NMR (CDCl3,600 MHz)δ:9.56 (1H,s,H-1),7.24 (1H,d,J=4.0 Hz,H-4),6.53 (1H,d,J=4.0 Hz,H-3),4.70 (2H,s,H-6);13C NMR (CDCl3,150 MHz)δ:178.0 (s,C-1),160.7 (s,C-2),152.6 (s,C-5),122.6 (d,C-3),109.5 (d,C-4),57.5 (t,C-6)。上述数据与文献值[12]报道一致,确定该化合物为5-羟甲基-糠醛。
1 Mao XL (卯晓岚).The Macrofungi in China (中国大型真菌).Zhengzhou:Henan Science and Technology Press,2000.356.
2 Ueno A,Fukushima S,Saiki Y,et al.Studies on the components of Phaeolus schweinitzii (Fr.)Pat.Chem Pharm Bull,1964,12:376-378.
3 Lu YD(陆云德),Guo HY(郭怀宇),Liu JK(刘吉开),et al.Chemical constituents of the fermentation broth of Tyromyces chioneus.Nat Prod Res Dev (天然产物研究与开发),2013,25:1510-1514.
4 Li X (李想),Yao YH (姚燕华),Zheng YN (郑毅男),etal.Chemical study on fermentation of endophyte fungus GT6105.Chin J Nat Med (中国天然药物),2007,5:20-23.
5 Lu HM (卢慧明),Xie HH (谢海辉),Yang YF (杨宇峰),et al.Chemical constituents from the macroalga Gracilaria lemaneiformis.J Tropic Subtropic Botany (热带亚热带植物学报),2011,19:166-170.
6 Geng JL (耿家玲),Geng CA (耿长安),Chen JJ (陈纪军).Chemical constituents of Swertia cincta.Nat Prod Res Dev (天然产物研究与开发),2012,24:42-46.
7 Du ZW(杜子伟),Liu JS(刘劲松),Wu PY(吴培云),et al.Chemical constituents of Hexagonia speciosa.Chin Tradit Pat Med (中成药),2012,34:1305.
8 Molyneux RJ,Mahoney N,Bayman P,et al.Eutypa dieback in grapevines:differential production of acetylenic phenol metabolites by strains of Eutypa lata.J Agric Food Chem,2002,50:1393-1399.
9 Yin W(尹伟),Wu PY(吴培云),Liang YM(梁益敏),et al.Chemical constituents of sarcocarp of Crescentia cujete.Chin Tradit Pat Med (中成药),2012,34:1523-1528.
10 Cai Q(才谦),Liu YQ(刘玉强),Ma Z(马哲).Isolation and identification of chemical constituents from the fruit and calyx of Physalis alkekengi L.Var.franchetii(Mast.)Makino.J Shenyang Pharm Univ (沈阳药科大学学报),2009,26:807-810.
11 Gao YJ(高云佳),Zhao QC(赵庆春),Min P(闵鹏),et al.Chemical constituents of Lasiosphaera fenzlii Reich.Chin J Med Chem (中国药物化学杂志),2010,20:47-49.
12 Yin HQ(尹宏权),Qi XL(齐秀兰),Hua HM(华会明),et al.The chemical constituents from Saussurea lappa C.B Clarke.Chin J Med Chem(中国药物化学杂志),2005,15:217-220.

