儿童间质性肺疾病的分类、诊断和治疗的新观点
·专家对谈录·
儿童间质性肺疾病的分类、诊断和治疗的新观点
刘秀云主任医师 很荣幸受《中国循证儿科杂志》编辑部的委托,与申昆玲教授邀请的来自美国哈佛大学医学部麻省总医院儿童呼吸中心主任T. Bernard Kinane 教授就儿童间质性肺疾病(interstitial lung disease, ILD)分类、诊断和治疗进行交流,一同参与交流的还有北京儿童医院放射科彭芸主任医师、病理科周春菊主任医师。
1 儿童间质性肺疾病的分类
刘秀云主任医师 ILD是以影像学弥漫性渗出和气体交换障碍为特点的慢性肺疾病,也称为弥漫性肺实质性疾病(diffuse parenchymal lung diseases, DPLD)。病因复杂,病种庞大,已有200多种。
2002年美国胸科学会(ATS)和欧洲呼吸学会(ERS)共同制定了成人DPLD的新分类,包括:①已知病因的,②特发性间质性肺炎,③肉芽肿性的DPLD,④其他少见的DPLD。并将特发性间质性肺炎分为7型,包括了淋巴细胞间质性肺炎(LIP)和隐原性机化性肺炎(COP)。2012年ERS又对ILD做了进一步的分类,除保留2002年的主要分类框架外,特发性间质性肺炎:从遗传角度分为家族性和非家族性;从临床方面分为慢性、急性和亚急性肺纤维化;吸烟相关的间质性肺炎;根据疾病的罕见程度分为常见、少见和不可分型。
然而,儿童ILD类型与成人不尽相同。其中涵盖一些儿童特有的ILD,包括肺生长和发育障碍、神经内分泌细胞过度增生(NEHI)、滤泡性支气管炎、肺间质糖原累积、婴儿慢性肺炎(CPI)和其他的类型。
周春菊主任医师 最近也有文献将儿童ILD分为:①婴儿特有的ILD;②原发于肺部的ILD(特发性间质性肺炎、特发性肺含铁血黄素沉着症、肺泡蛋白沉着症、肺泡微石症等);③伴肺浸润的系统疾病;④已知原因的ILD[蓄积疾病、吸入综合征、感染后闭塞性细支气管炎(BO),药物诱发的肺疾病、过敏性肺炎等]。
刘秀云主任医师 Deutsch等将1999至2004年北美11个儿科研究中心具有肺活检结果的185例年龄<2岁DPLD患儿分类为:①既往体健患儿发生的疾病;②免疫缺陷病患儿发生的疾病;③与全身性疾病相关的疾病;④类似ILD的疾病;⑤婴儿特有的肺疾病。其中婴儿特有的肺疾病的构成比最高,可分为以下4种亚类:a.弥漫性的肺发育障碍,如先天性肺泡发育不良、肺泡毛细血管发育不良伴肺静脉错位;b.表面活性物质功能障碍,如表面活性蛋白B基因(SP-B)、表面活性蛋白C基因(SP-C)和ATP结合盒转运蛋白基因(ABCA3)的突变,组织学特点可为先天性肺泡蛋白沉着症、CPI、脱屑性间质性肺炎和非特异性间质性肺炎;c.肺泡简单化(alveolar simplification)导致的肺生长障碍;d.未知原因的特殊类型的疾病如NEHI和肺间质糖原累积。
Kinane教授您在北京儿童医院做学术访问期间做过一个有关间质性肺炎的学术报告,提出的分类方法明显有别于既往文献报道的分类方法。
Kinane教授 儿童肺间质疾病是一组累及肺间质的疾病。显著临床特点是持续性低氧血症、持续性肺细爆裂音,同时患儿一般无明显的免疫疾病或综合征或先天代谢紊乱。该病的发病率较低,有一定的家族聚集性。目前麻省总医院儿童呼吸中心主要依据解剖部位对该病进行分类(表1)。

表1 儿童ILD的分类
儿童ILD的分类到目前均不令人满意。分类的目的是为了更好的诊断此组疾病。儿童ILD有其自身特点。从解剖位置来分类(图1),如肺泡疾病、气道疾病和间质疾病。可以先确定病变是在肺泡、小气道还是间质。
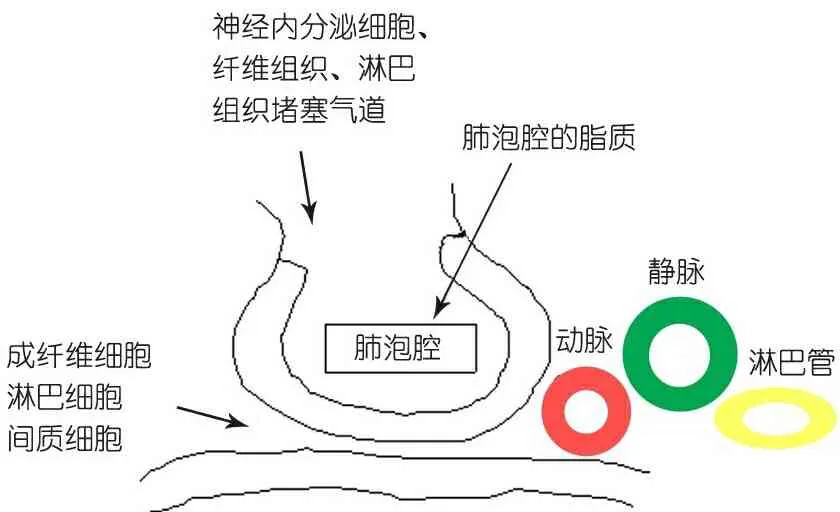
图1 肺泡的解剖结构示意图
肺泡内病变与基因突变相一致,如患儿肺泡内病变,其基因突变的概率几乎达100%,不必再进行病理分类。小气道疾病可从肺部影像学诊断,以NEHI较常见,滤泡性支气管炎和BO少见。对发生于间质的ILD,以其中填充的细胞为分类依据。
在基因筛查前,许多ILD只有病理诊断,因此旧的分类主要依靠病理类型制定。既往的分类提到的CPI和婴儿肺泡蛋白沉着症,现在发现是由于表面活性物质途径基因的突变造成,因此在基因突变明确时,就不再对该组疾病进行病理分型或病理诊断。
2 儿童ILD的诊断方法
刘秀云主任医师 在ILD的诊断过程中,通常依据影像学提示是否为ILD。如为ILD需寻找病因,以确定是继发性或特发性的ILD。探索病因时,应先进行非侵入性检查,如病原学检查排除HIV、CMV和EBV感染;结合血清免疫学检查来诊断风湿性疾病、血管炎和免疫缺陷病。还要详细询问病史有无环境因素的暴露(如有害气体的吸入、大量吸入有机过敏原)。若非侵入性的检查不能明确病因,可进一步进行侵入性检查,如纤维支气管镜的支气管肺泡灌洗液的获取、肺组织病理检查。当然,基因突变也是儿童ILD很重要的因素。
Kinane教授 当遇到ILD患儿,可以从以下2个方面来判断,一是肺部听诊有没有爆裂音;二是从影像学特点来判断。如听诊有爆裂音, 肺CT上存在高灌注区和低灌注区交替的区域,应考虑到小气道病变。在美国,通气不均患儿绝大多数为NEHI,其他的类型少见。如X线胸片和肺CT可见弥漫性的实质浸润,要考虑到过敏性肺炎、肺泡出血和CPI等可能,既往健康的患儿出现弥漫性的实质浸润,多数是肺泡出血或过敏性肺炎,还应想到表面活性物质基因的突变。
因此,对于弥漫性肺实质浸润的患儿应进行基因筛查。表面活性物质的基因突变可引起婴儿肺泡蛋白沉着症、CPI和脱屑性间质肺炎,且基因突变所致的ILD病情均较重,查体可闻及爆裂音,但不密集,胸部X线和 CT 显示弥漫性的磨玻璃影。
彭芸主任医师 影像学可判断小气道病变和肺泡病变。肺CT马赛克灌注征、树芽征和小叶中心型结节通常为小气道的病变。北京儿童医院对于小气道疾病,常诊断为BO,也有诊断为弥漫性泛细支气管炎。胸部X线和CT弥漫性磨玻璃影一般为肺泡渗出性病变,也可见于特发性肺含铁血黄素沉着症、特发性间质性肺炎和过敏性肺炎等。但有时患儿的病变可累及到多个部位,从影像学上确定哪个位置的病变有时比较困难。
周春菊主任医师 目前,在ILD的诊断过程中,更强调临床-放射-病理的综合诊断。病理是ILD的诊断金标准。肺活检有不同方法如开胸肺活检、胸腔镜引导下肺活检、经支气管镜的透壁肺活检和经皮肺活检。
Kinane教授 临床-放射-病理的综合诊断很重要。肺部CT能很好地反映肺部病变的特点,可为ILD临床诊断提供线索。肺组织病理是ILD的诊断依据。麻省总医院儿童呼吸中心主要做开胸肺活检,通常由外科医生完成,大部分是微创的。胸腔镜引导下的肺活检在儿科应用广泛,取材也理想,创面小。经支气管镜肺活检由于标本小可能得不到足够多的信息,所以约50%的患儿行开胸肺活检。对于间质性肺炎,即便是成人,穿刺活检的效果也不理想。对于肺实体肿瘤患儿,可以做经皮穿刺的肺活检。
刘秀云主任医师 在北京儿童医院ILD通常采取胸腔镜引导下的肺活检,取材比较理想,创伤小。对于靠近胸膜的病灶,如大结节影或真菌感染,采取过针穿肺活检。开胸肺活检做的比较少。
3 几种常见的ILD的诊断要点
周春菊主任医师 在北京儿童医院肺活检的患儿,没有诊断为NEHI的病例,可能与<1岁患儿肺活检病例少有关。
彭芸主任医师 肺CT通气不均可能为NEHI、细支气管中心性肉芽肿和BO。北京儿童医院未能诊断出NEHI,不是没有NEHI的病例,是对其认识不足,错过了对NEHI的诊断。
Kinane教授 NEHI的特点为肺部爆裂音,低氧血症。早期发病的低氧血症一般在3~8 月龄发病,80%为足月儿,X线胸片显示过度通气,高分辨CT特征为区域性过度通气和磨玻璃影交替出现。肺活检一般无阳性发现,胃肠肽的免疫组化可发现神经内分泌细胞过度发育不协调。最近国际儿科间质性肺病的指南指出,婴儿肺部听诊有爆破音,X线胸片有过度通气,肺CT提示通气不均,足以做出NEHI的诊断。
周春菊主任医师 NEHI是神经内分泌细胞过度增生所致的呼吸急促,也称为婴儿持续性的呼吸增快。如果没有病理的证据能确诊NEHI吗?
Kinane教授 也许刚开始认识NEHI的时候,需要肺活检来证实。随着对NEHI的认识,目前大多数病例不需肺活检来诊断NEHI。过去3年,我在麻省总医院儿童呼吸科只做过3例NEHI的肺活检,因为病情太重才做了肺活检。在影像学证实的小气道病变中,NEHI应该是首先想到的诊断。如有爆裂音和过度通气,NEHI是目前为止的第1诊断。第2诊断是BO。通常,在美国诊断20例NEHI患儿之后,才可能诊断1例其他小气道疾病。
刘秀云主任医师 关于北京儿童医院一直以来没有诊断过NEHI的病例,是值得思考的。自2001年以来,北京儿童医院诊断了147例BO,多发生于1岁以后,多为急性肺损伤的后遗症,临床可表现为感染或急性肺损伤后持续性喘息、肺部可闻及喘鸣音和(或)爆裂音,肺部CT可有通气不均、支气管扩张。如何鉴别NEHI与BO呢?
Kinane教授 NEHI大多数在生后第1年发病,平均诊断年龄是8月龄,可于生后2~3个月起病。 通常误认为RSV感染的患儿,其实是NEHI。而大多数BO发病较晚。所以我的观点是NEHI很普遍。
滤泡性支气管炎与 NEHI有一定重叠,麻省总医院儿童呼吸中心报道的6例特发性的滤泡性支气管炎,均于出生后6周就诊。在6和18月龄症状达高峰,主要症状为呼吸快,咳嗽,中等度的呼吸困难。肺内有爆裂音。影像学表现为间质性改变。病理可见支气管周围的淋巴组织过度发育,压迫支气管腔、淋巴细胞的生发环围绕细支气管,细支气管腔内有少量的急性脓性分泌物,支气管中心型的肉芽肿很少见。
刘秀云主任医师 滤泡性支气管炎在成人有1/3与风湿性疾病有关,还有与感染如HIV和免疫缺陷有关。北京儿童医院还诊断过儿童感染因素所致的滤泡性支气管炎。
Kinane教授 细胞间质性肺炎/肺间质糖原累积比较少见,发病年龄与NEHI一致,均<1岁。诊断比较困难。病变部位在间质, 可见间充质细胞, 缺乏炎症,病变细胞可和淋巴细胞混淆。电镜下可见单一含糖原的颗粒,无其他细胞器。考虑为肺细胞的分化异常。
周春菊主任医师 细胞间质性肺炎/肺间质糖原累积是发育过程中,肺部有糖原细胞的累积,是一良性的病程,与糖原累积病的概念不同。诊断主要靠病理。
刘秀云主任医师 在继发性的ILD中,过敏性肺炎应该多见,但临床易混淆为特发性间质性肺炎(如非特异性肺炎)。而且不是所有的环境暴露者均可导致过敏性肺炎,也不是所有过敏性肺炎的病理均有肉芽肿的存在,沉淀抗体也可有假阴性。因此,过敏性肺炎的诊断其实很困难。
Kinane教授 这是个非常有意思的问题,因为过敏性肺炎的诊断的确很困难,在麻省总医院儿童呼吸中心有一个过敏性肺炎的专家小组。诊断方法和贵院相似,有特征性的暴露史,多数有肺部爆裂音。但在ICU发现的一些重症患儿,肺内听不到爆裂音。进行免疫沉淀抗体检测,若为阳性,就不必做肺活检,如阴性且没有过敏的证据,才需要进行肺活检。
彭芸主任医师 过敏性肺炎影像学特点为弥漫的细小结节影和磨玻璃影,临床诊断的病例主要为亚急性的病例。慢性过敏性肺炎还可见小气道阻塞的表现,如影像学提示马赛克灌注征、呼气相的气体滞留。
周春菊主任医师 曾有病例影像学为弥漫的细小结节影和磨玻璃影,病史也有环境暴露史,但病理并未证实为过敏性肺炎。过敏性肺炎的病理诊断中,找到非干酪样的肉芽肿或多核巨噬细胞是确诊的依据。
Kinane教授 从病理学的观点来看,没见到肉芽肿诊断过敏性肺炎的确非常困难。有时只能看到淋巴细胞浸润意义并不大。另外还可以从支气管肺泡灌洗液中淋巴细胞尤其是CD8+为主的T细胞增加可以协助诊断。淋巴细胞如CD8+T细胞和过敏性肺炎高度相关。
刘秀云主任医师 有关这方面的儿科研究表明,支气管肺泡灌洗液中的确发现淋巴细胞增加,但并无CD8+T细胞的增加。
Kinane教授 麻省总医院儿童呼吸中心每年确诊2~3例过敏性肺炎,病情都很严重,但预后较好,患儿年龄大多>10岁,多与鸟类如鸽子接触有关。
4 关于基因突变研究进展
刘秀云主任医师 在儿童ILD领域的一个重要发展是发现了表面活性物质代谢异常,包括SP-B、SP-C和ABCA3基因的突变。这些基因的突变可引起儿童ILD。
Kinane教授 SP-B、SP-C为肺表面活性蛋白的成分。ABCA3为细胞膜表面转运蛋白。SP-B缺乏症是一种常染色体隐性遗传病,SP-B基因位于人的2号染色体上,约9.5 kb的基因编码一个2 kb mRNA转录本,该转录本可转录为381氨基酸前蛋白,经糖基化和一系列的蛋白水解产生79氨基酸疏水的成熟SP-B蛋白。最常见的原因是121ins2基因突变,即在基因位置编码121的g.1549的GAA替换C 。这一基因突变占SP-B缺乏症的70%。通常表现为生后不久的肺泡蛋白沉着症,也可以为脱屑性间质性肺炎。
SP-C基因突变为常染色体显性遗传,是引起婴儿、儿童甚至成年急、慢性肺部疾病的少见原因。临床表现多样,婴儿可表现为与SP-B基因突变类似的新生儿期的RDS。也可以成年期起病,逐渐出现呼吸功能不全、低氧血症、生长困难以及X线胸片间质性肺炎的改变。
ABCA3基因突变表现多样化,是足月新生儿致命性肺疾病和ILD的一个原因,其临床表现类似于SP-B缺乏症。可表现为肺泡蛋白沉积症、脱屑性间质性肺炎和非特异性间质性肺炎。病理为肺泡Ⅱ型上皮细胞的过度发育,肺泡腔内有泡沫细胞,电镜可见板层体的异常。
刘秀云主任医师 儿童脱屑性间质性肺炎、CPI预后差,主要与ABCA3、SP-C基因突变有关。肺泡蛋白沉着症主要与SP-B、ABCA3基因突变有关。ABCA3基因位于常染色体16p13.3,包含33个外显子,其中前3个外显子不被翻译,该基因包括80 000个碱基,转录为6 500 bp的mRNA,指导合成含1 704个氨基酸的ABCA3蛋白,该蛋白质在肺中高度表达,位于Ⅱ型肺泡细胞的板层状小体的界膜上,其主要功能是运输表面活性物质的重要脂质。
彭芸主任医师 表面活性物质的基因测序和筛查也可能存在很多问题,比如有的患儿SP-C基因突变,其表面活性物质缺乏,但功能可能正常,有的发病早,有的可能到成年才发病。
Kinane教授 是的,SP-B、SP-C和ABCA3基因突变,存在基因表达的多样性。通常两条染色体上有一对等位基因。 对于杂合子,通常有一半的基因突变,另一半的基因功能正常。但临床上表现为75%正常, 25%不正常。然而,也有一些基因突变的病例随着年龄增长,基因甲基化会做出代偿,病情因多种原因可得到改善。尽管如此,仍建议做SP-B、SP-C和ABCA3基因筛查。
刘秀云主任医师 在儿童ILD中SP-B、SP-C和ABCA3基因突变的发生率有多大?
Kinane教授 <6个月怀疑ILD的患儿,50%的患儿存在基因突变;<1岁ILD患儿基因突变占较大的比例,而且病情较重。基因突变在<1岁肺泡疾病患儿中非常普遍,因此应行表面活性物质的基因筛查。当遇到1例严重ARDS的患儿时,需要做SP-B、SP-C和ABCA3基因突变筛查。
周春菊主任医师 在ILD中唯一致死性的疾病为基因突变所致的ILD,当然基因检查未突变的患儿,可依据临床和影像的特点,考虑下一步的诊断方法如肺活检,对其进行病理诊断。
5 儿童ILD的治疗
刘秀云主任医师 儿童ILD一般可应用糖皮质激素治疗,也有一些ILD不用糖皮质激素治疗(如肺泡微石症、肺泡蛋白沉着症)。糖皮质激素治疗可使部分病情可得到改善,但也有一些病例病程长,对糖皮质激素治疗反应差。
Kinane教授 气道疾病,婴儿多数为NEHI、滤泡性细支气管炎。NEHI患儿病情可自行缓解,大多数症状3年内得到了改善,但也有部分患儿的症状持续到青春期,但相对来说NEHI是一个良性的过程。以往尝试过的各种治疗对肺状态没有改善,因此NEHI患儿可采取对症治疗。滤泡性细支气管炎预后也较好,可不需治疗。
肺泡疾病中脱屑性间质性肺炎、CPI预后均不良,对糖皮质激素治疗反应不明显。而过敏性肺炎、急性间质性肺炎、非特异性间质性肺炎和机化性肺炎对糖皮质激素治疗反应好。特发性肺含铁血黄素沉着症的急性出血对糖皮质激素治疗也有很好的效果。基因突变所致的ILD预后很差,存在SP-B基因突变的患儿,大多数于生后6个月死亡。SP-C和ABCA3基因突变大多数于18岁前死亡。对于ABCA3基因突变,羟氯喹可能有效。
细胞间质性肺炎/肺间质糖原累积的预后较好,但呼吸快可持续4~18个月。此病为良性病程,对羟氯喹治疗有反应。
刘秀云主任医师 非常高兴与Kinane 教授、彭芸主任医师和周春菊主任医师就儿童ILD的分类、诊断和治疗进行讨论,希望能对国内临床医师认识儿童ILD有所启迪,如①婴儿的小气道疾病,应考虑到NEHI、滤泡性支气管炎;②<2岁的肺泡性疾病或起病早治疗效果差的儿童ILD要考虑到SP基因突变;③从病变位置对儿童ILD进行分类简单、易掌握。
10.3969/j.issn.1673-5501.2013.01.001
T. Bernard Kinane Department of Respiratory, Harvard University School of Medicine, Massachusetts General Hospital;刘秀云,彭芸,周春菊 首都医科大学附属北京儿童医院 北京,100045
刘秀云,E-mail:liuxiu_yun@126.com

T.BernardKinane 教授刘秀云 主任医师彭芸 主任医师周春菊 主任医师
2012-10-20
2012-12-27)
张崇凡)

