0Cr15Ni5Cu3Nb不锈钢在Cl-介质中的点蚀行为
李元松,杨树和,黄 鑫,方明敏
(扬州大学 机械工程学院,江苏 扬州 225127)
0 引言
0Cr15Ni5Cu3Nb不锈钢以其优良的耐蚀性能广泛应用于管道、航空等领域,工作在高温、高湿的腐蚀性环境中[1]。在特定的环境下,如Cl-存在时,其常常会产生点蚀,点蚀可以作为裂纹源,引起设备过早破坏,甚至发生灾难性事故。
用电化学法测量该不锈钢的点蚀,化学浸泡法选择质量分数为6% 的FeCl3溶液[2]。为防止试验过程中因腐蚀产物、试验参数选择等原因的影响,故同时采用电化学测量法和化学浸泡法两种方法[3]。
1 实验方法
1.1 实验材料
以0Cr15Ni5Cu3Nb 不锈钢为主要研究对象,其化学成分见表1。

表1 0Cr15Ni5Cu3Nb不锈钢的化学成分(质量分数) %
1.2 试样制备
将材料加工成Φ30 mm×2 mm 的圆形试样片。逐级打磨后,水洗并用丙酮除油,去离子水清洗后吹干。选择质量分数为50%的硝酸钝化液进行常温化学钝化,钝化时间为30min。
1.3 测试方法
动电位实验介质是质量分数为3.5% 的NaCl标准溶液,实验在电位稳定后进行,从自腐蚀电位开始扫描,扫描速率为120mV/min。
FeCl3浸泡实验参照GB433417-1984。
2 实验结果与讨论
2.1 动电位极化实验
2.1.1 动电位阳极氧化曲线
图1为两种试样的阳极氧化曲线,由图1可以看出,两个曲线都分为3段区域[4]。第一区域位于腐蚀电位附近,两条极化电流随着极化电位的增大而增加,受电子转移的电化学活化控制。第二区域中,极化电流虽随极化电位的升高而增大,但极化曲线的斜率越来越小,这时两个试样的电极化过程阻力增大。第三区域中,极化电位进一步升高,曲线出现转折点,出现了点蚀,极化曲线2在外加电位达到1 138mV 左右时出现了拐点,此时腐蚀电流不像曲线1那样出现点蚀,并稳定了一段时间,在此期间钝化膜的修复和被Cl-破坏呈现一个接近平衡的状态,这是钝化后点蚀击穿电位升高的原因。可见采取适当钝化工艺,可提高该钢在Cl-介质中的耐点蚀性能。
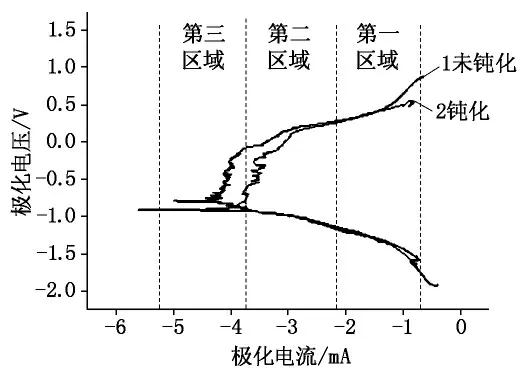
图1 两种试样的阳极氧化曲线
2.1.2 SEM 分 析
图2、图3 分别为两种试样的表面形貌。由图2、图3可明显看出未钝化的试片表面有许多小鳞片状凸起,从而导致表面形貌的不完整,而硝酸钝化的试片表面显得较为平整,有效清除了材料表面微观凸起部分,降低了表面粗糙度和表面物理缺陷可能造成的活性点,在一定程度上避免了在含有Cl-的腐蚀介质中形成的局部点蚀。
2.2 FeCl3 浸泡实验
2.2.1 腐蚀速率
采用FeCl3溶液作为点蚀的加速实验溶液,用失重法计算出各个腐蚀时间的腐蚀速率。腐蚀速率曲线见图4,各组试样腐蚀速率见表2。

图2 未钝化的试样表面形貌

图3 钝化的试样表面形貌
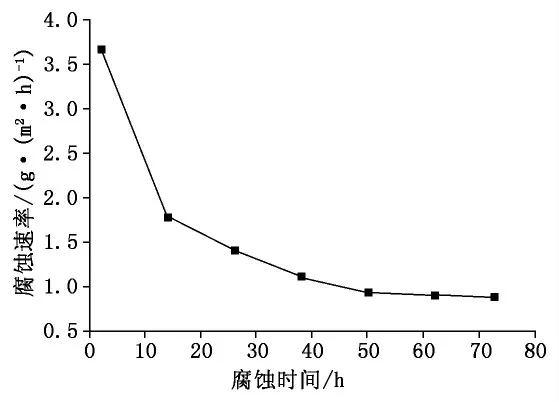
图4 试样不同时段的腐蚀速率曲线
由表2和图4中可以明显看出,试样在前12h的腐蚀速率非常快,但在36h后腐蚀速率趋于平缓,两者相差将近3倍。这表明:对于0Cr15Ni5Cu3Nb不锈钢基于氯离子环境下的腐蚀,初期阶段是防护的重点。
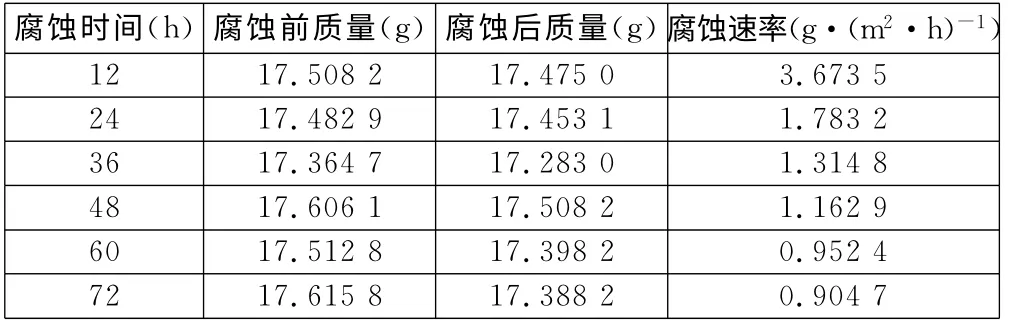
表2 各组试样腐蚀速率
2.2.2 SEM 分 析
由于闭塞电池效应[5,6],内层形成的金属氯化物溶液更加浓缩,这种富集Cl-的溶液可以使被腐蚀的金属表面断续的维持活性。随着时间的推移,不仅初生蚀孔自身长大外,还会在内壁形成核并产生新的点蚀小孔,如图5所示。新核形成使蚀孔迅速穿进,以至穿透壁厚。所以防止0Cr15Ni5Cu3Nb 不锈钢点蚀,要避免Cl-集中,比如加快阀门或管道中含有Cl-溶液的流动性。

图5 蚀孔内新核的形成
3 结论
(1) 适 当 的 钝 化 工 艺 有 效 清 除 了0Cr15Ni5Cu3Nb不锈钢表面微观凸起部分,一定程度上避免了由于Cl-形成的局部点蚀。
(2)对于0Cr15Ni5Cu3Nb不锈钢基于氯离子环境下的腐蚀,开始阶段的腐蚀速率要比末期快,所以初期阶段是防护的重点。
(3)富集Cl-的溶液不仅可以使0Cr15Ni5Cu3Nb不锈钢表面的初生蚀孔自身长大外,还在初生蚀孔内壁形成核并产生新的点蚀小孔。
[1] 陈美艳,童洪辉.15-5PH 不锈钢表面多弧离子镀高结合性能TiN膜层研究[J].功能材料,2012,43(13):1802-1805.
[2] Frankel G S. Pitting corrosion of metal[J].J Electrochem Soc,1998,145(6):2186-2198.
[3] 王常青,丁毅,马立群,等.304和2304不锈钢在Cl-介质中的耐蚀行为[J].压力容器,2007,24(5):1-4.
[4] 周萍,汪小琳.铀在三种溶液中的动电位极化和电化学阻抗谱研究[J].中国腐蚀和防护学报,2008,28(4):215-218.
[5] 曹楚南.腐蚀电化学原理[M].第2版.北京:化学工业出版社,2004.
[6] Souto R M,Gonzalez-Garcia Y,Gonzalez S.In situ monitoring of electroactive species by using the scanning electrochemical microscope: Application to the Investigation of degradation processes at defective coated metals[J].Corrosion Science,2005,47(12):3312-3323.

