D2EHPA/TBP协同萃取除铁铬锰制备超纯硫酸氧钒*
郭秋松,刘志强,朱 薇,戴子林
广东省工业技术研究院(广州有色金属研究院),广东 广州 510650
全钒液流电池(VRB)是一种优秀的储能装置,硫酸氧钒是全钒液流电池电化学反应的活性物质及电能的载体,是全钒液流电池的关键材料,对电池综合性能有影响[1-5].以高纯度硫酸氧钒配制电解液,有利于提高电池的稳定性、循环性能及能源密度和充放容量.由元素周期表可知,铁、铬、锰等黑色金属元素的原子序数与钒的临近,同属具有较高丰度的第一过渡系,它们的离子半径相近,均属化合价易变化元素,各自具有活跃的特定电化学性质,铁、铬、锰等黑色金属元素是影响钒电池综合性能的敏感杂质,即便少量混入电解液中,也会严重干扰钒的充放电行为,不仅会使全钒液流电池的电活性降低,而且会使电极的可逆性变差.
我国拥有丰富的炼钢钒渣及含钒石煤资源,以它们为原料,经水浸或酸浸所得粗钒溶液,经结晶、沉淀、萃取初步提纯后,溶液中仍含较高的铁、锰、铬等黑色金属杂质元素,溶液中钒与铁、锰、铬三杂质元素总量的质量比常小于50,不能直接用作全钒液流电池的电解液,需对其进行深度除杂与纯化[6].传统工艺中,通常采用铵盐沉钒方法净化含钒溶液,将其转化为高纯五氧化二钒后加酸复溶,此过程需要经历溶液氧化、铵盐选择性沉钒、过滤、煅烧、酸溶、还原等工序,工艺复杂、成本高、钒利用率低,而且纯化过程必须加入的化学品又会将有关杂质元素重新带入溶液中[7].
在湿法冶金过程中,溶液除杂纯化始终是受到关注的关键步骤.当前应用最广的溶液纯化方法主要是化学沉淀法和溶剂萃取法,其中溶剂萃取法是利用离子在两种互不相溶的液相间分配性质的差异,来达到分离和提纯目的,该法有平衡速度快、处理容量大、分离效果好、回收率高、操作简捷及经济性优等特点,是稀土元素分离、镍钴湿法冶金、稀有金属提取及放射性核素浓缩过程中的主流方法[8-9].
本文以石煤提钒酸浸液为研究对象,采用D2EHPA-TBP-磺化煤油协同萃取体系对含钒溶液进行深度除杂纯化,同时分别研究溶液的初始pH值、相比、反萃取综合条件等因素对萃取过程的影响,以获取制备超纯硫酸氧钒电解液的优化萃取工艺参数.
1 实验部分
1.1 原料及试剂
试验初始原料为经硫酸两段循环浸出并初步除杂的含钒溶液,该溶液由陕西渭南某石煤钒矿提供,该溶液中含钒量为(以V2O5计)88.07g/L,杂质元素铁、锰、铬含量分别为1983mg/L,15.1mg/L和36.2mg/L,溶液初始pH 值为0.63.
主要试剂:D2EHPA(P204)由洛阳奥达化工公司生产,磷酸三丁酯(TBP)由天津富宇精细化工公司生产,浓度25%的氨水和浓硫酸由广州化学试剂厂生产,抗坏血酸由上海伯奥生物科技公司生产.上述试剂均为分析纯,实验中不需进一步纯化而直接使用.磺化煤油用作稀释剂,由市售普通煤油自制.
D2EHPA与TBP组成协同萃取体系,其中萃取剂D2EHPA、协萃剂TBP和稀释剂磺化煤油的体积比为20︰5︰75,配制时搅拌混匀.溶液pH值用浓度为25%的氨水调整,除pH值条件实验外,溶液起始pH值均控制在2.6.抗坏血酸为还原剂,浓硫酸经稀释后用作反萃剂.
1.2 测试方法及仪器
溶液中金属杂质含量采用ICP-AES法测试,光谱仪为PS-6真空型,美国贝尔德公司生产;采用硫酸亚铁铵标准滴定法测试溶液中的钒含量;用精密pH计测试溶液的pH值,pH计为pH500台式酸碱度计,美国CLEAN公司生产.
仪器:250mL的分液漏斗;江苏金坛富华仪器公司生产的KS-2型康式电动振荡机,振幅为36 mm,振动频率为4Hz.
1.3 协同萃取
所有萃取及反萃取的实验均是在室温下进行的,初始溶液的pH值用浓度为25%的氨水调节后,再加入按被还原杂质含量化学计量比1.2倍的抗坏血酸还原溶液,按照一定相比将有机相和待萃水相置于分液漏斗中,用康氏振荡器振荡15min.分别测试水相萃取前及萃取后所含的钒及杂质元素的含量,并用减量法推算钒及杂质元素萃入有机相中的量.有机相经洗涤后,进行反萃取.
分配比D为萃取平衡时金属在有机相中浓度与水相中浓度的比值,由分配比计算出金属的萃取率E=D×100/[D+(Vaq/Vorg)],其中Vaq和Vorg分别为水相和有机相的体积.金属回收率TM为反萃收液中所含金属量对萃前液中所含金属量的百分比(M分别代表Fe,Mn和Cr元素),反萃收液中钒与铁、锰及铬杂质的质量比K=m(V)/m(Fe+Mn+Cr).
2 结果与讨论
2.1 起始pH值的影响
酸性萃取剂的反应是发生在两相间的可逆阳离子的交换过程,所以萃取过程是一个不断产酸的过程,当用碱中和不断产生的酸,有利于萃取连续进行及提高金属的萃取量,所以原料液起始pH值对萃取过程中的D值和E值影响显著.由于起始溶液pH值大于3时,会产生钒沉淀现象,因此起始pH值的考察范围设定为1.5~3.0之间.
常温下将含钒原料液加入烧杯中,边搅拌边加入过量的抗坏血酸,以还原溶液中杂质离子,再加浓度为25%的氨水将含钒溶液的pH值精确调整到实验所需,然后将溶液装入250mL分液漏斗中进行三级逆流协同萃取.萃取过程在康氏振荡器上进行,其中相比为V(O)/V(A)=1︰1,萃取(振荡)时间为15min以达到萃取平衡.然后对载钒有机相用去离子水洗涤5min,用浓度为1mol/L的稀硫酸按相比1︰1进行二级逆流反萃取,反萃取10min后对反萃收液中钒及杂质元素含量进行测定,以计算钒的回收率及杂质去除率.不同起始pH值条件下萃取结果列于表1.
由表1可知,随着溶液初始pH值的增加,钒萃取率随之提高,二者基本呈线性关系,初始pH值越高,越有利于钒的萃取,但同时铁、锰及铬等杂质元素的被萃率也相应有一定程度提高.当起始溶液pH值为2.3,2.6及2.9时,经二级逆流反萃取后,钒的直接回收率分别为60.1%,63.6%和68.5%,有机相中钒的平均反萃率约为91%,反萃收液中钒与杂质质量比从初始溶液的43.3大幅度地提高至1083~1135之间,表明实验所采用的协同萃取体系适合于从含钒溶液中分离铁、锰和铬.起始溶液pH值从1.7增加到2.9时,杂质去除率在96.0%到96.2%的狭窄范围内上升,说明起始溶液pH值对除杂效果影响较小,为了钒有较高的被萃取率,起始溶液pH值应调整在2.5~3.0范围内较适宜.
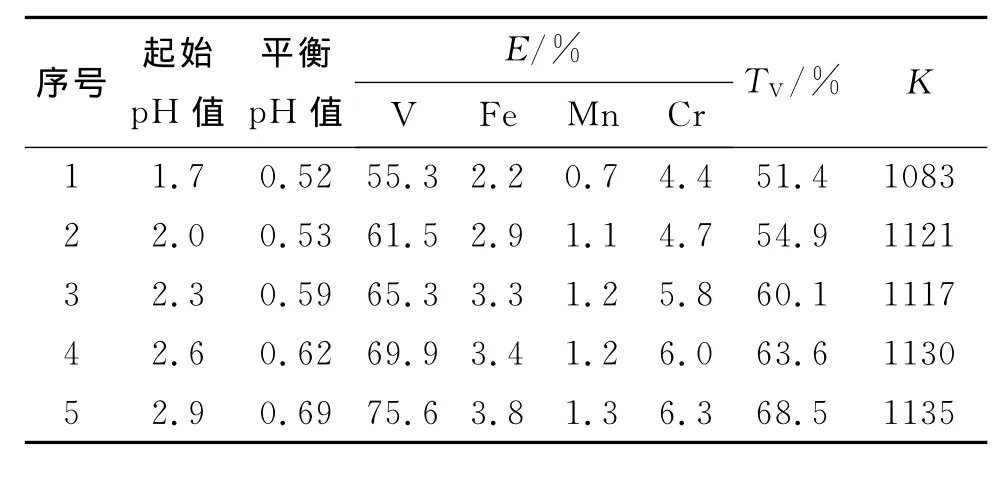
表1 不同起始pH值下萃取实验结果Table1 Results of extraction experiments with different pH value
2.2 相比对萃取过程的影响
相比是萃取及反萃过程中的重要技术参数之一,可通过相比来调控反萃收液的浓度,萃取过程中有机相与水相之比大时,金属萃取率相应上升,易萃组份直收率提高,但是萃取过程中有机相投入相应增多,会使有机相损失加大,增加萃取运行成本.
将过量还原剂加入初始溶液中后,再加25%的氨水,并将含钒溶液的pH值精确调整至2.6,控制有机相与水相的比值分别为3,2,1.5,1和0.5,考察不同相比对萃取过程的影响.表2为不同相比条件下金属萃取率及反萃后钒回收率TV及反萃收液钒与铁锰铬杂质的质量比K的结果.
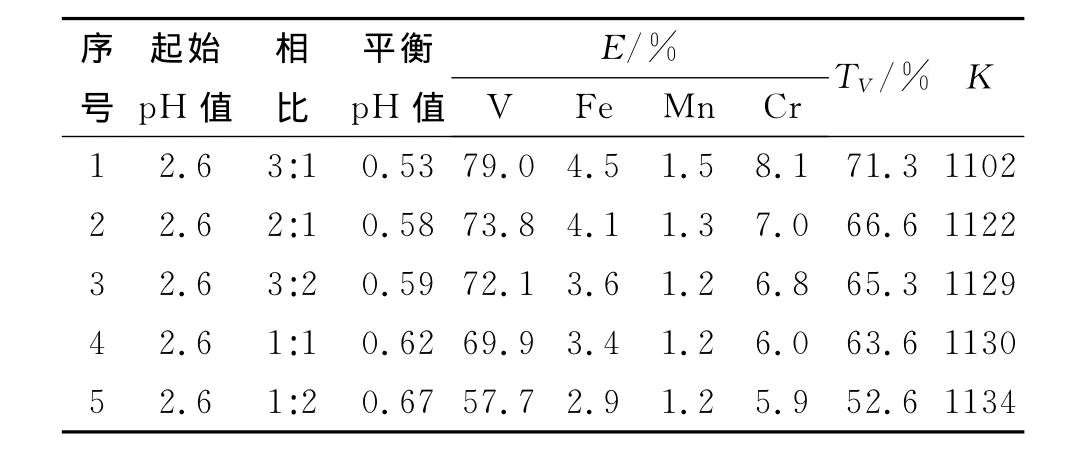
表2 不同相比下的萃取结果Table 2 Results of extraction experiments at different A/O ratios
由表2可知:有机相与水相的比值对钒萃取率影响较大,同时也轻微影响杂质元素的萃取率;高的相比有利于提升钒的萃取率,但杂质元素的萃取率也有轻微上升;相比值对杂质的脱除率影响较小.综合考虑,为保证钒有较高的萃取率及萃取剂投入成本和运行成本较低,应选取相比为2︰1较适宜.
2.3 反萃综合条件对萃取过程的影响
通过反萃取获取高纯溶液,为了提高萃取和反萃取过程中的钒与杂质元素分离效率,针对载钒有机相进行严格的洗涤是必要的.
在起始pH值为2.6、萃取相比为2︰1条件下,用稀硫酸洗涤所得载钒有机相,控制洗涤相比为1︰1,洗涤时间5min,洗涤过程在康氏振荡器上进行.表3为不同浓度的稀硫酸洗涤载钒有机相的实验结果.

表3 不同浓度稀硫酸洗涤载钒有机相结果Table 3 Results of scrubbed to the loaded organic phase using various H2SO4concentrations
由表3可知:当洗涤稀硫酸pH值由5.0降至1.7时,铁的洗脱率由0.3%升至44.2%,相应钒的洗脱率也由0.01%升高至38.7%;当所用洗涤稀硫酸的pH值低于2时,伴随钒的同步洗脱,洗涤作用不明显,而用pH值高于2的稀酸洗涤,铁的洗脱率低,同样效果不好.
对载钒有机相用低浓度纯钒溶液进行洗涤,控制洗涤相比为1︰1,洗涤时间5min,不同钒含量的纯钒液洗涤载钒有机相的实验结果列于表4.
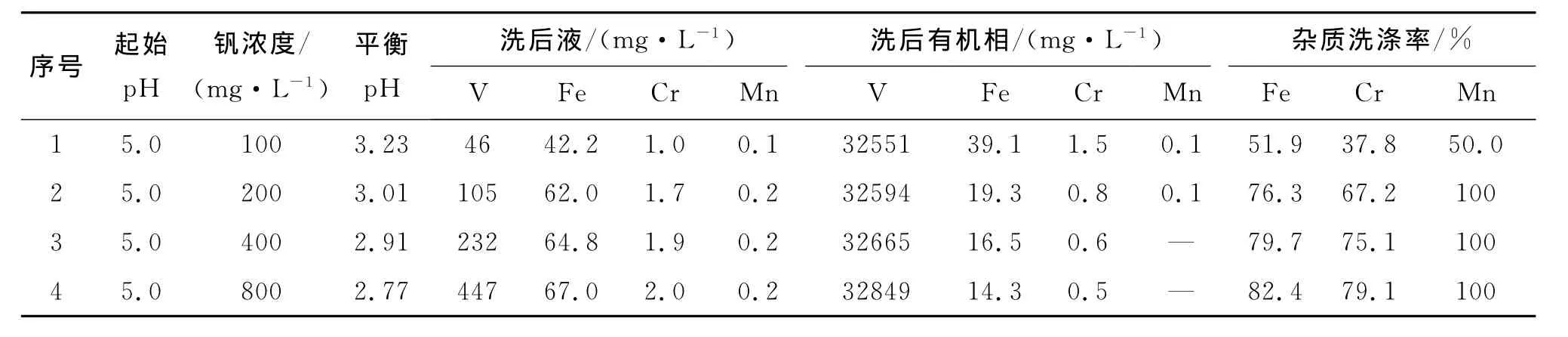
表4 不同浓度纯钒液洗涤载钒有机相结果Table 4 Results of scrubbed to the loaded organic phase using various pure vanadium solution concentrations
由表4可知,用低浓度的纯钒溶液洗涤载钒有机相,当洗液钒的浓度由100mg/L增加到800 mg/L时,铁的洗脱率由51.9%提升至82.4%,同时铬和锰的洗脱率也相应上升.从工程化及经济性考虑,采用钒浓度为200mg/L的纯钒液洗涤载钒有机相是适宜的.
用适宜浓度的硫酸溶液可从载钒有机相中反萃取钒,铁等杂质不易被反萃取,从而可使钒与共萃取的杂质有效分离[7].对经浓度为200mg/L的纯钒液洗涤的载钒有机相开展反萃取实验,实验结果列于表5.
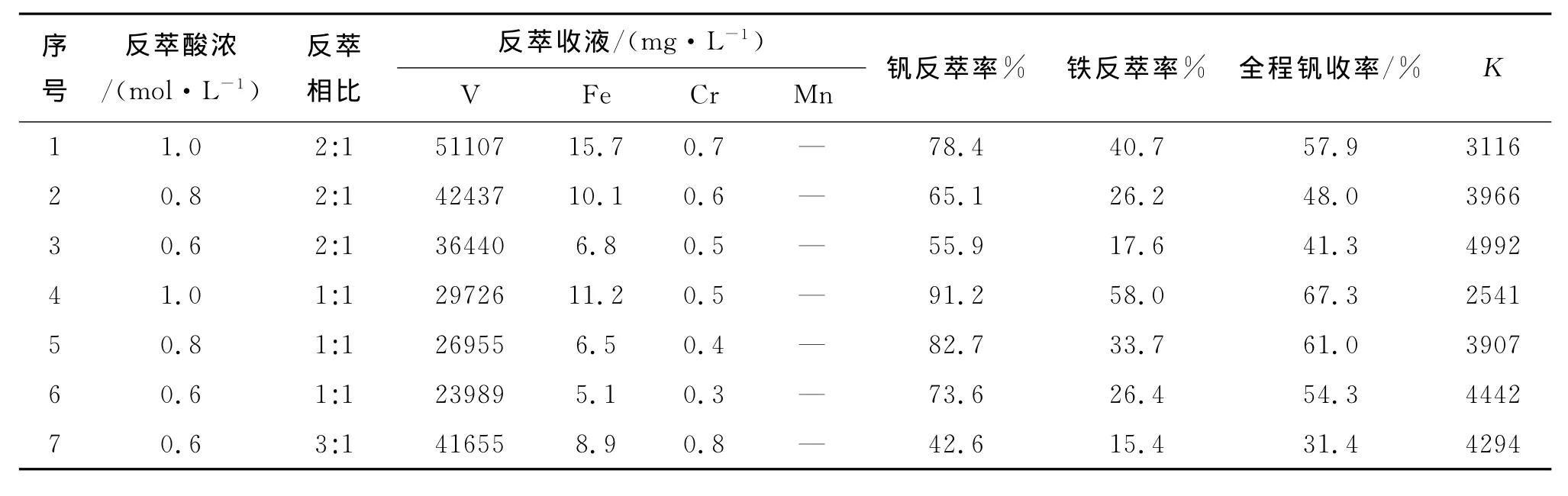
表5 不同条件下载钒有机相反萃取实验结果Table 5 Results of stripping to the loaded organic phase at different condition
由表5可知:不同浓度反萃剂及不同反萃相比对钒、铁的反萃率有明显影响,反萃酸浓度降低,钒及杂质铁的反萃率相应降低;反萃相比提高,同样也会降低钒及杂质铁的反萃率.但从收液钒杂质量比来看,控制反萃相比为2︰1,用0.6mol/L硫酸反萃载钒有机相,除杂效果最好,所得硫酸氧钒溶液的纯度最高,全过程铁、锰、铬等杂质去除率为99.1%.由此可知,反萃过程的最佳参数为反萃相比2︰1,稀硫酸浓度为0.6mol/L.
2.4 二段萃取对含钒溶液除杂纯化的影响
通过对表5中3号反萃条件所得的硫酸氧钒溶液测算硫酸氧钒纯度,可知溶液中所含铁、铬、锰量约为0.02%.按全钒液流电池行业提出的品质控制要求,铁、铬、锰等黑色金属杂质量仍然超出技术要求10~20倍.为进一步深度纯化硫酸氧钒溶液,研究二段萃取再次除杂的效果.
常温下将1000mL的含钒36440mg/L、含铁6.8mg/L、含铬0.5mg/L的硫酸氧钒溶液加入烧杯中,边搅拌边加入2.0g的抗坏血酸以还原溶液中的杂质离子,再加浓度为25%的氨水,将含钒溶液pH值精确调整至2.6,然后每次取少量溶液置于250mL分液漏斗中进行三级逆流协同萃取.萃取过程在康氏振荡器上进行,相比为V(O)︰V(A)=2︰1,萃取(振荡)时间为15min.对载钒有机相用浓度为200mg/L的纯钒溶液洗涤5min,然后用浓度为0.6mol/L的稀硫酸及洗涤相比为2︰1进行二级逆流反萃取,反萃取时间为10min,最后测定反萃收液中钒及杂质元素含量.实验结果列于表6.

表6 第二段萃取及反萃取实验结果Table 6 Results of experiments at the second segment extractive and stripping
由表6可知:采用二段协同萃取方式,所获得的超纯硫酸氧钒溶液中钒含量为21.8g/L,铁含量仅为0.43mg/L;溶液中钒与铁、铬、锰等杂质元素的质量比为34602;第一、二段协同萃取全过程钒的直接回收率为24.7%,铁、铬、锰等杂质总去除率合计为99.87%.
3 结 论
(1)采用 D2EHPA-TBP-磺化煤油的协同萃取体系,对复杂含钒溶液萃取除铁、锰、铬等杂质,制备超纯硫酸氧钒溶液是可行的.
(2)最适宜的萃取条件为:溶液起始pH值为2.6,萃取相比V(O)/V(A)为2︰1,萃取时间为15 min,采用200mg/L的低浓度纯钒液洗涤负载有机相,反萃酸浓度为0.6mol/L.
(3)控制最适宜的萃取条件,采用二段协同萃取方式,全过程铁、铬、锰等杂质总去除率为99.87%.
[1]FABJAN C,GARCHE J,HARRER B,et a1.The vanadium redox-battery:an efficient storage unit for photovoltaic systems [J].Journal of Electrochimica Acta,2001,47(5):825-831
[2]JOERISSEN L,GARCHE J,FABJAN C,et a1.Possible use of vanadium redox-flow batteries for energy storage in small grids and stand-alone photovoltaic systems[J].Journal of Power Sources,2004,127:98-104.
[3]LUO Q T,ZHANG H M.Modification of Nation membrane using interfacial polymerization for vanadium redox flow battery applications[J].Journal of Membrane Science,2008,311(1-2):98-103.
[4]LUO X L,LU Z Z,XI J Y,et al.Influences of permeation of vanadium ions through pvdf-g-pssa membranes on performances of vanadium redox flow batteries[J].J Phys Chem B,2005,109:20 310-314.
[5]刘素琴,史小虎,黄可龙.钒液流电池用电极材料的改性研究[J].无机化学学报,2008,7(24):1073-1084
[6]HU J,WANG X W,XIAO L S,et al.Removal of vanadium from molybdate solution by ion exchange[J].Hydrometallurgy,2009,95:203-206.
[7]鲁兆伶.用酸法从石煤中提取五氧化二钒的试验研究与工业实践[J].湿法冶金,2002,21(4):175-183.
[8]WANG M Y,ZHANG G Q,WANG X W,et al.Solvent extraction of vanadium from sulfuric acid solution[J].Rare Metals,2009,28(3):209-211.
[9]李桂英,戴子林,唐谦.水相pH值和有机相配比对从石煤酸浸液中萃取钒影响的研究[J].材料研究与应用,2010,4(2):142-144.

