三脉紫菀总皂苷的提取工艺研究
★ 刘爱红 袁金斌 刘荣华 钟国跃 郑燕梅 任刚 (.南昌大学分析测试中心 南昌0047;.江西中医学院现代中药制剂教育部重点实验室 南昌0004;.江西中医学院中药资源与民族药研究中心 南昌0004)
三脉紫菀(Aster ageratoidesTurcz.)为菊科(Compositae)紫菀属植物,具有清热解毒、祛痰镇咳的功效[1]。在江西民间三脉紫菀是治疗咳喘病的有效单方,并在当地因此得名“换肺草”。1971 年全国攻克老年慢性气管炎工作会议上,三脉紫菀被定为全国18 个有效方剂之一。紫菀属植物的化学成分主要包括黄酮类(地上部分)和皂苷类(地下部分),此外还含有三萜、倍半萜、二萜、单萜、甾醇、脂肪酸和肽类等成分[2]。其中根部的三萜皂苷类是紫菀属特征性成分,也是三脉紫菀祛痰作用的主要药效物质基础之一[2]。前期研究中,笔者建立了三脉紫菀总黄酮的提取工艺[3],本研究继续对总皂苷的提取工艺进行了研究,以期为三脉紫菀总皂苷的进一步化学、药理研究打下基础。
1 仪器与材料
1.1 仪器
UV-2550 型紫外分光光度计(日本Shimadzu公司)、R -210 型旋转蒸发仪(瑞士Buchi 公司)、Sartorious BT 124S 型万分之一天平(北京赛多利斯科学仪器有限公司)、GZX -9070MBE 型数显鼓风干燥箱(上海博讯实业有限公司医疗设备厂)、高速中药粉碎机(瑞安市永历制药机械有限公司)、KQ-300DB 型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 材料
三脉紫菀于2010 年采于江西省吉安市永新县郊外,经江西中医药大学刘荣华教授鉴定为菊科紫菀属植物三脉紫菀。齐墩果酸标准品购自南昌市药品检验所(批号:110709 -201104)。香兰素、浓硫酸为国药集团化学试剂有限公司产品,甲醇、乙醇、冰醋酸等有机溶剂均为上海振兴化工一厂产品,蒸馏水自制。
2 方法与结果
2.1 三脉紫菀总皂苷含量测定
2.1.1 药材的处理
取三脉紫菀根除尽尘土,阴干,粉碎过40 目筛,密封保存备用。
2.1.2 标准溶液的配制
精确称取齐墩果酸标准品11.0mg,乙醇溶解并定容至50mL,得0.22mg·mL-1的齐墩果酸标准品母液。
2.1.3 测定波长的选择
称取“2.1.1”项制备的药材粉末1.5g,置于回流装置,加入30mL75%乙醇,于70℃浸提2 小时,过滤,滤液转移至50mL 容量瓶中,加乙醇定容至刻度,摇匀,得样品溶液。
分别吸取0.2mL 齐墩果酸标准品溶液和样品溶液于具塞试管中,挥干溶剂,准确加入新配置的5%香草醛-冰醋酸0.2mL,再加入72%的浓硫酸3mL,振摇。于60℃水浴中加热,20 分钟后取出,流水冷却至室温。标准品管以未加标准品的相同试剂作空白,样品管以未加显色溶液的样品溶液为空白,在400 -700nm 波长范围内进行扫描,得紫外吸收光谱图(见图1)。图上可见,标准品及样品在536nm 处有共同的最大吸收波长,因此选择536nm为测定波长。
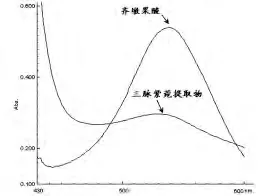
图1 三脉紫菀提取物与齐墩果酸的紫外-可见光吸收图谱
2.1.4 标准曲线的制备
精确吸取上述齐墩果酸母液0.5,0.7,0.9,1.0,1.1mL,分别加入具塞试管中挥干溶剂,加入新配置的香草醛-冰乙酸溶液0.2mL,再加入72%的浓硫酸溶液3mL,振摇。在60℃水浴中加热20 分钟取出,流水冷却至室温。在536nm 处测定各试管中溶液的吸光度。以齐墩果酸的质量(X)为横坐标,吸光值(Y)为纵坐标绘制标准曲线,以最小二法线性回归,得线性回归方程:Y =1.9416X +0.1392,相关系数为r=0.9989。
2.1.5 供试品溶液的制备及测定
准确称取“2.1.1”项制备的药材粉末5g 干燥至恒重,按正交设计的提取条件回流提取。提取液过滤后减压浓缩,浸膏用适量乙醇溶解,过滤,滤液移至50mL 容量瓶中,加乙醇定容至刻度,摇匀即得待测样品溶液。按“2.1.4”项的操作方法测定吸光度,根据标准曲线方程计算总皂苷含量。
2.1.6 精密度实验
取同一供试品溶液,在536nm 处重复测定六次,根据标准曲线方程得到总皂苷含量,结果表明精密度良好,RSD 为0.23%(n=6)。
2.1.7 稳定性考察
取同一供试品溶液,分别于0,0.25,0.5,0.75,1,1.5,2,4,8 小时分别进行测定,计算RSD 为2.86%(n =9),表明总皂苷含量在8 小时内基本稳定。
2.1.8 重现性实验
精密称取同一批次三脉紫菀药材粉末5 份,按照“2.1.5”项下方法制备样品溶液,照“2.1.4”项下的操作方法测定吸光度,结果表明该方法重复性良好,RSD 为1.30%(n=5)。
2.1.9 加样回收率实验
准确称取已知含量的三脉紫菀药材粉末0.5g,加入齐墩果酸适量,“2.1.5”项下方法制备样品溶液,照“2.1.4”项下的操作方法测定吸光度,计算回收率。结果表明,平均回收率为97.08%,RSD 为1.22%,说明该方法测得的结果准确。
2.2 提取工艺研究
2.2.1 正交实验设计
选择乙醇体积浓度(A)、提取时间(B)、料液比(C)、提取次数(D)4 个因素为考察因素,每个因素3 个水平,以L9(34)正交设计表安排试验,以三脉紫菀中总皂苷含量为评价指标。因素水平表见表1。

表1 实验因素水平表
2.2.2 正交实验结果
分别精密称取三脉紫菀药材粉末50g,按照正交表的设计进行实验,用紫外分光光度法测定总皂苷含量,并进行方差分析。结果见表2、3。根据表2中的极差R 值分析可知,各个因素对三脉紫菀总皂苷提取效果影响大小依次为A >C >D >B。方差分析结果(如表3)表明,乙醇浓度为影响总皂苷提取的显著因素,而提取次数、料液比及提取时间对总皂苷的提取没有显著影响。以上分析综合经济环保角度考虑,确定最佳提取工艺条件为A1C1D1B1,即50%乙醇、料液比为1∶6、回流提取2 次,每次1 小时。
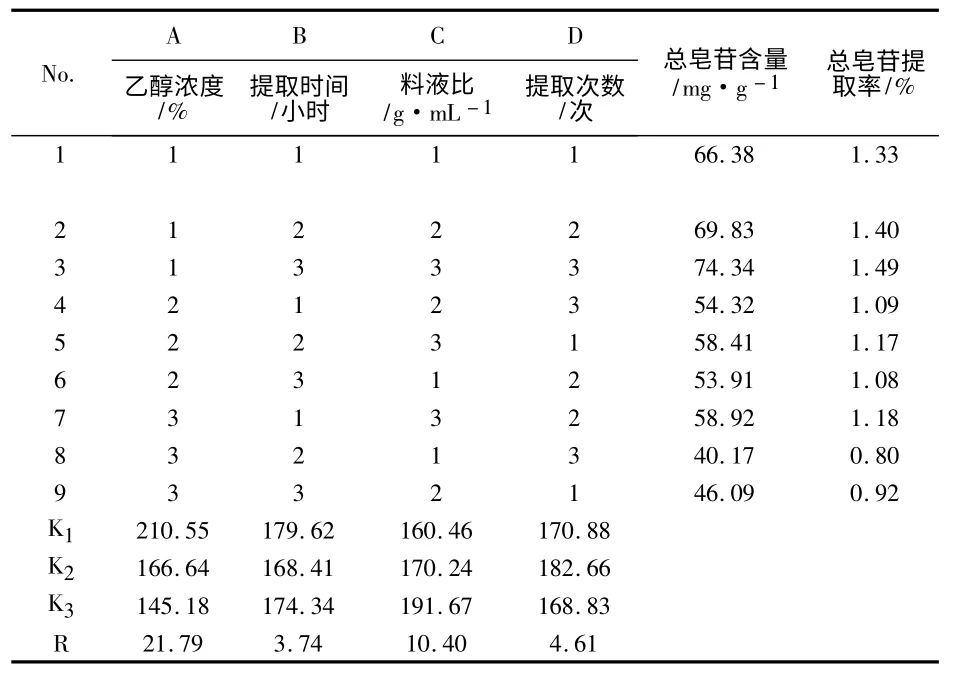
表2 正交实验结果
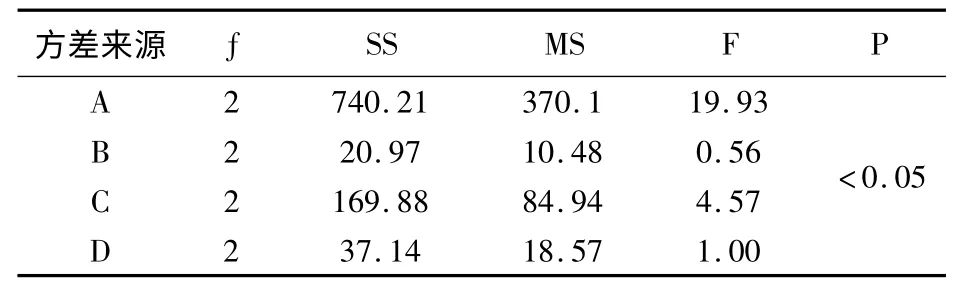
表3 方差分析结果
2.2.3 最佳提取工艺的验证准确称取三脉紫菀根粉末5.0g,共3 份。按上述最佳提取工艺:即三脉紫菀药材加6 倍量50%乙醇,回流提取2 次,1 小时/次。提取液浓缩定容至50mL 容量瓶中,取样,显色测定总皂苷含量。结果总皂苷的平均含量为75.23mg·g-1,总皂苷提取率为1.51%,RSD =1.56%(n =3),说明此工艺条件稳定、可行。
3 讨论
前人对三脉紫菀的化学成分研究表明,齐墩果烷型三萜皂苷是其皂苷的主要存在形式[4-5]。鉴于此,本研究采用了齐墩果酸作为对照品。在选择显色剂方面,我们曾尝试用香草醛-冰醋酸-浓硫酸法和香草醛-冰醋酸-高氯酸法分别对三脉紫菀总皂苷显色,多次实验表明,前者显色更稳定,且样品与对照品的最大吸收波长对应性好。因此本研究采用了香草醛-冰醋酸-浓硫酸显色法。
在建立三脉紫菀总皂苷含量测定方法的基础上,采用正交试验对总皂苷的提取工艺进行了筛选。结果表明50%乙醇、料液比1∶6、回流提取2 次、1小时/次,所得总皂苷含量为75.23mg/g,RSD =1.56%(n=3)。该工艺简便、实用,可以为三脉紫菀总皂苷的工业化生产提供参考。
[1]郑朝宗.浙江植物志(第6 卷)[M].杭州:浙江科学技术出版社,
1993:238.
[2]刘可越,赵昱波,刘海军,等.紫菀属植物化学成分与生物活性研究进展[J].现代药物与临床,2009,24(5):276 -278.
[3]周志望,黄慧莲,邵峰,等.三脉紫菀总黄酮的提取纯化工艺优选[J].中国实验方剂学杂志,2012,18(18):7 -10.
[4]Yan F L,Wang A X,Jia Z J. Pentacyclic triterpenoids from Aster ageratoides var. pilosus[J].Pharmazie,2004,59(11):882 -884.
[5]Sakai K,Nagao T,Okabe H. Triterpenoid saponins from the ground part of Aster ageratoides var. ovatus[J]. Phytochemistry,1999,51(2):309 -318.

