超声波耦合Fenton氧化对污泥破解效果的研究——以粒径和溶解性物质为例
宫常修,蒋建国,杨世辉 (清华大学环境学院,固体废物处理与环境安全教育部重点实验室,北京 100084)
剩余污泥是城市污水处理过程中的主要固体废弃物,在应用微生物在曝气池中的增长来消除污染物的污水处理过程中不可避免会产生剩余污泥[1],剩余污泥体积庞大、成分复杂制约着污泥的减量化和资源化,污泥的脱水性能是决定污泥减量化的最重要问题[2].由于污泥的产量巨大(2009年中国城市污水处理厂产生的含水率80%的污泥达2336万t)[3],含水率高且不易脱水,有机物含量高容易腐化发臭.因此,如何对污泥进行减量化、无害化、资源化处理成为国内外学者普遍关注的问题[4-6].
超声波是一种常用经典的污泥预处理方法.超声波泛指频率在 20kHz以上的声波[7],能够破解微生物细胞,改变活性污泥的物理、化学和生物学特性,增强污泥的厌氧消化[8].超声波能在水中产生瞬间的局部高温、高压、急剧的放电和超高速射流等一系列极端条件[9],这些极端条件破坏了污泥菌胶团结构,使其中的有机物和水分释放出来[7].Fenton氧化是H2O2在Fe2+催化下,产生活泼的羟基自由基(OH·),从而引发和传递链反应,加快有机物和还原物质的氧化反应[10].Fenton试剂的氧化处理可以破坏污泥结构,使污泥中的水分和有机物释放出来,同时,Fenton试剂可以氧化还原性的恶臭物质,减少恶臭物质的释放,杀灭病原菌,稳定化污泥[10-13].
对于超声波处理污泥和Fenton氧化处理污泥已有大量研究,但是对于超声波耦合Fenton氧化工艺预处理污泥的研究却鲜有报道.本研究提出采用超声波和Fenton氧化协同作用破解污泥,以污泥粒径、溶解性物质,污泥上清液中多聚糖和蛋白质含量等指标,来表征污泥的破解程度.
1 材料与方法
1.1 污泥来源与性质
浓缩污泥取自北京市某污水处理厂.该污水处理厂采用卡罗塞尔氧化沟延时曝气活性污泥处理工艺,主要处理城市生活污水,污泥在消化池短暂停留后经过重力浓缩形成浓缩污泥.为防止污泥变质,试验当天从污水处理厂取浓缩污泥,处理完毕后迅速分析各项指标,当天未能分析的须将原污泥样品及处理后的污泥一起置于 4 ℃恒温冰箱中,冷藏的污泥2d内分析完毕.
浓缩污泥基本性质如表1所示.
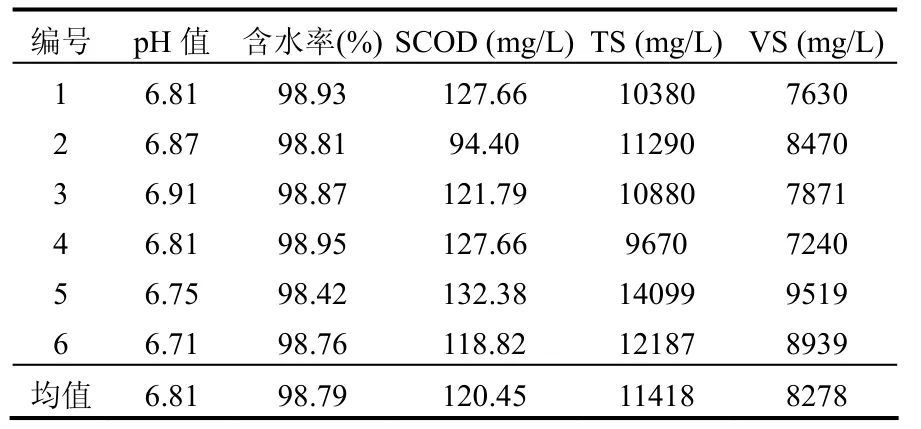
表1 实验污泥基本性质Table 1 Characteristics of the tested sludge
从表1可以看出,实验用浓缩污泥pH值接近中性,含水率高达 98.79%,而VS/TS较高,说明实验污泥中的有机物含量相对较高.污泥SCOD较低,说明污泥本身有机质溶出较少.
1.2 污泥破解前处理
取试验用污泥,用稀盐酸调节污泥的 pH值为 3,加入 0.4g/L 的 Fe2+和 0.50g/L 的 H2O2,用锡箔纸封口,在常温用磁力搅拌(Fenton)和频率为25kHz,声能密度为 100W/L的超声波强化(US+Fenton)破解.
1.3 污泥粒径的测定
破解前处理0.5h和1.5h后测定污泥的粒径分布.采用激光粒度分析仪对污泥的粒径进行测定.激光粒度分析仪是英国荣马尔文公司的Micro-plus型 Mastersizer,分析范围为 50nm~555μm.
1.4 溶解性化学需氧量的测定
破解前处理0.0,0.25,0.5,0.75,1.0,1.5,2.0,2.5、3.0.3.5,4.0,5.0h,处理后离心(5000r/min,5min),测定上清液中的COD含量,即为SCOD.
操作时污泥先用布氏漏斗抽滤,然后再用0.45μm的滤膜过滤,之后的滤液用快速密闭催化消解法(含光度法)测定CODcr[14].COD消解仪是上海欧陆科仪有限公司ET3150B系列消解器,温度控制范围为 105~160℃,时间设定范围为0~31h.
2.5 多聚糖和蛋白质的测定
破解前处理 0.0,0.25,0.5,0.75,1.0,1.5,2.0,2.5,3.0,3.5,4.0,5.0h,处理后离心(5000r/min,5min),测定上清液中的多聚糖和蛋白质的含量.
测定方法:多聚糖采用苯酚-硫酸法进行测定,以葡萄糖为测定标准物质[15].蛋白质采用考马斯亮蓝法进行测定,以牛血清白蛋白为测定标准物质[16].
2 结果与讨论
2.1 粒径分布
从图1 可以看出,Fenton氧化和US+Fenton氧化处理后污泥粒径分布发生了明显变化.原污泥在 41.43μm 处的体积百分比最大(7.25%),而Fenton氧化和US+Fenton氧化0.5h和1.5h后的污泥则是在 35.56μm 处体积百分比最大,而且US+Fenton氧化处理污泥1.5h后,0.36μm左右的污泥颗粒量明显增加.
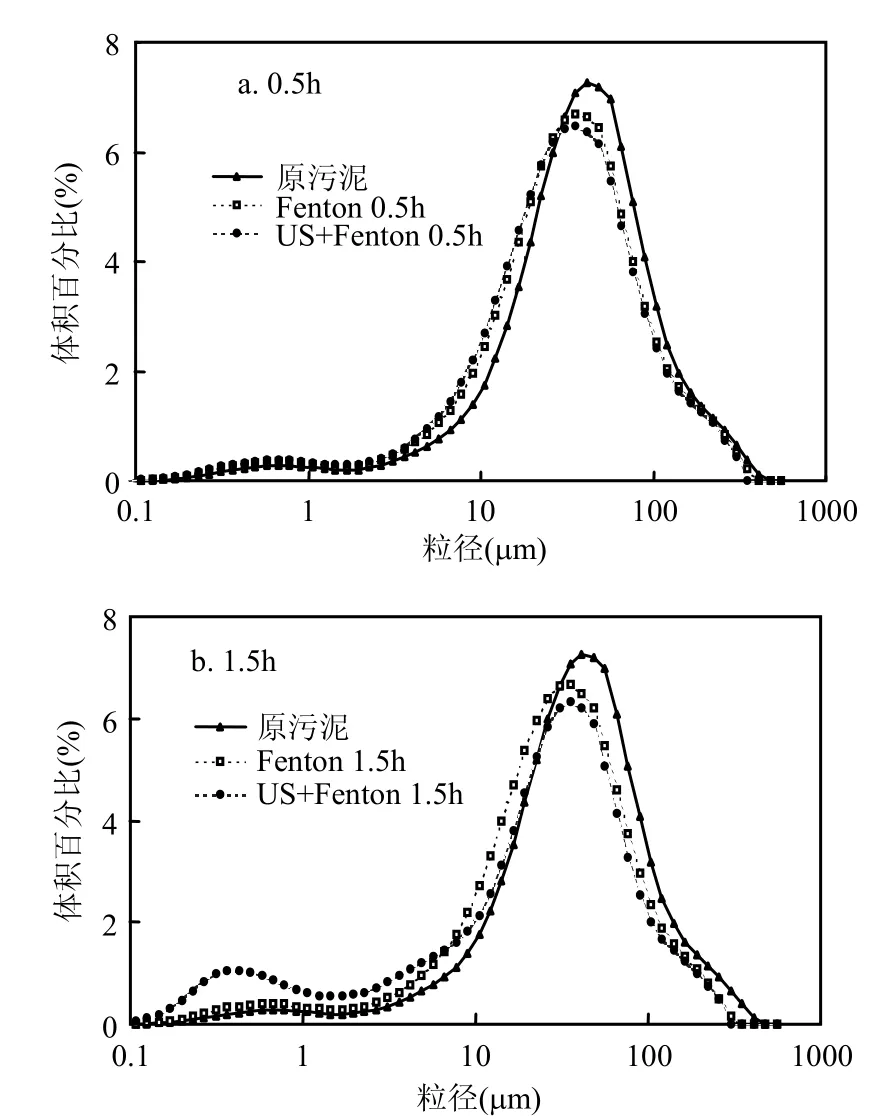
图1 Fenton和US+Fenton对污泥粒径分布的影响Fig.1 Impact of Fenton and US+Fenton oxidation on the particles size distribution of sludge
对污泥粒径分布进一步分析,识别出污泥粒径分布的几个特征指标,列入表2.
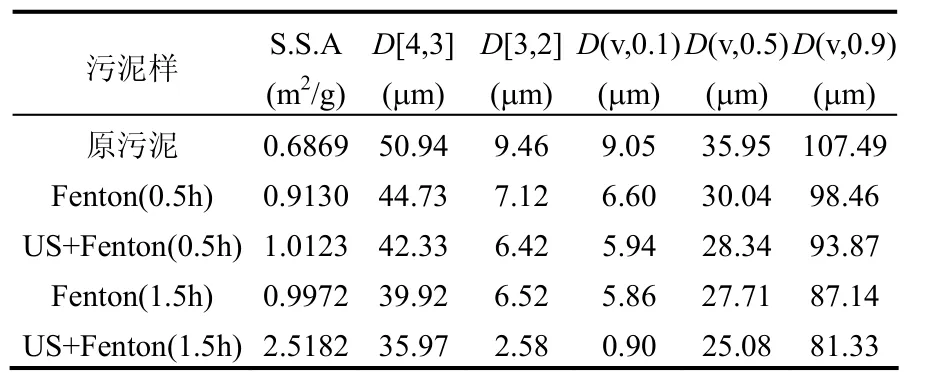
表2 污泥粒径分布变化情况Table 2 Sludge particle size after Fenton and US+Fenton oxidation
从表 2可以看出经过 Fenton氧化和 US+Fenton氧化处理后,污泥比表面积明显增加,体平均粒径和索太尔平均径都明显降低,粒径累积分布曲线上各个百分比对应的粒径值也明显降低,这说明经过处理后,污泥的絮凝体结构遭到了氧化破解,污泥的脱水性能和稳定性能得到了改善.
超声对于促进Fenton氧化破解污泥絮凝体结构具有显著作用.处理1.5h后,单独采用Fenton氧化破解污泥的比表面积从处理前的0.6869m2/g增加到0.9972m2/g,增幅45.17%,而采用超声波耦合后,污泥的比表面积能从处理前的0.6869 m2/g增加到2.5182m2/g,增加2.6倍;单独采用Fenton氧化破解时,污泥体平均粒径和索太尔平均径分别从原污泥的50.94μm和9.46μm降低到 39.92μm 和 6.52μm,降幅分别为 21.63%和31.08%,而采用超声波耦合后,污泥平均粒径和索太尔平均径分别从原污泥的 50.94μm 和9.46μm 降低到 35.97μm 和 2.58μm,降幅分别为29.39%和72.73%.
2.2 溶解性物质
污泥中的微生物通过各自细胞表面的有机物的相互作用形成稳定的污泥絮体结构,可以容纳大量水分,同时细胞表面大量的亲水性有机物可以附着大量的水分,使污泥脱水性能变差.细胞表层的胞外聚合物(EPS)起很重要作用[17-19].利用US+Fenton氧化对污泥进行破解调质,可破坏微生物胞外聚合物(EPS),使其中的物质释放到污泥上清液中.胞外聚合物(EPS)主要由多聚糖和蛋白质组成,通过测定污泥滤液中溶解性化学需氧量(SCOD)、多聚糖浓度和蛋白质浓度来表征污泥的破解程度.
2.2.1 溶解性化学需氧量(SCOD)从图2可以看出,Fenton氧化和US+Fenton氧化处理后污泥中的SCOD都有明显的增加,而且超声波强化对于污泥中 SCOD的增加促进作用也十分明显.Fenton氧化处理后污泥SCOD能从120.45mg/L增加到 585.47mg/L,增加 3.86倍,而 US+Fenton氧化处理后,污泥中SCOD则能从120.45mg/L增加到767.47mg/L,增加5.37倍.
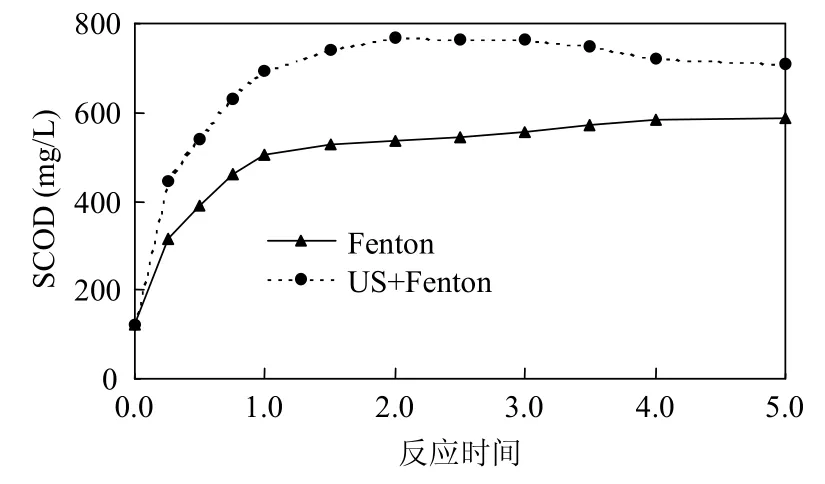
图2 Fenton和US+Fenton处理污泥SCOD变化情况Fig.2 Impact of Fenton and US+Fenton on the concentration of SCOD in sludge
随着反应时间的延长,Fenton氧化处理污泥后污泥中SCOD逐渐增加,但是当反应时间大于1.5h后,SCOD增幅逐渐降低,维持在580mg/L左右,而US+Fenton氧化处理后污泥的SCOD开始时也是快速增加,反应时间大于1.5 h时SCOD逐渐稳定在760mg/L左右,当反应时间大于3h时,污泥中 SCOD反倒有一定程度的降低,从760mg/L左右降低到700mg/L左右.
污泥 SCOD随反应时间的变化规律说明Fenton氧化和 US+Fenton氧化处理污泥时,Fenton试剂开始时快速破解污泥,使污泥中的有机质溶解,后来由于Fenton试剂的消耗,污泥破解速度逐渐降低,污泥SCOD逐渐趋向稳定.超声强化污泥Fenton氧化破解后期污泥SCOD逐渐降低是因为污泥结构在Fenton作用破解的同时还伴随着破解产物的进一步氧化[20],超声波提高了Fenton试剂的利用率,使得反应体系中羟基自由基富余,这些富余的羟基自由基进一步氧化溶液中的有机物,使得污泥中SCOD逐渐降低.
2.2.2 多聚糖和蛋白质 由图3可以看出,污泥经Fenton氧化和US+Fenton氧化处理时,随着反应的进行,污泥上清液中多聚糖的浓度上升,最后逐渐趋于平缓.仅采用Fenton氧化处理时污泥上清液中多聚糖最高浓度为 209.74mg/L,相对于原污泥的57.81mg/L增加了2.63倍,而采用超声强化污泥Fenton氧化处理后污泥上清液中多聚糖最高浓度则为 433.68mg/L,相对于原污泥增加了6.50倍.另外,当处理时间大于 2h后,US+Fenton氧化处理污泥后上清液中多聚糖的浓度略微下降,这是由于US+Fenton氧化过程中过量的羟基自由基氧化破解了多聚糖.
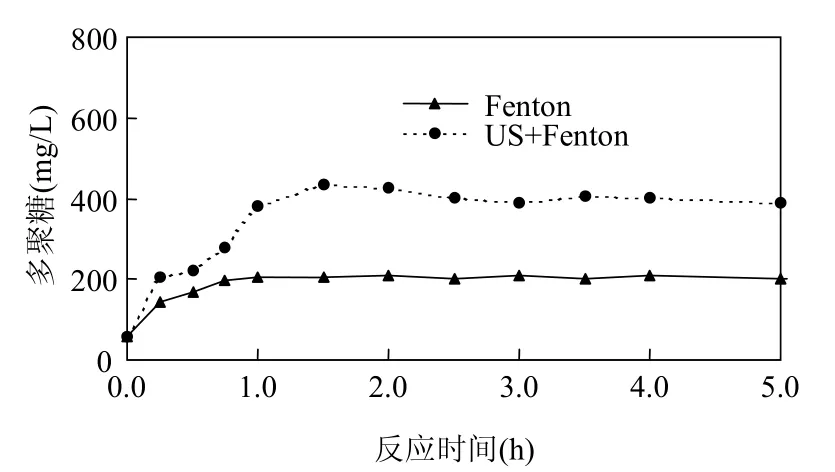
图3 Fenton和US+Fenton处理过程中多聚糖变化情况Fig.3 Concentration of polysaccharide in Fenton and US+Fenton oxidation
由图 4可以看出,污泥经 Fenton氧化和US+Fenton氧化处理时,随着反应的进行,污泥上清液中蛋白质浓度快速上升,然后又逐渐降低.Fenton氧化处理时污泥上清液中蛋白质最高浓度为84.87mg/L,相对于原污泥的33.33mg/L增加了1.55倍,而采用US+Fenton氧化处理后污泥上清液中蛋白质最高浓度则为94.87mg/L,相对于原污泥增加了 1.85倍.相对于污泥上清液中的多聚糖浓度变化,污泥蛋白质降低的情况更为迅速,这可能是由于蛋白质比较容易变性,而 Fenton氧化处理污泥的环境条件较为复杂,pH值较低(3~4),而且离子强度也较高,蛋白质发生了变性.
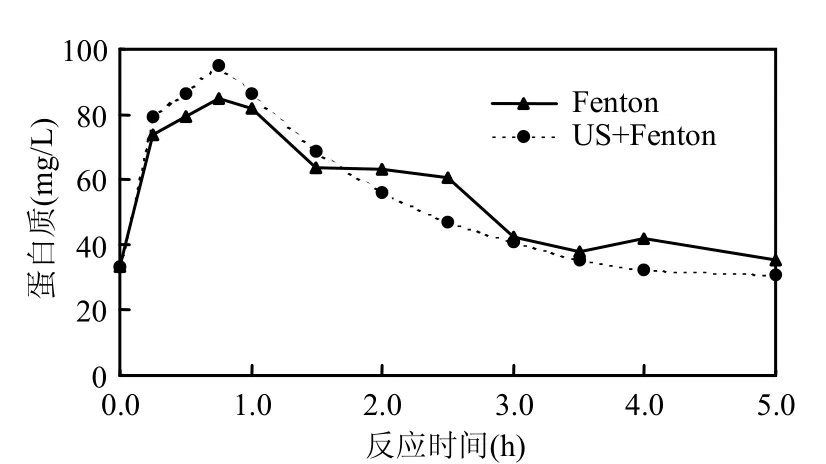
图4 Fenton和US+Fenton处理过程中蛋白质变化情况Fig.4 Concentration of protein in Fenton and US+Fenton oxidation
3 结论
3.1 污泥经过Fenton氧化和超声波耦合Fenton氧化处理后,污泥体平均粒径和索太尔平均粒径明显降低,比表面积明显增加,粒径累计分布曲线上各个百分比对应的粒径值明显降低,表面污泥经过这 2种氧化处理后,絮体结构遭到了氧化破解,改善了污泥的脱水性和稳定性.
3.2 Fenton氧化和US+Fenton氧化处理后污泥中的SCOD和多聚糖都有明显的增加,而且超声波耦合对于污泥中 SCOD和多聚糖的增加促进作用十分明显.2种氧化处理后,污泥的SCOD浓度相对于原泥分别增加3.85倍和5.37倍,多聚糖含量分别增加了2.63和6.50倍.
3.3 2种氧化处理后,污泥上清液中蛋白质的浓度都呈现先增加后降低的趋势,在处理50min时达到最大值,并且 US+Fenton氧化高于单独的Fenton氧化处理.在氧化1h后, 2种氧化污泥中的蛋白质浓度都快速下降,原因可能是处理后污泥的pH值较低(3~4),而且离子强度也较高,蛋白质发生了变性.
[1]Chockalingam L R, Georg S, Johannes M, et al. Influence of ultrasonic disintegration on sludge growth reduction and its estimation by respirometry [J]. Environmental Science and Technology, 2004,38;5779-5785.
[2]Vaxelaire J, Cézac P. Moisture distribution in activated sludges: a review [J]. Water Research, 2004,38(9);2215-2230.
[3]徐 涛,任宝莹.中国环境统计年鉴 [M]. 北京:国家统计局和环境保护部, 2010:24.
[4]Chon D H, Rome M, Kim Y M. Investigation of the sludge reduction mechanism in the anaerobic side-stream reactor process using several control biological wastewater treatment processes[J]. Water Research, 2011,45(18):6021-6029.
[5]Talat M, Allan E. A review of secondary sludge reduction technologies for the pulp and paper industry [J]. Water Research,2006,40:2093-2112.
[6]Hazrati H, Shayegan J. Upgrading activated sludge systems and reduction in excess sludge [J]. Bioresource Technology, 2011,102(22);10327-10333.
[7]Susan T L H. Bacterial cell disruption: A key unit operation in the recovery of intracellular products [J]. Biotechnology Advances,1991, 9(2):217-240.
[8]Clark P B, Nujjoo I. Ulrasonic sludge pretreatment for enhanced sludge digestion [J]. Water and Environment Journal, 2000,14(1):66-71.
[9]Monnier H, Wilhelm A M, Delmas H. The influence of ultrasound on micromixing in a semi-batch reactor [J]. Chemical Engineering Science, 1999,54:2953-2961.
[10]Neyens E, Baeyens J. A review of classic Fenton’s peroxidation as an advanced oxidation technique. Journal of hazardous materials [J]. 2003,98(1-3):33-50.
[11]Buyukkamaci N. Biological sludge conditioning by Fenton's reagent [J]. Process Biochemistry, 2004,39(11):1503-1506
[12]Pham T T H, Brar S K, Tyagi R D, et al. Influence of ultrasonication and Fenton oxidation pre-treatment on rheological characteristics of wastewater sludge [J]. Ultrasonics Sonochemistry, 2010,17(1):38-45
[13]He M H, Wei C H. Performance of membrane bioreactor (MBR)system with sludge Fenton oxidation process for minimization of excess sludge production [J]. Journal of Hazardous Materials,2010,176(1-3):597-601
[14]国家环境保护局.水和废水监测分析方法 [M].4版. 北京:中国环境科学出版社, 2002:216-219.
[15]Gaudy A F. Colorimetric determination of protein and carbohydrate [J]. Industrial Water Wastes, 1962,7:17-22.
[16]Lowry O H, Rosebrough N J, Farn A, et al. Protein measurement with the folin phenol reagent [J]. Jouranl of Biological Chemistry 1951,193:265-275.
[17]Sekyiamah K, Kim H. Biosolids odor reduction by solids inventory management in the secondary activated sludge treatment system [J]. Water Science and Technology, 2009,59(2):241-247.
[18]Cooper C D, Godlewski V J, Hanson R, et al. Odor investigation and control at a WWTP in Orange County, Florida [J].Environmental Progress, 2001,20(3):133-143.
[19]Barbosa V, Hobbs P, Sneath R, et al. Investigating the capacity of an activated sludge process to reduce volatile organic compounds and odor emissions [J]. Water Environment Research, 2006,78(8):842-851.
[20]李 娟,张盼月,曾光明,等. Fenton氧化破解剩余污泥中的胞外聚合物 [J]. 环境科学, 2009,30(02):475-479.

