高效液相色谱法测定滴眼液中利巴韦林和诺氟沙星的含量
武晓红,肖 娴,赵 辉
(河南大学 药学院,河南 开封475004)
利巴韦林又名三氮唑核苷(Ribavirin),主要用于①幼儿呼吸道合胞病毒肺炎。②甲型、乙型流感和副流感病毒感染。③流行性出血热。④单纯疱疹。⑤麻疹、腮腺炎、水痘、带状疱疹等。利巴韦林滴眼液,适用于单纯疱疹病毒性角膜炎。诺氟沙星,氟喹诺酮类抗菌药,具广谱抗菌作用,尤其对需氧革兰氏阴性杆菌的抗菌活性高。
诺氟沙星为杀菌剂,通过作用于细菌DNA螺旋酶的A亚单位,抑制DNA的合成和复制而导致细菌死亡。诺氟沙星滴眼液主要用于敏感致病菌引起的眼部感染如结膜炎,角膜炎,沙眼,泪囊炎及眼睑炎。
红眼灵滴眼液是河南省人民医院眼科研究所研制的一种滴眼液,用于治疗“红眼病”和腺病毒角结膜炎,有较好的疗效,弥补了眼科制剂的不足,为解决患者的病痛提供了更为方便的选择,该制剂在该院临床广泛使用。其处方组成为:利巴韦林(1%),诺氟沙星(0.3%),氯化钠(0.5%),羟苯乙脂(0.04%)。
文献[1-2]曾报道用差示紫外分光光度法和高效液相色谱法测定诺氟沙星含量,用紫外分光光度法[3]和高效液相色谱法[4]测定利巴韦林含量。但是文献当中基本没有对本复合制剂的含量检测方法,而我们建立了HPLC法同时测定红眼灵滴眼液中利巴韦林和诺氟沙星含量,该法简便、准确 ,可为制定红眼灵滴眼液质量标准及产品质量控制提供依据。
1 仪器与与方法
1.1 仪器与试药
Agilent 1100型高效液相色谱仪;自动进样器;DAD检测器;Agilent Chemsstation色谱工作站;甲醇为色谱纯;磷酸为分析纯。利巴韦林和诺氟沙星对照品由中国药品生物制品检定所提供,红眼灵滴眼液(规格:8mL:利巴韦林80mg与诺氟沙星24mg)由河南省眼科研究所制剂室制备。
1.2 色谱条件
色谱柱:Diamonsil(钻石)C18柱(250mm×4.6mm,5μm),0.025mol/L磷酸溶液(用三乙胺调pH 至3.0±0.1)-乙腈(85∶15),流速:1.0mL/min,检测波长:207nm,进样量:20μL。结果:利巴韦林与诺氟沙星的保留时间分别为2.70min,10.80min,理论塔板数分别为3 770,5 360,分离度大于1.5,符合 测试要求。空白样品溶液试验表明:处方中辅料对测定无干扰。色谱图见图1。

图1 对照品(A)、阴性样品(B)、样品色谱图(C)1.利巴韦林2.诺氟沙星3.溶剂
1.3 线性范围
精密称取经105℃干燥至恒重的对照品利巴韦林80mg、诺氟沙星24mg,置100mL量瓶中,加超纯水溶解并稀释至刻度,摇匀,作为储备液。精密吸取此溶液0.5、1.0、2.0、3.0、4.0、5.0mL分别置25mL量瓶中,超纯水稀释至刻度,摇匀。取标准系列溶液各20μL注入液相色谱仪,按上述色谱条件测定峰面积,以峰面积为纵坐标,浓度(g/mL)为横坐标,绘制利巴韦林和诺氟沙星标准曲线。回归方程、相关系数(n=6)分别为:① 利巴韦林:A =56.89C+1.230,r=0.9998。②诺氟沙星:A=58.32C+2.635,r=0.9997。
结果表明,利巴韦林在10.0~100.0μg/mL和诺氟沙星在3.0~30.0μg/mL浓度范围内呈良好线性关系。
1.4 方法专属性考察
取样品各5mL,经以下条件处理:①置100℃放置12h;②在光强度为(4000±300)μ条件下放置12h;③加1mol/L氢氧化钠溶液1mL于100℃放置12h;④加1mol/L盐酸溶液1mL于100℃放置12h;⑤加l%过氧化氢溶液1mL于80℃放置12h。然后对破坏样品进行中和,照样品含量测定项下稀释、滤过,分别取滤液20μL注入液相色谱仪,记录色谱图,见图2。结果表明:样品处理后较处理前有新的杂质峰出现,杂质含量升高,各杂质峰与主要峰分离良好(R>1.5)。
1.5 最低检测限
取线性范围测定项下的对照品溶液逐级稀释并进样,按信噪比为3倍计,作为检测限。经测定,本色谱系统条件下利巴韦林和诺氟沙星的最低检测限分别为5ng和4ng。
1.6 精密度试验
1.6.1 精密度 同一样品溶液重复进样6次,记录利巴韦林和诺氟沙星色谱峰峰面积,求得利巴韦林和诺氟沙星的RSD分别为0.10%和0.13%(n=6)。1.6.2 重复性 取红眼灵滴眼液样品,重复取样6次,记录利巴韦林和诺氟沙星色谱峰峰面积,求得利巴韦林和诺氟沙星的RSD 分别为0.57%和0.63%(n=6)。
1.7 稳定性试验
取精密度试验项下的溶液,室温放置,保持色谱系统稳定,于0、1、2、4、8、12h测定,利巴韦林和诺氟沙星的RSD分别为1.5%和0.67%,说明样品溶液在12h内稳定性良好。
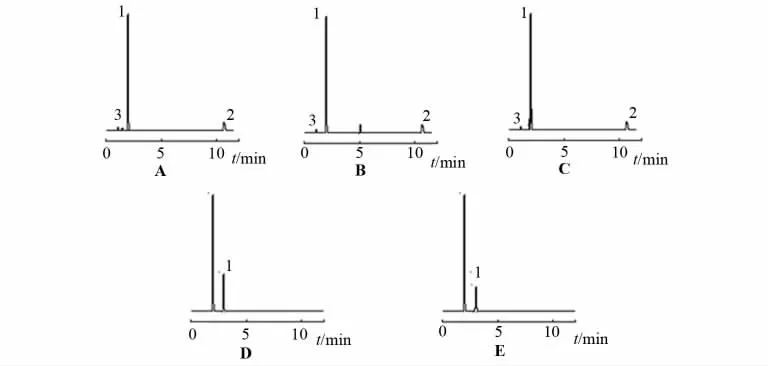
图2 HPLC方法专属性考察图谱A.样品加热破坏B.样品光照被破坏C.碱破坏样品D.酸破坏样品E.氧化破坏样品
1.8 回收率试验
按处方比例分别精密称取利巴韦林和诺氟沙星对照品,并加入适量辅料配制成含利巴韦林和诺氟沙星80.0%~120.0%的模拟样品9份,按“样品含量测定”项方法进行测定,计算回收率及RSD,结果利巴韦林和诺氟沙星平均回收率(n=9)分别为99.5%和99.7% ,RSD分别为0.70%和0.56%。
1.9 样品含量测定
精密量取样品5mL,置100mL量瓶中,加超纯水定容。精密量取上述稀释液5mL,置50mL量瓶中,加超纯水定容,进样20μL,在上述色谱条件下测定;同时另取利巴韦林和诺氟沙星对照品适量,用超纯水稀释成每1mL含利巴韦林50μg和诺氟沙星15μg的溶液作为对照品溶液,同法测定;记录色谱峰面积,以外标法计算含量,结果见表1。
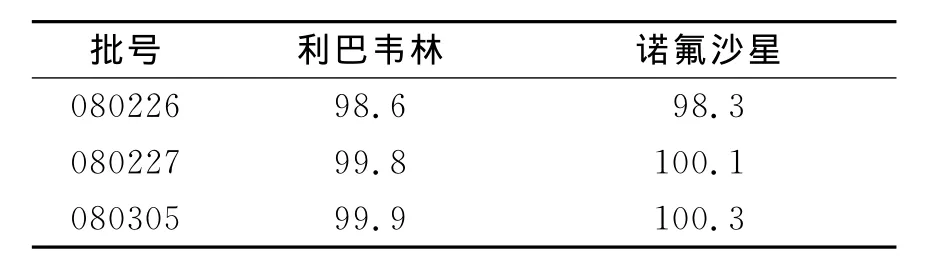
表1 样品测定结果(标示量%,n=3)
2 讨论
虽然选择文献中流动相0.025mol/L磷酸溶液(用三乙胺调pH至3.0±0.1)-乙腈(87∶13)利巴韦林与诺氟沙星能达到较好的分离,但诺氟沙星峰有明显拖尾,并且保留时间相对较晚,而将0.025mol/L磷酸溶液(用三乙胺调pH至3.0±0.1)-乙腈比例改为85∶15,虽改为87∶13后诺氟沙星保留时间大大提前但是相对受乙腈的影响也越大故最后选择85∶15,此比例下的流动相有效地改变了诺氟沙星的色谱行为,保留时间明显缩短,柱效明显提高。
由于诺氟沙星在水中微溶,在酸中极易溶解,所以在配制对照品溶液时先加入1.0mol/L盐酸溶液2mL使诺氟沙星溶解后,再用超纯水进行稀释。
[1]姜玲.差示紫外分光光度发测定诺氟沙星滴眼液的含量[J].安徽医药,2004,9(2):112.
[2]王中兰,陈菊,冯碧敏.HPLC测定诺氟沙星滴眼液的含量[J].哈尔滨医药,2006,26(1):102.
[3]唐志立,彭贤东,陈建勋等.紫外分光光度法测定利巴韦林注射液的含量[J].四川医学,2001,12(12):3-4.
[4]国家药典委员会.中华人民共和国药典(二部)[S].北京:化学工业出版社,2005:260.
[5]敬永生,胡海廷,徐晓燕.高效液相色谱法测定盐酸川芎注射液的含量[J].河南大学学报:医学版,2009,28(1):47-48.

