荧光光谱研究多种印染助剂对活性深蓝M-2GE结合丝素肽的影响*
马明明,杨家彪,苏新科
(西安工程大学环境与化工学院,陕西西安 710048)
丝素肽 (SP)是丝素蛋白水解后的大分子多肽物质,含有18种氨基酸,生物相容性优异[1],作为添加剂可以改善产品的性能,在印染工业、食品、化妆品、医药等[2-3]等领域有较多应用。特别是添加到印染体系后,可以显著提高织物的染色指标[4-5]。然而,并没有丝素肽与染色织物的染料小分子结合机理的相关文献报道。因此开展染料小分子结合丝素肽的工作就十分必要。
活性深蓝M-2GE(RDBMG)是双偶氮荧光钠盐染料,适用于涤棉、涤黏染色[6],化学结构式如图1所示。荧光光谱法简单,灵敏,依据荧光峰位或强度的变化可迅速判断两组分是否有相互作用,进一步推算出二者的结合机制。本文应用荧光光谱法研究了活性深蓝M-2GE对丝素肽在305nm处荧光的猝灭,探讨了猝灭机理,紫外可见、同步荧光光谱也进一步证实了这一结果。印染工艺中常见物质纺织淀粉、氨基酸、离子液体、氧化剂、表面活性剂、金属离子对二者结合体系有不同的影响,为今后丝素肽在活性深蓝M-2GE印染体系中的工艺条件选择提供了依据。
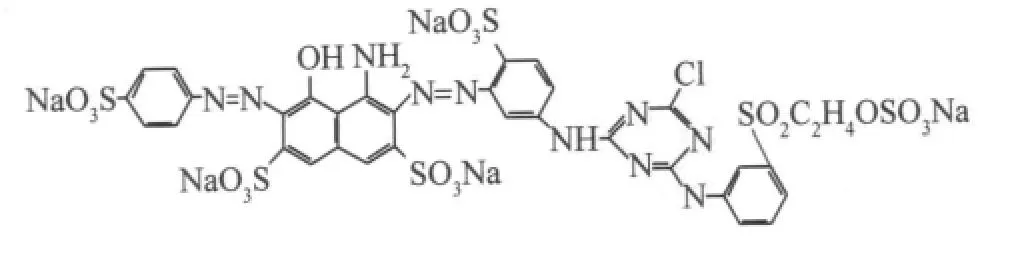
图1 RDBMG的化学结构式Fig.1 The chemical structural formula of RDBMG
1 实验部分
1.1 仪器与试剂
荧光分光光度计 (RF-5301PC,日本岛津);紫外可见分光光度计 (UV-2450,日本岛津);三用恒温水浴箱 (H-60,国华化学仪器);1×10-4mol/L、1 ×10-3mol/L 活性深蓝 M-2GE(江苏申新),储备液;1.0 g/L丝素肽 (浙江丝绸科技研究有限公司)储备液;溴化-1-己基-2,3-二甲基咪唑 (上海成捷化学有限公司);1-乙基-2,3-甲基咪唑双三氟甲磺酰亚胺盐 (上海成捷化学有限公司);氯化羟乙基三甲基胺 (上海成捷化学有限公司);磷酸氢二钠 (天津市登峰化学试剂厂);磷酸二氢钠 (天津市博迪化工有限公司);原淀粉、聚丙烯醛胺、醛酸酯淀粉、氧化淀粉和磷酸酯淀粉浆料 (西安工程大学纺织材料学院);L-组氨酸、L-天冬氨酸、L-赖氨酸、L-精氨酸、L-甲硫氨基酸、L-白氨酸、L-脯氨酸、L-苯丙氨酸、L-丝氨酸、L-苏氨酸 (国药集团化学试剂有限公司),试剂均为分析纯,实验用水为原子级水。
1.2 实验方法
在一系列25 mL比色管中,分别加入0.26 g/L丝素肽、2 mL B.R.(pH 6.37)缓冲溶液和一定量体积的1×10-4mol/L活性深蓝M-2GE,用水稀释至刻度,摇匀,室温下静置10 min;将待测溶液倒入石英比色皿,置于样品室,发射与激发狭缝宽度均为5 nm,在荧光光度计上记录荧光发射光谱。在荧光猝灭实验中,激发波长选择275 nm,扫描范围为280~400 nm,在305 nm峰位记录荧光强度。同步荧光光谱测定中Δλ=15 nm(其中λem=280 nm,λex=265 nm)和 Δλ =60 nm(λem=280nm,λex=220 nm),Δλ =λem-λex,并在紫外可见分光光度计上扫描 (220~800 nm)吸收光谱;同步荧光扫描中λem=λex=275 nm。
2 结果与讨论
2.1 RDBMG与SP作用机制
2.1.1 RDBMG与SP相互作用的荧光光谱特征
采用单因子轮换法,对RDBMG猝灭SP荧光强度的条件如SP浓度、结合时间、缓冲溶液种类及其pH等进行了优化。结果显示,当SP浓度为0.26 g/L,作用时间为10 min,B.R.缓冲溶液 pH为6.37时,RDBMG对SP荧光强度猝灭条件最佳。在最佳实验条件下,研究了RDBMG猝灭SP荧光强度原理。图2是295 K在不同浓度RDBMG存在下,SP荧光强度F与RDBMG浓度 ([Q])的F0/F~[Q]关系图。由图可见,随着RDBMG浓度的增加,F0/F 不断增大,在 1.0×10-6~2.0×10-5mol/L范围内,F0/F与 [Q]并不是全呈线性关系;当 RDBMG浓度大于1.4×10-6mol/L时,曲线向上弯曲,说明SP与RDBMG作用后,使SP的内源荧光发生猝灭。猝灭有静态、动态猝灭或二者兼而有之。对动态猝灭,遵循 Stern-Volmer[7]等式:F0/F=1+Kqτ0[Q]=1+KSV[Q],F0、F分别是SP在加入猝灭剂 (RDBMG)前后的荧光强度,Kq是生物大分子的荧光猝灭速率常数,τ0是无猝灭剂时SP的平均寿命,KSV是动力学猝灭常数,[Q]是猝灭剂的浓度。τ0取10-8s。计算出不同温度下的Kq均大于生物大分子的限制扩散系数 2 ×1010L·mol-1·s-1[8-9],说明 RDBMG 引发SP猝灭不是动力学碰撞,而是二者结合为配合物后使其荧光猝灭。对静态猝灭,符合等式:lg [(F0-F)/F]=lg K+nlg [Q][8],其中 KA是猝灭剂与生物大分子的结合常数,n是猝灭剂与每个生物大分子的结合点数,[Q]是猝灭剂浓度。研究发现在295~318 K的温度范围内,随温度增加,RDBMG与SP结合常数出现先逐渐减小后增大,但结合位点数基本不变,大约为1。

图2 295 K温度下RDBMG+SP结合体系荧光光谱曲线及Stern-Volmer曲线Fig.2 The fluorescence spectrum of SP+RDBMG at 295K and Stern-Volmer plot
根据 Förster非辐射能量转移理论[10],能量转移效应不仅与给体与受体之间的距离有关,还与临界转移距离R0有关。其中,能量转移效率E与R0之间存在下列等式:E=,E=1 -F/F0=8.8 × 10-25Κ2Ν-4Φ J,r为荧光给体与受体结合距离,K2为偶极子空间定向因子,N为介质的折射指数,Φ为荧光给体荧光量子产率,J为给体荧光光谱和受体紫外-可见吸收光谱的重叠积分。光谱重叠积分符合下列关系

F(λ)是给体在波长λ处的荧光强度,ε(λ)是受体在波长 (处的摩尔吸收系数。图3是SP荧光发射光谱 (1)和RDBMG(2)紫外可见光谱重叠图,在图中通过OriginPro7.5软件计算J=3.46×10-14cm3·L·mol-1。已知 K2=2/3,N=1.336,Φ =0.15[11],算得 R0=3.14 nm,实验数据 IF=414.232,=918.35 ,得 E=0.55 代入 (1)式,r=3.04 nm。SP与 RDBMG 作用距离 r=3.04 nm,小于7 nm,符合非辐射能量转移条件,说明能量由SP转移给RDBMG的概率非常大,因此RDBMG对SP的的荧光猝灭属于静态猝灭。
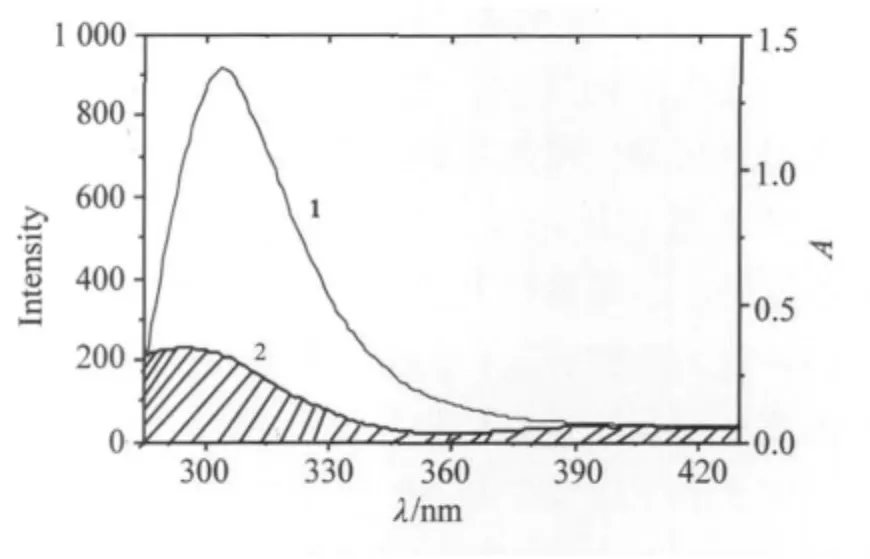
图3 SP荧光光谱 (1)和RDBMG紫外吸收光谱 (2)的重叠图ig.3 The overlay of the fluorescence emission spectrum of SP(1)and the absorption spectrum of RDBMG(2)
2.1.2 RDBMG与SP相互作用的紫外光谱 由于动态猝灭是猝灭剂与激发态分子碰撞作用,对吸收光谱无影响,而静态猝灭是与基态分子作用,形成缔合物,会引起吸收光谱的改变。考察了SP+RDBMG体系的紫外吸收光谱。图4是1×10-5mol/L RDBMG和0.26 g/L SP以及两者混合时的紫外吸收光谱。

图4 RDBMG与SP的紫外光谱图Fig.4 The absorption spectrum of RDBMG and SP
由图4知,SP在275 nm处有一吸光度比较小,RDBMG在295 nm处有一峰,两者混合后,0.18 g/L SP在275 nm处的峰完全消失,当加大SP浓度到0.50 g/L时,由于SP过量造成,在275 nm又出现SP峰 (图中曲线5);同时SP在205 nm处峰红移至218 nm处,以上可说明二者发生反应。
2.1.3 同步荧光光谱 同步荧光光谱通常可以探究蛋白质构象的变化。当Δλ=15 nm时,同步荧光光谱显示蛋白质酪氨酸残基的荧光;若Δλ=60 nm,则为蛋白质色氨酸残基的荧光。由于蛋白质中酪氨酸、色氨酸残基的最大荧光发射波长与其所处的环境的极性有关,因此,根据最大荧光发射波长的改变可判断蛋白质构象的变化。
图5为RDBMG与SP相互作用的同步荧光光谱图。由图5(A)知,RDBMG的加入使SP酪氨酸残基在最大发射波长处的荧光强度逐渐减小;由图5(B)可以看出SP色氨酸残基在最大发射波长处的荧光强度由于RDBMG的存在而逐渐减弱,290 nm处峰位没有移动,但327 nm处峰位出现红移,因此RDBMG与SP结合改变了酪氨酸、色氨酸残基所处的环境。

图5 RDBMG+SP体系的同步荧光谱图Fig.5 The sychronous fluorescence spectra of RDBMG+SP
2.2 印染工艺中常用物质对RDBMG结合SP的影响
2.2.1 表面活性剂对RDBMG结合SP的影响 表面活性剂可以改善染料的溶解度和染色性能,提高匀染性、上染速率和染色牢度[11-12]。当结合体系中存在曲拉通X-100、十二烷基苯磺酸钠、CTAB等表面活性剂时,结合常数由3.37×105分别变为4.56×106、1.85 ×106和 3.55 ×106。可见,无论是哪种类型的表面活性剂,均能使结合体系结合常数增加,且增加倍数超过5倍。这与表面活性剂在体系中形成胶束,增强RDBMG溶解度,使RDBMG小分子更易于进入SP肽链结构有关。
2.2.2 常用氧化剂对结合体系的影响 染色工艺中,染料隐色体以钠盐形式存在,在染色后需要在氧化剂作用下生成不溶性的染料,恢复染料原来的颜色,在此过程中,选择氧化剂的种类和用量非常重要,均对染色深浅和色光影响较大,氧化不足造成色浅,氧化过度染色加深,色光暗。试验了K2S2O8、K2Cr2O7、H2O2三种氧化剂对结合参数的影响。结果显示三种氧化剂的存在并没显著改变结合位点,但使结合常数变小,即由原来的结合常数3.37 ×105分别变为 0.15 ×105、2.04 ×105、2.89×105;且氧化剂氧化性越强,结合常数减小越明显。这主要是由于氧化剂可氧化肽链氨基酸残基[13],破坏发色基,将发色基变为可降解结构,从而使染料与丝素肽的结合力下降造成的。
2.2.3 金属离子对结合体系的影响 金属离子在纺织领域主要表现在染色、对丝素蛋白的作用、真丝的改性和防脆化处理以及抗菌、消臭、助燃、导电和防电磁波辐射等作用上[14]。研究发现大多数金属离子是通过形成空杂化轨道以接受纤维或织物上氨基、羧基、羟基、氰基等极性基团的孤对电子,通过配位键形成络合物。其中,在与蛋白质纤维络合时,一个中心金属离子还可以与多个氨基酸形成环状络合物,且络合物形成的环数愈多配位愈多,络合盐的稳定性愈好。Ca2+、Zn2+、Ba2+、Cu2+四种离子分别存在时对结合常数有不同的影响。除了Cu2+使结合常数变小外,其他三种离子都使其增大。Ca2+、Zn2+、Ba2+与SP存在螯合作用,诱导SP的结构由无规则的SilkⅠ向 β-折叠构象转变[15],形成相对稳定的环境,增强RDBMG与SP的结合,但Cu2+还可以与 RDBMG上的-形成键能较大的化学键,封闭了染料的水溶性基团,导致RDBMG与SP结合减弱,结合常数会减小。
2.2.4 离子液体对结合体系的影响 离子液体作为良好的溶剂,常用作染料的分散剂,蚕丝、纤维素和羊毛的再生纺丝溶剂,苎麻和羊毛纤维的改性试剂以及用于染色废水处理[16]等。试验了三种离子液体溴化-1-己基-2,3-二甲基咪唑、1-乙基-2,3-甲基咪唑双三氟甲磺酰亚胺、氯化羟乙基三甲基胺对结合体系的影响,结果见表1。离子液体的存在大幅增加结合常数,说明具有优良溶解性能的离子液体增强SP和RDBMG亲水结合环境,使SP和RDBMG更易结合。
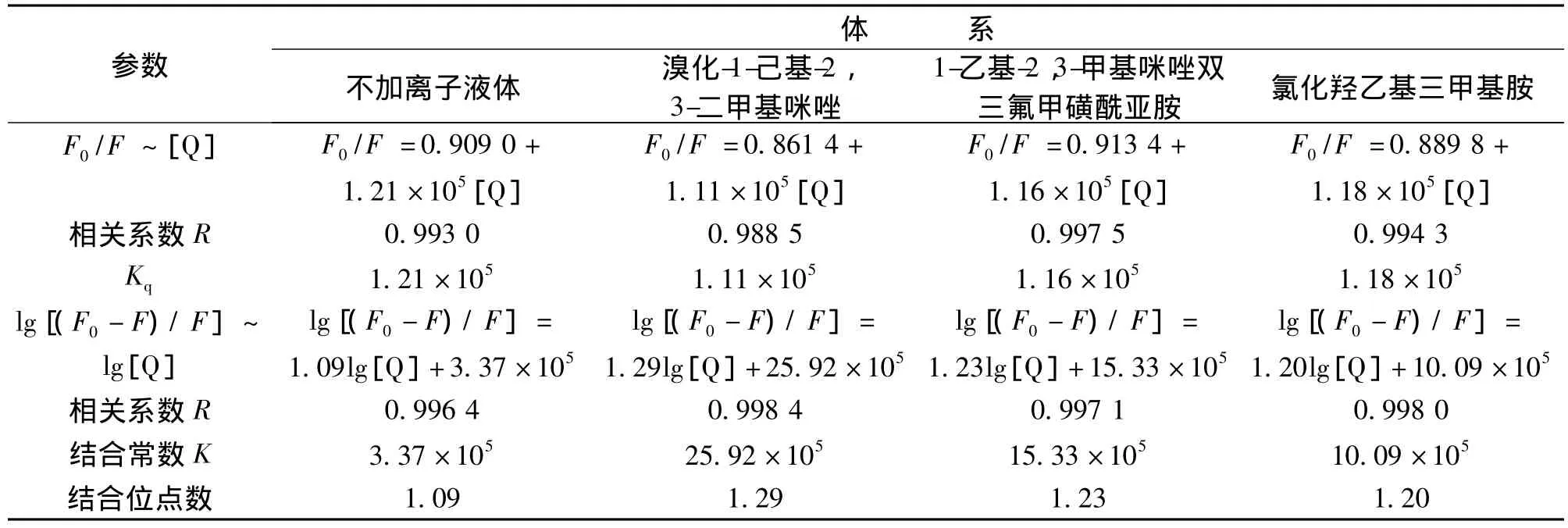
表1 室温下离子液体存在下SP-RDBMG体系的静态猝灭方程Table 1 Static quenching equation of SP-RDBMG – ionic liquids system at room temperature
2.2.5 纺织浆料对结合体系的影响 纺织浆料是使纱条表面光滑、耐磨、柔韧且有一定强度的浆膜。可以使纱条表面的缠绕纤维紧贴纱条的主干,降低纱条表面的摩擦系数,同时使部分浆液渗入纱线内部,增加纤维之间的黏付力,提高纱线的抗拉强度,以适应织造过程中的大张力、中打纬,减少断头提高效率。常见浆料以淀粉为主要原料。本文试验了几种不同结构的浆料对结合体系静态猝灭方程的影响。聚丙烯醛胺和醋酸酯淀粉结构复杂,空间位阻较大,在结合体系存在时会阻碍SP与RDBMG结合,导致结合常数下降。而原淀粉、磷酸酯淀粉、氧化淀粉结构相对简单,官能团之间交联程度小,能促进SP表面活性位点增多,有利于RDBMG的结合,因此这三种淀粉存在时结合体系结合常数增加。
2.2.6 氨基酸对结合体系的影响 氨基酸是两性物质,含有—COOH和—NH2,在染色体系中能改善染料染色性能。本文试验了11种不同氨基酸对SP结合RDBMG的影响。L-苯丙氨酸、L-丝氨酸、L-苏氨酸和甘氨酸能够降低SP与RDBMG的结合常数;而L-天冬氨酸、L-组氨酸、L-赖氨酸、L-精氨酸、L-甲硫氨基酸、L-白氨酸、L-脯氨酸则使二者结合常数增大,其中L-白氨酸使结合常数增加最大,比最初的结合常数高约30倍。这与氨基酸的性能密切相关。L-苯丙氨酸、L-丝氨酸、L-苏氨酸和甘氨酸的亲水性差,导致RDBMG不易和SP结合;而其余几种氨基酸亲水性较好,有利于SP结合RDBMG,因此能提高结合常数。
3 结论
1)RDBMG与SP结合形成作用距离为3.04 nm、结合为1∶1的复合物后,以静态猝灭方式猝灭SP内源荧光,从而改变了酪氨酸、色氨酸残基所处的环境,引起SP肽链构象结构缩聚变化。
2)表面活性剂、盐类、氧化剂、离子液体、氨基酸和浆料能改善丝素的染色性能。实验表明三种表面活性剂CTAB、十二烷基苯磺酸钠、曲拉通X-100有利于RDBMG与SP结合作用;双氧水、K2S2O8和K2Cr2O7三种氧化剂对二者结合都不利,氧化性越强影响程度越大;CaCl2、Zn(NO3)2和BaCl2三种盐都能使结合体系结合常数变大,由于Cu(NO3)2·3H2O能与RDBMG螯合导致结合常数变小;离子液体溴化1-乙基-2,3-二甲基咪唑、1-乙基-2,3-甲基咪唑双三氟甲磺酰亚胺盐、氯化羟乙基三甲基胺三种离子液体都较大程度增大了结合常数,在染色过程中可考虑加入此类离子液体;原淀粉、磷酸酯淀粉、氧化淀粉都有利于RDBMG与SP结合,其中氧化淀粉对二者结合最有利,聚丙烯醛胺和醛酸酯淀粉浆料会减弱SP和活性深蓝M-2GE的结合。11种氨基酸中,只有 L-苯丙氨酸、L-丝氨酸、L-苏氨酸和甘氨酸使RDBMG与SP结合常数变小,因此体系中不宜含有这四种氨基酸。
[1]ELEANOR M P,PATRICK B D,FIORENZO O,et al.Physical and chemical aspects of stabilization of compounds in silk[J].Biopolymers,2012,97(6):479 -498.
[2]张雨青.丝胶蛋白的护肤、美容、营养与保健功能[J].纺织学报,2002,23(2):150-152.
[3]周凤娟,许时婴,杨瑞金,等.可溶性丝素蛋白的功能性质[J].食品科技,2007,28(11):71-75.
[4]陈荣圻,陈岚.有机颜料表面改性及其助剂(三)[J].印染助剂,2001,5:1-6.
[5]唐增荣.浅论防沾污皂洗剂与色牢度[J].印染助剂,2009,6:1-7.
[6]何海兰.精细化工产品手册,染料[M].北京:化学工业出版社,2004.
[7]ZHANG H Y,HU C X,LIU C P,et al.Screening and analysis of bioactive compounds in traditional Chinese medicines using cell extract and gas chromatography–mass spectrometry[J]Journal of Pharmaceutical and Biomedical Analysis,2007,43(1):115 -117.
[8]YAN W Y,COLER C L.Investigating noncovalent squarylium dye-protein interactions by capillary electrophoresis– frontalanalysis[J].Journal of Chromatography A,2006,1135(1):115-121.
[9]JOLANTA S,BUMELIS V A.Examination of dye-protein interaction by gel-permeation chromatography [J].Biomedical Chromatography,2006,20(2):195-199.
[10]FÖRSTER T,SINANOGLU O.Modern Quantum Chemistry[M].New York:Academic Press,1965.
[11]KRAANA M V,FERNANDEZ M V,WOERLEEB G F et al.Acid-catalysed methanolysis reaction of non-polar triazinyl reactive dyes in supercritical carbon dioxide[J].The Journal of Supercritical Fluids,2007,39(3):389-398.
[12]张幼珠.纺织应用化学[M],上海:东华大学出版社,2009,98.
[13]赵为陶.载银桑蚕丝纤维的制备及其结构与性能研究[D].苏州:苏州大学,2007.
[14]徐孝旭,张宝砚.金属离子在蚕丝蛋白构象转变中的作用机理研究[J].高分子通报,2008,3:48-51.
[15]袁久刚,王强,范雪荣.针织物染整技术[M].北京:中国纺织出版社,2004.
[16]刘妙丽,李秀艳,叶建军.纺织化学[M].北京:中国纺织出版社,2007:184.

