紫杉醇脂质体联合卡培他滨治疗晚期胃癌临床观察
陆明洁 王 建 刘 平 束永前
胃癌为我国常见肿瘤,其发病率及死亡率均位于我国肿瘤的前列[1]。由于发病早期缺乏特异症状,很多病例确诊时均已处于无法手术根治的晚期。目前,对于晚期胃癌的治疗主要采用化疗或最佳支持治疗。对于一般情况尚可、能耐受化疗的患者,有证据表明,化疗较最佳支持治疗可明显改善生存时间[2]。现阶段,全世界范围内晚期胃癌尚缺乏公认的最佳化疗方案。ToGA研究虽已证实,曲妥珠单抗联合化疗可显著改善患者的生存时间[3],但在我国,胃癌标本检测 HER2(+++)率较低,同时赫赛汀价格相对高昂,故其临床实际应用限制较大。紫杉醇脂质体为近年来我国自主研发的紫衫醇的新剂型,在治疗肺癌、卵巢癌、乳腺癌及头颈部肿瘤均有较好疗效。卡培他滨为近年来治疗胃肠道肿瘤常用药物,在疗效上基本等同于5-氟尿嘧啶(5-FU),临床上有取代5-FU的趋势。本研究将上述药物联合使用治疗晚期胃癌患者,并比较目前常用的多西他赛、顺铂联合氟尿嘧啶方案,以观察评价其疗效,毒副反应。
1.材料与方法
1.1 材料 自2008年12月~2011年12月,我科收治的经胃镜或手术病理证实为胃癌,影像学(包括胸片、B超、CT、MR及PET/CT)检查确诊TNM分期为IV期,未接受过化疗,共计64例患者。其中实验组34例,资料如下:男性21例,女性13例;年龄范围38~77岁,中位年龄64岁;腺癌25例,黏液腺癌9例;肝转移19例,肺转移7例,后腹膜淋巴结转移11例,左锁骨上淋巴结转移7例,肾上腺转移3例。对照组30例,具体资料为:男性17例,女性13例;年龄范围33~69岁,中位年龄55岁;腺癌22例,黏液腺癌7例,印戒细胞癌1例;肝转移11例,肺转移5例,后腹膜淋巴结转移9例,左锁骨上淋巴结转移9例,肾上腺转移1例,骨转移1。所有患者化疗前ECOG评分均≤2分,所有患者化疗周期均≥2周期。
1.2 给药方法 实验组给予紫杉醇脂质体联合卡培他滨化疗,具体为:紫杉醇脂质体(力扑素,南京绿叶思科药业)135mg/m2,加入5%葡萄糖500ml,静滴3小时,d1。卡培他滨(希罗达,罗氏制药)2000mg/m2.d,口服,2次/天,d1-14,21天/周期。力扑素用药前,给予乘晕宁(茶苯海明)、地塞米松、西咪替丁行预处理治疗。对照组给予多西紫杉醇联合顺铂、5-氟尿嘧啶化疗,具体为:多西紫杉醇(多帕菲,齐鲁制药)75mg/m2,加入生理盐水(或5%葡萄糖)250ml,静滴1小时,d1;顺铂(齐鲁制药)20mg/m2,加入生理盐水250ml,静滴d1-5;5-氟尿嘧啶(天津金耀)350mg/m2,加入生理盐水250ml,静滴4-6小时,d1-5,21天/周期;为防止水钠潴留,多西紫杉醇用药前、中、后3天,常规予地塞米松口服治疗。两组均予5HT3受体拮抗剂(昂丹司琼)止吐治疗。
1.3 观察指标 疗效评价采用:RECIST(VER1.1)标准,分为完全缓解(CR),部分缓解(PR),稳定(SD),进展(PD)。治疗有效率RR(response rate)为CR+PR占总病例数的比例,疾病控制率(disease control rate,DCR)为CR+PR+SD占总病例数的比例。治疗过程中出现的毒性反应以NCI-CTC化疗药物不良反应分度以0~IV度进行评价。
1.4 随访 通过电话、信件及门诊定期随访,随访时间15~36个月,中位随访时间24个月,末次随访时间为2013年3月10日,所有病例均获得随访。
1.5 统计学方法 采用SPSS19.0软件行统计学分析。计数资料采用χ2检验,采用Kaplan-Meier法计算全组中位无疾病进展生存时间(PFS)及总生存时间(OS),并绘制生存曲线,采用Log-Rank检验比较PFS及OS差异。P<0.05认为差异有统计学意义。
2.结果
2.1 疗效和生存 对照组:30例患者,总计化疗122周期,平均化疗4.07周期,其中CR 2例,PR 12例,SD 7例,PD 9例,近期有效率RR为46.7%(14/30),疾病控制率DCR为70%(21/30),中位PFS为6.9个月,中位OS 12.5个月。实验组:34例患者,总计化疗169周期化疗,平均化疗4.97周期,其中PR14例,SD9例,PD11例,无1例取得CR,近期有效率RR为41.2%(14/34),疾病控制率DCR为67.6%(23/34),中位PFS为6.2个月,中位OS12个月。将两组的RR和DCR进行统计学分析,发现均P>0.05,表明差异统计学上无显著性(详见表1)。将两组生存数据绘制无进展生存曲线及总生存曲线,P>0.05,同样说明差异统计学上无显著性(详见图1、图2)。
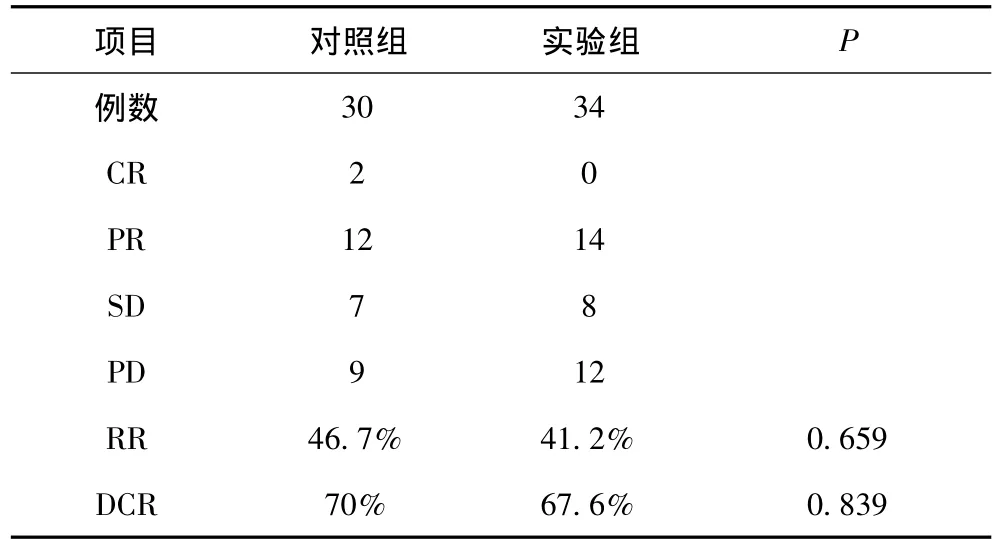
表1 两组患者客观疗效比较
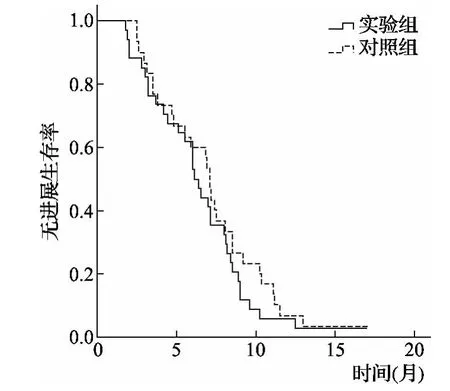
图1 两组患者无进展生存曲线

图2 两组患者总生存曲线
2.2 毒副反应 化疗中,两组患者出现的毒副反应均主要表现在血液学毒性方面。对照组:28例患者出现白细胞减少,Ⅲ~Ⅳ度发生率为56.7%;出现贫血23例,Ⅲ~Ⅳ度发生率为13.3%。非血液学毒性方面,发生比例最高的为腹泻和疲乏,Ⅲ~Ⅳ度发生率均为13.3%,其次为恶心呕吐10%。实验组:25例患者出现白细胞减少,Ⅲ~Ⅳ度发生率为17.6%;17例患者出现血小板减少,Ⅲ~Ⅳ度发生率为2.9%;贫血患者15例,Ⅲ~Ⅳ度发生率为2.9%。非血液学毒性方面,发生比例最高的为恶心、呕吐,共有20例患者出现,但仅有1例为Ⅲ度,其余均为Ⅰ~Ⅱ度;手足综合征出现14例,其中有2例达到Ⅲ度,Ⅲ~Ⅳ度发生率为5.9%;共有14例患者出现不同程度的脱发症状,但无Ⅲ~Ⅳ度出现。其余毒副反应如腹泻、口腔炎、肝功能异常、神经毒性及肌痛,发生率较低,且均为Ⅰ~Ⅱ度。值得一提的是,34例患者中仅有1例患者在使用力朴素治疗中出现一过性气喘、胸闷的轻度过敏症状。
3.讨论
我国是世界胃癌高发地区,据统计,2009年发病率约为36.21/10万,年死亡率25.88/10万[1~3]。由于该肿瘤早期缺乏特异症状,且我国整体医疗诊治水平不高,绝大多数患者确诊时已属晚期,无法手术根治,化疗成为该期患者延长生存时间,改善生存质量的重要手段。FAM方案(5-fu,阿霉素,丝裂霉素)曾经是上个世纪八、九十年代晚期胃癌治疗的一线金标准方案,但骨髓抑制及恶心呕吐等毒副反应较大[4]。2006年报道的V325研究结果表明:由多西紫杉醇、顺铂和5-fu组成的DCF方案可明显延长晚期胃癌患者的TTP及OS,由此奠定了DCF在晚期胃癌治疗的一线推荐治疗方案的地位[5]。由于V325研究数据主要来自欧美人群,DCF方案在我国推广以来,逐步体现出毒副反应较大,患者耐受性差的缺点,目前较多用于围手术期化疗、追求近期有效率及状态评分较好的病例。
紫杉醇目前已广泛用于治疗难治性卵巢癌、乳腺癌及非小细胞肺癌的化疗,但该药在临床应用的难点在于紫杉醇的原药极难溶于水,无法达到治疗浓度。现阶段,临床上使用的紫杉醇是以原药溶于聚氧乙烯蓖麻油与无水乙醇以1∶1混合的溶媒中使用。聚氧乙烯蓖麻油据报道有一定的毒副作用,甚至可导致致命性的过敏反应。为预防及减轻溶媒所导致的不良反应,常于用药前给予高剂量的抗组胺药及糖皮质激素。但这些预防性用药可影响紫杉醇在人体内的药代动力学及药效学。为解决这一难题,Sharma and Straubinger[6]通过大量试验研制出了紫杉醇的脂质体剂型。脂质体技术即是人工合成的一层或多层的脂质囊泡将药物、疫苗或是生物酶包裹后进入人体内并作用于特定细胞。周卫等[7]发现脂质体紫杉醇在人体内只要分布于肝、脾及肺组织,与普通紫杉醇的分布有较大差异,同时脂质体紫杉醇在体内的分布浓度远高于普通紫衫醇。脂质体包裹的紫衫醇可以更有效的将药物转运至肿瘤组织的血管内皮细胞内,进而抑制肿瘤的增殖。
卡培他滨是一种新型口服给药的氟尿嘧啶氨基甲酸酯。该药通过胃肠道吸收,于肝脏被先后代谢转化5'-脱氧氟胞苷、5'-脱氧氟脲苷,后进入细胞内最终在胸腺磷酸化酶的作用下转化成5-氟尿嘧啶而发挥抗肿瘤作用。由于肿瘤细胞内胸腺磷酸化酶的浓度较高,故卡培他滨可在肿瘤细胞内被高效转化,从而选择性的杀伤肿瘤细胞,正常组织细胞内转化率较低,影响较小,故该药在体内的作用模式具有一定的靶向性。同时,药物的代谢动力学发现该药体内的代谢转化具有持续性,可以模仿5-fu的静脉持续泵入。REAL-II试验证实卡培他滨疗效上不劣于5-fu,可以替代,且有一定优势[8]。
本临床研究采用DCF方案为对照组,取得了近期有效率46.7%,疾病控制率DCF70%,中位PFS为6.9个月,与其他研究者的观察结果十分接近[9],具有较高的疾病控制率。但该方案不良反应较大,尤其在血液学毒性、腹泻和疲乏方面,极大地限制了该方案的使用人群。实验组以脂质体紫杉醇(力朴素)联合卡培他滨(希罗达)为治疗方案对34例晚期胃癌患者行治疗,取得了近期有效率41.2%,疾病控制率DCR67.6%,中位PFS6.2个月。对比疗效,我们发现脂质体紫杉醇联合卡培他滨的治疗方案在近期有效率和疾病控制率均接近DCF方案,但在毒副反应反应方面却明显降低。两组患者的总生存曲线走势基本相同,差异无显著性,说明两方案在延长晚期胃癌患者的生存时间上,疗效相似。
综上所述,紫杉醇脂质体联合卡培他滨在晚期胃癌的治疗上虽然在近期有效率上低于DCF方案,但两方案在总生存时间上并无明显差异。考虑到晚期胃癌目前不可治愈,治疗目的主要以延长生存时间,改善生活质量为主,故紫杉醇脂质体联合卡培他滨这一治疗方案仍具有低毒优效的优势,尤其适合状态评分差或年老患者,值得临床进一步推广。
1 郑朝旭,郑荣寿,陈万青.中国2009年胃癌发病与死亡分析[J].中国肿瘤,2013,(5):327-332.
2 Wagner A D,Unverzagt S,Grothe W,etal.Chemotherapy for advanced gastric cancer[J].Cochrane Database Syst,Rev,2010,17,(3):CD004064.
3 Bang Y J,Van Cutsem E,Feyereislova A,etal.Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer(ToGA):a phase 3,open-label,randomised controlled trial[J].Lancet,2010,376(9742):687.
4 Cullinan S A,Moertel C G,Fleming T R,etal.A comparison of three chemotherapeutic regimens in the treatment of advanced pancreatic and gastric carcinoma.Fluorouracil vs fluorouracil and doxorubicin vs fluorouracil,doxorubicin,and mitomycin[J].JAMA,1985,253(14):2061-2067.
5 Van Cutsem Eric,Moiseyenko Vladimir M,Tjulandin Sergei,etal.Phase III study of docetaxel and cisplatin plus fluorouracil compared with cisplatin and fluorouracil as first-line therapy for advanced gastric cancer:a report of the V325 Study Group[J].J Clin Oncol,2006,24(31):4991-4997.
6 Sharma A,Straubinger R M.Novel taxol formulations:preparation and characterization of taxol- containing liposomes[J].Pharm Res,1994,11(6):889-896.
7 周卫,翁帼英,陈文忠.紫杉醇脂质体在大鼠体内的组织分布[J].中国药学杂志,2005,40(18):1402-1404.
8 Cunningham D,Okines A F,Ashley S.Capecitabine and oxaliplatin for advanced esophagogastric cancer[J].N Engl J Med,2010,362(9):858-859.
9 Chen Xiao-Long,Chen Xin-Zu,Yang Chen,etal.Docetaxel,Cisplatin and Fluorouracil(DCF)Regimen Compared with Non-Taxane-Containing Palliative Chemotherapy for Gastric Carcinoma:A Systematic Review and Meta-Analysis[J].PLoSOne,2013,8(4):e60320.

