CaO催化剂对松木锯末快速热解制备生物油的影响
袁亮,刘运权,王夺,臧云浩
(厦门大学能源研究院,福建 厦门 361102)
目前,对全球变暖和能源安全的关注使生物质能源受到了越来越多的重视[1-2]。快速热解可以将能量密度低的农林废弃物转化为高能量密度的液体,故生物质作为一种可替代能源具有较大的潜力替代石油[3-5]。不过,生物质热解的主要产物——生物油成分极其复杂,存在热值低、酸度大、含氧量高等缺点,一般不能直接用作动力设备的燃料[6]。此外,生物油也较不稳定,随着储存时间的增加,易发生聚合导致大分子有机物的形成,使黏度、含水率和平均分子量都增加[6],这些都限制了生物油的广泛应用。有文献报道指出,生物油中存在的大量含氧有机物是导致生物油热值低、腐蚀性强、稳定性差的主要原因。故目前许多研究者都在借鉴石油化工的脱氧方法,采用催化剂对生物质热解蒸汽进行在线处理,以降低生物油的含氧量。比如,Williams等[7]使用ZSM-5型沸石分子筛作催化剂,一定程度上降低了生物油的氧含量,同时使多环芳烃也增加。Scholze[8]采用板岩为载体的MnO作为催化剂获得了热值更高,含水率更少的生物油,该生物油在80℃ 时仍能保持较低黏度,然而,其稳定性却没有获得明显改善。有鉴于此,有必要对催化热解进一步研究。CaO作为热解催化剂因具有价格低廉,能提高生物油pH值和降低生物油含氧量等优势目前受到广泛研究。比如,Lin等[9]发现CaO具有良好的脱氧效果;Wang等[10]指出CaO对降低生物油酸性和提高生物油中烃类含量具有一定作用。此外,为了提高热解的经济性,研究者们也正在尝试各种增加生物油产率的方法,包括改善热解蒸汽的冷凝系统等[11-12]。本研究在自制的1 kg/h连续热解反应器中,采用多级冷凝的手段,以CaO作为催化剂,考察了不同冷凝条件、CaO添加量等因素对热解生物油组成以及储存稳定性的影响,以期为生物油品质的改善提供理论基础。
1 实验
1.1 原料
实验采用的原料为松木锯末,粒径为1~2 mm。催化剂为CaO粉末,分析纯(含量不小于98%),粒径小于50 μm。松木锯末首先在105℃ 干燥箱中烘干至恒重,然后与CaO粉末机械混合。本实验共制备了4种配比的物料:即纯松木锯末、CaO占混合物质量分数分别为10%、20%、30% 的混合物料进行热解试验。松木的元素组成用德国Elementar公司的Vario EL CHNS分析仪进行测定,测得其元素组成为:C 49.41%、N 6.28%、H 0.24% 和 O 44.07%。
1.2 实验装置
实验装置及其流程如图1所示。
实验装置由进料系统、预热器、反应器、旋风分离器和冷凝系统等组成。实验所采用的流态化气体为氮气,由两条路线进入装置:一条从反应器底部经预热后进入预热器(预热器由电热丝进行加热);另一条从进料口前部进入,以防止负压使物料从反应器倒流至进料口导致进料受阻。反应器采用鼓泡流化床,石英砂作为传热介质,以实现物料的快速均匀受热。整个实验装置装有多个热电偶和压力传感器,能及时在线反馈数据,保证操作时系统能安全稳定地运行。
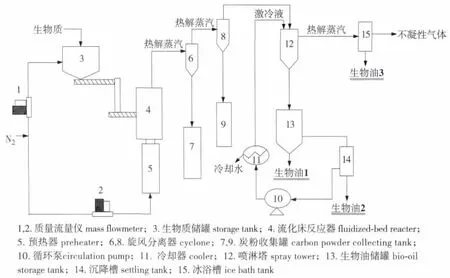
图1 生物质快速热解流程图Fig.1 The schematic diagram of biomass fast pyrolysis
实验时先通入氮气,使流化床内的传热介质流化起来,然后将预热器和反应器加热至一定温度,待达到预定的温度并稳定下来后,通过进料系统将生物质颗粒推入反应器中。生物质颗粒一旦进入反应器中就迅速裂解为蒸汽,热解蒸汽先经旋风分离器除去固体炭粉(收集在储炭罐中)。除炭后的裂解蒸汽再进入喷淋塔进行冷却。此时,大部分高沸点和大分子有机物在喷淋塔中被冷凝下来形成生物油1;不过生物油1储罐中有些密度较小尚来不及沉降的生物油有可能被循环泵抽至下一级沉降槽中,于是在该级沉降下来得到生物油2;喷淋塔中未被冷凝的热解蒸汽再进入冰浴槽中进一步冷凝形成生物油3,余下的不凝性气体经流量计计量后排空。
1.3 实验条件及分析方法
快速热解的实验条件为:热解温度500℃,常压;进料速率约为1 kg/h。原料热重分析通过美国TA仪器公司SDT-Q600热重分析仪进行,高纯氦气(纯度99.999%)作为载气,采用程序升温控制:由室温30℃ 升温至800℃,升温速率为20℃/min。获得的生物油组成采用日本岛津QP2010SE GC-MS进行分析。具体方法是:每次抽取收集到的生物油1 mL与丙酮配成生物油体积分数为5% 的溶液,然后用滤膜抽取1 mL待检测。GC程序升温控制:50℃ 保持3 min、升温速率4℃/min、终温280℃ 并保持3 min。离子源温度为280℃。根据NIST谱库并参考其它生物油组分,确定所得生物油的化学组成。生物油含水率采用瑞士METTLER-TOLEDO KF-V30卡式水分测定仪测定。pH值采用奥豪斯仪器(上海)有限公司starter 3C PH计测定。热值采用上海密通机电科技有限公司MTZW-A4高精度两用全自动量热仪测定。
本实验对生物质进行热重分析时,0~100℃区间内原料失重率即为其含水率。烘干后,纯松木和含3种不同比例催化剂的原料含水率均约为5%。
2 结果与分析
2.1 CaO催化剂对松木快速热解制备生物油的影响
2.1.1 CaO添加量对热解产物产率的影响 CaO添加量对热解产物分布和产率的影响见图2。由图2可见,随着CaO添加量的增加,生物油产率降低,气体产率增加,焦炭产率也增加。气体产率的增加可能是CaO使热解过程中脱羧反应增强,导致CO2增加所致;而焦炭产率增加可能是CaO从反应器中带出后在旋风分离器的作用下,被部分收集于炭罐中,使得焦炭的产率看上去好像是增加了。

图2 CaO添加量对热解产物产率的影响Fig.2 The effect of CaO addition on the pyrolysis products yield
2.1.2 CaO添加量对生物油中主要成分质量分数的影响 生物油1、2、3中主要含有酚、醛、酮、酯、酸等物质,其中以酚和酮含量最多,占生物油的一半以上,另外还含有少量的烃类。CaO添加量对酚、酮、烃和酯类含量具有一定的影响,见表1。酚在生物油1、2中的质量分数大于生物油3。加入CaO后生物油中酯类和酚类减少,但烃类和酮类增加。生物油中的酚主要是2-甲氧基苯酚、2-甲氧基-4-甲基苯酚、2-甲氧基-4-乙基苯酚、(E)-2-甲氧基-4-(1-丙烯基)苯酚,约占生物油中酚类总含量的70%左右。随着CaO的增加,生物油1、2、3中酚类质量分数由未添加CaO时的30%左右降至20%以下。生物油中的酚类减少可能是由于生物油中酸性官能团酚羟基与CaO反应,或CaO的催化作用将酚分解生成CO[13]。生物油中的烃一般为芳香烃,主要有乙苯和二甲苯两种,加入CaO后这两种物质均增加,并随着CaO含量的增加而增加。有研究指出这是由于CaO的作用导致热裂解过程产物脱羧所致[14-15]。生物油中酮的含量也随着CaO的加入有所增加,这可能是因为钙的羧酸盐在400~500℃ 下按反应式(1)、(2)分解为酮和CaCO3所致[16-17]。酯类含量降低可能是由于pH值升高导致其水解。
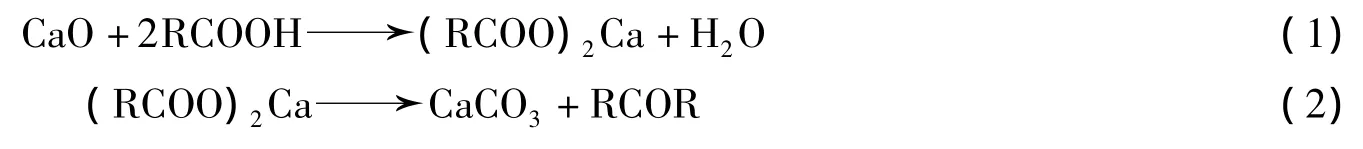
表1 CaO添加量对生物油中各主要成分的影响Table 1 The effect of CaO addition on the major components in bio-oils
2.1.3 CaO添加量对生物油含水率、热值和pH值的影响 CaO添加量对生物油的含水率、热值和pH值的影响见表2。

表2 CaO添加量对生物油含水率、热值和pH值的影响Table 2 The effect of CaO addition on the content of water、heating value and pH value of bio-oils
从表2可以看出:在未添加CaO的松木锯末热解生物油中,生物油1、2和3的含水率分别是13.6%、22.3% 和27.3%,表明了生物油中的大部分重组分在第一级即被冷凝下来,而在第2级和第3级获得的轻组分较多。即第一级生物油以油相为主,后两级以水相为主。随着CaO添加量的增加,各级收集到的生物油含水率均有明显增加。当松木锯末中CaO质量分数达30% 时,生物油1、2和3的含水率分别增加至20.5%、25.6% 和42.6%,这表明CaO能够使生物油中的部分含氧化合物催化脱氧,转化为H2O留在生物油中。
不同CaO添加量下生物油热值:生物油1>生物油2>生物油3。这是因为生物油1中酸类、水含量较低,酚类化合物含量较高,因此其热值最高。随着CaO添加量的增加,生物油1、3的热值略有下降,这可能是因为其含水率增加所带来的热值降低效应比含氧量下降所带来的热值升高效应更明显。扣除水分,生物油中有机相的热值随着CaO质量分数的增加逐渐增大,这可解释为CaO参与脱氧使得生物油含氧量下降。生物油2为激冷塔底部暂储罐下降过程中被循环泵抽过来的生物油,所以含水率变化不大,其热值随着CaO添加量的增加而略有增大,可解释为其含氧量下降所带来的热值升高效应大于含水率增加所带来的热值降低效应。
在未添加CaO得到的生物油中,生物油1、2和3均有较高的酸度,pH值依次是2.5、2.4和2.4。随着CaO量的增加,生物油的酸度得到明显改善。30%的CaO添加量使生物油1的pH值提高至4.4,这可解释为生物油中酸类物质在CaO作用下得到了较大程度的转化,表明添加CaO对于降低生物油酸度具有较好效果。Wang和Lin等[9-10]也得到相似的结果,这可解释为两个原因,第一是热解过程中CaO与羧基等酸性基团或“富氧中间体”碎片直接反应生成可二次分解的糖醛酸钙等钙盐[18],阻碍了酸类物质的生成。第二是加入CaO后,CaO参与如反应式(3)所示的脱羧反应,使得生物油中酸含量减少。

2.2 CaO添加量对生物油稳定性的影响
将生物油在室温下密闭保存30 d后,再次对生物油的组分、含水率、热值和pH值进行测定。生物油中酚类、酯类和呋喃类质量分数的变化如表3。由表3可以看到,放置一段时间以后生物油中酚类含量增加,酯类含量减少,未加CaO的生物油中酚类含量增加约10%~20%。加了CaO的生物油中酚类含量增加约30%~50%。可知CaO对生物油放置过程中酚类含量的增加有促进作用,这是因为木质素热解过程中热力学未达平衡所致。由表1和表3还可以看到,没加CaO的生物油在储存过程中呋喃类化合物会增加,加了CaO后的生物油中呋喃类化合物反而减少。
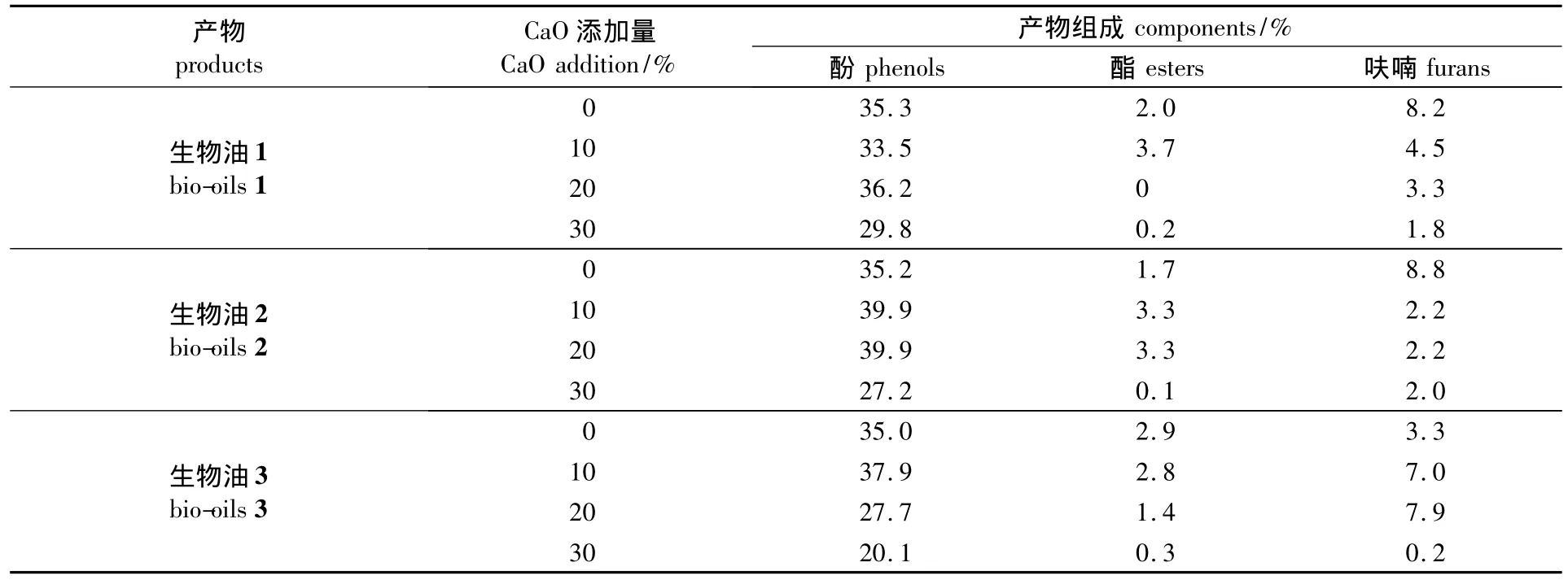
表3 放置30 d后生物油组分的变化Table 3 The change of components in bio-oils after stored for 30 days
生物油储存过程中含水率、热值和pH值的变化如表4。生物油在储存过程中含水率增加,可能是由于生物油中不饱和键的缩合反应[19],如羰基和羟基的酯化反应,副产物是水。储存过程中的酯化反应也能增加含水率。储存过程中生物油热值略有降低,大约降低了2% ~4%,这与生物油中烃类含量降低有关。未加CaO的生物油储存过程中pH值基本没变化,加入CaO的生物油1、2其pH值略有下降,但与CaO添加量关系不明显。可解释为碱性条件下酯类物质水解所致,如反应式4所示。由于钙盐在生物油1、2处全部沉积下来,所以对生物油3没有影响。
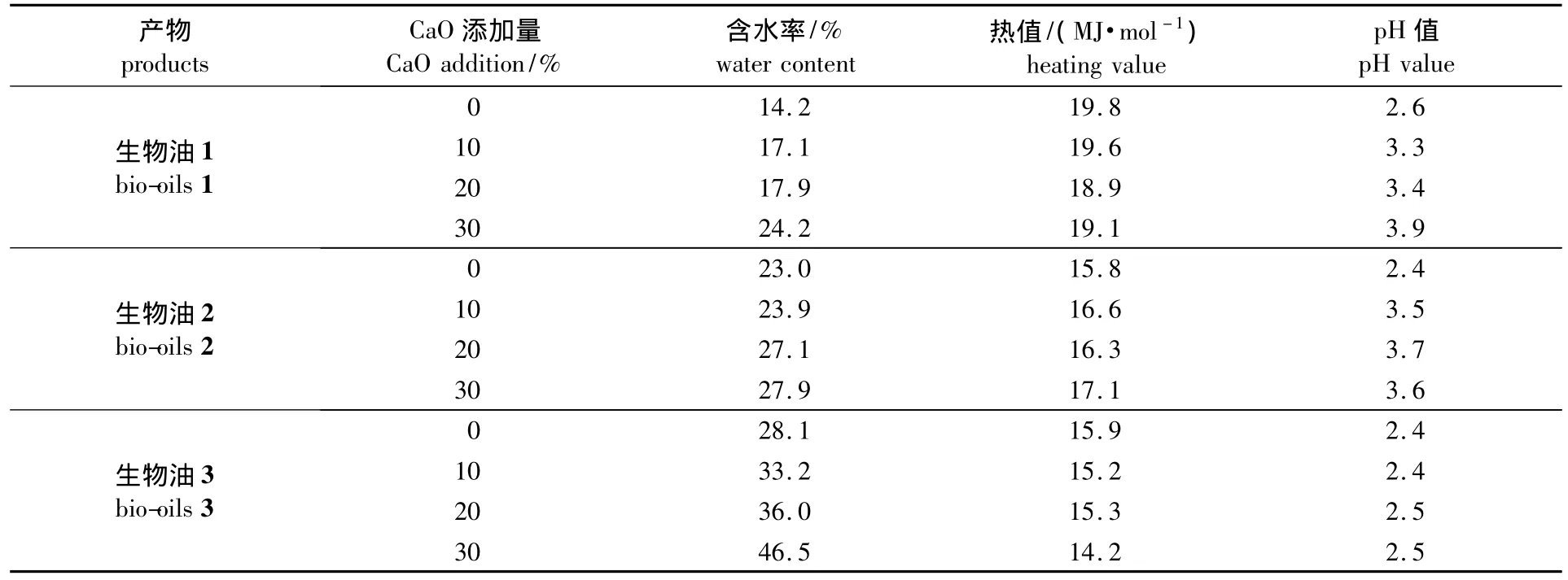
表4 放置30 d后生物油含水率、热值和pH的变化Table 4 The change of water content,heating value and pH value in bio-oils after stored for 30 days
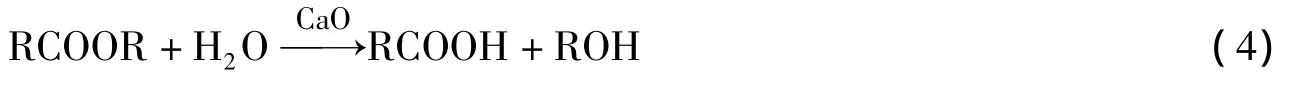
3 结论
在小型鼓泡流化床反应器中,对添加CaO催化剂的松木锯末进行了快速热解制备生物油的研究。热解蒸汽采用多级冷凝,以尽可能回收更多的液体产物,同时实现液体产物的初步切割分馏。其中第一级冷凝采用循环冷却介质进行喷淋激冷,第二、三级分别采用间壁式水冷和冰浴冷却,收集到的液体产物依次命名为生物油1、生物油2和生物油3。
3.1 CaO催化剂的加入使得生物油含水率增加,酚类减少,酮类含量增加,热值下降。
3.2 生物油储存过程中,酯类减少,含水率和酚类增加,呋喃化合物在未加CaO的生物油中增加,而在加入CaO的生物油中则减少。
3.3 多级冷凝可获得不同组成和物性差异的生物油,相当于对生物油进行了初步切割分馏。各段生物油呈现下列特点:含水率:生物油1<生物油2<生物油3;热值:生物油1>生物油2>生物油3;酚类含量:生物油1>生物油2>生物油3;pH值:生物油1>生物油2>生物油3。
[1]MOHAN D,PITTMAN C U,STEELE P H,et al.Pyrolysis of wood/biomass for bio-oil:A critical review[J].Energy Fuels,2006,20(3):848-889.
[2]OASMAA A,SOLANTAUSTA Y,ARPIAINEN V,et al.Fast pyrolysis bio-oils from wood and agricultural residues[J].Energy Fuels,2010,24(2):1380-1388.
[3]廖益强,黄彪,陆则坚.生物质资源热化学转化技术研究现状[J].生物质化学工程,2008,42(2):50-54.
[4]郑志锋,蒋剑春,戴伟娣.生物质能源转化技术与应用(Ⅲ)[J].生物质化学工程,2007,41(5):67-77.
[5]蒋剑春.生物质能源转化技术与应用(I)[J].生物质化学工程,2007,41(3):59-65.
[6]CZERNIK S,BRIDGWATER A V.Overview of application of biomass fast pyrolysis oil[J].Energy Fuel,2004,18(2):590-598.
[7]WILLIAMS P T,NUGRANAD N.Comparison of products from the pyrolysis and catalytic pyrolysis of rice husks[J].Energy,2000,25(6):493-513.
[8]SCHOLZE B.Long-term stability,catalytic upgrading and application of pyrolysis oils-improving the properties of a potential substitute for fossil fuels[D].Hamburg:University of Hamburg,2002.
[9]LIN Yu-yu,ZHANG Chu,ZHANG Ming-chuan,et al.Deoxygenation of bio-oil during pyrolysis of biomass in the presence of CaO in a fluidizedbed reactor[J].Energy & Fuels,2010,24:5686-5695.
[10]WANG Deng-hui,XIAO Rui,ZHANG Hui-yan,et al.Comparison of catalytic pyrolysis of biomass with MCM-41 and CaO catalysts by using TGA-FTIR analysis[J].Journal of Analytical and Applied Pyrolysis,2010,89(2):171-177.
[11]WESTERHOF R J M,BRILMAN D W F,VAN SWAAIJ W P M,et al.Effect of temperature in fluidized bed fast pyrolysis of biomass:Oil quality assessment in test units[J].Industrial& Engneering Chemistry Research,2009,49(3):1160-1168.
[12]CHEN Tian-ju,DENG Chun-jian,LIU Rong-hou.Effect of selective condensation on the characterization of bio-oil from pine sawdust fast pyrolysis using a fluidized-bed reactor[J].Energy & Fuel,2010,24(11):6616-6623
[13]FRANKLIN H D,PETERS W A.HOWARD J B.Mineral matter effects on the rapid pyrolysis and hydropyrolysis of a bituminous coal(1):Effects on yields of char,tar and light gaseous volatiles[J].Fuel,1982,61:155-160.
[14]DING Lian-hui,RAHIMI P,HAWKINS R,et al.Naphthenic acid removal from heavy oils on alkaline earth-metal oxides and ZnO catalysts[J].Applied Catalysis(A):General,2009,371(1/2):121-130.
[15]ZHANG Ai-hua,MA Qi-sheng,WANG Kang-shi,et al.Naphthenic acid removal from crude oil through catalytic decarboxylation on magnesium oxide[J].Applied Catalysis(A):General,2006,303(1):103-109.
[16]LU Hong,KHAN A,SMIRNIOTIS P G.Relationship between structural properties and CO2capture performance of CaO-based sorbents obtained from different organometallic precursors[J].Industrial& Engineering Chemistry Research,2008,47(16):6216-6220.
[17]YANG Xu-lai,ZHANG Jian,ZHU Xi-feng.Decomposition and calcination characteristics of calcium-enriched bio-oil[J].Energy & Fuels 2008,22(4):2598-2603.
[18]谭洪.生物质热裂解机理实验研究[D].杭州:浙江大学硕士学位论文,2005.
[19]CZERNIK S,JOHNSON D K,BLACK S.Stability of wood fast pyrolysis oil[J].Biomass Bioenergy,1994,7(1/2/3/4/5/6):187-192.

