紫外分光光度法测定茶碱缓释片中茶碱的含量
程弘夏,吴沁林,冉林荣,许腊英
(武汉理工大学华夏学院,湖北 武汉 430223)
2013-09-29
作者简介:程弘夏(1970-),女,天津人,博士,副教授,主要从事药物制剂研究,E-mail:chenghx70@aliyun.com。
doi
:10.3969/j.issn.1672-5425.2013.12.020
紫外分光光度法测定茶碱缓释片中茶碱的含量
程弘夏,吴沁林,冉林荣,许腊英
(武汉理工大学华夏学院,湖北 武汉 430223)
以蒸馏水为提取溶剂,检测波长为272 nm,采用紫外分光光度法测定了茶碱缓释片中的茶碱含量。结果表明,茶碱浓度在1.5~13.5 μg·mL-1范围内线性关系良好(R=0.9997),平均加标回收率为97.34%,RSD为0.70%。该法操作简单、快速,结果准确,适用于茶碱缓释片中茶碱含量的测定。
紫外分光光度法;茶碱缓释片;茶碱;含量测定
茶碱为甲基嘌呤类药物,具有强心、利尿、扩张冠状动脉、松弛支气管平滑肌和兴奋中枢神经系统等作用,临床主要用于治疗支气管性与心源性哮喘,也可用于心源性水肿的治疗。由于茶碱治疗窗窄,普通制剂血药浓度波动大,疗效不稳定,为此国内外相继研发出各种规格的茶碱缓释制剂,如茶碱缓释片、缓释胶囊、缓释小丸等。这些缓释制剂可降低血液浓度峰谷差值,减少毒副作用。
茶碱的测定方法一般有HPLC法、GC法、TLC法、磷光分析法等[1,2],2010版《中国药典》采取容量分析方法测定茶碱缓释片含量[3]。作者在此建立了茶碱缓释片含量测定的紫外分光光度方法。
1 试药与仪器
茶碱对照品(纯度100%),中国药品生物制品检定所;茶碱缓释片(批号:20110902、20111207、20121101,规格0.1 g),广州某制药公司。
TU-1900型双光束紫外可见分光光度计,北京普析通用仪器有限责任公司;KQ600E型超声清洗器,昆山市超声仪器有限公司;AN7388型分析天平,上海民桥精密科学仪器有限公司。
2 方法与结果
2.1 检测波长的确定
分别取茶碱对照品及3个批号茶碱缓释片细粉适量,加热水使其溶解,过滤,配制成适宜浓度,摇匀。以水为空白,在200~400 nm范围内进行扫描,结果见图1。
由图1可以看出,茶碱在272 nm处有最大吸收,缓释片溶液与对照品溶液的吸收曲线形态基本一致,说明辅料对茶碱光谱特征无干扰。故选择272 nm作为茶碱缓释片含量测定波长。
2.2 最优提取方法的确定
2.2.1 提取溶剂的选择
分别取不同批号的茶碱缓释片各20片,精密称定并计算平均片重,研细。每个批号精密称取茶碱缓释片细粉适量(约相当于无水茶碱0.1 g)各3份,置具塞锥形瓶中,分别加入等量蒸馏水、无水乙醇、无水氯仿,超声20 min使充分溶解,过滤,续滤液定容于100 mL容量瓶中,摇匀。取1 mL至100 mL容量瓶中,加相应的溶剂稀释至刻度,在272 nm处测定吸光度,结果见表1。
表1不同提取溶剂对茶碱含量测定的影响
Tab.1Effectofdifferentextractionsolventsondeterminationoftheophyllinecontent

由表1可以看出,在相同的提取条件下,以蒸馏水为提取溶剂时的平均吸光度较高,提取效果较好。
2.2.2 水浴提取时间的选择

图1 茶碱对照品(a)和茶碱缓释片(b~d)的紫外吸收光谱Fig.1 UV Spectra of theophylline standard(a) and theophylline sustained-release tablets(b~d)
分别取不同批号的茶碱缓释片各20片,精密称定并计算平均片重,研细。每个批号精密称取茶碱缓释片细粉适量(约相当于无水茶碱0.1 g)各5份,在70 ℃水浴中,以蒸馏水为提取溶剂分别提取10 min、20 min、30 min、45 min、60 min。充分溶解,过滤。续滤液按2.2.1方法定容后,在272 nm处测定吸光度,结果见表2。
表2水浴提取时间对茶碱吸光度的影响
Tab.2Effectofextractiontimeforwaterbathonabundanceoftheophylline
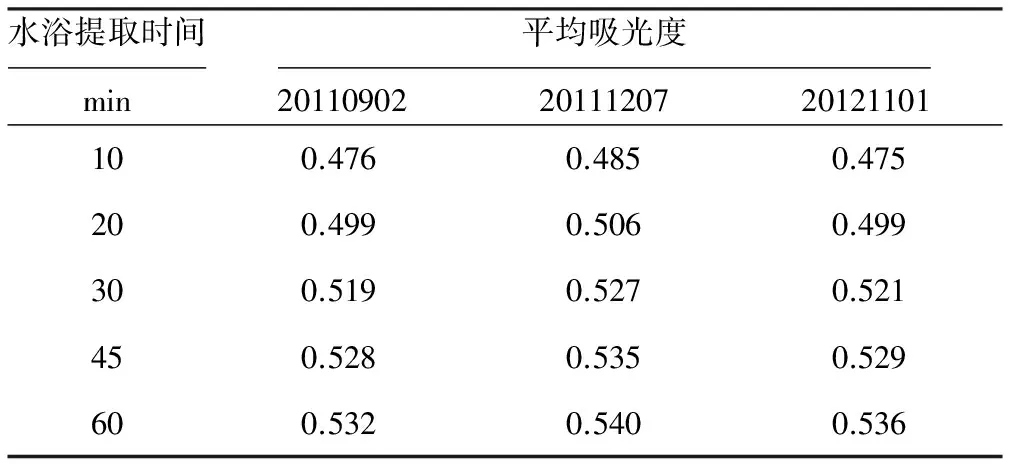
由表2可知,在相同的水浴温度下,前30 min的吸光度随提取时间的延长上升较快,30 min后吸光度升幅趋缓。
2.2.3 超声提取时间的选择
分别取不同批号的茶碱缓释片各20片,精密称定并计算平均片重,研细。每个批号精密称取茶碱缓释片细粉适量(约相当于无水茶碱0.1 g)各5份,以蒸馏水为提取溶剂分别超声提取10 min、20 min、30 min、45 min、60 min。充分溶解,过滤。续滤液按2.2.1方法定容后,在272 nm处测定吸光度,结果见表3。
表3超声提取时间对茶碱吸光度的影响
Tab.3Effectofextractiontimeforultrasoundonabundanceoftheophylline
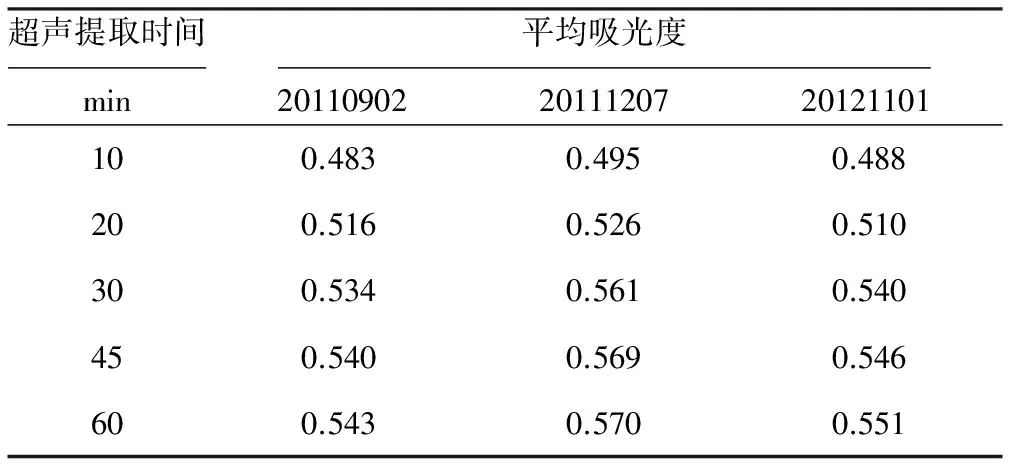
由表3可知,在超声提取中,前30 min的吸光度随超声时间的延长上升较快,30 min后吸光度变化不显著。
因此,确定以蒸馏水为提取溶剂,在70 ℃水浴中超声30 min提取茶碱缓释片中的茶碱,用于含量测定。
2.3 线性关系考察
精密称取茶碱对照品7.5 mg,置具塞锥形瓶中,加热水适量,在70 ℃水浴中超声30 min使充分溶解,放冷。定量转移至100 mL容量瓶中,用水稀释至刻度,摇匀,得75 μg·mL-1茶碱对照品贮备液。分别精密量取1.0 mL、2.0 mL、3.0 mL、4.0 mL、5.0 mL、6.0 mL、7.0 mL、8.0 mL、9.0 mL对照品贮备液置50 mL容量瓶中,加水稀释至刻度,摇匀。以水为空白,在272 nm处测定吸光度。以吸光度(y)为纵坐标、茶碱浓度(x)为横坐标绘制标准曲线,并进行回归分析。得到回归方程为y=0.06614x+0.01704(R=0.9997),茶碱在1.5~13.5 μg·mL-1浓度范围内有良好线性关系。
2.4 精密度考察
分别配制3 μg·mL-1、9 μg·mL-1、12 μg·mL-1低、中、高三个浓度茶碱对照品溶液,连续测定5次吸光度,RSD分别为1.67%、1.02%、0.72%。表明方法的精密度良好。
2.5 稳定性实验
精密量取同一浓度对照品溶液,在0 h、2 h、6 h、8 h、10 h、24 h分别测定吸光度,RSD为0.86%。表明供试品溶液在24 h内稳定。
2.6 样品测定
分别取3批茶碱缓释片各20片,精密称定并计算平均片重,研细。精密称取茶碱缓释片细粉适量(约相当于无水茶碱0.1 g ),放入研钵中,加热水分次研磨,并转移至具塞锥形瓶中。在70 ℃恒温水浴中超声提取30 min,充分溶解,过滤。续滤液用水定容于100 mL容量瓶中,摇匀。取1 mL至100 mL的容量瓶中,加水稀释至刻度,摇匀,作为供试品溶液,测定吸光度,利用回归方程计算各样品的茶碱含量,结果见表4。
2.7 加标回收率实验
分别精密量取0.4 mL已知含量(约1000 μg·mL-1)的供试品母液9份,加入到100 mL容量瓶中,再依次精密加入400 μg·mL-1茶碱对照品溶液1 mL、1.5 mL、2 mL,加水稀释至刻度,摇匀,测定茶碱含量。结果表明,茶碱平均加标回收率为97.34%(n=9),RSD为0.70%。
表4不同批号茶碱缓释片中茶碱含量测定结果(n=3)
Tab.4Thedeterminationresultsofcontentoftheophyllineindifferentbatchesoftheophyllinesustained-releasetablet

3 结论
以蒸馏水为提取溶剂,在70 ℃水浴中超声30 min提取茶碱缓释片中的茶碱,并采用紫外分光光度法测定其含量。结果表明,茶碱浓度在1.5~13.5 μg·mL-1范围内线性关系良好(R=0.9997),平均加标回收率为97.34%,RSD为0.70%。该法操作简单、快速、经济、高效,且不受辅料干扰、重现性好,结果准确可靠,适用于茶碱缓释片中茶碱含量的测定。
[1] 卫艳丽,董川,杨颖.可可碱、咖啡因、茶碱的滤纸基质室温磷光测定[J].分析化学,2002,30(3):301-303.
[2] 蔡涛,祝业光.高效液相色谱法测定茶碱的缓释片中茶碱的含量[J].中国药事,2007,21(1):46-47.
[3] 中华人民共和国卫生部药典委员会.中国药典(2010版)二部[M].北京:化学工业出版社,2010:514.
DeterminationofContentofTheophyllineinTheophyllineSustained-ReleaseTabletbyUltravioletSpectrophotometry
CHENG Hong-xia,WU Qin-lin,RAN Lin-rong,XU La-ying
(WuhanUniversityofTechnologyHuaxiaCollege,Wuhan430223,China)
The content of theophylline in theophylline sustained-release tablet was determined by ultraviolet spectrophotometry by using distilled water as solvent.The detection wavelength was 272 nm.The calibration curve was linear in the range of 1.5~13.5 μg·mL-1(R=0.9997) and the average recovery was 97.34%,RSD was 0.70%.The method was rapid and simple with accurate result,which could be used for the quality control and determination of content of theophylline in theophylline sustained-release tablet.
ultraviolet spectrophotometry;theophylline sustained-release tablet;theophylline;determination of content
O 657.32
A
1672-5425(2013)12-0075-03

