低熔点铅在Graves眼病放疗中的剂量学优势分析
赵卫东,宁健,赵水喜,杨书明,郑子薇,穆晓峰
Graves眼病是一种常见的眼眶良性病,放射治疗是其有效治疗手段[1-2],Graves眼病在放疗时应在给予靶区治疗剂量的同时尽量降低患者晶体受量。目前放疗应用的主流加速器都配有电动多叶光栅(multileaf collimator,MLC),为实施复杂的照射技术及临床治疗带来了诸多便利,但眼眶部位存在范围小、结构复杂、MLC分辨率低和半影大的缺点,而低熔点铅(low-melting-point lead,LML)分辨率高,半影小,在传统放射治疗中具有剂量学优势。本研究旨在对LML和MLC两种照射野成形方法在眼眶放疗中的剂量学差异进行比较,以便使用晶体剂量更低的技术用于临床Graves眼病的治疗。
1 资料与方法
1.1 研究对象 均已确诊为单侧或双侧Graves眼病的患者各10例,主要表现为眼肌肥厚,有不同程度的突眼症状[1],将其分为单侧眼病组和双侧眼病组。
1.2 主要仪器 Precise Plan治疗计划系统和Precise三光子加速器(Elekta,瑞典)。
1.3 CT模拟定位与治疗计划 患者采取仰卧位,用头部固定架及热塑头膜固定,于头膜上粘贴金属标记点,在85cm大口径CT模拟机上进行CT扫描,扫描范围从头顶至颅底,层厚3mm,将CT图像通过局域网传至Precise Plan治疗计划系统,物理师接收图像后,由同一名医生按相同的原则勾画靶区,包括大体肿瘤体积(gross tumor volume,GTV)、临床靶区(clinical target volume,CTV)和计划靶区(planning target volume,PTV),PTV处方剂量2000cGy/10次[3],由物理师设计治疗计划,分别用LML和MLC在射野视线观(beam eye view,BEV)下形成照射野(图1),单侧眼病组的布野方案为2个X线平野+1个电子线野,双侧眼病组的布野方案为2个X线平野+2个电子线野(表1)。
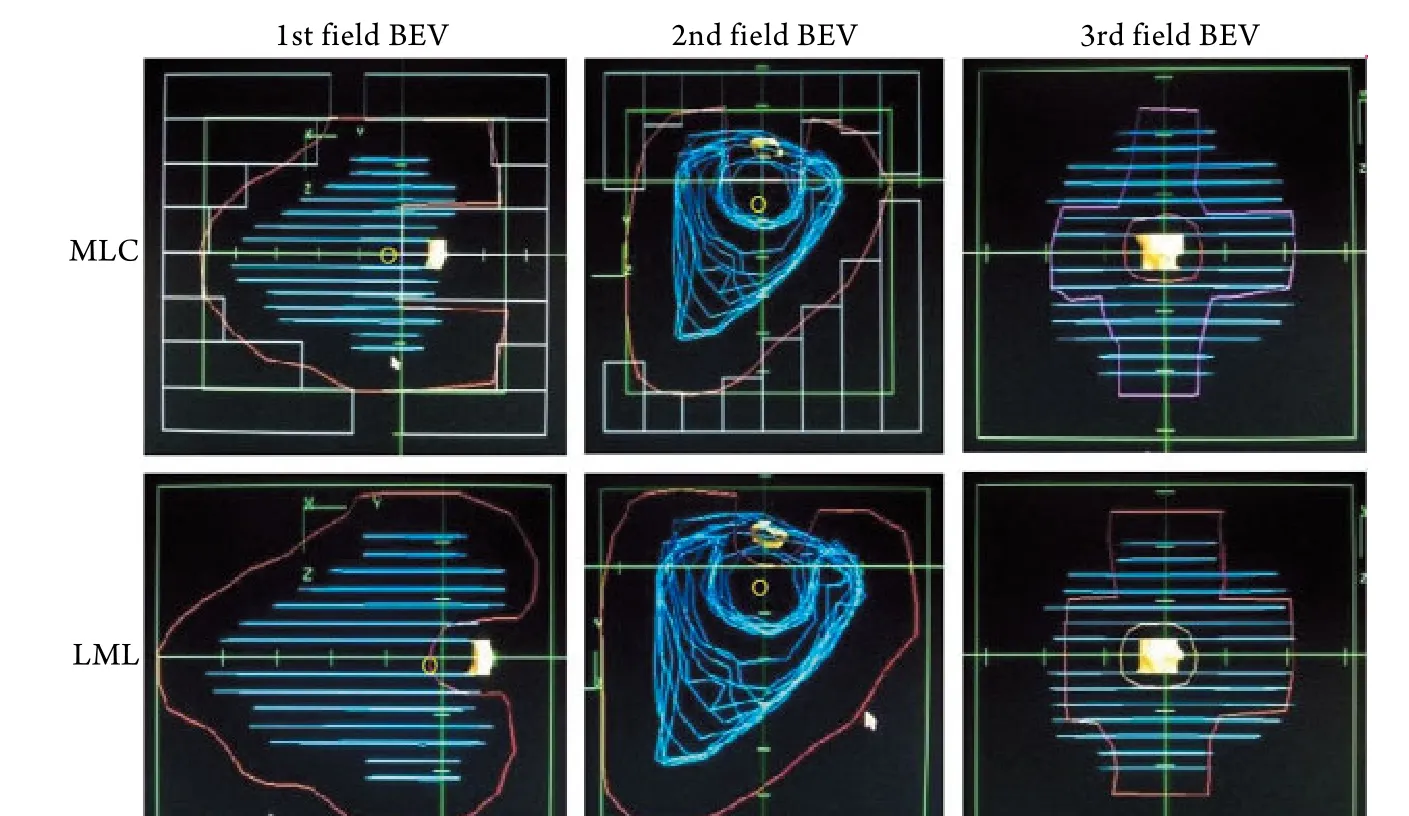
图1 MLC和LML两种方法形成的照射野的射野视线观(BEV)视图举例Fig. 1 Beam eye view (BEV) of radiation fields formed by MLC and LML
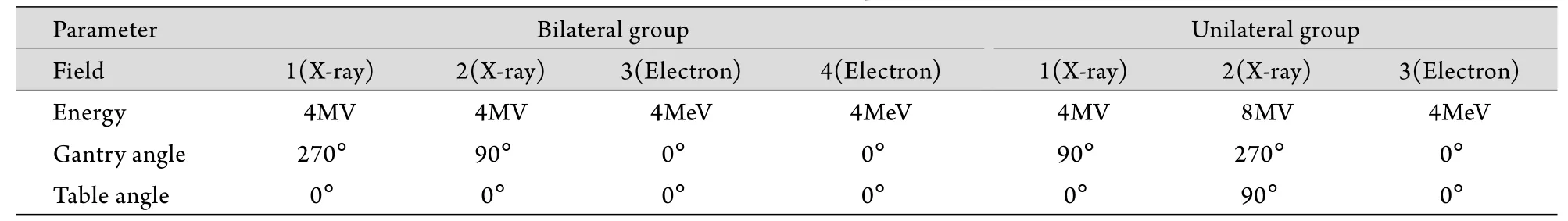
表1 照射野参数Tab. 1 Radiation field parameters
1.4 X线野布野方法 在实际布野过程中,在BEV下微调机架角和床角使患者两侧晶体尽量重合,有利于计划设计及减少晶体受量。所有的电子线野均添加圆柱形挡铅遮挡晶体。对于双侧眼病组患者,先微调两X线射野机架角,再对两电子线射野机架角也进行相应微调,尽量使电子线中心轴与X线中心轴垂直。等中心选在图1所示的O位置点,晶体的正下方,V型靶区上凹边的最低处,这样选择等中心就会使第一野形成半野照射,可进一步减少晶体所受的散射剂量。对单侧眼病和双侧眼病患者都分别采用LML和MLC形成两个计划照射野,三光子加速器的X线能量为4、8、15MV,MLC叶片等中心厚度为10mm,计算网格采用1mm。治疗时将患者眼部的头膜部分剪掉,以便患者睁眼,叮嘱患者盯住眼前的圆柱形挡铅。
1.5 治疗计划评估参数 包括靶区适形指数(conformal index,CI)和剂量体积直方图(dose volume histogram,DVH)。CI=(TVRI/TV)×(TVRI/VRI),其中TVRI为90%参考等剂量曲线所包括的靶体积,TV为靶体积,VRI为参考等剂量曲线的体积。
1.6 半影测量 采用EBT免冲洗胶片,分别用LML和MLC形成5cm×5cm 的X线照射野,其中X1=-5cm,X2=0cm,Y1=-2.5cm,Y2=2.5cm,形成半野照射野,X线能量选择4MV和8MV,用固体水夹紧胶片,胶片上置4cm厚固体水,与射野中心轴夹角为90°,照射完成2h后扫描,采用剂量分析软件分析半野中心轴处半影大小[4]以及射野边缘不同距离处的散射量大小。
1.7 统计学处理 采用SPSS 11.0软件进行统计学分析。计量资料采用表示,比较采用配对t检验,总误差计算用Rosenthal方法。P<0.01为差异有统计学意义。
2 结 果
2.1 DVH和剂量分布对比结果 图2为1例单侧眼病组和1例双侧眼病组患者两种计划方式的DVH比对结果。单侧眼病组患者在MLC和LML两种照射野成形方式下,患侧晶体剂量分别为582±34cGy和252±45cGy,用LML者明显低于用多叶光栅者,约低16.5%,差异有统计学意义(P<0.01)。健侧晶体剂量分别为160±22cGy和148±19cGy,差异无统计学意义(P>0.01),应用LML的患者并未得到明显改善。MLC和LML两种方式的靶区适形度分别为0.69和0.71(P>0.01),也未得到改善。
对于双侧眼病组患者,采用M LC成野的结果为左晶体剂量591±47cGy,右晶体剂量585±52cGy,靶区适形度0.67;LML方式的结果为左晶体剂量247±44cGy、右晶体剂量256±42cGy、靶区适形度0.68,可见对于双侧患者,采用LML时的双侧晶体平均剂量也明显低于采用MLC者(约降低12%),差异有统计学意义(P<0.01),但对靶区适形度并无明显改善(P>0.01)。
图3为1例单侧患者的剂量分布对比图,等剂量线选择100%、90%、50%、30%。对于靶区最大剂量点此计划比对没有做特殊要求,这是因为靶区总剂量是2000Gy,靶区不均度不是关注要点,只要高剂量区域在靶区范围内即可。
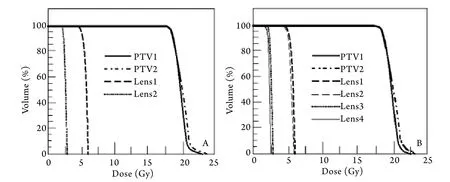
图2 两种计划方式的DVH结果Fig. 2 DVH results by the planned technique of MLC and LML
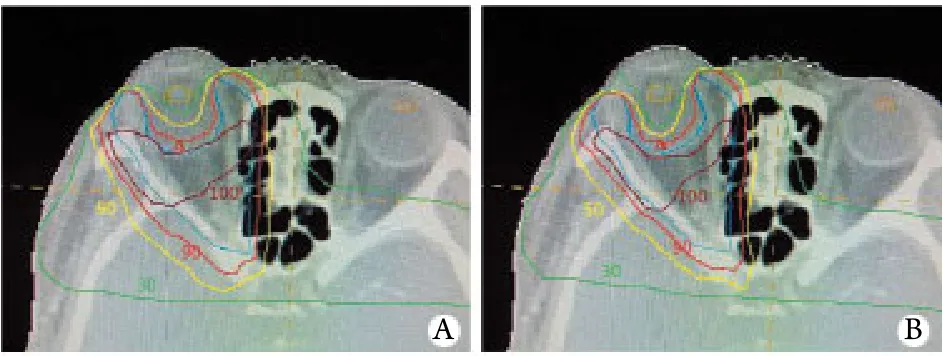
图3 1例单侧眼病组患者两种成野方式的剂量分布Fig. 3 Dose distribution of a patient in unilateral group formed by MLC and LML
2.2 半野照射野半影和散射剂量结果 MLC和LML两种成野方式形成5cm×5cm半野照射野,参考深度取4cm,能量4MV时半影大小分别为MLC 8.2mm、LML 5.0mm,能量8MV时半影大小分别为MLC 8.0mm、LML 4.8mm,LML照射野的半影(20%~80%)约3.0mm,小于MLC[5]。表2为单个X线照射野边缘不同距离处所受的散射剂量,对于单个X线野在距离照射野边缘相同的距离处(5~10mm),LML的散射剂量要比MLC小3.26%~2.26%(4MV)或5.35%~1.86%(8MV)。
3 讨 论
目前业已证实,放射治疗Graves眼病是有效的手段,剂量多选择2000Gy/10次[3]。由于现在主流加速器都配有电动MLC,采用MLC的优点是方便、快捷、效率高,可完成比较复杂的照射技术,缺点则是叶片间易形成漏射,半影大,分辨率低。应用MLC等中心处1cm宽的叶片治疗眼部疾病时,由于眼部面积小(仅5cm×5cm),结构复杂,其缺点就暴露出来,尤其是当靶区是较复杂的V字形时,计划不能很好地完成。如图1的BEV视图所示,用MLC形成照射野时,叶片宽度为1cm,用一个叶片遮挡晶体时宽度不够,散射线会造成晶体剂量过高,用两个叶片时,叶片的左右两个角会深入靶区内,造成靶区欠剂量,而用LML形成照射野时,就不存在上述问题,可完美遮挡晶体。用LML技术能显著降低晶体剂量的主要原因是其半影较MLC更小,射野边缘整齐,对于5cm×5cm照射野参考深度为4cm,距离照射野边缘相同的距离,LML方式的散射量比MLC方式少2%~5%。LML技术对单侧和双侧眼病患者的晶体受量均有显著改善,由于Graves眼病是良性病,所以控制晶体受量,降低以后发生视力受损和白内障等并发症显得尤为重要,虽然LML比MLC的治疗技术更为复杂,但在有条件的单位可逐步开展。
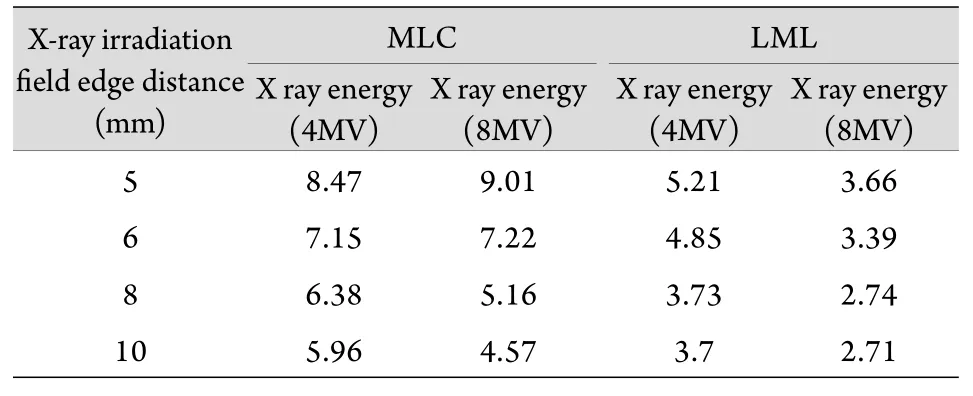
表2 单个X线照射野边缘不同距离处所受散射剂量(%)Tab. 2 Scatter dose at different distances from the edge of single X-ray radiation field (%)
[1]Ning J, Zhao SX, Zhao WD, et al. To evaluate the dose distribution of conformal radiotherapy for Graves'ophthalmopathy[J]. Chin J Pract Ophthalmol, 2005, 23(7): 666-669. [宁健, 赵水喜, 赵卫东, 等. 适形放射治疗Graves眼病剂量分布评价[J]. 中国实用眼科杂志, 2005, 23(7): 666-669.]
[2]Liu C, Guo JJ. Treatment Modalities for Graves'Ophthalmopathy[J]. Chin J Pract Intern Med, 2010, 30(3): 286-288.[刘超, 郭剑津. Graves眼病治疗模式的合理选择[J]. 中国实用内科杂志, 2010, 30(3): 286-288.]
[3]Mourits MP, van Kempen-Harteveld ML, Carcia MB, et al.Radiotherapy for Graves' orbitopathy: randomised placebocontrolled study[J]. Lancet, 2000, 355(92/4): 1505-1509.
[4]Saur S, Frengen J. GafChromic EBT film dosimetry with flatbed CCD scanner: a novel bac kground correction method and full dose uncertainty analysis[J]. Med Physics, 2008, 35(7): 3094-3101.
[5]LoSasso T, Chui CS, Kuatcher GJ, et al. The use of multi-leaf collimator for conformal radio therapy of carcinomas of the prostate and nasopharynx[J]. Int J Radiat Oncol Biol Phys, 1993,25(2): 161-170.

