龙胆泻肝颗粒质量标准研究
刘 颖,胡 琴,陶志国
(北京市药品检验所,北京 100035)
龙胆泻肝颗粒现正式批准生产的有两种剂型,其中颗粒(A)收载于《卫生部药品标准》中药成方制剂第十一册,标准号为WS3-B-2108-96,规格为每袋装6 g,原标准收载了栀子苷的薄层色谱鉴别;颗粒(B)收载于《卫生部药品标准》新药转正标准第33册,标准号为WS3-197(Z-187)-2001(Z),规格为每袋装4 g,原标准收载了甘草、栀子、泽泻、地黄的显微鉴别以及黄芩苷、龙胆苦苷的薄层色谱鉴别和高效液相色谱法测定黄芩中黄芩苷的含量。经折算,两种规格日服用生药量一致,颗粒(A)与颗粒(B)主要的区别在于:颗粒(A)制法主要采用提取挥发油及水煮,颗粒(B)制法为药材全原粉包衣。考虑到两种龙胆泻肝颗粒的制法差异甚大,且处方量、性状、规格、用法与用量等项均不同,标准较难统一,故此次研究工作分别开展,以下品名均以“龙胆泻肝颗粒(A)”与“龙胆泻肝颗粒(B)”区别(或简称“颗粒(A)”、“颗粒(B)”)。为控制药品的内在质量及系列标准的统一,对处方中龙胆、柴胡、黄芩、栀子、泽泻、当归、地黄、甘草进行了薄层色谱鉴别,并采用高效液相色谱法测定了制剂中龙胆苦苷、栀子苷、黄芩苷的量。所建立的方法具有操作简便、分离效果好、重现性好,专属性强,准确等优点,可以有效地控制本品的质量。
1 仪器与试药
岛津LC-20A高效液相色谱仪,配备二极管阵列检测器(PDA)型;硅胶G预制板及高效硅胶GF254预制板(烟台市化学工业研究所,青岛海洋化工厂分厂)。
对照品黄芩苷(批号110715-200212)、龙胆苦苷(批号 110703-200322)、栀子苷(批号110749-200714)、甘草苷(批号111610-200604)、阿魏酸(批号0773-9910)与对照药材柴胡(批号120992-200705)、泽泻(批号121081-200302),地黄(批号121180-200402)均购于中国食品药品检定研究院。
龙胆泻肝颗粒(A)样品 3批:100201,100202,100203。龙胆泻肝颗粒(B)样品3批:101006,101007,101008。
甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
对第三层级的研究对象进行建模后,参考埃森曼的探讨习惯和伊塔罗·格伯利尼的建筑“构成符号”分类[1]41,将对象的建筑符号分为平面符号、连接符号、围护符号、相互交流符号和屋顶符号等5个部分进行图解分析。且因为 “能指”与“所指”的任意性,为了更贴近集中含义3),在对应语义三角关系前已经对研究对象的设计语境(其内容包括设计师言论、地方文化、地理气候等)进行了资料收集。
2.1.2 混播禾草种类对混播植物POD活性的影响 A2处理禾草POD活性最高,其次是A3处理。其中,A2处理禾草POD活性分别比A1,A3和A4处理高250.04%,20.22%和350.42%倍,差异均达极显著水平(P<0.01);A3处理禾草POD活性分别比A1和A4处理高191.18%和274.68%(P<0.01)。A1和A4处理之间差异不显著(表1)。A1处理下苜蓿POD活性比A4处理高19.47%(P<0.01);A3处理POD活性比A4处理高16.40%(P<0.05);其余处理之间无显著差异。
2 薄层色谱鉴别[1]
3.1 色谱条件 Phenomenex Luna C18色谱柱(5μm,4.6 mm×250 mm);流动相A为甲醇,以0.1%磷酸溶液为流动相B,进行梯度洗脱(0~25 min,22%A;25~30 min,22% ~43%A;30~55 min,43%A)。柱温为30℃,龙胆苦苷检测波长为270 nm,栀子苷检测波长为238 nm,黄芩苷检测波长为280 nm。理论板数按龙胆苦苷、栀子苷和黄芩苷峰计算均应不低于3000。
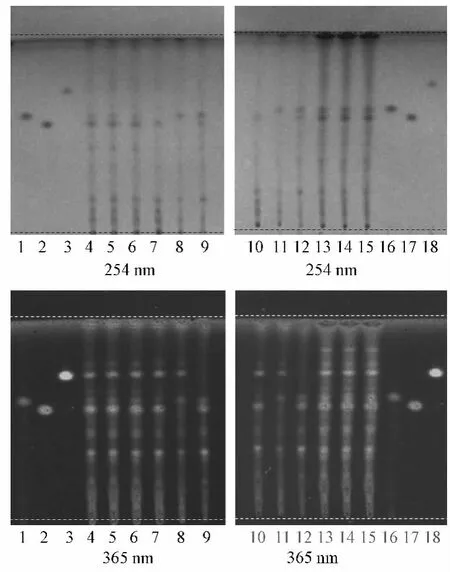
图1 龙胆泻肝颗粒(A)及颗粒(B)中龙胆苦苷、栀子苷、甘草苷的TLC图谱Fig.1 TLC chromatograms of gentiopicrin,geniposide and liquiritin
本研究结果表明,研究组治疗总有效率显著高于对照组(P<0.05),治疗后两组患者的IL-6、PCT水平及APACHEⅡ评分较治疗前均显著降低,且研究组低于对照组,两组比较差异具有统计学意义(P<0.05),两组患者均未发生不良反应。
2.2 泽泻的薄层色谱鉴别 取颗粒(A)15 g,颗粒(B)4 g,研细,加石油醚(60~90℃)50 mL,超声处理30 min,滤过,滤液挥干,残渣加石油醚(60~90℃)1 mL使溶解,作为供试品溶液。另取不含泽泻的颗粒(A)阴性制剂15 g,同法制成颗粒(A)泽泻阴性溶液。取龙胆泻肝颗粒(B)阴性制剂4 g,同法制成颗粒(B)泽泻阴性溶液。另取泽泻对照药材1 g,同法制成对照药材溶液。吸取上述供试品、对照药材及阴性溶液各10μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-甲酸(15∶2∶0.5)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。缺泽泻阴性样品无相应斑点。见图2。
充分发挥创新作为引领发展的第一动力作用,推动新技术、新产业、新业态加快成长,以体制机制创新促进共享经济发展,建设共享平台,壮大高技术产业、现代服务业等新兴产业集群,打造动力强劲的新引擎;运用信息网络、“ABC金三角(人工智能、大数据、云计算)”等现代技术,推动生产、管理和营销模式变革,重塑产业链、供应链、价值链,改造提升传统动能,使之焕发新的生机与活力。
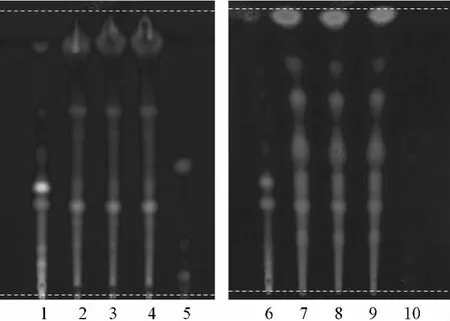
图2 龙胆泻肝颗粒(A)及颗粒(B)中泽泻的TLC图谱Fig.2 TLC chromatograms of Alismatis Rhizoma
巨型鲕粒样品的核心普遍为方解石构成的内碎屑或陆源碎屑(有些鲕粒核心已溶蚀,形成孔洞)。呈近椭圆状,粒径约1mm。多已重结晶,部分被白云石交代。鲕粒的核心可能是原地沉积的内碎屑,也可能是搬运而来。从核心的成因可以推断,在成鲕之前是一个流水或波浪的动水环境。

图3 龙胆泻肝颗粒(A)及颗粒(B)中地黄的TLC图谱Fig.3 TLC chromatograms of Rehmanniae Radix
3 HPLC法测定龙胆中龙胆苦苷、栀子中栀子苷、黄芩中黄芩苷[2-10]
2.1 龙胆、栀子、甘草的薄层色谱鉴别 取颗粒(A)8 g,颗粒(B)4 g,研细,加甲醇50 mL,超声处理10 min,滤过,滤液蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。分别取不含龙胆、栀子、甘草的阴性制剂颗粒(A)8 g,颗粒(B)4 g,分别同法制成龙胆、栀子及甘草的阴性溶液。另取龙胆苦苷对照品、栀子苷对照品、甘草苷对照品,分别加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。吸取上述供试品溶液、对照品溶液及阴性溶液各2μL,分别点于同一高效硅胶GF254薄层板上,以乙酸乙酯-丙酮-水(6∶6∶1)为展开剂,展开两次,取出,晾干,置紫外光灯(254 nm)下检视。供试品色谱中,在与龙胆苦苷对照品、栀子苷对照品色谱相应的位置上,显相同颜色的斑点;缺龙胆、栀子的阴性样品无相应斑点。再喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯(365 nm)下检视。供试品色谱中,在与甘草苷对照品色谱相应的位置上,显相同颜色的荧光斑点。缺甘草阴性样品无相应斑点。见图1。
3.2 对照品溶液的制备 取龙胆苦苷、栀子苷和黄芩苷对照品适量,精密称定,分别加甲醇制成每1 mL含龙胆苦苷10μg、栀子苷20μg、黄芩苷65μg的溶液,即得 [颗粒(A)测定用]。分别加甲醇制成每1 mL含龙胆苦苷20μg、栀子苷25μg、黄芩苷80μg的溶液,即得 [颗粒(B)测定用]。
3.3 供试品溶液的制备 取颗粒(A)混匀,取约2 g,颗粒(B)混匀,取约1g,精密称定,置具塞锥形瓶中,精密加入50%甲醇50 mL,密塞,称定质量,加热回流40 min,放冷,再称定质量,用50%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.3 地黄的薄层鉴别 取龙胆泻肝颗粒(A)15 g,颗粒(B)4 g,研细,加乙酸乙酯50 mL,超声处理30 min,滤过,滤液蒸干,残渣加乙酸乙酯1 mL使溶解,作为供试品溶液。取不含地黄的颗粒(A)阴性制剂15 g,颗粒(B)阴性制剂4 g,同法制成地黄阴性溶液。另取地黄对照药材1 g,同法制成对照药材溶液。吸取以上供试品、对照药材及阴性溶液各10μL,分别点于同一硅胶G薄层板上,以二甲苯-乙酸乙酯(3∶1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。缺地黄阴性样品无相应斑点。见图3。
3.4 阴性样品溶液的制备 分别按处方比例及制剂制备工艺制备不含龙胆、栀子、黄芩的阴性样品,再按3.3项下方法制备,即得。
适应辅助服务市场化的自动发电控制调频容量实时计算方法//仇进,吴继平,滕贤亮,徐瑞,于昌海//(8):16
2019款奥迪A4L全系增加的2个USB充电口,很大程度上解决了“机不离手”的年轻消费者在手机电量不足时的需求。除此之外,2019款A4L根据不同车型还为消费者们提供了包括“冬季包”、“豪华包”、“都市包”、“驾驶辅助包”在内的众多选装包套件,这些选装配置的组合包括了前排座椅加热、矩阵式LED大灯、B&O音响、自动泊车、主动车道保持、奥迪侧向辅助系统等,为用户驾驶带来诸多便利。相比前代车型,2019款A4L不变的是我们所熟悉的虚拟驾驶舱,作为同级别车型中最具科技表现力的配置之一,它能让你从此忘却平凡的机械结构仪表板。
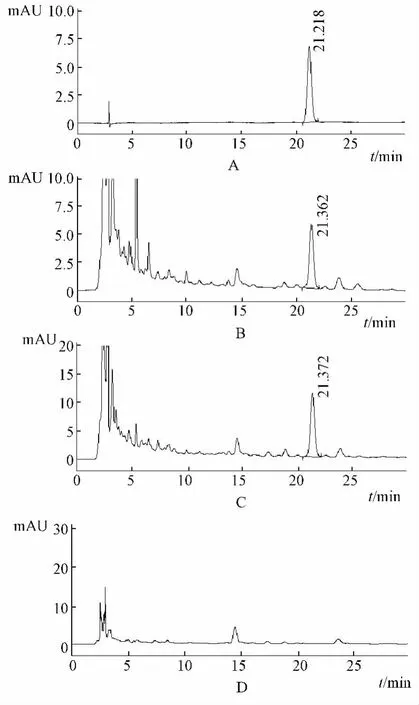
图4 龙胆苦苷测定HPLC图谱Fig.4 HPLC chromatograms of gentiopicrin
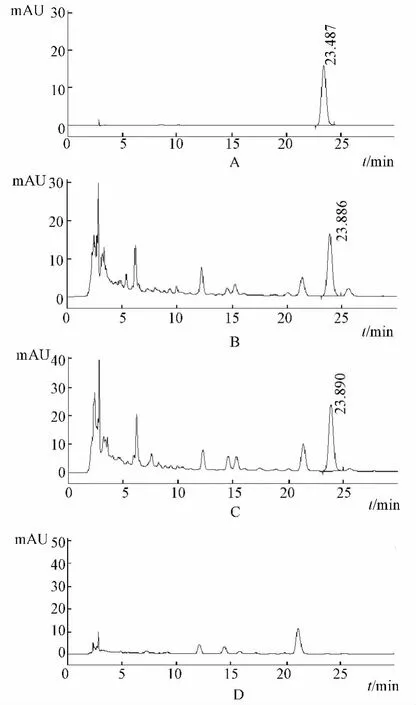
图5 栀子苷测定HPLC图谱Fig.5 HPLC chromatograms of geniposide
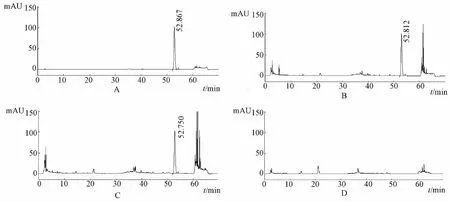
图6 黄芩苷测定HPLC图谱Fig.6 HPLC chromatograms of baicalin
3.6 线性关系考察 分别精密吸取龙胆苦苷对照品溶液(0.03306 mg/mL)1、2、3、4、6、8、10、12、15μL;栀子苷对照品溶液(0.0761 mg/mL)1、2、3、4、6、7、8、10、12、15μL;黄芩苷对照品溶液(0.1072 mg/mL)2、4、6、8、10、12、14μL,注入高效液相色谱仪,以进样量为横坐标,峰面积为纵坐标,其回归方程:龙胆苦苷为y=1321542.6x+788.1(r=1.0000),表明其在0.03306μg~0.4959μg范围内线性关系良好;栀子苷为y=1563674.5x-1620.3(r=1.0000),表明其在 0.0761μg ~1.1415μg 范围内线性关系良好;黄芩苷为y=3595816.7x+14494.7(r=1.0000),表明其在0.2144~1.608μg范围内线性关系良好。
3.7 稳定性试验 取同一份供试品溶液 [颗粒(A)批号100201,颗粒(B)批号:101006],按样品测定方法,颗粒(A)在制备后0、2、4、6、10、14 h进样测定,颗粒(B)在配置后0、2、4、8、12、14、16 h进样测定。颗粒(A)结果峰面积RSD龙胆苦苷为0.22%,栀子苷为0.23%,黄芩苷为0.19%,表明供试品溶液在14 h内基本稳定。颗粒(B)结果峰面积RSD龙胆苦苷为0.37%,栀子苷为0.32%,黄芩苷为0.36%,表明供试品溶液在16 h内基本稳定。
3.11 样品测定 按上述测定方法,分别测定3批龙胆泻肝颗粒(A)及颗粒(B)样品,结果见表1。
3.5 专属性试验 取对照品溶液、供试品溶液和阴性样品溶液各10μL,分别注入液相色谱仪,依法测定,结果龙胆、栀子、黄芩阴性样品分别在龙胆苦苷、栀子苷、黄芩苷相应保留时间处未见色谱峰,表明阴性样品对检测无干扰。见图4、5、6。
3.9 龙胆泻肝颗粒(A)加样回收率试验 采用加样回收法,设计3个质量浓度,每个质量浓度各制备3份供试品溶液。精密称取已知含有量的同一批样品(批号100201,龙胆苦苷为0.2811 mg/g,栀子苷为0.7776 mg/g,黄芩苷为2.0580 mg/g),①(低浓度)取约0.5g精密加入对照品混合溶液(含龙胆苦苷0.002239 mg/mL,栀子苷0.005830 mg/mL,黄芩苷 0.017125 mg/mL)50 mL;②(中浓度)取约1 g精密加入对照品混合溶液(含龙胆苦苷 0.004478 mg/mL,栀子苷 0.01166 mg/mL,黄芩苷0.03425 mg/mL)50 mL;③(高浓度)取约2 g精密加入对照品混合溶液(含龙胆苦苷0.008956 mg/mL,栀子苷0.02332 mg/mL,黄芩苷0.06850 mg/mL)50 mL。按供试品溶液同法制备,测定。结果龙胆苦苷平均回收率98.95%,RSD=1.6%;栀子苷平均回收率98.24%,RSD=1.8%;黄芩苷平均回收率102.15%,RSD=2.7%。
3.10 龙胆泻肝颗粒(B)加样回收率试验 采用加样回收法,设计3个质量浓度,每个质量浓度各制备3份供试品溶液。精密称取已知含有量的同一批样品(批号101006,龙胆苦苷为1.1117 mg/g,栀子苷为2.2352 mg/g,黄芩苷为4.1833 mg/g),①(低浓度)取约0.25 g精密加入对照品混合溶液(含龙胆苦苷0.005105 mg/mL,栀子苷0.004150 mg/mL,黄芩苷0.01936 mg/mL)50 mL;②(中浓度)取约0.5 g精密加入对照品混合溶液(含龙胆苦苷0.01021 mg/mL,栀子苷0.00830 mg/mL,黄芩苷0.03872 mg/mL)50 mL;③(高浓度)取约1 g精密加入对照品混合溶液(含龙胆苦苷0.02042 mg/mL,栀子苷0.01660 mg/mL,黄芩苷0.07744 mg/mL)50 mL。按供试品溶液同法制备,测定。结果龙胆苦苷平均回收率97.58%,RSD=0.36%;栀子苷平均回收率102.73%,RSD=1.5%;黄芩苷平均回收率99.74%,RSD=1.5%。
3.8 重复性试验 分别取颗粒(A)约2 g及颗粒(B)约1 g,研细,精密称定,依法测定。颗粒(A)龙胆苦苷RSD为0.68%,栀子苷为0.65%,黄芩苷为1.4%,方法重复性良好。颗粒(B)龙胆苦苷RSD为0.82%,栀子苷为0.49%,黄芩苷为0.63%,方法重复性良好。
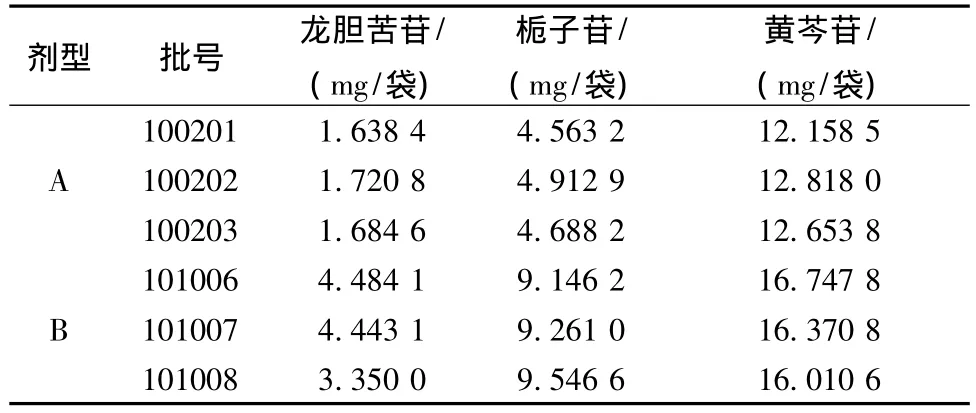
表1 龙胆苦苷、栀子苷、黄芩苷测定结果Tab.1 Determination results of gentiopicrin,geniposide and baicalin
4 讨论
4.1 龙胆泻肝颗粒(A)及龙胆泻肝颗粒(B),处方中均由十种药味构成,本研究共进行了其中五种药味的薄层色谱鉴别研究,木通及车前子未能购买到中国生物制品检定所提供的对照药材,故未进行研究。
4.2 龙胆苦苷、栀子苷、甘草苷的薄层鉴别中,由于3种成分较难分离,经过大量研究实验,最终确定用高效薄层板,以同一展开剂,展开2次的方法进行分离,得到了较理想的结果。
4.3 除前文介绍的3种薄层色谱外,还对柴胡、黄芩及阿魏酸的薄层色谱进行了研究,其中在进行颗粒(B)柴胡对薄层色谱研究中发现,其柱色谱分离时间较长,振摇提取乳化严重,分析原因可能由于颗粒(B)有包衣,该辅料对柱色谱及振摇提取均有影响,为除去该辅料,经大量实验研究,最终确定在提取前对其颗粒不进行研细处理,而是进行加热水60 mL,搅拌1 min,纱布滤过处理,使其包衣辅料除去后,再进行提取,得到了较理想的结果。
4.4 此次研究的6个薄层色谱,耐用性考察结果表明,采用不同品牌薄层板,在不同温度和湿度条件下,均能获得较好的薄层色谱分离。
4.5 本研究采用了同一样品,分别在其最大吸收波长下,同时测定3种成分的量,前处理简单,实验操作简便,可较大的节省实验中的人力及物力消耗。
4.6 分别采用不同品牌色谱柱 [(1)Phenomenex luna C18(5μm,250 mm×4.6 mm)、(2)Tech-Mate C18(5μm,250 mm×4.6 mm)、(3)Kromasil 100-5C18(5μm,250 mm×4.6 mm)] 进行测定,结果龙胆苦苷、栀子苷、黄芩苷峰分别在各种色谱柱均分离良好,空白无干扰,不同色谱柱间测定,龙胆泻肝颗粒(A)中龙胆苦苷的RSD为1.2%,栀子苷的RSD为1.5%,黄芩苷的RSD为0.85%;龙胆泻肝颗粒(B)中龙胆苦苷的RSD为1.7%,栀子苷的RSD为1.2%,黄芩苷的RSD为1.2%,表明本HPLC方法有较好的耐用性。
[1]郑小平,申丽莎.龙胆泻肝片的薄层鉴别方法[J].中国药业,2008,17(16):39-40
[2]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:7.
[3]李春红,梅志强,何 兵,等.HPLC同时测定龙胆泻肝制剂中黄芩苷、汉黄芩苷、黄芩素、汉黄芩素的含量[J].生物学通报,2012,47(4):60-62.
[4]王晓雷.高效液相色谱法测定龙胆泻肝丸中黄芩苷的含量[J].中国医药导报,2009,6(10):66-67.
[5]金齐武,张青云,蒲婧哲.HPLC法测定龙胆泻肝丸(水丸)中栀子苷的含量[J].安徽医药,2008,12(7):604-605.
[6]冯亦颖,王巨存,徐学锐.高效液相色谱法测定龙胆泻肝丸中栀子苷的含量[J].天津药学,2008,20(3):11-13.
[7]刘天柱,莫结丽.HPLC法测定龙胆泻肝片中栀子苷的含量[J].中国医药导报,2008,5(10):34-35.
[8]冯亦颖,王巨存,徐学锐.HPLC法测定龙胆泻肝丸中黄芩苷的含量[J].天津药学,2007,19(5):64-66.
[9]刘瑞新.HPLC同时测定龙胆泻肝丸中龙胆苦苷和栀子苷的含量[J].中成药,2007,29(8):1170-1172.
[10]沈美琼,徐 钢,张 庆.高效液相色谱法测定龙胆泻肝丸马兜铃酸 A含量[J].医药导报,2008,2(1):221-222.

