N,O双官能团配体铅配合物的合成、表征及荧光性质研究
谢 静,葛书旺,洪 波,刘汉明
(1.湖北工程学院 城建学院环境工程系,湖北 孝感432000;2.孝昌县一中,湖北 孝昌432900)
近年来,金属 有机骨架(MOFs)因具有多变的拓扑结构及在功能材料、医药、生物化学等诸多领域表现出潜在的应用价值,成为人们普遍关注的研究领域[1-3]。含氮芳香羧酸配体能同时提供N和O原子参与配位反应,配体的刚性骨架——含氮芳香环和柔性手臂——羧酸能够适应多种金属离子的配位需求,此外芳香羧酸配体还可以提供大量骨架构筑所需的氢键及π…π、C-H…π等相互作用,因此常被用于构筑混合金属配合物或具有多维网格结构的金属-有机骨架[4-5]。
大量含氮芳香羧酸类配合物是以d10电子组态的过渡金属和镧系金属为形成体,它们通常具有较强的配位能力和潜在的荧光性质,而关于主族金属元素与含氮芳香羧酸形成的配合物的研究并不多见[6]。p电子构型的主族金属是继3d电子构型的过渡金属和4f电子构型的稀土金属后的第三类分立发光中心,是光学材料发展的新方向[7],其中Pb(II)的配合物以其丰富的配位结构及在离子交换和光学等领域中的应用前景,引起了广泛关注。一方面,铅的原子半径与镧系金属相近,可以形成较高的配位数,如9~10的配位数;另一方面,Pb(II)的6s轨道上有一对惰性电子,它对成键电子对的排斥常使Pb(II)周围的配位键分布在半球形区域内,从而导致配位数相对较低,如可以形成配位数为2~5的配合物。当配位数为6~8时,惰性电子对的立体化学活性及由此带来的配合物几何构型上的变化受到配体及配位原子本性的强烈影响。一般而言,体积较大的配体,和较软的配位原子会弱化惰性电子对的立体化学活性,从而配位键可以分布于Pb(II)全部球形区域内。这种配位特征在d区及其它元素中是少见的,导致Pb(II)成为一种很有研究意义的金属离子[8-13]。
本文选择吡啶-3-甲酸作为配体,通过溶液法与硝酸铅发生配位自组装反应,利用红外光谱、电子光谱、热重分析等手段表征了所得配合物,并研究了配合物室温下的固态荧光性质。
1 实验部分
1.1 实验试剂与仪器
硝酸铅(AR),吡啶-3-甲酸(AR),氢氧化钠(AR),甲醇(AR);Vario elemental III(德国),Nicolet-380智能型傅立叶红外光谱仪(美国),SDTQ600型差示扫描量热仪(美国),TU -1901型紫外光谱分析仪(北京),FLS920全功能型荧光光谱仪(英国)。
1.2 配合物的合成
称取0.0993g(0.3mmol)硝酸铅于小烧杯中,加入8mL甲醇溶解成清液。另取0.0369g(0.3mmol)吡啶-3-甲酸,溶解于8mL甲醇中。室温下混合上述两种澄清溶液,并于搅拌下向混合液中加入1mL饱和氢氧化钾醇溶液,得无色透明澄清液。继续搅拌2h,过滤反应液,滤液于室温下缓慢挥发3天,得无色微晶。洗涤、干燥,收率为91.2%。C12H8N2O4Pb的计算值(%):C 31.93,H 1.79,N 6.21;实测值(%):C 32.56,H 2.48,N 6.35。
2 结果与讨论
2.1 配合物的红外光谱
利用KBr压片法测得配合物的红外光谱如图1所示。

图1 配合物的红外光谱
与配体的红外相比较(图2),配合物在1700 cm-1左右归属于羧酸C=O双键伸缩振动吸收峰的消失表明配合物结构中来自配体上的羧基已经完全去质子化。同时在1602cm-1和1562cm-1处出现的吸收峰可归属于为羧酸根的反对称伸缩振动与对称伸缩,两者之差为40cm1,小于文献报道的200cm1,表明羧基基团以双齿形式与中心金属离子配位[14]。配体吡啶环在1220、990、805、609cm-1等处的红外特征峰分别蓝移至1252、1069、816、617cm-1处,说明配体吡啶环上氮原子参与了配合物的形成,吡啶环的呼吸振动受阻,导致能量升高[15-16]。
2.2 配合物的热重-差热分析
为考察配合物的热稳定性及其受热分解的基本过程,在静态空气,升温速率为10℃/min,温度范围为30~700℃的条件下测试配合物的热重-差热分析,结果如图3所示。
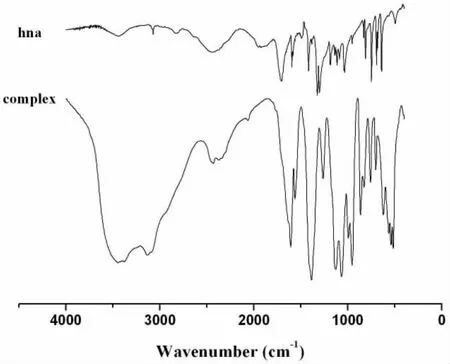
图2 配体和配合物红外光谱对比

图3 配合物的TG-DSC曲线
从图3的热重曲线可以看出,配合物在实验温度范围内具有较好的热稳定性,其受热分解的起始温度为240℃,分解温度区间240~430℃,在该温度区间,配合物的受热分解主要为配体的燃烧分解,失重率为44.82%(理论值为50.56%),此后配合物保持恒重,其恒重形式为PbO。热重分析数据说明配合物的组成与元素分析结果相符,其化学式为[Pb(C6H4NO2)2]。差示扫描量热分析曲线上两个吸热峰表明该配合物的热分解过程总体分为两步进行,第一步分解峰温291℃,第二部分解峰温在404℃[17]。
2.3 配合物的电子光谱
以甲醇溶液为参比溶液,测试了浓度为1×10 -4mol/L的样品甲醇溶液的电子光谱(图4)。配合物在紫外区产生的强吸收谱带位于210nm处,在244nm附近处出现次强吸收,并表现为肩峰。其强吸收谱带属于烟酸吡啶环的π -π*跃迁吸收光谱(λmax=210nm),与配体烟酸的吡啶环π π*跃迁吸收光谱(λmax=220nm)相比,最大吸收峰发生了紫移,说明烟酸与铅发生配位后,造成吡啶环上电荷分布不均匀,对称性降低[18]。出现肩峰可能是金属离子的轨道作用引起π和π*轨道发生分裂所致,也可能是配合物的振荡结构所引起的[19]。

图4 配合物的电子光谱
2.4 配合物的荧光性质研究
室温条件下,我们对固态配合物的荧光性质进行了测定(图5)。

图5 配体及配合物的荧光光谱
由图5可知,配体的特征荧光发射峰分别位于380nm(λexex=250nm)处。自由配体的荧光发射峰可以归属为π-π*跃迁。配合物的最强荧光吸收峰位于563nm(λex=400nm)处。与配体相比,配合物的荧光发射峰位置和激发光都发生了明显的改变,其最大发射峰位置相对于配体而言发生了183nm的红移,显示出绿光,其发射光谱主要仍归属于配体的π- π*跃迁,发生较明显红移的原因可能是配体与铅形成配合物后,配体的共轭程度增强,或者由金属离子干预下的配体间电荷跃迁所造成[20]。
由此可见,配合物是一类潜在的新型绿光发光材料。
3 结论
综合上述对配合物红外光谱、电子光谱、热重及差示扫描量热分析和荧光光谱分析结果,可以得到如下结论:
1)利用吡啶-3-甲酸和硝酸铅为反应物,采用溶液合成法能够得到配合物的微晶。
2)红外光谱分析结果表明:配合物中金属离子与配体上的N,O原子配位,其中配体的羧基基团以双齿形式参与配位。
3)由热重分析曲线得出配合物在通常状态下具有一定的稳定性。当加热至240℃时配合物开始分解,分解温度区间为240~430℃,失重率为44.82%,此后保持恒重,且恒重形式为PbO。由差示扫描量热曲线得出,配合物的热分解为吸热过程,总体分为两个步骤:第一个步骤分解最高温度为291℃,第二步分解最高温度为404℃。
4)荧光光谱分析结果表明:配合物的固体粉末样品在400nm的光的激发下,能发出波长为536nm的绿色荧光,表现出与配体完全不同的发光现象,说明配合物具有良好的荧光性质,可以作为潜在的绿光发光材料。其发光主要来自于配体本身的π-π*跃迁,最大发射峰发生较明显红移的原因可能是配体与铅形成配合物后,配体的共轭程度增强导致的;或者由金属离子干预下的配体间电荷跃迁所造成。
[1]Piovezan C,Silva J M R,Neves A,et al.Design of a Dinuclear Nickel(II)Bioinspired Hydrolase to Bind Covalently to Silica Surfaces:Synthesis,Magnetism,and Reactivity Studies[J].Inorg Chem,2012,51(11):6104-6115.
[2]马凤,赵莲花,陈兆祥,等.三维超分子化合物[Cu2(phen)2(H2O)4]·(SO4)2的水热合成、晶体结构及荧光性质研究[J].淮阴师范学院学报:自然科学版,2011,10(1):39-44.
[3]张冬升.二维层状超分子化合物[Mn(C8H5NO6)(H2O)2]n的合成及晶体结构研究[J].精细与专用化学品,2011,19(2):27-29.
[4]郭玉华,郁有祝,吕垒,等.含吡嗪甲酸配体的双核铬配合物的水热合成、晶体结构及荧光性质[J].无机化学学报,2012,28(4):846-850.
[5]李翠金,郭清兵,尹国强,等.基于吡啶多羧酸和N,N’-桥联混合配体的钴配合物的合成及结构分析[J].无机化学学报,2011,27(12):2501-2506.
[6]戴俊,杨娟,陈曦.苯甲酸与含氮配体构筑的两种铅配合物的水热合成、结构与性质研究[J].无机化学学报,2011,27(8):1617 -1624.
[7]徐军,苏良碧.主族金属离子激光材料 激光材料领域发展的新方向[J].无机材料学报,2011,26(4):347-353.
[8]唐龙,吴亚盘,付峰,等.二维网状Pb(II)的合成、晶体结构及荧光性质[J].无机化学学报,2011,27(12):2501-2506.
[9]李秀颖,徐占林,刘春波,等.新型锰配合物的水热合成与晶体结构[J].吉林师范大学学报:自然科学版,2008,29(4):95-97.
[10]Yaghi O M.T Shaped Molecular Building Units in the Porous Structure of Ag(4,4’-bpy)·NO3[J].J Am Chem Soc,1996,17(4):95-96.
[11]Stabenow F,Saak W,Marsman H,et a1.Hexxaryleyclotripumbane:A Molecule with a Homonuclear Ring System of Lead[J].J Am Chem Soc,2003,123(34):366-36.
[12]Yang B P,Sun Z M,Mao J G.Synthesis,Characterizations and Crystal Structures of Two Lead(II)Diphosphonates:Pb2[NH(CHPO3)2]·2H2O and Pb3[HO2C(CH2)3NH(CH2PO3)2·2H2O][J].Inorg Chem Acta,2004,357:1583-1588.
[13]Yilmaz V T,Hamamc S,Andac O,et al.A Three-Dimensional Lead(II)Polymer with Bridging Saccharinate and Unusually Coordinated Acetate Ligand Synthesis,IR Spectra and Crystal Structure of[Pb(H2O)(u OAc)(usac)][J].Z Anorg Allg Chem,2003,629:172-176.
[14]林雪,景远,刘艳.配合物[Pb(2,2’bipy)(CH3COO)2]的水热合成与晶体结构[J].北华大学学报:自然科学版,2009,10(5):398-400.
[15]梁福沛,陈自卢,胡瑞祥,等.过渡金属 4,4’-联吡啶配合物的合成及晶体结构[J].化学学报,2001,59(3):405-412.
[16]赵永亮,赵凤英.铕镧苯甲酸α,α’联吡啶配合物的合成及性质研究[J].光谱学与光谱分析,2002,22(6):987-989.
[17]陈勇强,王秀丽,刘国成,等.新型的二维铅配位聚合Pb(dpq)(bdic)的合成、晶体结构及荧光性质[J].东北师大学报:自然科学版,2009,41(4):91-94.
[18]王敏,徐志栋,冯殿忠.Eu(III)烟酸、邻菲咯啉三元配合物的合成、光谱性质及荧光性能的研究[J].光谱学与光谱分析,1999,19(3):484-486.
[19]胡军福.Co(III)联吡啶配合物的合成及紫外光谱研究[J].光谱实验室,2006,23(5):1026-1027.
[20]杨娟,缪娟,戴俊,等.对位取代苯甲酸与2,2’-联吡啶配体构筑的两种铅配合物的合成、晶体结构及性质[J].无机化学学报,2010,26(11):1992-2000.

