聚吡咯/二氧化锰复合材料的合成与性能
李 亮,李兰艳,王 牌
(武汉工程大学材料科学与工程学院,湖北 武汉 430074)
0 引 言
超级电容器是一种应用前景很广的新型储能装置.由于超级电容器具有容量大、效率高、充放电能力强、稳定性好、无污染等优点使它的应用非常广泛,比如在汽车、电力、通讯等方面.已经有很多关于金属氧化物、碳素材料和导电聚合物作为电极材料在超级电容器中的应用研究,其中导电聚合物作为超级电容器电极材料是一个研究的热点.
共轭聚合物聚吡咯是一种重要的导电高分子,已被广泛研究了几十年,经掺杂后可形成优良的导电材料.由于聚吡咯有很好的环境稳定性、易于制备和掺杂、无毒害等优点被广泛用作电极材料.然而,聚吡咯也有不足之处,比如难溶解、难熔融、力学性能差等.因此,聚吡咯常与金属或金属氧化物进行复合以改善其机械、电化学性能,这使得聚吡咯复合材料成为研究的热点.聚吡咯及其复合材料的合成方法及机理在国内外已有很多研究.比如钱人元[1]等人提出的聚吡咯的质子酸掺杂机理,成功解释了以质子酸或者部分非氧化性路易斯酸为掺杂剂的掺杂反应的过程.目前,聚吡咯及其复合材料在二次电池、电容器、化学传感器、生物电极、导电材料等领域的研究也层出不穷.但是由于聚吡咯的电导率低、生产成本高、寿命短等缺点使得聚吡咯及其复合材料的应用在有些方面还没有达到实际生产的要求,这也是国内外科研工作者的研究重点.
二氧化锰由于成本低、比表面积大、可逆性高、电化学性能稳定、环境友好等优点引起了科研工作者的兴趣[2].二氧化锰优越的电化学性能使它可用作充电电池的电极材料.二氧化锰在电池以及超级电容器电极材料等领域已展现出极其优越的性能和潜在的商业价值[3].
为了结合聚吡咯和二氧化锰的优点,得到更好的超级电容器电极材料,我们首次采用甲基橙作为模板运用一步法把聚吡咯和二氧化锰进行复合,得到聚吡咯/二氧化锰复合材料.经过测试,我们发现得到的聚吡咯/二氧化锰复合材料既有很高的比电容又有很好的循环性,相对于聚吡咯来说性能有了巨大的提高.这样既降低了成本又提高了其稳定性以及电化学性能,因而,在超级电容器电极材料上会有更广泛应用.如果应用于生产中我们将得到电容高、寿命长的电极材料.
1 实验部分
30mL浓度为5mmol/L的甲基橙(MO)溶液调节至pH=1,加入70μL减压蒸馏过的吡咯(Py)单体,得到Py-MO溶液.0.27g KMnO4溶于10mL水中,把KMnO4水溶液缓慢滴加到Py-MO溶液中,在室温下磁力搅拌24h.用蒸馏水洗涤至滤液无色,然后真空干燥即得到PPy/MnO2复合物.
红外光谱(FT-IR)测试采用TJ270红外光谱仪;扫描电子显微镜(SEM)测试 、能量色散X射线光谱(EDX)测试采用JSM-5510LV型扫描电子显微镜;X射线衍射(XRD)测试采用Bruker D8X射线粉末衍射仪.
以铂丝电极作为对电极,Ag/AgCl电极作为参比电极,与PPy/MnO2复合材料修饰的电极作为工作电极组成三电极体系,NaSO4溶液构成电解池.采用CHI-660D型电化学工作站(上海辰华仪器有限公司)进行循环伏安法及计时电位法测试.
2 结果与讨论
2.1 聚吡咯与聚吡咯/二氧化锰的FT-IR表征
PPy及PPy/MnO2复合材料的红外表征如图1所示.PPy及PPy/MnO2复合材料的特征峰如下:在3400~3420cm-1处的特征峰来源于NH和O-H键的伸缩振动,1560~1630cm-1处的特征峰来源于吡咯环中C=C键的平面伸缩振动,1380~1400cm-1处的特征峰来源于吡咯环中C-N或C-H键的变形振动,1180~1190 cm-1处的特征峰来源于吡咯环的伸缩振动,1010~1040cm-1处的特征峰来源于C-H和N-H键的平面振动,917~947cm-1处的特征峰来源于吡咯环中面外C-H键的变形振动[4].由此可知,是否复合MnO2对PPy的结构基本没影响.

图1 (a)PPy及(b)PPy/MnO2 复合材料的红外表征图谱Fig.1 FT-IR spectra of(a)PPy and(b)PPy/MnO2composite
2.2 聚吡咯与聚吡咯/二氧化锰的XRD表征
PPy及PPy/MnO2复合材料的X射线衍射图谱如图2所示.PPy在2θ=26°处有一个较宽的峰,这是PPy的特征衍射峰;PPy/MnO2复合物的特征衍射峰在2θ=25°,37°和66°处.2θ=25°处可以看到PPy的特征衍射峰,2θ=37°和66°处的峰非常明显,是MnO2的衍射峰,由于PPy分子链很弱的堆积排列,从而使PPy的特征衍射峰强度明显低于 MnO2的衍射峰[5].由此可以看出我们由一步法制得了PPy/MnO2复合材料.

图2 (a)PPy及(b)PPy/MnO2 复合材料的X射线衍射图谱Fig.2 XRD pattern of(a)PPy and (b)PPy/MnO2composite
2.3 聚吡咯与聚吡咯/二氧化锰复合物的SEM、EDX表征
PPy及PPy/MnO2复合材料的SEM图如图3所示,由图可知PPy颗粒的直径约为500~800 nm,PPy/MnO2复合材料颗粒的直径约为100 nm.由此可知,掺杂 MnO2使得PPy/MnO2复合材料颗粒粒径与PPy相比减小了很多倍.
PPy/MnO2复合材料的成分分析如表1所示,由表可知PPy/MnO2复合材料含有C,O,Mn元素[6],由此可知O和 Mn元素被掺杂到了聚吡咯中.

表1 PPy/MnO2复合物的成分分析表Table 1 Component analysis of PPy/MnO2composite

图3 (a)PPy及(b)PPy/MnO2 复合材料的扫描电镜图Fig.3 SEM images of(a)PPy and(b)PPy/MnO2composite
2.4 电化学表征
2.4.1 循环伏安法 图4为PPy及PPy/MnO2复合材料在扫描速率分别为1,2,5,10mV/s时,在1mol/L Na2SO4溶液作电解液的循环伏安图.由图可知,扫描速率越小循环伏安图越接近于矩形.根据公式(1)如下:

其中CS是电容,∫idV是循环伏安曲线的面积,m是工作电极上产品的质量,ΔV是电压范围,S是扫面速率[7].由此可知扫描速率越小电容越大.比较(a)(b)可知相同扫描速率下 PPy/MnO2复合物的循环伏安曲线的面积比PPy大几倍,因而相同条件下PPy/MnO2复合物的电容比PPy大很多.这表明PPy/MnO2复合材料比PPy电容性更好.

图4 (a)PPy及(b)PPy/MnO2 复合材料在扫描速率为1,2,5,10mV/s下的循环伏安图Fig.4 Cyclic voltammograms of(a)PPy and(b)PPy/MnO2composite electrode at the scan rates of 1,2,5and 10mV/s,respectively
2.4.2 计时电位法 图5为PPy及PPy/MnO2复合材料在电流密度分别为0.2,0.5,1,2,5,10和20A/g,在1mol/L Na2SO4电解液中的计时电位图.由图可知在电流密度为1,2,5,10和20A/g时计时电位曲线比较对称,这就说明PPy及PPy/MnO2复合材料在此条件下表现了很好的电容特性.但是在电流密度为0.2和0.5A/g时充电和放电曲线不对称,这是内阻的原因.当电流密度大于1A/g时,内阻相对来说比较小,对计时电位曲线没多大影响,但是当电流密度小于1A/g时,内阻相对来说比较大,对计时电位曲线的影响就比较大.根据公式(2)如下:

其中C表示电容,i表示放电电流,m表示工作电极上产品的质量,Δt表示放电时间,ΔV 表示放电电压.比较(a)(c),(b)(d),根据公式(2)计算可以得出PPy及PPy/MnO2复合材料在不同电流密度下的电容.电流密度为1A/g时PPy的电容为23F/g,但是PPy/MnO2复合材料的电容与PPy相比有很大的增加,达到559F/g.在电流密度相同的情况下,PPy/MnO2复合材料的电容比PPy大几十倍.这说明PPy/MnO2复合材料比PPy电化学性能好很多.
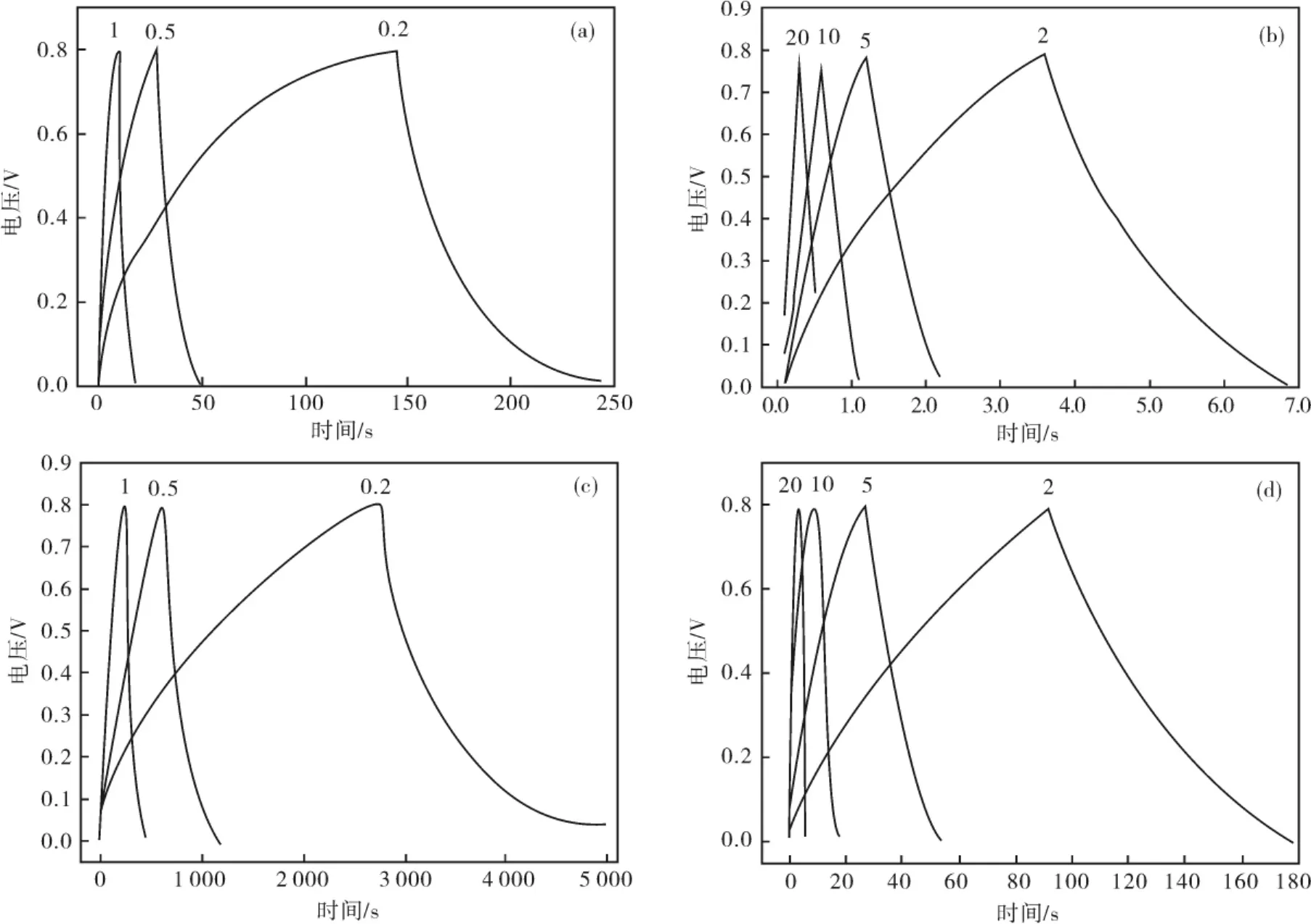
图5 (a)(b)PPy及(c)(d)PPy/MnO2 复合材料在电流密度分别为0.2,0.5,1,2,5,10,20A/g的计时电位图Fig.5 Constant current charge/discharge curves of(a)(b)PPy and(c)(d)PPy/MnO2composite electrode at different current density:0.2,0.5,1,2,5,10,20A/g
图6显示了在电流密度为5A/g,电压范围为0~1.0V条件下用计时电位法得到的PPy及PPy/MnO2复合材料扫描1000圈的圈数-电容的保持率比较图.由图可以看出PPy的保持率在前100圈急速下降,之后达到稳定,大概在45.66%,也就表明在1000圈之后PPy的电容大概损失了一半.PPy/MnO2复合材料的曲线比较平稳,在扫描1000圈之后电容保持率仍为98.64%.由此可以得出PPy/MnO2复合材料比PPy的电容保持率好很多,因而有更好的电化学性和循环性.所以PPy/MnO2复合材料比PPy更适合作电极材料.

图6 PPy及PPy/MnO2复合材料的循环圈数-电容保持率曲线比较图Fig.6 Comparison of cycle number and retention rate of capacitance between PPy and PPy/MnO2composite
3 结 语
我们采用一步法合成PPy/MnO2复合材料,经过各种表征测试证实PPy/MnO2复合材料与PPy相比,具有良好的电化学性和循环性.这种复合材料有望在超级电容器电极材料领域展开应用.
[1]Qian R Y,Pei Q B,Huang Z T.The role of H+ions in the electrochemical polymerization of pyrrole in aqueous media [J].Makeromol Chem,1991,192:1263.
[2]程富民.二氧化锰-聚合物复合材料的循环伏安法制备及性能研究[D].石家庄:河北师范大学,2010.
[3]张熊.二氧化锰及其纳米复合材料的可控制备与性能研究[D].北京:北京化工大学,2008.
[4]朱寒冰,黄瑜,李亮.甲基橙掺杂聚吡咯纳米管的合成及其性能[J].武汉工程大学学报,2011,33(7):17-21.
[5]Lakshinandan Goswami,Neelotpal Sen Sarma,Devasish Chowdhury.Bias-Induced Enhancement of Conductivity in Polypyrrole[J].The Journal of Physical Chemistry,2012,116:6446-6452.
[6]Junyu Lei,Xiaofeng Lu,Wei Wang,et al,Fabrication of MnO2/graphene oxide composite nanosheets and their application in hydrazine detection[J].The Royal Society of Chemistry,2012,2:2541-2544.
[7]Jianfeng Zang,Xiaodong Li.In situ synthesis of ultrafine β-MnO2/polypyrrole nanorod composites for high-performance supercapacitors[J].Journal of Materials Chemistry,2011,21,10965-10969.

