尤瑞克林治疗急性脑梗死的有效性和安全性的Meta分析
李俊山 田 野
1.解放军第三〇九医院药剂科,北京 100091;2.解放军总后勤部管理保障局第一门诊部,北京 100842
脑梗死又称缺血性卒中,其发病机制为局部脑组织血液供应障碍导致脑组织缺血缺氧性病变坏死,进而产生临床上对应的神经功能缺失表现,约占所有脑卒中的80%。脑梗死发病起病急,迅速出现局灶性神经功能缺失症状并持续24 h以上,症状可在数小时或数日内逐渐加重,致残率及高致死率均很高。
尤瑞克林又名人尿激肽原酶,是一种从人尿中提取的一种由238个氨基酸组成的丝氨酸蛋白酶,为国家一类新药,以急性脑梗为适应证。临床前药效学研究显示该药能增加脑血流量、提高红细胞变形能力;动物实验显示该药能缩小梗死面积、减轻脑梗后行为障碍。1999年12月经原国家药品监督管理局批准进入临床研究阶段,2000年4月至2004年12月在浙江大学医学院第二附属医院国家药品临床研究基地完成Ⅰ、Ⅱ、Ⅲ期临床研究[1]。2005年10月经国家食品药品监督管理局批准上市后广泛用于临床,本文采用循证医学的方法系统评价尤瑞克林对急性脑梗死的治疗作用。
1 资料与方法
1.1 文献检索
计算机检索Cochrane Library、PubMed、SCI、EMbase、中国生物医学文献数据库、中国期刊全文数据库、中文科技期刊数据库、中华医学会数字化期刊等数据库,检索时间为1990年至今。收集国内外发表的随机对照试验(Randomized Controlled Trials,RCTs),半随机对照试验(Quasi-randomized Controlled Trials,q-RCTs),无论是否隐藏或采用盲法。随机方法可采用随机数字表、计算机随机、抽签法或抛硬币法等。半随机方法可按患者身份证号码的尾数,或就诊日期,或病历顺号尾数的奇偶数等方式来分组。英文数据库检索词为“Human urinary kallidinogenase”and “brain infarction”or“cerebral embolism”。 中文数据库的检索词为“人尿激肽原酶”或“尤瑞克林”和“脑梗死”或“脑栓塞”。
1.2 文献筛选
根据检索结果,由两人独立进行文献筛选,如有争议通过协商解决,必要时参考第三者的意见。纳入标准:①尤瑞克林治疗急性脑梗的临床随机对照研究(RCT)病例,分为治疗组和对照组(n≥20),治疗组除应用尤瑞克林外其余常规治疗与对照组相同,两组患者年龄、性别、用药前神经功能缺损评分、梗死部位、伴发疾病等经统计学处理差异均无显著性。②发病在48 h内的急性脑梗死患者,诊断符合全国第四届脑血管病学术会议制定的脑梗塞疾病诊断要点并经头颅CT和/或MRI证实。③观察指标采用美国国立卫生研究院卒中量表(NIHSS)评分、全国脑血管病学术会议制定的脑梗死疗效评定标准或其他神经功能缺损评分。临床疗效采用以下标准评定:①基本痊愈,神经功能缺损评分减少90%~100%,病残程度0级;②显著进步,神经功能缺损评分减少46%~89%,病残程度1~3级;③进步,神经功能缺损评分减少18%~45%;④无变化,神经功能缺损评分减少或增加18%以内;⑤恶化,功能缺损评分增加18%以上;⑥死亡。以基本治愈+显著进步+进步计算有效率;基本治愈+显著进步计算显效率。
排除标准:①未注明诊断标准及疗效评价标准;②未采用随机对照试验设计;③入选标准未排除以下情况者:合并脑出血或全身有活动性出血或出血倾向;有严重心、肝、肾功能不全,意识障碍;已知服用或将必须使用血管紧张素转化酶抑制剂(ACEI)类药物患者;治疗前神经功能缺损情况已明显改善者;既往有脑血管疾病并遗留严重神经功能障碍而影响观察者。

表1 纳入Meta分析文献的基本信息
质量评价方法:临床试验的质量评价标准使用改良的Jadad评分。①随机序列的产生1为恰当:计算机产生的随机数字或类似方法(2分);2为不清楚:随机试验但未描述随机分配的方法(1分);3为不恰当:采用交替分配的方法如单双号(0分)。②随机化隐藏1为恰当:中心或药房控制分配方案、或用序列编号一致的容器、现场计算机控制、密封不透光的信封或其他使临床医生和受试者无法预知分配序列的方法(2分);2为不清楚:只表明使用随机数字表或其他随机分配方案(1分);3为不恰当:交替分配、病例号、星期日数、开放式随机号码表、系列编码信封以及任何不能防止分组的可预测性的措施(0分);4未使用(0分)。③盲法1为恰当:采用了完全一致的安慰剂片或类似方法(2分);2为不清楚:试验陈述为盲法,但未描述方法(1分);3为不恰当:未采用双盲或盲的方法不恰当,如片剂和注射剂比较(0分)。④撤出与退出1:描述了撤出或退出的数目和理由(1分);2:未描述撤出或退出的数目或理由(0分)。修改后Jadad量表共7分,1~3分视为低质量,4~7分视为高质量。

1.3 数据分析及结果判定
本研究采用Review Manager(RevMan)4.2软件进行系统评价,该软件是由国际Cochrane协作网制作并于2003年推出的专用Meta分析软件。分别将有效率和显效率分两次输入RevMan 4.2分析系统,首先进行异质性检验(齐性检验),如果研究间变异很小,即作异质性检验时研究间差异无统计学意义,可采用固定效应模型;如果研究间变异较大,且有统计学意义,则应采用随机效应模型,最后合并统计量并图示单个试验和合并后的优势比(OR值)、权重及95%的置信区间,绘制森林图及倒漏斗图。
森林图中垂直线(OR=1)将图分为左右两半,用于判断结果差异有无统计学意义:横线/菱形与垂直线相交则表明该RCT中不同治疗措施之间差异无统计学意义。对于不利结局如死亡、残废事件等,横线/菱形完全在垂直线左侧表示治疗组更有效,完全在右侧表示对照组更有效,对于有利结局如本研究则刚好相反。每一横线代表一个试验结果的置信区间(confidence interval,CI),横线中央的蓝点是点估计值,置信区间是真值可能存在的范围,反映结果的准确性,横线越长,说明样本量越小,结果欠准确可靠;横线越短,说明样本量越大,准确性越高,结果越可信。最下方的菱形代表多个RCT的综合结果。“Weight”表示各个试验的权重,本研究为计数资料,使用样本量作为权重的衡量依据,样本量越大,权重越大。

倒漏斗图用于反应文献潜在的发表偏倚。在没有偏倚的情况下,图形形状类似于一个倒置的漏斗。如果存在偏倚,就会出现图形不对称或缺角。
2 结果
2.1 纳入研究基本特征
根据以上标准筛选的文献隐去杂志名称及题名并按第一作者编上号码,共纳入29篇文章,其中高质量2篇,低质量27篇,全部为中文文献。入选病例2926例,其中治疗组1591例,对照组1335例。见表1。
2.2 尤瑞克林对急性脑梗治疗总有效率的影响
纳入的29个文献全部报道了总治疗有效率,有效率=(基本治愈+显著进步+进步)/入组所有患者。提取数据,进行同质性检验,结果实验组比对照组无异质性(P=0.66,I2=0%),采用采用固定效应模型进行Meta分析。结果显示:实验组和对照组治疗总有效率分别为89.50%和74.23%,两组差异有统计学意义[OR=3.06,95%CI(2.45,3.81),P <0.01]。见图1。对纳入该Meta分析的研究做倒漏斗图,左下角有缺角现象,提示可能存在发表偏倚。见图2。
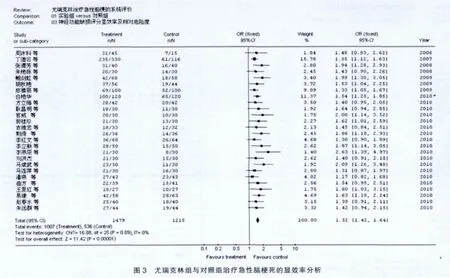
2.3 尤瑞克林对急性脑梗死治疗显效率的影响
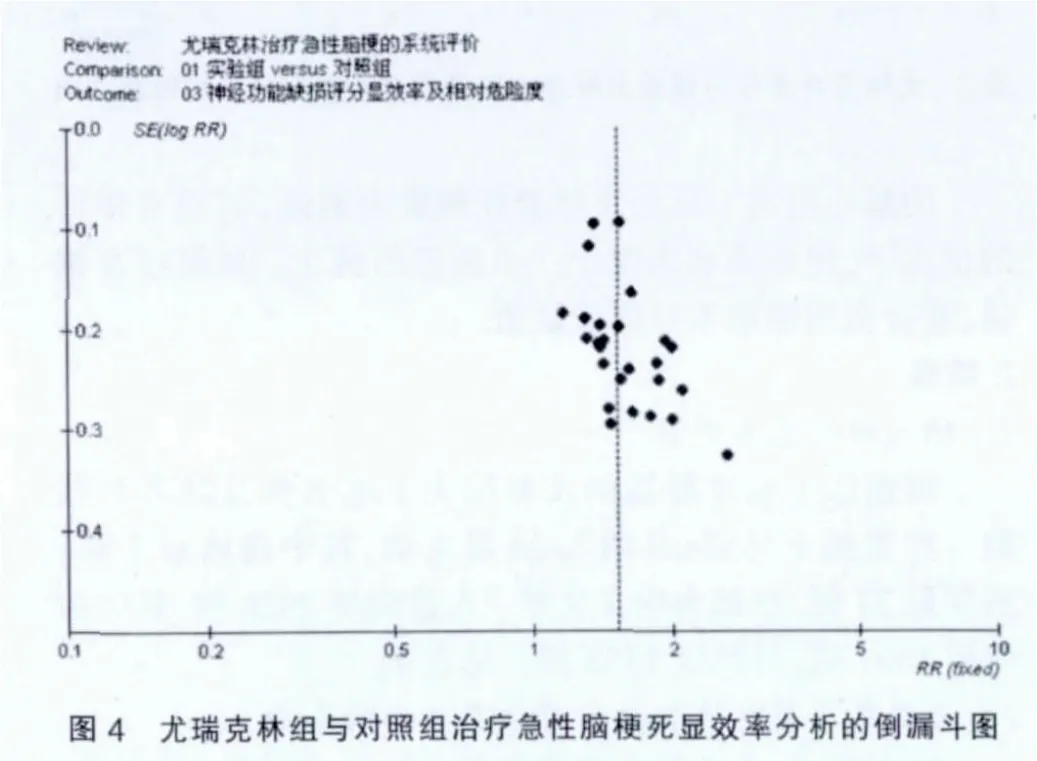
26个研究报道了治疗显效率,显效率=(基本治愈+显著进步)/该组所有患者。提取数据,尤瑞克林组1479例,对照组1215例。同质性检验结果显示两组无异质性(P=0.89,I2=0%),采用采用固定效应模型进行Meta分析。分析结果显示:实验组和对照组治疗显效率分别为68.09%和44.12%,合并统计量后尤瑞克林组比对照组有更高的显效率,差异有统计学意义[OR=1.52,95%CI(1.42,1.64),P <0.01]见图3。同上,对纳入的研究做倒漏斗图,见图4。
2.4 不良反应
本研究观察的患者共2916例,其中治疗组1591例患者,观察到的不良反应共113例次,对照组1335例患者中不良反应共19例次。不良反应类型以轻度血压下降最为常见,占所有不良反应的36%;其次为面部潮红、球结膜充血以和恶心、呕吐伴心悸,分别占所有不良反应的23%和20%,大多数减慢低速后可耐受,无需停药;小部分患者出现头痛、头昏症状;治疗组观察到谷丙转氨酶(ALT)一过性轻度升高1例,心衰1例;治疗组和对照组均观察到注射部位红痒1例。见表2。
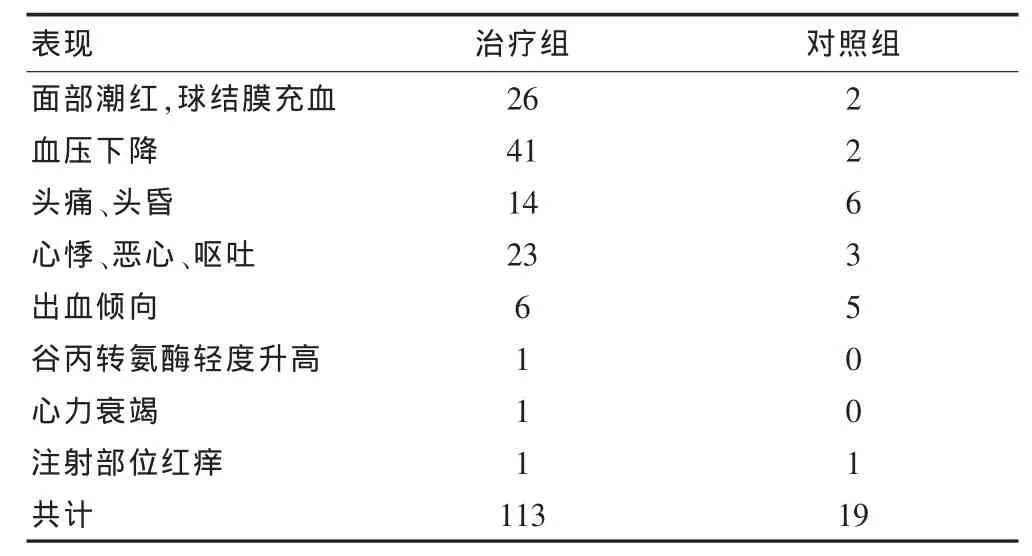
表2 纳入研究的实验组与对照组不良反应发生情况(例)
3 讨论
急性脑梗死病灶分为中心坏死区和周围的缺血半暗带[31-32]。中心坏死区因严重而完全的缺血导致脑组织坏死;而缺血半暗带内仍有部分侧支循环存在,尚有可存活的脑细胞,抢救缺血半暗带的可逆性损伤神经元是治疗急性脑梗死的关键。尤瑞克林治疗急性脑梗死的主要机制可能为选择性扩张缺血半暗带的微动脉,改善局部血液循环,缩小梗死面积并加快神经功能缺损的恢复[33]。尤瑞克林即人尿激肽原酶主要通过激肽系统发挥其药理作用,它作用于激肽原形成胰激肽,胰激肽及其降解产物与激肽系统β1受体结合激活一氧化氮-GMP和前列腺环素-GMP等信号通路,从而发挥多种生理作用,如调节血管舒缩、调整血压,改善脑组织供血、供氧、能量代谢等。而β1受体仅在受损组织主要是缺血性损伤组织中表达,这就形成了尤瑞克林作用的靶向性[34]。另一方面,尤瑞克林能显著抑制急性梗死区的炎性反应,降低NADPH氧化酶的活性及超氧化物的产生,减轻缺血再灌注损伤,降低神经细胞凋亡,从而改善急性期神经功能缺损症状[35]。此外,尤瑞克林还能诱导的血管新生和神经再生[36-39],可能对急性脑梗死患者远期预后有一定的帮助。
Meta分析结果显示实验组在治疗总有效率和显效率上较对照组明显提高。两次检验的倒漏斗图(图2、4)均显示缺角,提示存在发表偏倚,发表偏倚的最主要原因是阴性结果的文章发表困难。此外方法学质量低下、治疗组和对照组基线资料的差异等因素也会导致倒漏斗图的不对称分布。本文纳入的29篇随机对照研究来自不同层次医疗机构,对急性脑梗的基础治疗差异较大,各研究对照组的治疗有效率和显效率差异大,且大多数研究患者入院时未按病情程度进行分层分组,这可能是导致各研究异质性及发表偏倚的主要原因。未搜到国外关于尤瑞克林的临床随机对照研究。而国内研究大多缺乏设计严谨性,主要表现在未进行随机化隐藏,未采用盲法及安慰剂对照。尽管该Meta分析及几乎所有纳入的研究均显示尤瑞克林组治疗有效率及显效率高于对照组,但仍有必要开展相关的大样本、高质量随机对照研究。
通过对所纳入研究所观察的所有不良反应进行分类汇总,可见尤瑞克林最常见的不良反应为轻度血压降低,这可能与该药和某些降压药物存在协同作用有关。中山大学药学院对尤瑞克林与降压药物相互作用进行研究,发现尤瑞克林与ACEI类降压药存在协同效应,而与其他降压药相互作用不明显。有研究观察了合并有高血压的急性脑梗患者静脉滴注尤瑞克林期间血压变化情况,结果显示患者血压在正常范围内波动平稳,与治疗前相比差异无统计学意义。两组中均有部分患者出现头晕、头痛、心悸、恶心呕吐等不适,这些症状与脑梗后的颅压增高症状难以区分。出血倾向与各研究机构的脑梗常规治疗方案相关。此外,治疗组观察到一过性肝转氨酶升高及急性心衰各1例,尚不能确定是否与药物相关。因此,尤瑞克林常见的不良反应可能主要为面部潮红、球结膜充血及消化道症状,但多数较轻微,可耐受。
综上,现有的证据表明尤瑞克林对急性脑梗死的治疗有效且较安全。然而,受纳入研究数量和质量所限,上述结论仍需更多大样本、多中心、前瞻性的随机对照研究加以验证。
[1]丁德云.新药临床研究之路[J].中国处方药,2005,44(11):64-66.
[2]丁德云,吕传真,丁关萍,等.忍尿激肽原酶治疗急性脑梗死多中心随机双盲安慰剂对照试验[J].中华神经科杂志,2007,40(5):306-310.
[3]周沐科,何俐,孔双艳.人尿激肽原酶治疗急性脑梗死的随机双盲对照试验[J].华西药学杂志,2006,21(4):356-358.
[4]朱艳栋,李波,袁学良,等.尤瑞克林治疗急性脑梗死临床疗效的随机对照研究[J].山东医药,2008,48(31):16-17.
[5]潘燕,张保朝.尤瑞克林对急性脑梗死炎性反应物及血管内皮的影响[J].中华脑血管病杂志,2010,4(3):172-176.
[6]刘洪杰.尤瑞克林联合奥扎格雷钠治疗急性脑梗死的疗效与安全性观察[J].药物与临床,2010,48(26):40-42.
[7]荆靳,绮彪.尤瑞克林联合降纤酶治疗进展性卒中疗效观察[J].山东医药,2010,50(37):92-93.
[8]易建,姚汉金,刘明瑜,等.尤瑞克林联合依达拉奉治疗急性脑梗死疗效及血清hs2CRP和VEGF水平变化[J].微循环学杂志,2010,20(3):48-49,52.
[9]朱远群,谭双全,阮海林.尤瑞克林联合依达拉奉治疗进展性脑梗死 44 例临床研究[J].蛇志,2010,22(2):116-117,149.
[10]官威,李金英.尤瑞克林联合依达拉奉治疗进展性脑梗死疗效观察[J].吉林医学,2010,31(20):3217.
[11]曲方,陈新,陈会生,等.尤瑞克林与奥扎格雷钠联合应用治疗急性脑梗死的疗效分析[J].沈阳部队医药,2010,23(1):12-14.
[12]胡秋艳.尤瑞克林与丹奥合用治疗急性脑梗死的临床疗效观察[J].药物与临床,2009,47(30):41-43.
[13]鲍剑虹,郑荣远,夏君慧,等.尤瑞克林在急性脑梗死治疗中的应用[J].中国神经精神疾病杂志,2009,35(4):231-233.
[14]李燕辰,于欣.尤瑞克林治疗30例急性脑梗死的疗效观察[J].宁夏医科大学学报,2010,32(7):825-826.
[15]耿昌明,朱雪红,韦道明.尤瑞克林治疗急性大脑中动脉脑梗死的疗效观察[J].临床军医杂志,2010,38(4):584-586.
[16]吉维忠,范丽君,郝文莉,等.尤瑞克林治疗急性后循环脑梗死 33例疗效观察[J].中国实用医药,2010,5(7):135-136.
[17]马连萍,苗成,刘惠萍.尤瑞克林治疗急性脑干梗死30例疗效观察[J].山东医药,2010,50(13):88-89.
[18]廖雅丽,陈伟,王丽玲.尤瑞克林治疗急性脑梗死100例疗效分析[J].吉林医学,2009,30(16):1736.
[19]李红文,李新,张伟.尤瑞克林治疗急性脑梗死的疗效观察[J].中国医药指南,2010,8(8):90-92.
[20]马斌武,陈建红,候晓林,等.尤瑞克林治疗急性脑梗死的临床观察[J].宁夏医学杂志,2010,32(11):1001-1002.
[21]白艳华.尤瑞克林治疗急性脑梗死疗效观察[J].现代中西医结合杂志,2010,19(16):2003.
[22]张渭芳,赵康仁,靳彪,等.尤瑞克林治疗急性脑梗死疗效及安全性观察[J].山东医药,2008,48(42):46-47.
[23]赵春水,何蕴,马丽丽,等.尤瑞克林治疗急性脑梗死临床观察[J].山东医药,2010,50(25):80-81.
[24]靳晓华,贾丽丽,王轩,等.尤瑞克林治疗急性脑梗死临床研究[J].临床医药实践,2010,19(9B):1241-1242.
[25]王夏红,何文龙,赵建民.尤瑞克林治疗进展性脑梗死的疗效观察.中华脑血管病杂志,2010,4(5):367-370.
[26]方立梅,黄昌凯.尤瑞克林治疗老年急性脑梗死的临床研究[J].中国老年学杂志,2010,30(10):1428-1429.
[27]段艳培,张其相,李爱琴.尤瑞克林注射液治疗急性脑梗死44例疗效分析[J].医学理论与实践,2010,23(8):939-941.
[28]张莉峰.尤瑞克林注射液治疗急性脑梗死的临床分析[J].中国实用神经疾病杂志,2010,13(19):34-35.
[29]郭桂珍.注射用尤瑞克林治疗急性脑梗死的疗效观察[J].医学信息,2010,23(8):2636-2637
[30]李立新,程桂林,刘丽娇,等.注射用尤瑞克林治疗老年急性脑梗死的临床研究[J].中国实用医药,2010,5(19):163-164.
[31]刘敏.早期康复治疗对急性脑梗死患者肢体功能及生活质量的影响[J].中国现代医生,2013,51(9):127-128.
[32]凌小林.脑梗死并发肺部感染的研究进展[J].中国现代医生,2013,51(7):25-27.
[33]Xia CF,Yin H,Yao YY,et al.Kallikrein protects against ischemic stroke by inhibiting apoptosis and inflammation and promoting angiogenesisandneurogenesis[J].HumGeneTher,2006,17(2):206-219.
[34]Ling L,Hou Q,Xing S,et al.Exogenous kallikrein enhances neurogenesis and angiogenesis in the subventricular zone and the peri-in-farction region and imp roves neurological function after focal cortical infarction in hypertensive rats[J].Brain Res,2008,1206:89-97.
[35]Nagano H,Suzuki T,Nagano H,et al.Pharmacological studies on human urinary kallidinogenase(SK-827): cerebral protective effects[J].Yakugaku Zasshi,1993,113(11):803-809.
[36]Campbell DJ.The kallikrein—kinin system in humans[J].Clin Exp Pharmacol Physiol,200l,28(12):l060-1065.
[37]刘洪杰.尤瑞克林联合奥扎格雷钠治疗急性脑梗死的疗效与安全性观察[J].中国现代医生,2010,(26):40-42.
[38]马明娟,王素娟,邢付强.尤瑞克林联合氯吡格雷治疗进展性脑梗死的疗效观察[J].中国现代医生,2011,49(20):87-88.
[39]陈汉杰,吴学良.尤瑞克林联合降纤酶治疗急性进展型脑梗死的疗效观察[J].中国现代医生,2012,50(16):88-89.

