Salen Co(Ⅱ)配合物催化氧化百里酚制备百里醌的研究
张婉莹,石晓红,于微微,孙志忠
(1.黑龙江大学 化学化工与材料学院,哈尔滨 150080;2.黑龙江省普通高等学校高效转化的化工过程与技术重点实验室,哈尔滨 150080)
0 引言
百里醌(thymoquinone)是中东国家的黑种草籽油中分离产物之一,其化学名称是2-异丙基-5-甲基-1,4-苯并醌。近年来研究发现百里醌具有潜在的防癌和抑癌效应,可抑制多种恶性肿瘤细胞生长和转移[1-2],并诱导细胞凋亡。合成百里醌的传统工艺是以百里酚为起始原料通过硝化、催化氢化、重氮化等多步反应[3],该合成方法路线比较长,多步反应总收率较低,污染较大。近年来采用不同氧化剂和催化剂对百里酚直接进行催化氧化合成百里醌引起了人们广泛关注。常用的氧化剂有分子氧、过氧化氢和二氧化铅等[4-6],常见的催化剂包括钴(Ⅱ)盐、甲基三氧化铼、锰(Ⅲ)/卟啉配合物和金属取代Keggin型杂多酸等[7-13]。Salen Co(Ⅱ)配合物具有结合氧的能力强、结构稳定、合成简便等优点,广泛用于催化氧化反应[14]和不对称手性合成[15]。双乙二胺水杨醛席夫碱合钴是比较易于制备的Salen Co(Ⅱ)配合物,本文选择以该配合物为催化剂,氧气为氧化剂,百里酚为原料在DMF溶液中30℃催化氧化反应制备百里醌。
1 实验部分
1.1 Salen Co(Ⅱ)配合物的合成
按照文献[16]方法通过乙二胺与水杨醛在甲醇中的缩合反应制备席夫碱Salen(N,N′-双(水杨醛乙二胺)),再与(CH3COO)2Co·4H2O 反应制备Salen Co(II)配合物。其分子式为:C16H14O2N2Co,分子量为:325.25g/mol,结构式如下:

1.2 百里醌的合成
向带有温度计、搅拌磁子的100mL 圆底烧瓶中加入3.00g(0.02 mol)百里酚,0.65g(2.0 mmol)Salen Co(Ⅱ)催化剂和30mL N,N-二甲基甲酰胺(DMF),在氧气气氛中置于30℃水浴锅中搅拌,密闭体系进行反应,采用GC 监测反应,反应完毕,加入60 mL 乙醚,用0.1 mol/L盐酸溶液60 mL 萃取混合物,分离有机层,再依次用60mL水、120mL饱和氯化钠溶液洗涤。分液后得到有机层,用无水Na2SO4干燥,过滤,脱溶剂,得到3.25g 亮黄色产品,收率为99.1%,熔点42~46℃[文献[3]43~45℃]。
反应方程式如下:

2 结果与讨论
2.1 催化剂的表征
对Salen Co(II)配合物进行红外表征见图1。
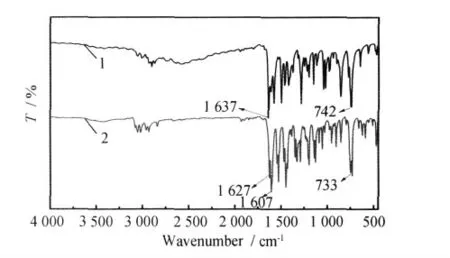
图1 催化剂的红外谱图Fig.1 IR spectra of catalysts
图1中,配体1的特征吸收峰1 637cm-1是C=N 双键的特征吸收峰,相比配体1,配合物2的C=N特征吸收峰是在1 627cm-1,红移10cm-1,可以证明席夫碱与金属发生了配位。
对Salen Co(II)配合物进行元素分析见表1。

表1 催化剂的元素分析Table 1 Elemental analysis of catalysts
由表1 可见,催化剂中各元素的实际含量与Salen Co(II)配合物中各元素的理论含量基本一致,因此可以确定这个化合物是理想的Salen Co(II)配合物。
2.2 催化氧化最佳条件的确定
2.2.1 催化剂的选择
以0.02 mol百里酚为原料,氧气为氧化剂,反应温度30℃,DMF 为溶剂,反应时间9h,分别以2.00 mmol(CH3COO)2Co·4H2O、2.00 mmol(CH3COO)2Co·4H2O 与2.00mmol Salen的混合物、2.00 mmol Salen Co(Ⅱ)为催化剂,考察了催化剂对反应的影响,结果见表2。

表2 催化剂对反应的影响Table 2 Effect of catalysts to reaction
由表2可见,在30℃,催化体系中单独使用醋酸钴或者将其与双水杨醛乙二胺席夫碱等摩尔混合,对百里酚的氧化反应均无法顺利进行,只有Salen Co(Ⅱ)的存在下,反应才顺利进行,并且表现出非常好的选择性。
2.2.2 催化剂量对反应的影响
以0.02mol百里酚为原料,在30℃条件下,DMF为溶剂,氧气为氧化剂,反应9h,考察了催化剂Salen Co(Ⅱ)的用量对反应的影响,分别加入0.60、1.20、1.40、1.60、1.80、2.00、2.20、2.40、2.60、2.80、3.60mmol的Salen Co(II)进行反应,以确定最佳的催化剂用量结果见图2。
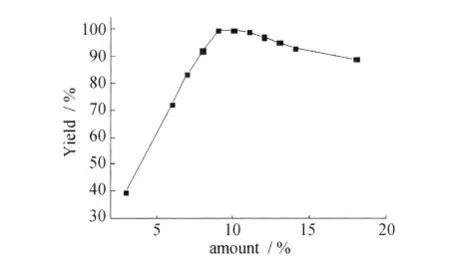
图2 催化剂用量对反应的影响Fig.2 Effect of the different amount of catalyst to reaction
由图2可见,随着催化剂用量的增加,转化率明显升高,当催化剂用量达到反应底物摩尔数10% 时,反应收率最高,产量为3.25g,收率达到99.1%。当继续增加催化剂用量,反应的收率反而下降。因此,该催化氧化反应的最佳催化剂用量为10% 。
2.2.3 溶剂对反应的影响
以0.02 mol百里酚为原料,在氧气存在下,30℃,使用10%的Salen Co(Ⅱ)为催化剂,反应9h,分别考察了乙酸、乙酸乙酯、丙酮、环己烷、甲苯、乙腈、二氯甲烷、氯仿和N,N-二甲基甲酰胺等溶剂对反应的影响,结果见表3。

表3 溶剂对反应的影响Table 3 Effect of the different solvents to reaction
由表3可见,反应在多数溶剂中都可进行,但在乙酸、乙酸乙酯、丙酮等溶剂中,反应的效果都不好,尤其是乙酸几乎不发生反应,其可能原因是有羰基的存在。环己烷、甲苯、二氯甲烷、氯仿、乙腈和N,N-二甲基甲酰胺的极性逐渐增大,实验结果与溶剂极性顺序大致相同,随着溶剂的极性增大,反应收率提高,其原因可能在于极性溶剂中催化剂溶解性好。其中效果最好的是氯仿和DMF,氯仿由于毒性较大,因此选择对环境友好的DMF为反应体系的溶剂。
2.2.4 温度对反应的影响
以0.02 mol百里酚为原料,采用氧气为氧化剂,DMF为溶剂,使用10%的Salen Co(Ⅱ)为催化剂,反应时间9h,考察了温度对反应的影响,结果见图3。
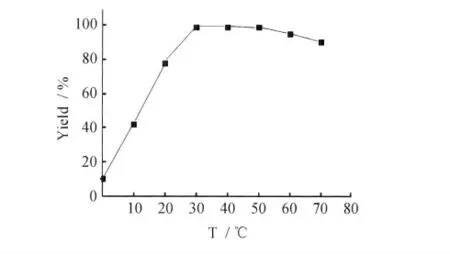
图3 温度对反应的影响Fig.3 Effect of temperature to reaction
由图3可见,随着反应温度的升高,收率不断增加,当达到30℃时反应收率达到最高,产量为3.25g,收率达到99.1%,随着反应温度继续增加反应收率有所下降,因此30℃为反应体系的较佳温度。
2.2.5 氧化剂对反应的影响
以0.02mol百里酚为原料,采用DMF 为溶剂,使用10%的Salen Co(Ⅱ)为催化剂,反应时间9h,在30℃的条件下,分别考察了空气和氧气作为氧化剂对反应的影响,结果见图4。
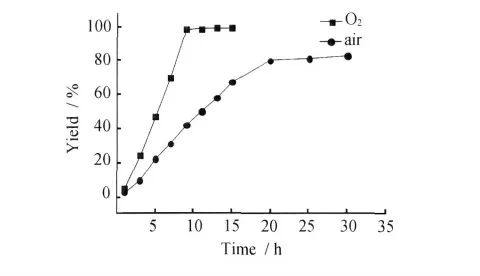
图4 氧化剂对反应的影响Fig.4 Effect of oxidants to reaction
由图4可见,氧气作为氧化剂时,反应9h就可以顺利完成,当用空气作为氧化剂,虽然仍可进行百里酚的定量氧化,但反应速度较低,并且转化率也低,不能反应完全。因此,与空气相比,氧气作为氧化剂表现出良好的优越性。
3 结论
百里酚经催化氧化合成百里醌的最佳反应条件为:10mol%Salen Co(Ⅱ)配合物为催化剂,DMF为溶剂,在氧气存在下30℃反应9h,收率可达99.1%。该工艺实现了高效、高选择性氧化百里酚,具有催化剂易得,溶剂污染小,反应选择性好,产品收率高等特点,具有工业化应用前景。
[1]Banerjee S,Kaseb A O,Wang Z,et al.Antitumor activity of gemcitabine and oxaliplatin is augmented by thymoquinone in pancreatic cancer[J].Cancer Res.,2009,69(13):5 575-5 583.
[2]Jafri S H,Glass J,Shi R,Prince M.et al.Kleiner-Hancock H.,Thymoquinone and cisplatin as a therapeutic combination in lung cancer:In vitro and in vivo[J].J Exp.Clin.Cancer Res.,2010,29:87-89.
[3]Kremers E,Wakeman N,Hixon R M.Thymoquinone[J].Org.Syn.,1941,1:511-512.
[4]Egusquiza M G,Romanelli G P,Cabello C,et al.Arene and phenol oxidation with hydrogen peroxide using'sandwich'type substituted polyoxometalates as catalysts[J].Catal.Commun.,2008,9(1):45-50.
[5]Noyori R,Aoki M,Sato K,et al.Green oxidation with aqueous hydrogen peroxide[J].Chem.Commun.,2003,(18):1 977-1 986.
[6]Omura K.Rapid conversion of phenols to p-benzoquinones under acidic conditions with lead dioxide[J].Synthesis.,1998,(9):1 145-1 148.
[7]Punniyamurthy T,Velusamy S,Iqbal J,Recent advances in transition metal catalyzed oxidation of organic substrates with molecular oxygen[J].Chem.Rev.,2005,105(6):2 329-2 364.
[8]Liotta D,Arbiser J,Short J W,Simple,inexpensive procedure for the large-scale production of alkyl quinones[J].J.Org.Chem.,1983,48(17):2 932-2 933.
[9]臧树良,岳 爽.新型高效催化剂——甲基三氧化铼(MTO)的研究发展[J].当代化工,2007,36(6):551-556.
[10]Meunier B,Metalloporphyrins as versatile catalysts for oxidation reactions and oxidative DNA cleavage[J].Chem.Rev.,1992,92(6):1 411-1 456.
[11]Zhang X.,Pope M.T.High-valent manganese in polyoxotungstates.4.catalytic and stoichiometric alkene oxidation[J].J.Mol.Catal.A,1996,14(1-3):201-208.
[12]Villabrille P I,Romanelli G P,Vázquez P G,et al.Vanadium-substituted keggin heteropolycompounds as catalysts for ecofriendly liquid phase oxidation of 2,6-dimethylphenol to 2,6-dimethyl-1,4-benzoquinone[J].Appl.Catal.A,2004,270(1-2):101-111.
[13]Villabrille P I,Romanelli G P,Gassa L,et al.Synthesis and characterization of Fe-and Cu-doped molybdovanadophosphoric acids and their application in catalytic oxidation[J].Appl.Catal.A,2007,324:69-76.
[14]Zhou X F,Liu J.Co(salen)-catalysed oxidation of synthetic lignin-like polymer:Co(salen)effects[J].Hem.Ind.,2012,66(5):685-692.
[15]Zhao Z P,Li M S,Zhang J Y,et al.New chiral catalytic membranes created by coupling UV-photografting with covalent immobilization of Salen-Co(III)for hydrolytic kinetic resolution of racemic epichlorohydrin[J].Ind.Eng.Chem.Res.,2012,51(28):9 531-9 539.
[16]Liu Z C,Liu F,Lu Y,et al.Studies oncharacters and synthesis of metal-salen complexes[J].Leshan Teachers College,2002,17(4):30-33.

