双氧水氧化处理低浓度含锰废水的研究
杨庆一,李道静
(1.贵州大学, 贵阳 550025;2.贵州省环境监察局, 贵阳 550081)
锰是人体必需的微量元素,然而过量摄入则会对机体产生毒性,影响中枢神经系统,临床表现症状类似于帕金森氏综合症[1]。在湿法冶炼电解锰生产过程中产生的大量废水含有锰、铬等污染物,对环境和人类健康危害极大[2];其中所占比例较少的工艺废水因锰、铬等污染物含量很大,都必须经过净化处理后再排放。然而受污染的其他水体,如厂区附近的水井水、厂区地下水(地下水)、电解锰冷却水等却常常被人忽视,若此类水不经处理任其自由排放,由此引起的水体污染和人体危害也不容忽视。松桃县巴坳村老卜刺水井每小时出水量360 m3(枯水期),是该地区非常重要的生活用水来源,由于松桃县锰矿资源丰富,加之附近的电解金属锰渣场渗透的影响,导致该水源中锰含量偏高,根据铜仁地区环境监测站对老卜刺水井的常规监测值为8~11 mg/L,另外 pH 为 5.0 ~7.0 左右,Cr6+未检出,氨氮含量为124 mg/L。锰和氨氮含量不仅高于地下水V类水标准 (Mn>1 mg/L,氨氮>0.5 mg/L),且锰含量已超过了GB 8978—1996《污水综合治理排放标准》规定的排放浓度(2 mg/L)。现以松桃县巴坳村老卜刺井水为研究对象,研究双氧水氧化对低浓度含锰废水的去除效果及其影响因素。
2 实验材料与方法
2.1 实验试剂和仪器
试剂:NaOH(分析纯),H2O2(30%,分析纯)
仪器:DJ1C增力电动搅拌器(江苏省金坛市大地自动化仪器厂),TD10002电子天平(余姚市金诺天平仪器厂),WFX-1E3型原子吸收分光光度计(北京瑞利分析仪器公司),便携式酸度计pHB-5型(杭州雷磁分析仪器厂)。
2.2 样本
取松桃巴坳村老卜刺含锰井水,实验室测定锰含量5~12 mg/L,pH 8.4左右,温度12~18 ℃。
2.3 实验方法
对井水进行取样分析,检测其中Mn的含量。准确量取一定体积的井水样于烧杯中,加0.3845 mol/L的NaOH调节pH值,再向其中加入质量比为30%的H2O2水溶液,搅拌一定时间后再静置一段时间,双层滤纸自然过滤后,取样分析其中Mn含量。其中Mn含量用火焰原子吸收分光光度法测量,溶液pH值采用便携式酸度计检测测量。实验均在室温(12℃)条件下进行。
在实验过程中,首先调节pH为7、7.5、8,在这三个 pH值条件下分别加入体积比为 5.0‰、2.5‰、1.0‰、0.5‰的 H2O2,搅拌 5 min,静置 25 min,过滤后分析滤液中锰含量,考察不同 pH和H2O2加入量对锰去除率的影响,根据实验结果进一步优化pH值和H2O2的加入量。在确定了最优的pH值和H2O2的加入量后,对影响双氧水氧化除锰的其他因素即搅拌时间和静置时间进行考察,最终得出最优的双氧水氧化除锰工艺条件。
3 实验结果与讨论
3.1 pH和H2O2加入量对锰去除率的影响
pH和H2O2加入量对锰去除率的影响见表1:

表1 pH和H2O2加入量与锰去除率相关性
由表1可知,随着pH的增大,氧化除锰的效果越来越好,当 pH 达到 8.0,H2O2加入量为 2.5‰、1‰、5‱时,溶液中Mn含量低于检出限,几乎能除尽。而在pH一定的情况下,H2O2加入量的增加并没有明显促进锰的去除。双氧水氧化去除二价锰的机理是由于H2O2具有强氧化性,在碱性环境中,能将溶液中 Mn2+氧化为 MnO2,方程如下[3]:

该反应分两步进行:

反应中生成的MnO2可作为催化剂,加速H2O2的分解,使反应快速进行,该反应是一个自催化反应。不过也有研究认为,在碱性环境下,Mn2+的去除主要是通过Mn2+的氧化产物水合二氧化锰胶体(MnO(OH)2)与Mn2+进行离子置换得以实现的[4]。由此可见,OH-浓度的增加有助于反应(1)向正方向进行,从而有利于Mn2+的去除,在反应过程中,当pH值为8时,OH-的浓度为10-8mol/L,远小于Mn2+的浓度,因此pH值越大,除锰效果越好。
3.2 氧化除锰综合实验优化
根据方程(1),H2O2与Mn2+在计量关系上的质量比为34∶55,实验中加入的H2O2最小量为0.5 ml,30%的H2O2水溶液密度为1.1 g/ml,由此得出在1 L水样中加入0.5 ml的30%的H2O2溶液,H2O2的浓度为165 mg/L,远大于Mn2+的浓度,因此H2O2加入量的增加对锰的去除效果影响不大,因此,我们降低 H2O2加入体积比至 5‱、2.5‱、1.0‱、0.5‱,并对影响双氧水氧化除锰的各因素进行了优化。
调节pH值为8,搅拌时间和静置时间分别为5 min和25 min,降低H2O2加入量并考察其对锰去除率的影响,实验结果如表2:

表2 H2O2加入量的优化实验结果
从实验结果可以看出,设置pH为8.0,H2O2加入体积比为0.5‱时,溶液中Mn仍可降到2 mg/L以下。
确定H2O2加入量为0.5‱,然后调节NaOH加入量,并设置不同的静置时间,确定最佳的pH值及实验静置时间。在不同pH值及静置时间下锰的去除效果如表3。
从实验结果中可以看出,当NaOH加入量为0.72‱,控制 pH值在9.2在以上,H2O2加入量为0.5‱时,只需要反应15 min溶液中锰即可降到2 mg/L以下,可满足排放标准。
实验最后考查了搅拌时间对H2O2氧化除锰效果的影响,结果如表4。
由实验结果可知,搅拌时间对于双氧水氧化除锰的效果不呈现规律性的关系,搅拌时间过长反而不利于锰的去除,这有可能是因为搅拌时间过长会破坏反应过程中形成的二氧化锰胶体(MnO(OH)2)形态,不利于其对Mn的吸附,因此在反应过程中要对搅拌时间严格控制。结果显示搅拌时间为1 min时,滤液中的Mn2+最低。
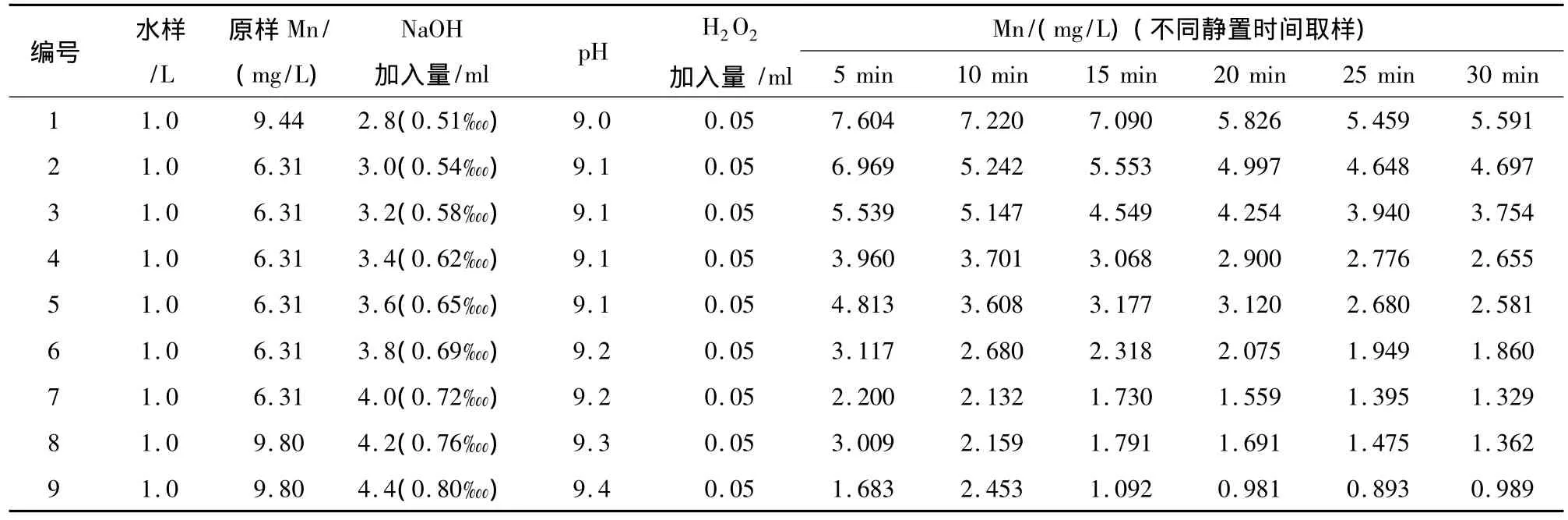
表3 不同NaOH加入量和静置时间下的锰去除效果

表4 搅拌时间对除锰效果的影响
4 结论
在双氧水氧化除锰实验中,pH的提高能明显促进锰的去除。在pH值固定的情况下,H2O2加入量过高对锰的去除率没有帮助,过低会降低锰的去除率。静置时间在一定范围内越长,锰的去除率越高,不过20 min以后趋于平缓。搅拌时间过长不利于锰的去除。对于低浓度的含锰废水,双氧水氧化除锰的最佳工艺条件pH为9.2~9.4,H2O2加入量为0.5‱,静置时间 15 min,搅拌时间为 1 min。
[1]师娟子,郭仁舆.锰的毒性[J].国外医学医学地里分册,1992,13(2):51-52.
[2]姚俊,田宗平,姚祖风,等.电解金属锰废水处理的研究[J].中国锰业,2000,18(3):25 -27.
[3]胡文华,吴慧芳,孙士权.过氧化氢预氧化去除受污染地下水中铁、锰的试验研究[J].水处理技术,2011,1:73-75.
[4]王琳,王宝贞,张维佳,等.含铁锰水源水深度处理工艺的运行试验研究[J].环境科学学报,2001,21(2):134-139.

