双源CT单能谱成像技术减低颅内动脉瘤夹伪影的研究
潘雪琳,李真林,程巍,袁元
随着神经外科金属夹材料和手术技术的日益成熟,动脉瘤颈夹闭术被认为是治疗动脉瘤的常用手段[1]。动脉瘤颈夹闭术后常见的并发症有脑血管痉挛、动脉瘤术中破裂、载瘤动脉远端闭塞、残留动脉瘤等。随着多层螺旋CT探测器的增宽,时间分辨率提高,常采用MSCT头部血管成像进行动脉瘤颈夹闭术后的疗效评价。但是,由于金属植入物具有明显的线束硬化伪影,影响对手术区精细解剖结构的观察[2],并且MSCT血管成像由于动脉瘤夹的线束硬化伪影影响去骨的效果,从而影响并发症的判断。双能量CT已经用于全身不同病变的检查,但是也没有完全避免线束硬化伪影的影响[3-5]。既往研究[6]发现单能量成像(monoenergetic imaging,MEI)可减除金属植入物的伪影,目前,四肢、脊柱金属植入物的单能量成像研究较多,头部金属植入物的金属伪影消除研究很少。本研究采用二代双源CT对颅内动脉瘤夹植入患者进行双能量头部血管扫描,探讨双源CT单能量成像技术在减除颅内动脉瘤夹伪影方面的价值,寻求图像质量较好的单能量成像点。
材料与方法
1.一般资料
2013年7月-2013年10月,48例颅内动脉瘤颈金属夹夹闭术后的患者接受双源CT双能量血管扫描,男21例,女27例,年龄38~68,平均(52.7±2.7)岁。
2.仪器与方法
采用Siemens Somatom Definition Flash双源CT机进行头部血管双能量扫描。扫描范围自颅底下方1cm水平至颅顶。扫描参数:A管管电压Sn 140kV,参考管电流量104mAs;B管管电压100kv,参考管电流量104mAs;准直器宽128i×0.6mm,螺距0.85,脚-头方向扫描,重建层厚0.75mm,层间距0.50mm,机架旋转一周时间0.5s。采用CT双筒高压注射器,经肘静脉以4~5mL/s的流率注射碘比乐(370mg I/mL)50mL,随后以相同的流率注射20mL生理盐水。监测层面置于颅底下方2cm水平,兴趣区放置在颈内动脉,阈值为100HU,当CT值达到100HU后自动触发扫描。
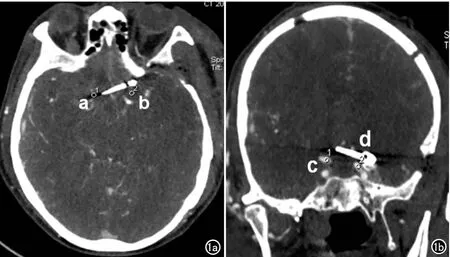
图1 层面选取,动脉瘤夹伪影最重的脑组织即动脉瘤夹长轴的尾部(a)、无动脉瘤夹伪影的脑组织即a的对称点(b)、受动脉瘤夹伪影影响最重的血管(c)、无动脉瘤夹伪影影响的血管即c的对称点(d)。a)横轴面图像;b)冠状面图像。
3.图像重建与数据处理
扫描完成后,将自动重组的Sn 140kV、80kV以及平均加权120kV数据传送到Siemens工作站Syngo Mmwp VE36A,使用双能量单能谱(Monoenergetic)软件进行处理分析,对40~120keV的单能量数据每隔10keV进行重建,共9组单能量图像。
4.测量方法
①典型层面(图1):a点位于动脉瘤夹伪影最重的脑组织即动脉瘤夹长轴的尾部;b点为a点的对称点,位于无动脉瘤夹伪影的脑组织内;c点位于受动脉瘤夹伪影影响最重的血管;d点为c点的对称点,位于无动脉瘤夹伪影影响的血管内。②测量方法:a、b两点位于相同层面镜像对称,c、d两点位于相同层面镜像对称;a尽量选择动脉瘤夹长轴尾部伪影最大处,c尽量选择在动脉瘤夹伪影影响最重的血管上。在测量c、d两点CT值时,ROI的范围大于血管面积1/2,尽量在血管中央进行测量。a、b两测量点的大小应与c、d保持一致。测量数据分别记录为CTa、CTb、CTc和CTd。计算a、b两点CT值的差值即|CTa-CTb|以及c、d两点CT值的差值即|CTc-CTd|。
5.统计学分析
所有统计学处理均使用SPSS 16.0统计软件,采用配对t检验分析不同keV时CTa与CTb之间以及CTc、CTd之间的差异,采用方差分析比较9组图像间|CTa-CTb|和|CTc-CTd|差异有无统计学意义。P<0.05为差异有统计学意义。
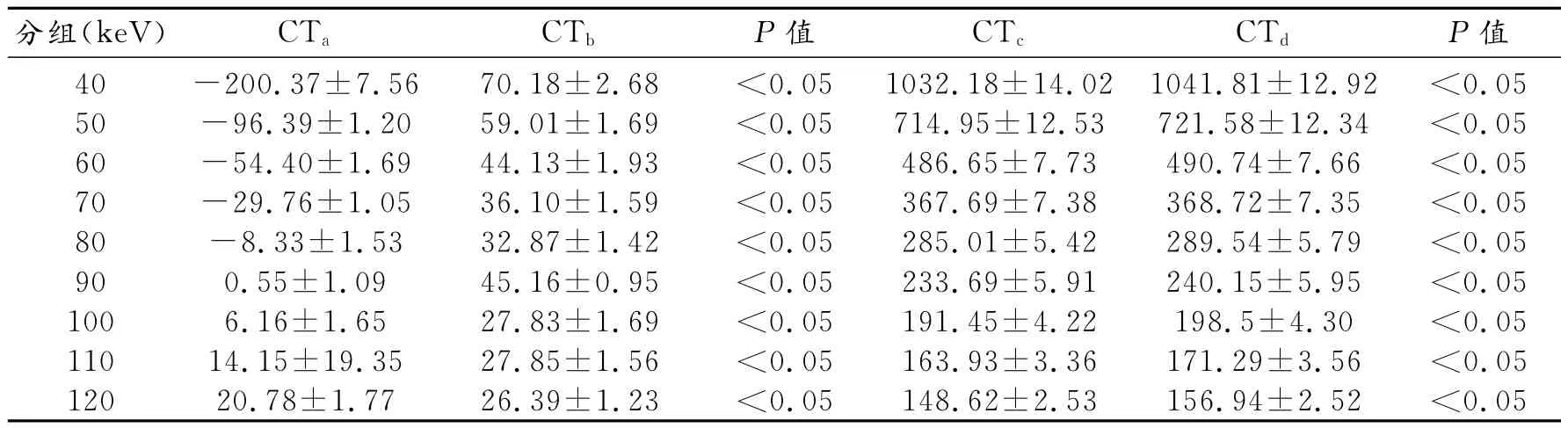
表1 不同keV下a、b、c、d四个测量点的CT值观察指标 (HU)
结 果
48例患者不同keV下a、b、c、d四个测量点的CT值见表1。9组图像中每一组a、b之间,c、d之间的CT值差异均有统计学意义(P<0.05)。
|CTa-CTb|和|CTc-CTd|测量结果见表2。
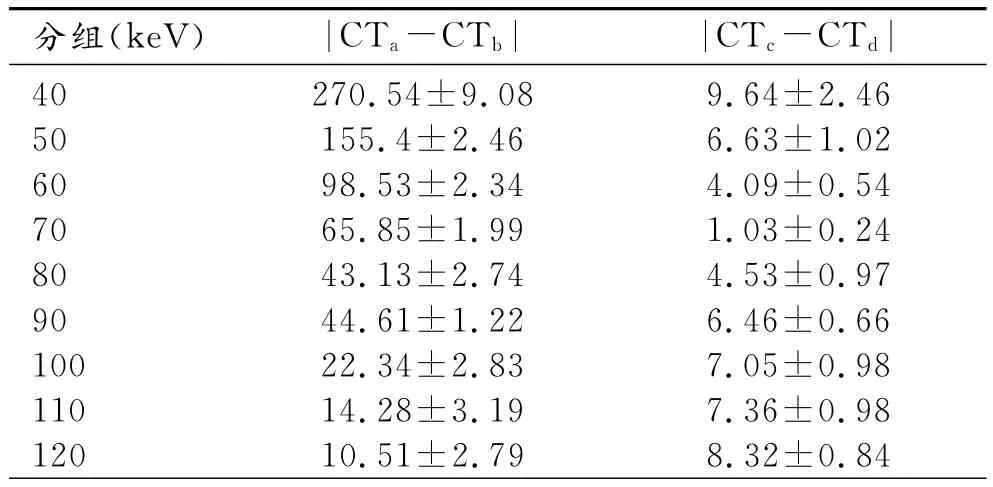
表2 不同keV时a、b间和c、d间的CT值差 (HU)
其中|CTa-CTb|在120keV时最小,为(10.51±2.79)HU,|CTc-CTd|在70keV时最小,为(1.03±0.24)HU(图2)。方差分析显示各组间两值的差异均有统计学意义(P<0.05),组间两两比较差异亦均有统计学意义(P<0.05)。
讨 论
在CT扫描或信息处理过程中,CT图像上出现的不属于机体正常信息的某些图像阴影称为伪影,可对诊断造成影响[7]。完美的CT图像不应扭曲被检部位任何断面的任何几何特征[7]。CT图像伪影可分为以下两大类:扫描采集过程中产生的伪影和CT机本身系统有关的伪影。而金属伪影可以在很大程度上降低图像质量,并使放射科医师对邻近结构的评价产生一定困难[8],对于金属物植入患者术后评估尤其如此。伪影的产生取决于金属物的内在特性,如密度、厚度及形状等。本组所有患者的金属植入物均为钛合金材料,密度、厚度及形状等基本一致。
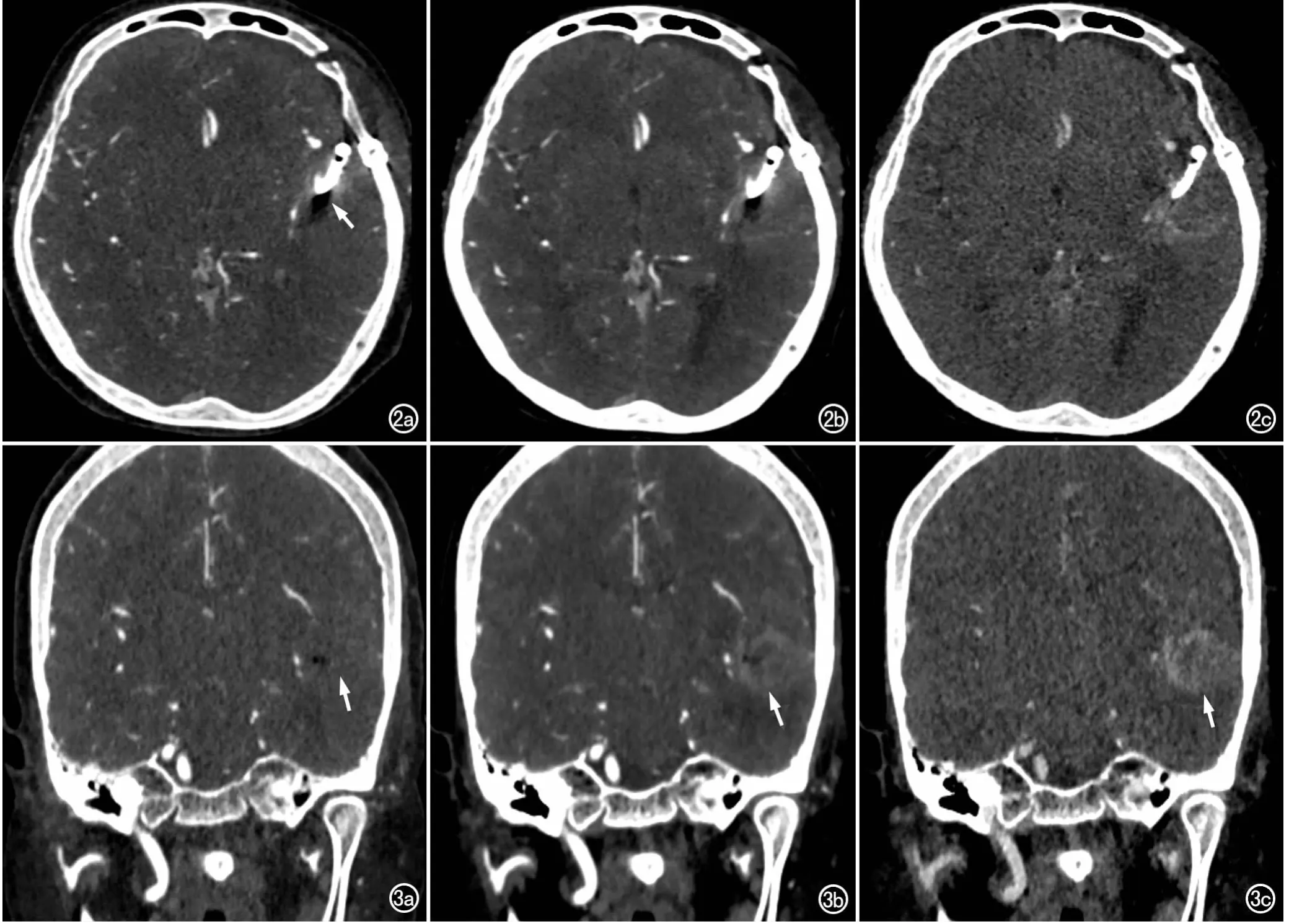
图2 同一层面不同keV横轴面图像。a)40keV时动脉瘤夹金属伪影较重(箭),颅内血管清晰可见;b)70keV时动脉瘤夹金属伪影有所降低,颅内血管清晰显示;c)120keV时动脉瘤夹金属伪影明显降低,颅内血管显示不佳。 图3 同一层面不同keV冠状面图像。a)40keV时动脉瘤夹旁未见出血征象(箭);b)70keV时动脉瘤夹旁可见少量出血征象(箭);c)120keV时动脉瘤夹旁可见少量出血征象(箭)。
随着MSCT扫描时间的缩短、分辨力的提高,动脉瘤夹闭术后患者常采用CT头部血管成像进行疗效评价。CT检查时,X线通过高密度的金属植入物时会被大量吸收,发生严重的衰减,金属夹区域产生条索状金属伪影。尽管低窗位、高窗宽有助于降低金属伪影的影响,但仍对金属夹周围的解剖细节显示不清,不能去除X线束硬化伪影。由于动脉瘤夹的线束硬化伪影影响去骨效果,从而影响对动脉夹周围体积较小的残留动脉瘤和出血性病变的观察,最终影响了常规CT血管成像对金属夹夹闭术后患者在疗效评价方面的临床应用价值。本研究使用的双源CT机比常规CTA技术有所改进,双源CT双能量成像采用100kV和Sn 140kV两种不同能量的X线进行数据采集。由于X线的衰减取决于X线能量,采用100kV和Sn 140kV的X线对同一组织进行扫描时,X线衰减不同,被扫描组织的X线衰减也会不同。金属植入物对低能量X线的衰减系数最大,在高能量X线条件下,其衰减系数减少了50%以上[9]。双源CT机单能谱技术即利用了X线的此种特性,对2个X线球管及探测器所产生的数据通过特殊计算后得到不同keV下的图像。另外,二代双源CT机通过能谱纯化(selected photon shield,SPS)技术,有效减少高能中无效的低能成分,能更好地分离组织,有效降低图像噪声。通过Monoenergetic重建技术得到40~190keV的图像,但是120keV时血管CT值在150HU附近,血管显示不佳,因此本研究旨在对40~120keV下动脉瘤夹伪影对周围脑组织、血管的影响,从而找到对图像质量影响较小的keV值,减少了伪影对周围组织的影响,以便更及时、准确地对动脉瘤夹闭术后患者的情况进行评价。
本研究发现颅内动脉瘤夹产生两种性质的伪影:①与动脉瘤夹长轴平行方向产生的低密度伪影,这类伪影对图像质量的影响最为严重,本文重点讨论此类伪影;②在动脉瘤夹旁边产生的高低混杂密度伪影,此类伪影较为轻,对图像质量的影响不大,本文未对其进行量化分析。
在40~120keV范围内,单能量CT图像上以低密度伪影为主(CTa-CTb<0,CTc-CTd<0),瘤夹周围组织CT值偏低。随着管电压增加,40~70keV时|CTa-CTb|和|CTc-CTd|数值减小,即CTa与CTb以及CTc与CTd的差异越来越小,受伪影影响较重的a、c两点的CT值分别和对称侧未受伪影影响的b、d两点的CT值越接近,伪影对图像质量的影响越小,图像质量越接近于未受伪影影响的优质图像。70~120keV时∣CTa-CTb∣逐渐减少,提示脑组织受金属夹伪影的影响逐渐减小;但是∣CTc-CTd∣逐渐增大,即头部血管受伪影的影响在逐渐增加,同时CTc和CTd仅约150HU,血管的显示不佳。因此总体上来说,70~120keV时随着keV的增加血管显示的清晰程度逐渐降低。本研究结果表明,70keV时|CTc-CTd|最小,即CTc与CTd之间差异最小,受伪影影响较重的血管与未受伪影影响的血管的CT值越接近,因此,70keV是降低颅内金属夹伪影的较好单能量成像点。
本研究评价了双能量CTA单能谱技术在48例患者动脉瘤夹闭术后复查的应用价值,结果显示对于颅内动脉瘤夹植入术后的患者而言,40keV时动脉瘤夹金属伪影较重,颅内血管清晰可见,动脉瘤夹旁未见出血征象;70keV时动脉瘤夹金属伪影有所降低,颅内血管清晰显示,动脉瘤夹旁可见少量出血征象;120keV时动脉瘤夹金属伪影明显降低,颅内血管显示不佳,动脉瘤夹旁可见少量出血征象(图2)。本研究结果表明双能量CTA单能谱技术不仅能够降低动脉瘤夹伪影对CT图像质量的影响,采用最佳的keV值还能提高图像对解剖细节的显示,满足临床上放射科医师、神经外科医师对患者治疗效果、并发症及预后的评价。本研究还优化了不同光子能量对单能谱技术重组后图像质量的影响,70keV可提供较好的图像质量。然而本组患者数量相对较少,还需要进一步搜集大组资料对本研究的结论进行验证。
综上所述,双源CT单能谱成像技术能够显著提高动脉瘤夹植入术后CT复查的影像质量,动脉瘤夹植入术后患者CT复查采用70keV进行重建可获得较好的图像质量,在临床中可应用单能谱技术提高图像质量,从而更清楚地显示术后的各种并发症。
[1]杨树源,只达石.神经外科学[M].北京:人民卫生出版社,2008:1.
[2]National Research Council.Health risks from exposure to low levels of ionizing radiation BEIRVII Phase 2[M].Washington,DC:National Academy Press,2006:550.
[3]卢光明 .积极开拓双源CT的临床应用范围[J].中华放射学杂志,2008,42(2):117-118.
[4]张宗军,卢光明 .双源CT及其临床应用[J].医学研究生学报,2007,20(4):416-418.
[5]傅强,赵宇冷,仁利,等 .矫形金属植入物CT扫描技术的初步经验[J].放射学实践,2007,22(5):531-533.
[6]Barrett JF,Keat N.Artifacts in CT:recognition and avoidance[J].Radiographics,2004,24(6):1679-1691.
[7]周泽俊,胡永胜,高斌,等.多层螺旋CT图像伪影的分析[J].中国CT和 MRI杂志,2008,6(5):72-75.
[8]Watzke O,Kalender WA.A pragmatic approach to metal artifact reduction in CT:merging of metal artifact reduced images[J].Eur Radiol,2004,14(5):849-856.
[9]Johnson TR,Krauss B,Sedlmair M,et al.Material differentiation by dual energy CT:initial experience[J].Eur Radiol,2007,17(12):1510-1517.

