生半夏对生川乌中生物碱溶出量的影响
杨慧波,张树峰,佟继铭
(河北省中药研究与开发重点实验室/承德医学院中药研究所,河北承德 067000)
乌头和半夏是出自“十八反”的药对,但从古至今在许多处方中配伍使用,如孙思邈《千金要方》中的大五饮丸、半夏汤,《金匮要略》中的赤丸方,宋代《太平惠民和剂局方》中的十四味建中汤等;以及近代外敷治疗膝骨性关节病的乌头半夏散,治疗乙肝的神丹等[1]。乌头和半夏能否共用,一直是学者们争论的焦点。本研究通过探讨生川乌与不同比例生半夏配伍后水浸液中3种生物碱(乌头碱、新乌头碱、次乌头碱,生物碱是乌头的主要毒性成分)的含量,探讨生川乌与生半夏毒性最小的配伍比例,以期为临床用药提供实验依据。
1 仪器与试药
1.1 主要仪器 安捷伦1200高效液相色谱仪,美国安捷伦公司;Hypersil BDS C18(5μm,4.6mm×250mm)色谱柱,大连伊利特分析仪器有限公司。
1.2 试药 乌头碱(批号:201101RS)、次乌头碱(批号:201101RS)、新乌头碱(批号:201101RS)对照品,云南特法特生物科技有限公司。生川乌(批号:090212),河北省光明饮生有限公司汉草饮生厂;生半夏(批号:100101),河北省安国市光明饮片加工厂。
2 方法与结果
2.1 色谱条件 流动相为甲醇-水-氯仿-三乙胺(70:30:2:0.1),检测波长235nm,流速1.0ml/min,柱温30℃,进样量10μl[2]。
2.2 对照品溶液的制备 分别取对照品精密称定,加二氯甲烷溶解,配成1ml含乌头碱50μg、新乌头碱100μg、次乌头碱160μg的混合对照品溶液。精密量取混合对照品溶液稀释成1ml含乌头碱分别为25μg、12.5μg、6.25μg、3.125μg、1.5625μg 的等比稀释溶液[3]。
2.3 供试品溶液的制备 称取单味生川乌2g(生川乌:生半夏=1:0),加3倍量水浸泡3次,每次24h,合并滤液,用等体积乙醚提取3次,乙醚萃取液合并后20℃下蒸干,加二氯甲烷溶解,即得供试品溶液。其余不同配伍比例组处理同单味生川乌[4-6]。
2.4 方法学考察
2.4.1 线性范围考察:分别精密吸取系列混合对照品溶液10μl,按照2.1的色谱条件进行测定。以峰面积为纵坐标,进样浓度(μg/ml)为横坐标,绘制标准曲线,得乌头碱、新乌头碱、次乌头碱的回归方程分别为:Y=14.502X+0.2743、r=0.9996,Y=11.216X-0.7607、r=0.9998,Y=11.624X-25.495、r=0.9996。乌头碱在1.5μg/ml-25.0μg/ml、新乌头碱在17.0μg/ml-85.0μg/ml、次乌头碱在16.0μg/ml-160.0μg/ml范围内,线性关系良好。
2.4.2 精密度试验:精密吸取乌头碱浓度为50μg/ml的混合对照品溶液10μl,连续进样5次,乌头碱、新乌头碱和次乌头碱的峰面积RSD值分别为1.02%、1.21%、1.08%(n=5),说明仪器精密度良好。
2.4.3 重复性试验:精密称取生川乌样品,按2.3的方法操作制备供试品溶液,重复测定5次,得新乌头碱、乌头碱和次乌头碱的平均含量分别为0.080mg/g、0.021mg/g、0.125mg/g,RSD 值分别为1.21%、1.16%、1.13%,表明实验有很好的重复性。
2.4.4 稳定性试验:在相同实验条件下,各供试品溶液分别于室温下放置0、4、8、12、24h 后测定,结果见表1,表明供试品溶液在24h内稳定性良好。
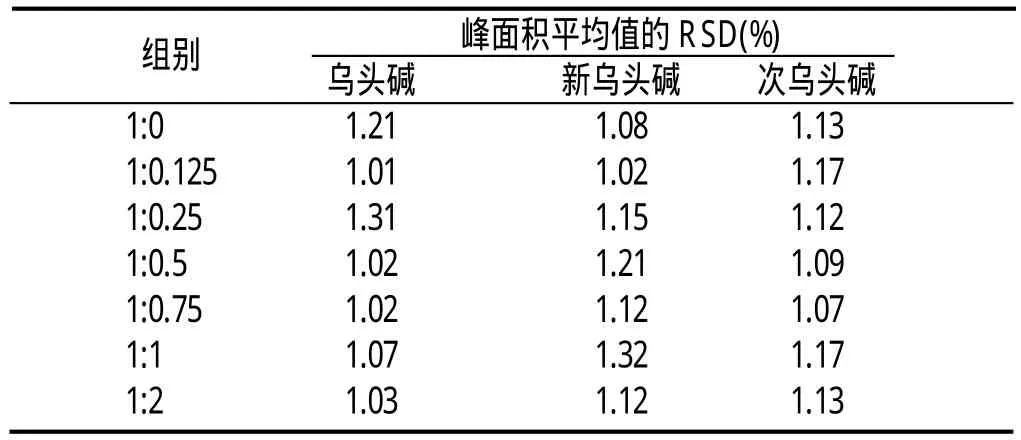
表1 稳定性试验结果(n=5)
2.4.5 加样回收率试验:精密吸取对照品溶液1ml,其中含乌头碱12.5μg、新乌头碱25μg、次乌头碱40μg,置于25ml三角烧瓶中,室温下挥去二氯甲烷,精密称取2g生川乌加入三角烧瓶,按照2.3的条件制备供试品溶液,按照2.1的色谱条件进行含量测定,计算回收率(n=5)。结果乌头碱、新乌头碱、次乌头碱的平均加样回收率分别为98.79%、97.34%、101.33%,RSD 值 分 别 为1.1%、1.08%1.21%。
2.5 供试品测定 分别精密吸取生川乌、生半夏不同比例配伍组供试品溶液10μl进行含量测定,结果见表2:随着半夏比例的增加,生川乌中3种生物碱的溶出量均下降,显示生川乌毒性降低。
表2 生川乌与不同比例生半夏配伍乌头碱、新乌头碱与次乌头碱含量(±s,n=5)

表2 生川乌与不同比例生半夏配伍乌头碱、新乌头碱与次乌头碱含量(±s,n=5)
组别 乌头碱(mg/g) 新乌头碱(mg/g) 次乌头碱(mg/g)1:0 0.02164±0.00051 0.08447±0.00089 0.12517±0.00016 1:0.125 0.01645±0.00017 0.06822±0.00075 0.10975±0.00024 1:0.25 0.01369±0.00032 0.05569±0.00155 0.09710±0.00253 1:0.5 0.01005±0.00027 0.04424±0.00148 0.06306±0.00324 1:0.75 0.00618±0.00020 0.03291±0.00073 0.034798±0.00110 1:1 0.00601±0.00012 0.02273±0.00227 0.02853±0.00029 1:2 0.00359±0.00023 0.01221±0.00017 0.01837±0.00045
3 讨论
乌头类生物碱是生川乌中的主要毒性成分,同时也是其主要有效成分。乌头类生物碱的测定方法有酸碱中和法、分光光度法、薄层扫描法等,目前最常用的是薄层扫描法中的高效液相色谱法(HPLC)[7]。2010版《中国药典中采用高效液相色谱法可以同时测定6种单酯型和双酯型生物碱的含量,操作简便,样品用量少,杂质分离效果好,乌头碱、次乌头碱、新乌头碱均达到了基线分离,回收率、重现性、精密度均很好[8]。本研究研究发现,生川乌中乌头碱、新乌头碱和次乌头碱的含量随生半夏加入量的增加而降低,说明生川乌的毒性和药效也会随着半夏加入量的增加而降低,但与十八反中二药合用会引起剧烈的毒性反应或副作用的说法不符,有待进一步的研究探讨。
[1]李振虎,李凡,胡江.“神丹”加味汤治疗慢性乙肝111例的临床观察[J].内蒙古中医药,2006,(4):6-7.
[2]罗霄,彭善贵,文永盛,等.HPLC测定制川乌中的乌头碱次乌头碱和新乌头碱[J].华西药学杂志,2010,25(4):472-473.
[3]梁生旺.中药制剂分析[M].第2版.北京:中国中医药出版社,2003.78-79.
[4]郑杭生,冯年平.中药饮品制川乌、制草乌中乌头碱、次乌头碱的HPLC测定[J].药物分析杂志,2005,25(1):34-36.
[5]刘岚,范智超,张志琪.HPLC同时测定成药中4种乌头类生物碱含量[J].药物分析杂志,2010,30(2):236-239.
[6]付宇,高建,赵宇,等.乌头碱含量测定方法的建立[J].化学工程师,2010,(11):29-30.
[7]周玲.乌头类中药化学成分及其生物碱含量测定方法的研究概况[J].中国中医药,2011,9(2):223-224.
[8]国家药典委员会.中华人民共和国药典[M].第1部.北京:中国医药科技出版社,2010.36-38.

