利用FTIR/ATR快速测定大豆油的过氧化值
杨本志 潘秋月 潘丹杰 孟祥河
(浙江工业大学生物与环境工程学院1,杭州 310018)
(中国农业大学食品科学与营养工程学院2,北京 100000)
(杭州市粮油中心检验监测站3,杭州 310014)
食用油是日常生活中不可或缺的必需品,同时也是现代食品加工业重要的原料。食用油中富含人体必须的维生素,脂肪酸,矿物质以及微量元素等,对人体的健康起着重要的调节作用,然而油脂氧化所产生的产物会对食用油的风味、色泽以及组织都会产生不良的影响,不仅降低食用油的商品价值和营养价值,而且氧化产物还会对膜、酶、蛋白质造成破坏,甚至可以导致老年化的很多疾病还可以致癌,严重危害人体健康。因此过氧化值是影响食用油质量的一个重要理化指标,如何对其进行快速、准确的测定,对油脂抗氧化以及提高产品质量都具有重要的意义。
目前,测定植物油过氧化值的方法主要有化学法、物理法、色谱法、光谱法、电化学法等[1]。这些方法不但非常耗时,并且须消耗大量有机溶剂,难以实现大批量快速定量检测。Gülgün Yildiz等[2]比较分析了化学法,比色法以及红外法,通过分析后发现红外法具有快速、无毒、准确性高等优点,可以替代传统的化学法。近年来,FTIR/ATR作为红外光谱法的重要试验方法之一,克服了传统透射法测试的不足,简化了样品的制作和处理过程,极大地扩展了红外光谱的应用范围[3]。Kangming Ma 等[4]将 TPP 与过氧化物反应生成TPPO,利用FTIR/ATR检测TPPO在1 118 cm-1的特殊吸收峰,利用峰高与过氧化值之间的关系,可以快速检测油样的过氧化值,但试验过程比较繁琐,使用化学试剂较多,试验时间较长,不能满足快速检测的需要。鉴于此,本试验利用傅里叶变换衰减全反射红外光谱法(FTIR/ATR)采集样品光谱,然后利用偏最小二乘法(PLS)建立过氧化值的快速预测模型[5],优化比较不同光谱预处理方法对建模效果的影响,期望为粮油加工业过氧化值精度测定提供一套高效、准确、快速的分析方法。
1 材料与方法
1.1 试剂与仪器
碘化钾:分析纯,天津市罗密欧化学试剂有限公司;硫代硫酸钠:分析纯,杭州化学试剂有限公司;三氯甲烷:分析纯,杭州化学试剂有限公司;冰醋酸:分析纯,天津市德恩化学试剂有限公司;淀粉指示剂(取可溶性淀粉配成10 g/L溶液):分析纯,无锡市晶科化工有限公司。
BRUKER TENSOR 27傅里叶红外光谱仪(配有ATR采样系统,OPUS操作软件):德国布鲁克公司。
1.2 样品
精炼大豆油购自超市。将样品进行相应处理后得到以下基础样品:A精炼大豆油;B用活化硅胶过滤;C加入5%水后放在空气中自然氧化60 d;D加热到150℃持续15 min,放置空气中60 d。待分析样品是基于这4种基础样品按一定比例配制获得的,具体过氧化值等相关样品信息见表1。
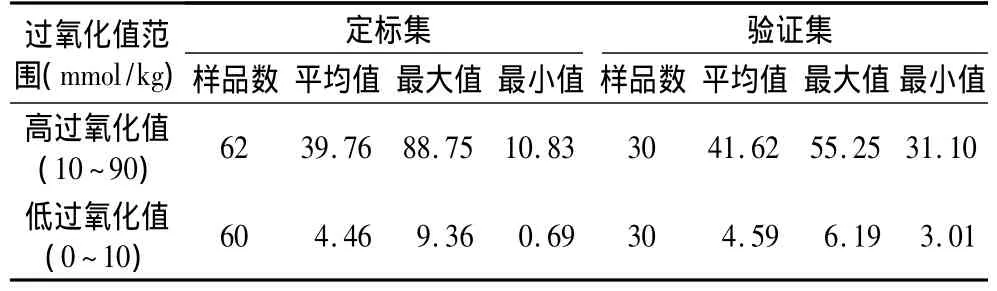
表1 样品信息
1.3 测定方法
1.3.1 光谱采集和参数设定
取适量样品均匀地滴在ATR附件的晶体材料(ZnSe)上,使其能完全覆盖晶体材料,仪器的光谱采集范围400~4 000 cm-1,光谱分辨率为2 cm-1,扫描次数为32次,测量环境的湿度需小于70%,温度保持在25℃左右,然后操作OPUS软件采集光谱。
1.3.2 化学法测定
通过碘量法(GB/T5 538—2 005)测定其过氧化值,每个样品测定3次,取其平均值。
1.4 数据处理
利用TQ Analyst光谱分析软件进行定标模型的建立,建立模型后需要验证模型的准确性和稳定性,其中准确性通过平均偏差和相对平均偏差进行评价,而稳定性需要标准以及变异系数来评价,相关指标的计算公式如下:

式中:n为样品测量次数;xi为样品测定值;珋x为n次测定结果的平均值
2 结果与分析
2.1 数据预处理
由于油样的主要吸收峰集中1 000~3 100 cm-1范围内,故本试验将此范围当作全波段,利用TQ Analyst定标软件在全波段范围内对采集的光谱依次进行SNV(标准归一化法),多点平滑,一阶导数等处理,SNV是用于消除光程长短或样品浓度等的变化对光谱响应产生影响比较理想的方法[6],采用偏最小二乘法(PLS)进行定标建模,平滑以及导数处理对R值,SEC和SEP的影响见表2,由表可以看出,在高氧化值组的预处理中,SNV、平滑和一阶导数的组合预处理方法虽然R值稍低,但是SEC和SEP值比较接近,模型稳定性较好,比较适合建模。在低氧化值组的预处理中,平滑和一阶导数的组合预处理方法所建模型比较稳定且准确度较高,适合建模。

表2 预处理方法对高过氧化物值组及低过氧化物值组模型准确性的影响
2.2 定量波段选择
选择合适的波段能使所建立的模型具有更好的预测性,能够提高模型预测的准确度和稳定性。M H MOH等[7]利用近红外透射法检测粗棕榈油的过氧化值,比较了在3 710~3 210 cm-1范围和在3 710 cm-1处所建立模型的优劣性,此范围主要包含了3 450 cm-1处—OH的伸缩振动峰,3 600~3 310 cm-1的-OH吸收峰,但此范围不能较全面地反映油脂的氧化过程。本文将光谱全波段平均分成7段,然后根据全波段,分波段以及分波段组合分别建立模型[8],结果见表3,利用主因子数,预测标准偏差均方值(PRESS),交互验证系数(R),以及预测方差(SEP)等指标综合评价模型的准确性,由表可知,基于1 600~3 030 cm-1波段所建立的模型较好。

图1 大豆油典型的的ATR光谱

表3 波段选择结果
根据油脂氧化过程中发生的基团变化,在这个波段内主要包含了在1 650 cm-1附近的C=C伸缩振动峰,在1 745 cm-1附近的C=O伸缩振动峰,3 010 cm-1附近的C=C—H伸缩振动峰等基团吸收峰的变化,结果见图1。
随着样品氧化过程的进行,油样中的羰基C = O基团在逐渐的增加,这是由于食用油中的C = C逐渐被氧化而生成醛、酮、酸等物质,从而使得C = O基团的吸收强度增加。同时油脂发生过度的氧化和分解,双键发生断裂,使得1 650 cm-1处的C = C及3010 cm-1附近的C=C—H含量下降,吸收强度降低。
2.3 异常波谱剔除及主因子数确定
为保障参与建模的所有波谱的有效性以及代表性,在进行建模前要将误差较大的光谱进行剔除,本试验利用杠杆值与残差检验工具对异常样品进行检验[9],但未发现需要剔除的光谱。采用PLS法建立定量校正模型时,为了充分利用光谱信号的有效信息,同时避免过度拟合现象,需对主因子的阶数进行合理选择[10]。按交互检验得到的主因子数与RMSECV(交互验证均方差)的关系进行选择[11](见图2),从图2中可以得出,当高氧化值和低氧化值模型的主因子数分别在8和5以后RMSECV基本趋于平稳,因此可以得到两组模型的最佳主因子数分别为8和5。

图2 主因子数与RMSECV的关系
2.4 模型的建立
利用FTIR/ATR采集光谱,综合上述的优化结果以偏最小二乘法建立定标模型,首先在过氧化值0~90 mmol/kg范围内建立定标模型,得到 R值为0.975 2,SEC 和 SEP 分别为 5.26 和 12.90,模型拟合较好但准确度并不理想。试验尝试将过氧化值分为高过氧化值(10~90 mmol/kg)和低过氧化值(0~10 mmol/kg)组分别建模(从两组样品中各选出30个样品作为验证集,剩余样品作为定标集),结果如图3所示。其中高氧化值模型得到R值为0.999 9,SEC和SEP分别为0.27、0.58。低氧化值模型得到R值为0.996 0,SEC 和 SEP 分别为 0.21、0.26。实际应用中,高氧化值模型适用于毛油以及高度氧化油的检测,而低氧化值模型则可以用于精炼大豆油的分析。
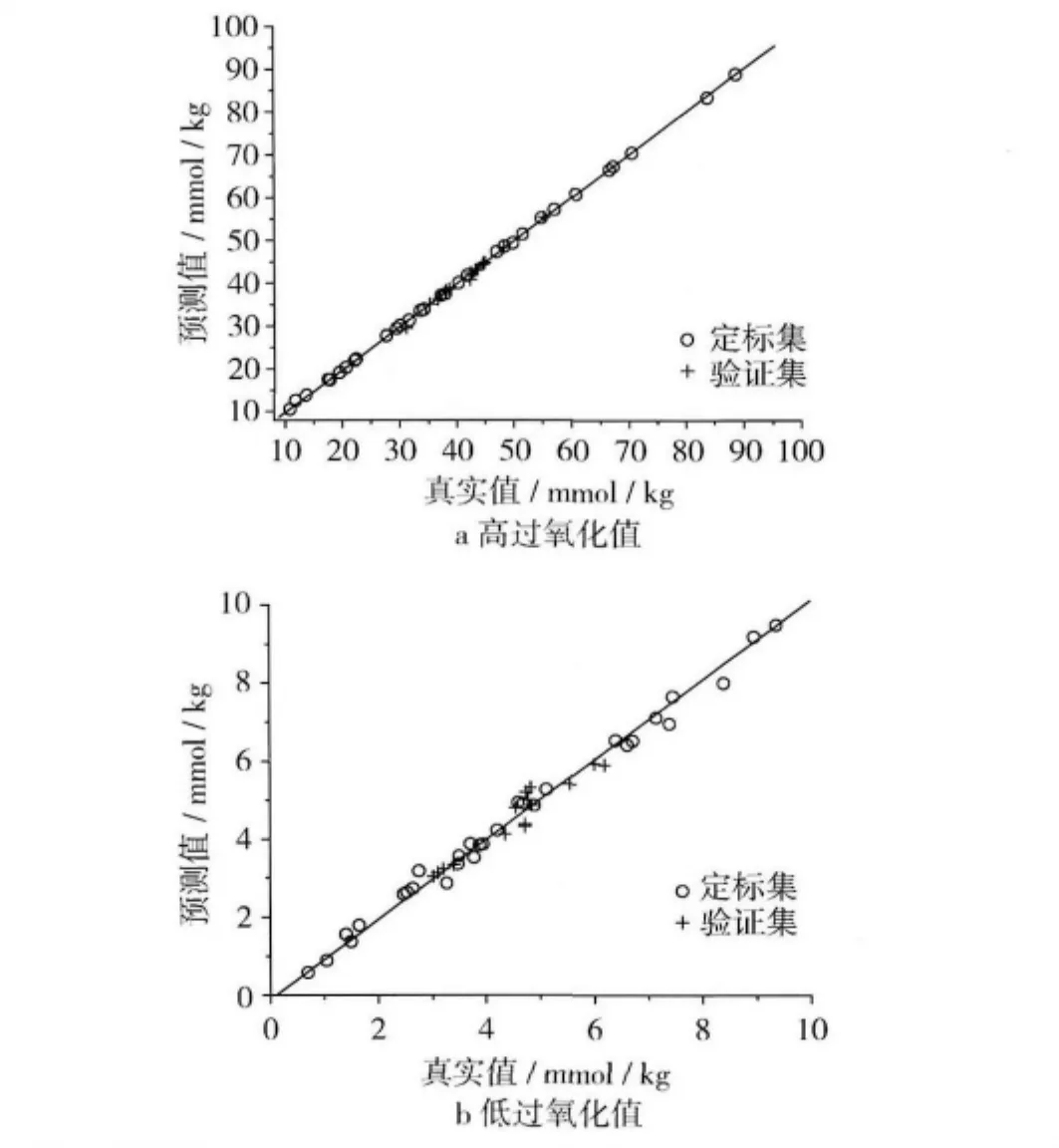
图3 食用大豆油过氧化值测定值与模型预测值的散点图
Van de Voort等[12]以丁基过氧化物代替初级氧化产物作为标准物质加入到植物油中,利用FTIR透射技术采集光谱,以偏最小二乘法建立定标模型,得到SEC以及SEP分别为1.30和2.66,模型精确度不高,且操作过程较复杂。G Setiowaty等[13]用透射法采集棕榈油的近红外光谱后建立测定过氧化值的定标模型,得到SEC以及SEP分别为0.15和0.17,精确度较高,但是样品池清洗比较困难,容易导致样品残留,可能会影响到模型的准确度。本文采用ATR技术,样品无需任何处理,仪器清洗容易,同时分析不使用任何有机试剂,而且通过分组建模实现了油脂过氧化值的在线、快速、精确分析,具有一定的实用性。
2.5 准确性试验
定标模型建立后,随机配制7个不同过氧化值的样品验证分析模型的准确性,并同碘量法测定值进行比较[14],得到高氧化值样品组的平均相对偏差为1.57%,低氧化值样品组的平均相对偏差为4.32%,两组样品的平均相对偏差均小于5%,模型的准确度较高,结果见表4。同时将化学测定值与红外预测值进行配对t检验,设定置信度为95%,两组样品的t值均小于理论t值,说明红外预测值和化学测定值之间没有显著(P>0.05),即用FTIR/ATR法取代碘量法对大豆油进行过氧化值的快速测定是可行的。

表4 准确性实验统计结果
2.6 稳定性试验
要建立一种稳定的分析方法,除了要有较高的精确度以外,所建立的模型要具有一定的稳定性[15]。利用本试验已建立的过氧化值定量分析模型对同一样品进行平行测定试验。以标准差、变异系数作为评价指标,以检验FTIR/ATR定量分析方法测定油样样品的稳定性。从验证集中随机挑选大豆油样品,分别采用化学法及FTIR法独立测定5次,数据如表5所示。结果显示,高过氧化值和低过氧化值两组样品红外预测值的标准差和变异系数均小于化学法的分析值,故两组模型的稳定性较好,能满足快速检测分析的需求。

表5 化学法与红外法的统计比较
3 结论
以大豆油为对象,利用FTIR/ATR采集调和油的红外光谱,采用TQAnalyst软件对采集的光谱数据进行处理,比较了多种预处理方法对PLS法建立模型的准确度的影响,并且对优化的定量模型进行了准确性和稳定性验证,结果表明,高氧化值组依次经过SNV、平滑以及一阶导数处理后所得模型的交互验证系数为0.999 9,SEC 和 SEP 分别为0.27 和0.58,低氧化值依次采用平滑和一阶导数处理后的交互验证系数为0.996 0,SEC 和 SEP 分别为0.21 和0.25,所建定量模型的稳定性良好。t检验表明红外预测值和化学测定值之间的没有明显差异(P>0.05),因此研究开发的基于FTIR/ATR快速分析食用大豆油过氧化物值的模型是有效的,具有明显的优势和实用性。
[1]李书国,薛文通,张慧.食用油脂过氧化值分析检测方法研究进展[J].粮食与油脂,2007,(7):35 -38
[2]G Yildiz,Randy L Wehling,Susan L Cuppett.Comparison of four analytical methods comparition for PV in oxidized soybean oil[J].J Am Oil Chem Soc,2003,80:103 - 106
[3]黄红英,尹齐和.傅里叶变换衰减全反射红外光谱法(ATR-FTIR)的原理与应用进展[J].中山大学研究生学刊:自然科学、医学版,2011,32(1):20 -21
[4]K M Ma,F R van de Voort,A A Ismail,et al.Monitoring peroxide value in fatliquor manufacture by fourier transform infrared spectroscopy[J].J.Am.Oil Chem.Soc.,2000,77:681-685
[5]F R van de Voort,A A Ismail,R Cox,et al.The determination of peroxide value by fourier transform infrared spectroscopy[J].J.Am.Oil Chem.Soc.,1999,71:921 -926
[6]徐玮,谭红,包娜,等.近红外光谱法快速测定白酒中的酒精度[J].中国农学通报,2010,26(19):70 -72
[7]M H Moh,T STang ,Y B Che Man,et al.Rapid determination of peroxide value in crude palm oil products using fourier transform infrared spectroscopy [J].J.Food Lipids ,1999)6):261-270
[8]M H Moh,Y BChe Man,F R van de Voort,et al.Determination of peroxide value in thermally oxidized crude palm oil by near infrared spectroscopy[J].J.Am.Oil Chem.Soc.,1999,76:19-23
[9]鲍丹青,毕艳兰,吴存荣,等.利用近红外光谱技术快速测定大豆油的过氧化值.中国粮油学报,2008,23(6):206-209
[10]崔晓君,袁昌明,徐立恒.花生油中过氧化物的近红外光谱分析[J].应用化学,25(3):375-376
[11]孙岩峰,袁洪福,王艳彬,等.近红外光谱用于过氧化氢含量的定量分析研究[J].分析化学研究简报,2005,33(10):1445-1448
[12]F R van de Voort,Sodman J,Dubois J,et al.The determination of peroxide value by FTIR spectroscopy[J].J.Am.Oil Chem.Soc.,1994,71:921 -926
[13]GSetiowaty,Y B Che Man,SJinap,et al.Quantitative determination of peroxide value in thermally oxidized palm olein by fourier transform infrared spectroscopy[J].Phytochem.Anal,2000,11:74 -78
[14]毕艳兰,鲍丹青,田原,等.利用傅里叶近红外技术快速测定食用植物油的过氧化值[J].中国油脂,2009,34(3):71-74
[15]陈萍,吴玉萍,业粉兰,等.近红外光谱预测云南香料烟中总糖﹑还原糖和总氮[J].光谱实验室,2012,29(1):95-98.

