复方丹参注射液辅助治疗小儿肺炎的系统评价
孙淑波,王 晶,赵旭伟,汪凤山,刘隽东,张沙莎
(1.佳木斯大学附属第一医院药剂科,黑龙江 佳木斯 154002;2.齐齐哈尔医学院第一附属医院科研科,黑龙江 齐齐哈尔 161041)
复方丹参(香丹)注射液是丹参和降香经提取制成的一种纯中药复方制剂,有效成分为丹参酮、丹参素、原儿茶酚醛、丹酚酸B等,具有消肿止痛、活血化瘀的功效。复方丹参注射液能扩张小血管,改善重要器官的微循环,抑制炎性介质释放,减轻肺组织和毛细支气管壁的水肿,加快肺泡内炎性渗出物的排出和吸收,故具有抗炎和促进炎症消散的作用,且有抗过敏、提高机体免疫力的功效[1-3]。大量研究发现,小儿肺炎在西医常规治疗的基础上加用复方丹参注射液有较好的临床疗效,但缺乏安全性和有效性的系统评价。本研究中对复方丹参注射液辅助治疗小儿肺炎的效果进行系统评价,以明确其疗效。
1 资料与方法
1.1 纳入与排除标准
研究设计:纳入公开发表的复方丹参注射液治疗小儿肺炎的随机对照试验(RCT)。纳入研究对象:按国内关于小儿肺炎诊断标准,经X线胸部摄片、CT或痰培养证实的小儿肺炎患者,不受其年龄、性别、种族、教育程度等的限制,随机分为试验组与对照组,其一般资料比较,差异无统计学意义(P>0.05)。干预措施:试验组为复方丹参注射液静脉滴注联合西医常规治疗,对照组为西医常规治疗,包括抗感染、退热、止咳平喘、祛痰、吸氧、调节电解质/水平衡等处理。疗效指标:主要指标为临床总有效率,以临床治愈、显效与有效合计为临床总有效;次要指标为临床症状的改善,如退热时间、咳嗽与咳痰消失、肺部罗音消失时间、肺部X线检查恢复正常、精神和饮食好转,均以天为单位考查平均住院天数;以药品不良反应评价安全性。排除标准:单纯的病例描述性研究;成人肺炎患者;试验组在常规治疗基础上给予复方丹参注射液静脉滴注以外的途径给药或与其他的药物联合用药;有严重的肝、肾功能损伤、心脏、血液、心脑血管及免疫系统疾病患者;其他无法比较的因素。
1.2 检索策略
计算机检索中国生物医学文献光盘数据库(CBM,1978~2010)、中国期刊全文数据库(CNKI,1979~2010)、中国科技期刊数据库(1989~2010)、万方数据库(1982~2010)。中文主要检索关键词为复方丹参、香丹、肺炎、肺部感染等,运用逻辑符、通配符、范围算符等制订检索式,纳入的文献语种为中文和英文。
1.3 资料提取和质量评价
资料提取:制订统一的提取表,由2名研究人员对纳入文献资料分别进行提取并做交叉核对,出现分歧时通过讨论解决。提取的文献信息包括原文题目、出处、作者、发表时间、研究对象、研究方法、试验及对照措施、结局疗效评价指标、不良反应报告及评价人等。
质量评价:纳入研究的文献方法学质量按照Juni等[4]和Cochrane系统评价员手册5.0.0版关于RCT的质量评价标准[5]进行文献质量评价;随机方法是否正确;分配隐藏情况;是否采用盲法;有无失访或退出,如有是否采用意向治疗分析(ITT)。所有质量标准均满足者,发生偏倚的可能性最低,评为A级;如其中任何1条或多条质量评价标准仅部分满足(或不清楚),则该研究存在相应偏倚的可能性为中等,评为B级;如其中任何1条或多条完全不满足(未使用或不正确),则该研究存在相应偏倚的高度可能性,评为C级。
1.4 统计学方法
采用Cochrane协作网推荐的RevMan 5.0进行Meta分析。计数资料用比数比(OR)作为疗效分析的统计量并以95%可信区间(CI)表示。使用 χ2检验进行异质性检验,检验水准为α=0.05,若研究间无统计学异质性(P>0.05),则采用固定效应模型进行Meta分析;若研究间存在统计学异质性(P<0.05),则采用随机效应模型进行Meta分析。
2 结果
2.1 纳入研究的一般情况
共收集到122篇有关复方丹参注射液治疗肺炎的中文文献,对这些文献进行筛选,排除不符合纳入标准的患者及重复发表的文献,最终符合纳入标准的研究文献共17篇[3,6-21],研究对象均为小儿肺炎患者。
2.2 纳入研究的特点和质量评价
纳入研究的17篇文献均为中文文献,共2 266例,其中试验组1 096例,对照组1 170例,各研究纳入对象例数为25~300例。纳入文献中,有3项研究[7,9,17]提及随机方法为“单双日”或“入院顺序”;1项研究[9]采用单盲法,其余文献均未提及分配隐蔽性及是否采用盲法;4 项研究[3,9,13,21]涉及退热天数,6 项研究[3,9,13,15,17,21]涉及咳嗽消失时间,5 项研究[3,13,15,17,21]涉及肺部罗音消失时间,1项研究[9]涉及X线恢复正常时间,1项研究[15]涉及精神、饮食好转天数,2项研究[7-8]涉及住院天数。17项研究均对基线情况,包括年龄、性别、病程、病情、临床表现等进行了统计学分析,组间无显著性差异。按照Juni等[4]对随机对照试验的评价标准,17篇纳入的研究均为C级,属于低质量文献。各研究的基本特征见表1。
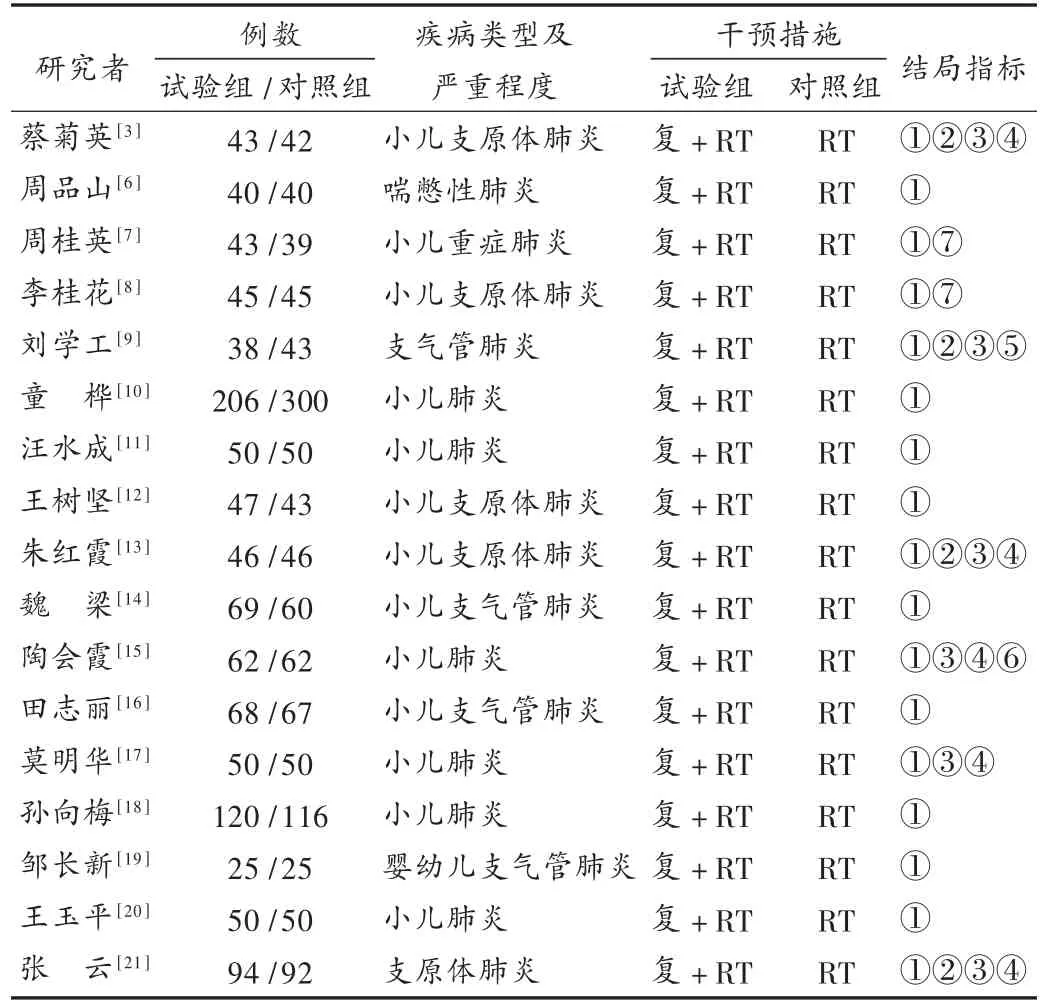
表1 纳入研究的基本特征
2.3 Meta分析结果
临床总有效率:17项研究以临床总有效率为结局指标对纳入文献进行评价。合并分析共2 266例,其中试验组1 096例,对照组1 170例,异质性检验结果显示,无统计学异质性(P=0.25,I2=17%),故按照固定效应模型进行Meta分析。结果显示,两组临床总有效率比较,试验组明显优于对照组[OR=5.36,95%CI(3.92,7.34),P <0.000 01],见图 1。
退热天数:有4项研究报道。合并分析共444例患者,其中试验组221例,对照组223例,异质性检验结果显示,有统计学异质性(P=0.06,I2=60%),故采用随机效应模型进行Meta分析。结果显示,两组退热天数比较,试验组明显优于对照组[WMD= - 0.33,95%CI(-0.58,-0.07),P=0.01],见图 2。

图1 两组临床总有效率的Meta分析
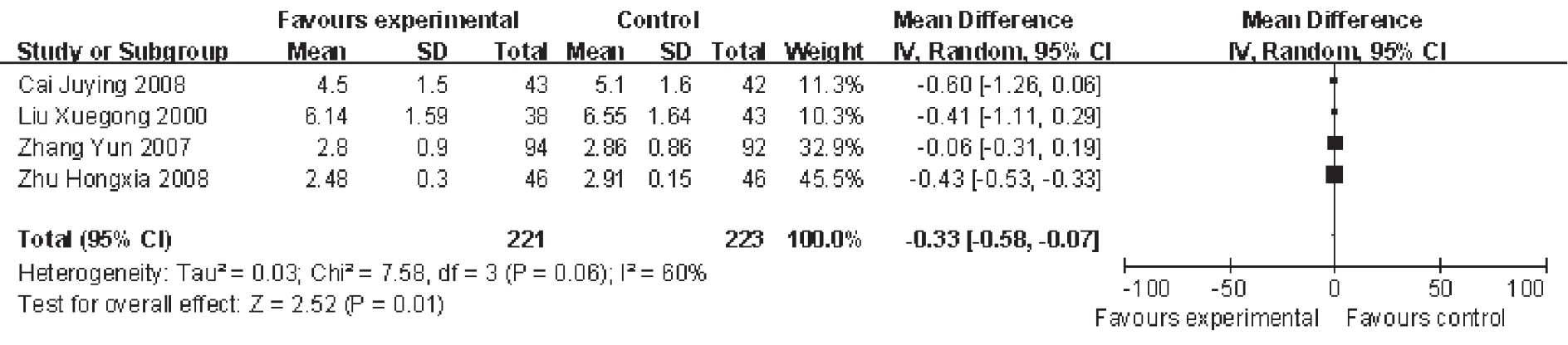
图2 两组退热天数的Meta分析
咳嗽消失:有6项研究报道。合并分析共668例,其中试验组333例,对照组335例,异质性检验结果显示,有统计学异质性(P<0.000 01,I2=93%),故采用随机效应模型进行Meta分析。结果显示,两组咳嗽消失天数比较,试验组明显优于对照组[WMD= -2.12,95%CI(-2.92,-1.32),P<0.00001],详见图 3。
肺部罗音消失:有5项研究报道。合并分析共587例,其中试验组295例,对照组292例,异质性检验结果显示,有统计学异质性(P=0.04,I2=61%),故采用随机效应模型进行 Meta分析。结果显示,两组肺部罗音消失天数比较,试验组明显优于对照组[WMD= -2.70,95%CI(-3.27,-2.13),P<0.000 01],见图 4。

图3 两组咳嗽消失天数的Meta分析
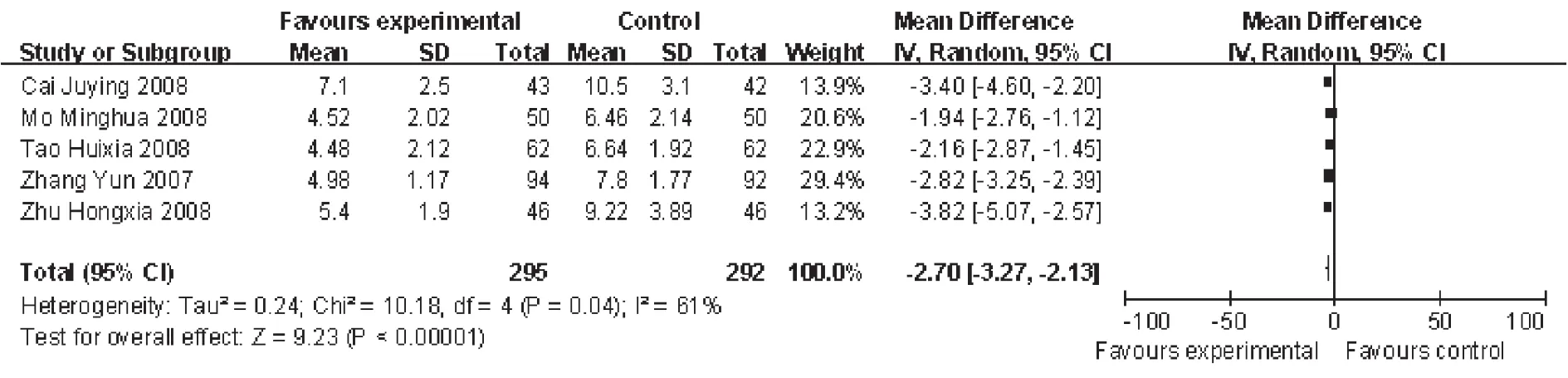
图4 两组肺部罗音消失天数的Meta分析
X线检查恢复正常:有1项研究报道。合并分析共81例,其中试验组38例,对照组43例,采用固定效应模型进行Meta分析。结果显示,两组X线检查恢复正常天数比较,试验组明显优于对照组[WMD= -3.18,95%CI(-6.00,-0.36),P=0.03],见图5。
精神、饮食好转:有1项研究报道。合并分析共128例,其中试验组64例,对照组64例,采用固定效应模型进行Meta分析。结果显示,两组精神、饮食好转天数比较,试验组明显优于对照组[WMD= -1.74,95%CI(-2.16,-1.32),P<0.00001],见图 6。
平均住院天数:有2项研究报道。合并分析共172例,其中试验组88例,对照组84例,异质性检验结果显示,有统计学异质性(P<0.000 1,I2=94%),故采用随机效应模型进行 Meta分析。结果显示,两组平均住院天数比较,试验组明显优于对照组[WMD= - 4.20,95%CI(-7.54,-0.85),P=0.01],见图 7。
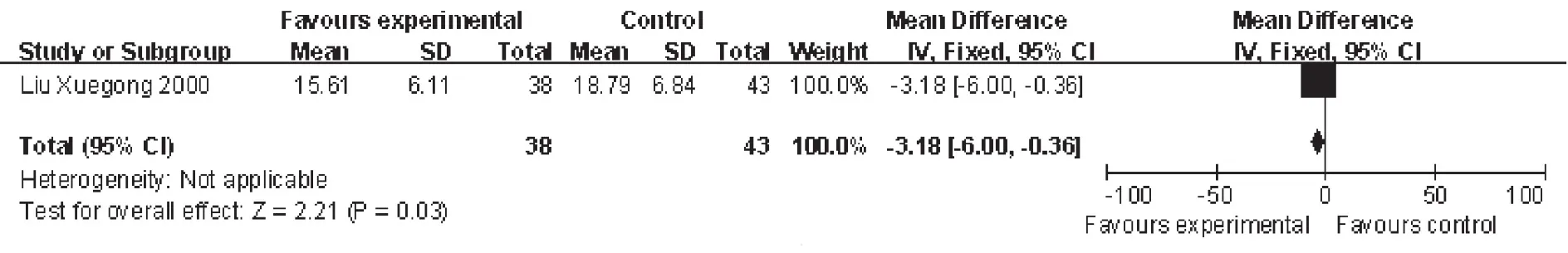
图5 两组X线检查恢复正常天数的Meta分析

图6 两组精神、饮食好转天数的Meta分析

图7 两组平均住院天数的Meta分析
2.4 发表偏倚评估
对17项研究中试验组和对照组的临床总有效率的影响进行漏斗图分析,见图8。倒漏斗图的分布明显不对称,结果提示可能存在发表的偏倚性,阴性结果的试验可能未发表。
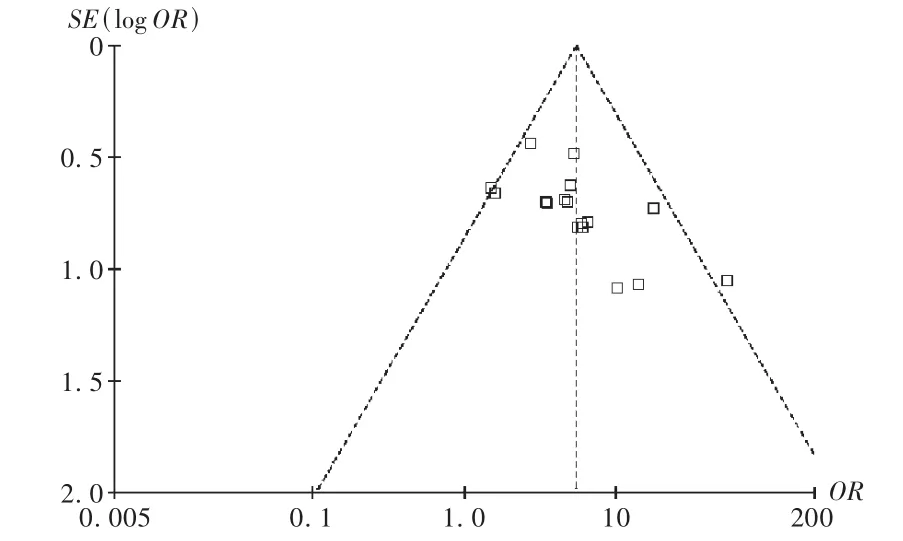
图8 两组临床总有效率比较的倒漏斗图
安全性:有 10 项研究报道。有 7 项研究[8-9,12,15-16,19-20]描述了在治疗期间未观察到不良反应。1项研究[14]报道了试验组有转氨酶升高2例、胃肠道反应2例;对照组出现转氨酶升高16例,胃肠道反应39例。1项研究[3]报道了试验组与对照组不良反应主要为使用阿奇霉素产生的副作用,主要表现为恶心、呕吐、上腹不适、腹痛、腹泻等消化道症状,但未描述产生不良反应例数,同时试验组出现2例皮肤潮红,对照组出现耳鸣2例、黄疸1例;1项研究[21]报道了试验组出现4例不同程度的恶心、呕吐、纳差、腹痛,而对照组出现8例。因纳入各项研究的不良反应无相同的评价指标,故未作Meta分析。
3 讨论
小儿肺炎为儿科多发病、常见病,是影响小儿身体健康的主要疾病之一,严重者可危及生命,故选择安全而有效的药物治疗尤为重要。
本系统评价结果表明,在临床西医常规治疗的基础上,应用复方丹参注射液治疗小儿肺炎能产生协同作用,其疗效无论是临床总有效率,还是退热、咳嗽消失、肺部罗音消失、X线检查恢复正常时间、精神饮食好转天数及平均住院天数等方面,试验组比对照组均有较明显的治疗效果。而在不良反应方面,治疗组与对照相比较,试验组未出现严重的不良反应,证明复方丹参注射液在辅助治疗小儿肺炎方面是安全的。
由于本研究的系统评价所纳入的文献质量均为C级,从而降低了系统评价结论的论证强度。纳入研究的局限性包括随机设计可能存在一定的问题,纳入的17项研究仅有3项提及随机方法,故存在偏倚的可能性;所纳入的研究仅1项采用单盲法,无1篇采用分配隐藏;治疗结果疗效指标无统一性;各纳入的研究指标不尽相同,少数指标只在个别文献中报道。临床总有效率的漏斗图呈现出分布不对称,提示可能存在发表的偏倚性。因此,复方丹参注射液在辅助治疗小儿肺炎方面虽优于单纯西医常规治疗。但由于纳入文献的质量及研究人群数量的限制,其结果的推广采取谨慎的态度。在以后的研究中应考虑现有研究的局限性,开展大样本、高质量的临床研究进一步确证,以得到最佳证据。
[1]丁淑兰.复方丹参注射液的临床应用[J].中国实用医药,2010,5(2):119.
[2]莫惠平,刘绍德,潘秋荣.复方丹参注射液的不良反应及防治措施[J].中国药房,2006,17(1):51.
[3]蔡菊英,刘慧清,陈玉勤,等.阿奇霉素联合香丹注射液治疗小儿支原体肺炎疗效观察[J].中国冶金工业医学杂志,2008,25(6):690.
[4]Juni P,Altman DG,Egger M.Systematic reviews in heath care:Assessing the quality of controlled clinical trials[J].BMJ,2001,323(7 303):42.
[5]Higgins JPT,Green S.Cochrane handbook for systematic reviews of interventions version 5.0.2[EB/OL] .http://www.cochrane- handbook.org.2009.
[6]周品山,林玉芳,李爱华.复方丹参辅助治喘憋性肺炎[J].滨州医学院学报,2000,23(2):185.
[7]周桂英.复方丹参治疗小儿重症肺炎43例疗效观察[J].右江民族学院学报,1995,17(3):311.
[8]李桂花,李 来.复方丹参注射液辅助治疗小儿支原体肺炎45例[J].中国中西医结合杂志,2002,22(11):821.
[9]刘学工,张积平,张淑芳,等.复方丹参注射液佐治肺炎支原体肺炎38 例[J].中国中西医结合杂志,2000,20(7):529.
[10]童 桦,孙淑娜.香丹注射液辅助治疗小儿肺炎206例临床观察[J].四川中医,2003,21(12):64.
[11]汪水成,袁春莉,董宝琴,等.香丹注射液佐治小儿肺炎100例临床分析[J].中华实用医学,2005,7(3):92.
[12]王树坚.阿奇霉素间歇给药联合复方丹参注射液治疗小儿支原体肺炎47例临床疗效观察[J].临床医药实践,2010,9(6B):757.
[13]朱红霞,黄鸣剑,谢金华,等.阿奇霉素联合复方丹参注射液治疗小儿支原体肺炎临床疗效观察[J].辽宁中医药大学学报,2008,10(7):89.
[14]魏 梁,张芳文.复方丹参注射液辅佐治疗小儿支气管肺炎69例[J].陕西中医,2008,29(7):812.
[15]陶会霞.复方丹参注射液佐治小儿肺炎124例临床观察[J].中国现代医生,2008,46(21):221.
[16]田志丽,郭志丽.复方丹参注射液佐治小儿支气管肺炎68例[J].中国社区医师,2008,10(24):153.
[17]莫明华.复方丹参注射液配合治疗小儿肺炎恢复期罗音不消50例[J].中医杂志,2008,49(2):146.
[18]孙向梅,范秀云.复方丹参注射液佐治小儿肺炎疗效观察与护理[J].齐鲁护理杂志,2006,12(9):1 706.
[19]邹长新.复方丹参和维生素K1治疗婴幼儿支气管肺炎疗效观察[J].中国现代医生,2008,46(7):100.
[20]王玉平.复方丹参治疗小儿肺炎湿罗音持续存在50例疗效观察[J].中国实用医药,2010,5(17):141.
[21]张 云,何兆坤,张 晓.复方丹参注射液佐治支原体肺炎的疗效观察[J].国际医药卫生导报,2007,13(11):74.

