CT引导下射频消融联合臭氧治疗极外侧型腰椎间盘突出症
陈振中 陈小勇 姜成龙 吴海波
海南省三亚市中医院,海南三亚 572000
随着人们生活水平的进一步提高,腰椎间盘突出症也在各类患者尤其是老年患者之中发病率呈逐年上升的趋势,其发病后往往会造成腰腿痛以及其他肢体活动不便,往往会给患者的生活及工作造成较大的影响。近年来,腰椎间盘突出的微创治疗得到迅速发展,其中臭氧融盘、射频、激光消融以及腔镜等技术已在很多医院开展。因其创伤小、见效快而被更多患者接受。近年来,医学界采取了不同的方法进行椎间盘突出症的治疗,取得了不错的效果,如射频消融以及臭氧治疗等,都取得了较好的疗效,尤其是臭氧治疗对患者的损伤小,在我国及国外都有非常广泛的应用。极外侧椎间盘突出为腰椎间盘突出症中的一种特殊类型[1],临床上并不少见,其发生率占整个腰椎间盘突出症的2.6%~11.7%[2],海南省三亚市中医院(以下简称“我院”)应用CT引导下射频消融联合臭氧注射治疗极外侧型腰椎间盘突出,效果显著,现报道如下:
1 资料与方法
1.1 一般资料
选择2009年1~12月在我院接受治疗的92例极外侧型腰椎间盘突出症患者作为研究对象,将其分为治疗组和对照组。治疗组53例,男33例,女20例;年龄20~59岁,平均43岁;病程2周~15年,平均8个月。对照组39例,男28例,女11例;年龄42~58岁;病程3周~2年,平均6个月。突出部位:L3/4椎间盘28例,L4/5椎间盘55例,L5/S1椎间盘39例,92例患者共计122个椎间盘。所有患者均接受了跟踪随访,随访时间为3~28个月。
1.2 入选及排除标准
所有患者术前均经保守治疗效果不满意,所有患者均有典型的神经根刺激症状,伴有或不伴有腰部疼痛。排除骨性椎管狭窄、腰椎峡部裂、滑脱和不稳。
1.3 手术适应证
①腰痛伴下肢放射痛,病程≤3年,直腿抬高试验<70°。②CT或MRI检查发现相关的极外侧型椎间盘突出,影像学显示突出物不超过椎管容积的40%。反之以下则为禁忌证:①突出物严重钙化、脱出、游离等;②合并心功能不全、肿瘤、出血倾向、精神障碍、安装起博器等其他疾病;③伴Ⅱ度或Ⅱ度以上椎体滑脱,椎管狭窄和严重脊柱退行性变;④有射频及臭氧治疗禁忌等。
1.4 治疗方法
患者俯卧于CT扫描床上,常规定位消毒局麻后,以专用穿刺针穿刺,经侧后方安全三角区穿刺入路,进针点的选择以脊柱中线为基准,在距该基准1 cm处小关节内缘部位以及距该基准4~6 cm处的小关节外缘部位选择为进针点。在实施穿刺进针时,尤其是内源性进针,往往会有较强的突破感,并且在进针的同时推注水气混合物,可使硬膜囊被推移,通过CT检测如果针尖已达到突出物的中间部位,而回抽不回血及脑脊液,这样表明穿刺成功,可以开始进行治疗。
1.4.1 治疗组 首先要通过检测确定被治疗的患者无神经根刺激征表现,治疗过程中如果患者出现过度刺激症状如出现烧灼感,则表明刺激部位与神经根距离太近,则需要将射频针退后少许再进行治疗。根据CT定位及引导将射频穿刺套针穿入椎间盘突出物的中后1/3处。确认正常后,给予70~90℃射频治疗2~3 min。另外,在原定位的基础上进行附近区域的治疗,定位区域为原定位点的0.5 cm左右。射频热凝术后。再注射浓度为50 μg/mL的臭氧20 mL,经CT扫描达到标准后于神经根旁注入40 μg/mL的臭氧5 mL,再次通过CT对盘内、盘外臭氧的分布进行扫描,满意拔针。
1.4.2 对照组 依上法直接在突出物中注射浓度为50 μg/mL 的臭氧 20 mL。
术后两组患者均常规静滴甘露醇125 mL加地塞米松5 mg,连续使用3 d,24 h后戴腰围下床,3个月内避免弯腰负重及重体力劳动。
1.5 疗效评价
记录患者下肢疼痛评分(采用视觉模拟评分法测量,VAS用于疼痛的评估在我国临床使用较为广泛,基本的方法是使用一条游动标尺,一面有10个刻度,两端分别为“0”分端和“10”分端,“0”分表示无痛,“10”分代表难以忍受的最剧烈的疼痛,让患者在直尺上标出能代表自己疼痛程度的相应位置,为其评出分数),疗效判定根据改良的Macnab疗效评定标准[3]进行评定。优:症状消失,工作和运动完全恢复;良:偶有腰部不适及下肢疼痛,工作无限制,一般情况下不需要特殊治疗;差:症状无明显改善,需用药对症处理。
1.6 统计学方法
应用SPSS 13.0统计软件进行数据处理,计量资料采用均数±标准差(±s)表示,组间比较采用t检验,计数资料采用百分率表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
两组患者均于术后3个月进行随访检查。治疗组与对照组治疗后疗效比较差异有统计学意义(P<0.05),治疗组明显优于对照组,见表1。治疗组以及对照组治疗前后下肢疼痛比较差异有统计学意义(P<0.05);治疗组与对照组治疗后比较差异有统计学意义(P<0.05),治疗组优于对照组,见表2。
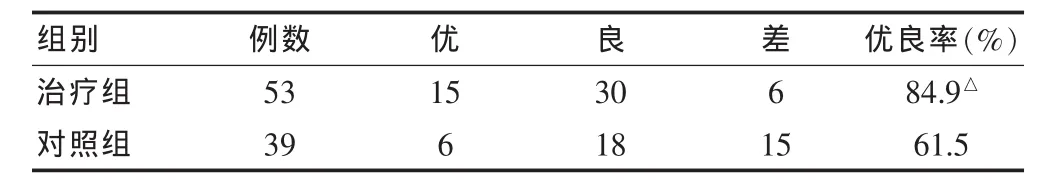
表1 两组临床疗效比较(例)
表2 两组治疗前后下肢疼痛评分比较(分,±s)

表2 两组治疗前后下肢疼痛评分比较(分,±s)
注:与本组治疗前比较,#P<0.05;与对照组治疗后比较,△P<0.05
治疗组对照组53 39 4.12±0.52 4.05±0.45 1.28±0.35#△1.64±0.65#组别 例数 治疗前 治疗后
3 讨论
极外侧型腰椎间盘突出是临床上较为特殊的一型,以往对其认识不充分而容易漏诊。临床分为椎间孔型和孔外型。极外侧型腰椎间盘突出症由于突出椎间盘组织位于椎间孔或椎间孔以外,与常见后外侧型椎间盘突出症累及下一序数神经根不同,本型病变常累及同序数的神经根。临床症状与其突出大小往往不成比例,临床表现主要以下肢持续疼痛为主,不能平卧,站立或行走时加重,和(或)下位神经根。本病确诊有赖于影像学,包括CT、MRI。近年来的文献报道也多集中于手术治疗方面,手术操作对组织结构的损伤和破坏较大,手术无论经椎板或峡部外缘均有一定难度到达患处,若过多切掉小关节会影响脊柱稳定性,易造成腰椎术后稳定性差,并发症多。由于腰神经根管的结构复杂,所以我们选择CT引导下有利于精准操作,避免盲穿所带来其他并发症。
多年来临床研究表明,对于大部分极外侧腰椎间盘突出症患者多数在发现时以是晚期,往往具有严重的症状及病理特征,因此多数需要通过手术进行治疗[4],随着研究的不断深入,对于该类手术的方式和方法有很多种类型,每种类型都有其优势和劣势,并且随着手术方式的不断发展,各个缺点也在不断的被弥补[5-6]。最早报道该类手术入路的是20世纪80年代的Watkins,该种方法可以在最大限度条件下减少对患者的骨组织造成的损伤,并且可以直接在直视的条件下进行突出髓核的摘除。随后Ohara等[7]提出Watkins的方法对于快速寻找脱出的椎间盘组织效果不好,从而经过临床研究发现脊神经后支作为一个手术入路可以快速地找到脊神经根和神经节,并且安全性更高。Ohara等[7]以及Porchet等[8]均通过横突间入路治疗极外侧腰椎间盘突出症,均取得了较好的效果,具有较高的优良率。因为通过横突间入路单纯切除椎间盘突出髓核,对患者造成的损伤较小,与其他手术入路相比,有各种明显的优越性,因此逐渐成为该类手术方法中的首选方法[9-10]。
据报道臭氧和射频消融治疗椎间盘突出症有效率在68%~79%之间[11],射频尚无确切报道。臭氧治疗腰椎间盘突出的主要机制:①即刻氧化作用:氧化髓核内的蛋白多糖,使髓核发生变性、坏死而萎缩,在降低椎间盘压力的同时也改变了局部的血液循环,增加氧供应而改善症状。②抗炎作用:通过拮抗免疫因子释放起到抗炎作用。③镇痛作用,臭氧的强氧化作用能迅速使上述炎性介质失活而达到止痛作用[12];而且还可通过破损的纤维环弥散和扩散到椎管内或椎旁发挥作用。临床发现随时间延长其疗效逐渐下降,推测可能与椎间盘减压不彻底有关。
射频消融其主要作用机制是将热凝与消融相结合以去除部分髓核,从而减小髓核体积,毁损窦椎神经和局部热效应发挥作用[13],以达到减压治疗目的,但作用范围较局限;对盘源性腰椎间盘突出疗效显著,对非包容性突出则需甄别应用[14-16]。
在本病的临床治疗过程中我们发现臭氧盘内溶盘治疗极外侧型腰椎间盘突出症疗效不佳,其主要原因是盘内治疗对突出于椎间孔内或椎间孔外的椎间盘组织的作用有限,经CT、MR复查发现突出物对神经根的卡压的根本问题未解决。表1表明其优良率不足65%,据此,本研究采用在CT引导下射频消融联合臭氧治疗,把重点放在椎间孔内外突出物的消融。依据极外侧型突出不同的层面表现,在CT引导下选择突出较大的层面;围绕突出物内外穿刺针可灵活变换角度,绕过椎间关节而扩大视野。直接靶点射频消融可使髓核内的压力减低,椎间盘突出部分有效回缩,达到对椎间盘周围组织如神经根、动脉、马尾神经等的减压目的[17],同时高温可灭活炎性因子、改善局部水肿。结合臭氧强氧化,抗炎和镇痛作用,可使蛋白多糖变性,髓核组织萎缩,从而迅速降低椎间盘压力[18],可达到优势互补的作用 。
本治疗组的3个月优良率仍保持在84%以上,说明射频和臭氧联合应用疗效明显高于单纯臭氧应用[19]。两者比较差异有统计学意义(P<0.05),两者联合弥补了单一技术的不足,使椎间盘内减压更彻底,扩大了经皮穿刺微创技术治疗腰椎间盘突出症的适应证,使以前需要手术的患者可以通过微创技术解决。但本组中效果不佳的6例中最终有3例仍选择了手术,术后症状缓解显著,说明对于神经根卡压严重,或疗效差的患者,手术仍是一种彻底治疗的手段。
CT引导下射频联合臭氧治疗极外侧型腰椎间盘突出症能确保穿刺达到理想位置,射频部位准确、臭氧能够达到理想的弥散状态。其操作较开放手术安全,创伤小,准确,不影响脊柱稳定性,经济负担少,疗效也较单纯臭氧注射显著提高,是治疗极外侧型腰椎间盘突出的一种新兴手段,值得临床推广,但仍需掌握一定适应证。
[1]胡有谷.腰椎间盘突出症[M].北京:人民卫生出版社,2001:217-225.
[2]Maroon JC,Kopitnik TA,Schulhof LA,et al.Diagnosis andmicrosurgical approach to far.Itlteral disc herelation in the hmbarspine[J].J Neurosurg,1990,72:378-382.
[3]滕皋军.经皮腰椎间盘摘除术[M].南京:江苏科学出版社,2000:89.
[4]孙凤翔,张文祥,季祝永,等.极外侧型腰椎间盘突出症发病机理及诊治探讨[J].中国矫形外科杂志,2003,11(7):494-496.
[5]Garg M,Kumar S.Interlaminar discectomy and selective foraminotomy in lumbar disc hemination [J].J Orthop Surg,2001,9(2):15-18.
[6]Ozveren MF,Bilge T,Barut S,et al.Combined approach for far lateral lumbar disc hemiation[J].Neurol Med Chir(Tokyo),2004,44(2):118-123.
[7]Ohara LJ,Marshall RW.Farlaterallumbar disc herniation[J].J Bone Joint Surg(Br),1997,79(11):943-947.
[8]Porchet,Fankhauser H,de Triboletn.Extreme lateral lumbar disc herniation:clinical presentation in 178 patients[J].Acta Neurochir Wien,1994,127(3):203-209.
[9]Tessitore E,de Triboletn.Far-lateral lumbar disc herniation:the microsurgical transmuscular approach[J].Neurosurgery,2004,54(4):939-942.
[10]谢晓勇,李平生,郭文荣,等.经椎板侧方手术入路治疗极外侧腰椎间盘突出症[J].中国骨与关节损伤杂志,2005,20(5):352-353.
[11]Velio B.Oxygen-Ozone therapy:a critical evaluation[M].Dordrecht:Kluwer Academic Publishers,2002:241-324.
[12]肖越勇.合理选择联合介入技术使椎间盘突出症微创治疗达到个体化或间盘化[J].中国疼痛医学杂志,2005,11:320.
[13]谢珺田,秀英,李祥俊.射频消融术[J].山东医药,2005,45:63-64.
[14]Yung CC,Sang-Heon L,Darwin C.Intradiscalpressure study ofdiscdecompressionwithnucleo-plastyinhumancadavers[M].NewYork:Nass Meeting of the Americans Ⅱ,2002.
[15]Stanley CJ,Ronald CF,Jamie MB.Sixmonth fol-low-up on lumbar disc nucleoplasty in 45 patients[M].NewYork:Nass Meeting of the AmericansⅡ,2002.
[16]Lewis S.Percutaneous disc decompression using nucleoplasty[M].NewYork:Nass Meeting of the Americans Ⅱ,2002.
[17]佘远举,刘军,张浩,等.射频消融髓核成形术改善腰椎间盘突出症患者症状效果评估[J].中国临床康复,2005,9(18):154-157.
[18]俞志坚,何晓峰,杨波,等.医用臭氧治疗腰椎间盘突出症:术后症状“反跳”的分析及处理[J].临床放射学杂志,2004,23(10):897-899.
[19]Nakano N,Nakano T,Nakano K.Long term results of anterior extra peritoneal lumbar discectomy[J].Acta Orthop Belg,1987,53:290-292.

