大肠癌术后患者营养状态与血清中肿瘤坏死因子-α、IL-18和IL-23的关系
周喜云 (平顶山市第一人民医院营养科,河南 平顶山 467099)
大肠癌术后患者病变发展中,营养状况不良与血清中相关炎性细胞因子有一定关联。肿瘤坏死因子(TNF)-α、白细胞介素(IL)-18、IL-23均是促炎因子,对机体的免疫和营养功能的调节均有重要作用,有观点认为大肠癌术后不良营养状态患者血清中TNF-α、IL-18和IL-23的表达升高,对营养失衡起一定促进作用〔1,2〕。本文探讨大肠癌患者营养状况与血清中TNF-α、IL-18和IL-23表达的关系及营养支持的作用。
1 材料与方法
1.1 材料 2010年1月至2011年12月行大肠癌根治术患者87例。年龄54~78(平均65.7)岁,男47例,女40例,术前均未进行放化疗,均为腺癌,其中高分化20例,中分化40例,低分化27例。根据营养状态分为营养状态正常组22例,年龄54~77(平均65.6)岁,男12例,女10例。潜在营养不良组35例,年龄54~78(平均65.6)岁,男19例,女16例。营养不良
组30例,年龄54~77(平均65.9)岁,男16例,女14例。3组一般资料无明显差别。
1.2 血清中 TNF-α、IL-18和IL-23蛋白表达的检测 TNF-α、IL-18和IL-23试剂盒均购自武汉博士德生物技术有限公司,于手术后次日(治疗前)和营养支持7 d后(治疗后)抽取患者的静脉血5 ml。应用酶联免疫吸附法(ELISA)法检测血清中TNF-α、IL-18和IL-23的表达。操作均由同一技师完成,避免人为误差,严格质量控制。
1.3 营养状况评估 采用微型营养评价法(MNA)评估患者围术期的营养状况〔3〕。每项2~5个等级,总分30分,根据评估逐项计划MNA得分和总分,做出评估和营养诊断。营养评估标准分为3级:MNA>24分为营养状况正常;17~24为潜在营养不良;<17分为营养不良。
1.4 营养支持疗法 对潜在营养不良和营养不良患者应用营养支持,即外周静脉输入10%葡萄糖溶液,7%复方氨基酸,10%脂肪乳剂,微量元素钾、钠、钙、镁等,按胰岛素1 U加葡萄糖6~10 g配制液体。
1.5 统计学方法 应用SAS6.12软件进行t检验或方差分析及线性相关分析。
2 结果
2.1 不同营养状态患者血清中TNF-α、IL-18和IL-23表达的比较 营养状况正常、潜在营养不良、营养不良各组患者血清中TNF-α、IL-18和IL-23的表达差别有统计学意义(P<0.05)。见表1。
表1 不同营养状态患者血清中TNF-α、IL-18和IL-23表达的比较(±s,mg/L)
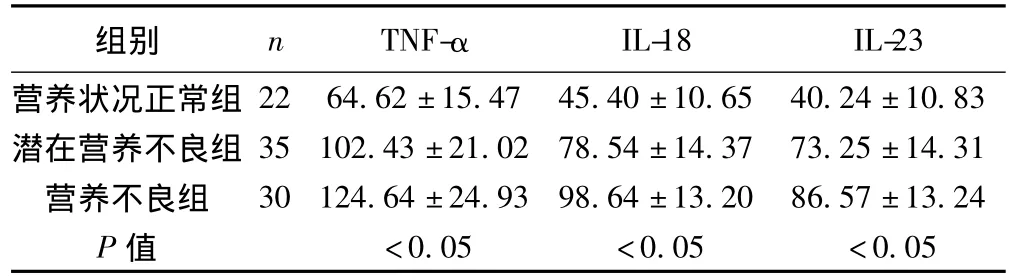
表1 不同营养状态患者血清中TNF-α、IL-18和IL-23表达的比较(±s,mg/L)
IL-18 IL-23营养状况正常组组别 n TNF-α 22 64.62±15.47 45.40±10.65 40.24±10.83潜在营养不良组 35 102.43±21.02 78.54±14.37 73.25±14.31营养不良组 30 124.64±24.93 98.64±13.20 86.57±13.24 P值 <0.05 <0.05 <0.05
2.2 潜在营养不良组和营养不良组干预后血清中TNF-α、IL-18和IL-23表达的比较 治疗1 w后两组血清中TNF-α、IL-18和IL-23的表达均下降(P<0.05),且接近营养状况正常的患者。见表2。
表2 潜在营养不良组和营养不良组干预后血清中TNF-α、IL-18和IL-23表达的比较(±s,mg/L)

表2 潜在营养不良组和营养不良组干预后血清中TNF-α、IL-18和IL-23表达的比较(±s,mg/L)
IL-18 IL-23潜在营养不良组组别 n TNF-α 35 67.63±13.24 47.48±5.48 46.36±10.88营养不良组30 65.37±11.32 50.53±5.21 49.26±10.19
2.3 观察组干预前、后MNA评分与TNF-α、IL-18和IL-23表达的相关性 干预前:MNA和 TNF-α(r=-0.45,P<0.05)、MNA和 IL-18(r= -0.42,P<0.05)、MNA 和 IL-23(r=-0.49,P<0.05)的表达呈负相关;干预后:MNA和TNF-α(r=-0.42,P <0.05)、MNA 和 IL-18(r= -0.44,P <0.05)、MNA和IL-23(r=-0.45,P<0.05)的表达呈负相关。
3 讨论
大肠癌患者根治手术患者,由于手术的创伤大,应激反应强,常引起能量消耗增加,同时由于术后早期不能进食,能量的摄入减少,因此患者常出现营养不良〔4〕,随着营养状况的改变,机体内环境中的相关蛋白也发生明显改变,其中最重要的是TNF-α、IL-18和IL-23的表达,三者也是引起机体炎性级联反应和免疫反应的重要启动蛋白。也有观点认为大肠癌术后机体蛋白尤其是免疫球蛋白的合成能力下降,不仅减缓了患者的恢复,也可能引起肿瘤细胞扩散加速〔5,6〕。因此,术后给予营养支持治疗有重要价值。术后患者进行营养支持须具备两个条件:①机体能接受并可以有效利用营养物质;②营养支持将对机体功能的恢复及免疫系统进行良性的调节〔7,8〕。
本实验结果提示TNF-α、IL-18和IL-23对营养不良有重要的调节作用。而营养支持可以提高患者的营养水平,同时可以有效下调血清中TNF-α、IL-18和IL-23的表达,提示三种蛋白与营养状态的关系随着营养状态的恢复而调节到正常水平。IL-18和IL-23在营养性失衡发展中的生物学特性主要有促进辅助淋巴细胞细胞分泌IL-1、IL-2等相关因子,诱导T细胞增殖,增强Fas-FasL系统介导的细胞毒作用,促进巨噬细胞分泌TNF-α水平提高,即IL-18对诱发炎性级联反应有重要促进作用。TNF-α是一种主要由单核巨噬细胞产生的细胞因子,常与其他细胞因子共同参与机体的生长发育和维持内环境稳定,同时又介导感染、创伤及免疫应答反应。机体营养不良时,TNF-α、IL-18和IL-23的表达升高,加速营养不良的进展,而积极的营养支持,不仅对术后起明显的恢复作用,还可以对血清中相关蛋白进行良性调节。由于三种蛋白均可作为免疫性炎症级联反应的启动蛋白,营养支持对TNF-α、IL-18和IL-23的下调,可以有效地抑制由TNF-α、IL-18和IL-23启动的促进营养不良发展时的级联反应,可以优化体内的微环境〔9〕。
1 王建军.大肠癌血清肿瘤坏死因子α、白细胞介素8和可溶性白细胞介素2受体水平的检测及其临床意义〔J〕.中国肿瘤临床与康复,2012;19(3):55-7.
2 韩明勇,钟 伟,郭其森,等.血清中IL-18含量的检测对结肠癌预后判断的价值〔J〕.实用癌症杂志,2004;19(3):44-6.
3 王庆华,杨玉霞,张新晶,等.老年结肠癌患者围术期营养评估与肠外营养支持〔J〕.护理学杂志,2008;23(18):70-2.
4 简 明,罗俊卿,李 畅.老年结肠癌患者术后早期肠内、外营养的联合应用〔J〕.中国普通外科杂志,2008;17(7):731-3.
5 梁伟雄,张 彤,洪 云,等.术前肠内免疫营养对结肠癌病人免疫功能的影响〔J〕.肠外与肠内营养,2006;13(6):346-9.
6 谷 欣.围手术期肠外营养支持对结肠癌患者术后康复的价值探讨〔J〕.昆明医学院学报,2011;20(7):107-9.
7 彭莉娜,赵端仪.肠内营养联合肠外营养对结肠癌手术后患者免疫功能的影响〔J〕.公共卫生与预防医学,2010;21(3):20-2.
8 张晓勇.老年结肠癌患者术后的肠内肠外营养支持〔J〕.中国老年学杂志,2011;31(9):1669-70.
9 陆爱国,郑民华,李东华,等.大肠癌患者细胞因子水平与临床关系的研究〔J〕.中华普通外科杂志,2001;32(10):14-5.

