Box-Behnken效应面法优化多西他赛微乳注射液制备工艺
果秋婷,张小飞(1.咸阳职业技术学院医学系,陕西咸阳712000;2.陕西中医学院药学院陕西省中药制药重点学科,陕西咸阳 712046)
多西他赛(Docetaxel)为紫杉醇类抗肿瘤药,是由赛诺菲-安万特公司在1995开发上市的一种紫杉醇烷类抗癌药,商品名:Taxotere®(泰素帝®)。其作用机制是通过干扰细胞有丝分裂和分裂间期细胞功能所必需的微管网络而起到抗肿瘤作用。临床上用于治疗乳腺癌、非小细胞肺癌、胰腺癌、软组织肉瘤、头颈癌、胃癌以及前列腺癌等多种肿瘤的治疗。由于多西他赛在水中的溶解度极低(约10mg/L),因此在制剂中加入了大量的聚山梨酯80(每支540mg)作为增溶剂来增加药物溶解性。然而聚山梨酯80在注射进入体内后,机体会产生明显的过敏反应[1],因此开发一种不含聚山梨酯80的多西他赛注射剂一直是研究的热点[2-3]。
微乳(Microemulsion)是一种较为稳定的O/W型乳剂,其粒径一般在0.1~1μm范围内,主要是以植物油(脂肪酸甘油三酯)为油相,以磷脂为乳化剂,可供静脉注射用,能完全被机体代谢利用,因此又被称为静脉注射用脂肪乳剂(Intravenous lipid/fat emulsion)。近年来,微乳制剂作为药物传递系统在制药领域也正发挥着越来越重要的作用[4]。本研究将多西他赛制备成微乳注射液,并通过Box-Behnken效应面法优化其制备工艺,旨在为多西他赛注射给药系统的开发与应用提供新的思路。
1 材料
1.1 仪器
高压均质机(加拿大ATS工业系统有限公司);高速剪切机(德国IKA集团公司);Agilent-1200高效液相色谱系统(美国Agilent科技有限公司);Mastersizer 2000粒度分析仪、Zetasizer Nano电位分析仪(英国马尔文仪器公司);JM21200EX透射电镜(日本电子公司);GC2120GX日立低温离心机(日本日立公司)。
1.2 药品与试剂
多西他赛对照品(中国食品药品检定研究院,批号:100666-201201,纯度:≥99.7%);多西他赛原料药(江苏奥赛康药业有限公司,批号:120122-1,纯度:≥99.5%);蛋黄卵磷脂(德国Lipoid公司,批号:1032881);大豆油(铁岭北亚药用油有限公司,批号:11020103-2-01);注射用甘油(浙江遂昌惠康药业有限公司,批号:100801,规格:每瓶500ml);油酸(德国Lipoid公司,批号:202640,纯度:≥99.0%);无水乙醇(国药集团化学试剂有限公司,批号:0214-2012);氢氧化钠(批号:20110203)、盐酸(批号:20120122)均来源于湖南尔康制药有限公司;注射用水为自制。
2 方法与结果
2.1 方法学考察
根据第35版《美国药典》中的多西他赛注射液含量测定方法操作。色谱柱:Kromasil C18(200mm×4.6mm,5μm);流动相:0.043mol/L醋酸铵溶液-乙腈(45∶55),流速:1.0ml/min;检测波长:232nm;柱温:25℃;进样量:20μl。称取多西他赛对照品约12.0mg,精密称定,置于同一个100ml量瓶中,加少量甲醇溶解后,加流动相稀释至刻度,摇匀,即得对照品贮备液。在此色谱条件下,精密量取对照品贮备液适量,定量稀释成含多西他赛0.6、1.2、6.0、12.0、24.0、48.0mg/L的溶液,以多西他赛峰面积(A)对其质量浓度(c)进行线性回归,得标准曲线方程为:A=40894c+3364.1(r=0.9999),表明多西他赛检测质量浓度线性范围为0.6~48.0mg/L。专属性试验考察结果表明,在此色谱条件下,辅料对多西他赛的测定无干扰,理论板数为6000,分离度>1.5,拖尾因子均在0.95~1.05;高、中、低水平的平均回收率为100.2%,RSD=0.8%(n=3);日内精密度RSD=0.9%(n=3),日间精密度RSD=1.1%(n=3)。
2.2 微乳的制备
2.2.1 处方确定。根据微乳的经典处方[5]和预试验结果,本品的处方初步筛选结果见表1。
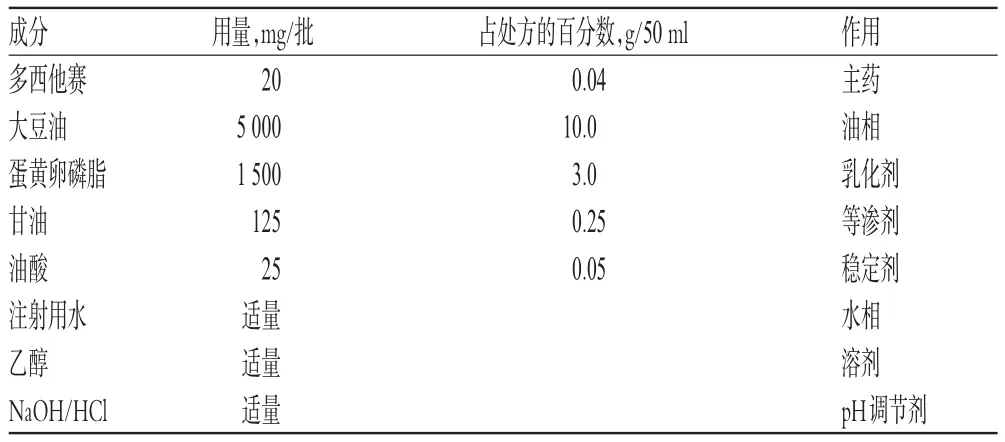
表1 处方初步筛选结果Tab 1 Results of initial screening of the formulations
2.2.2 制备工艺。水相制备:将处方量甘油、油酸加至80%注射用水中,置于磁力搅拌器中加热至65℃,搅拌溶解,即得。油相制备:将处方量油相加热至65℃;将处方量的多西他赛和蛋黄卵磷脂溶于适量无水乙醇中;将油相与多西他赛乙醇溶液混合,65℃保温,氮气流下挥干乙醇,得到澄清的含药油相。微乳制备:在高速剪切机搅拌下(20000r/min),将油相加入至水相中,持续高速剪切10min,制得初乳。将制备好的初乳转移至高压均质机中,控制制备温度,以一定的压力进行均质,并循环均质多次,即制备成多西他赛微乳。将微乳pH值调至6.0左右,用注射用水定容至全量。分装,冲氮气,封口,121℃旋转水浴灭菌10min,冷水浴迅速降温,即得。
2.3 Box-Behnken效应面法优化工艺
通过单因素考察,选取对微乳性质影响较显著的3个因素:制备温度(Temperature,X1)、均质压力(Pressure,X2)和均质次数(Times,X3)为考察对象,以粒径(Y1)、多分散系数(PDI,Y2)及包封率(EE,Y3)为评价指标,利用Box-Behnken效应面法优化工艺。试验设计水平见表2,试验设计与效应值见表3,三维效应面图见图1~图3。
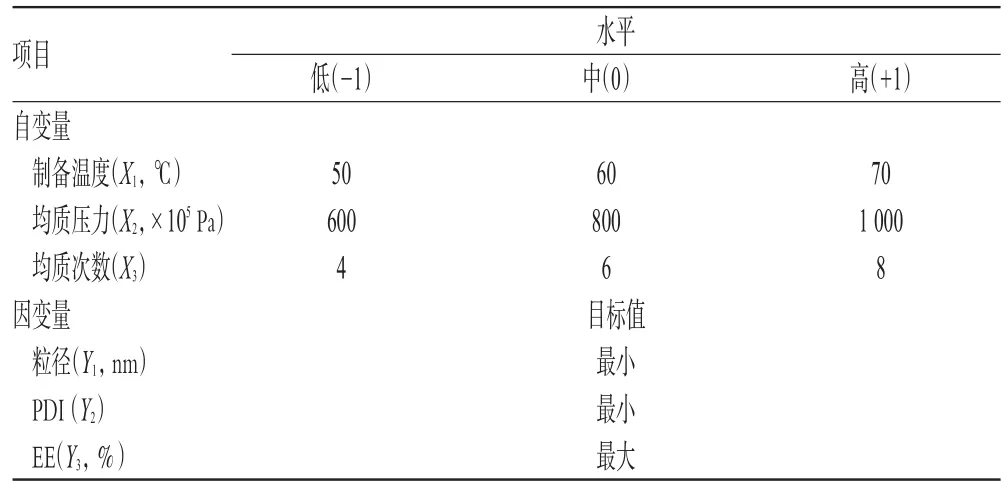
表2 试验设计水平表Tab 2 Experimental design level
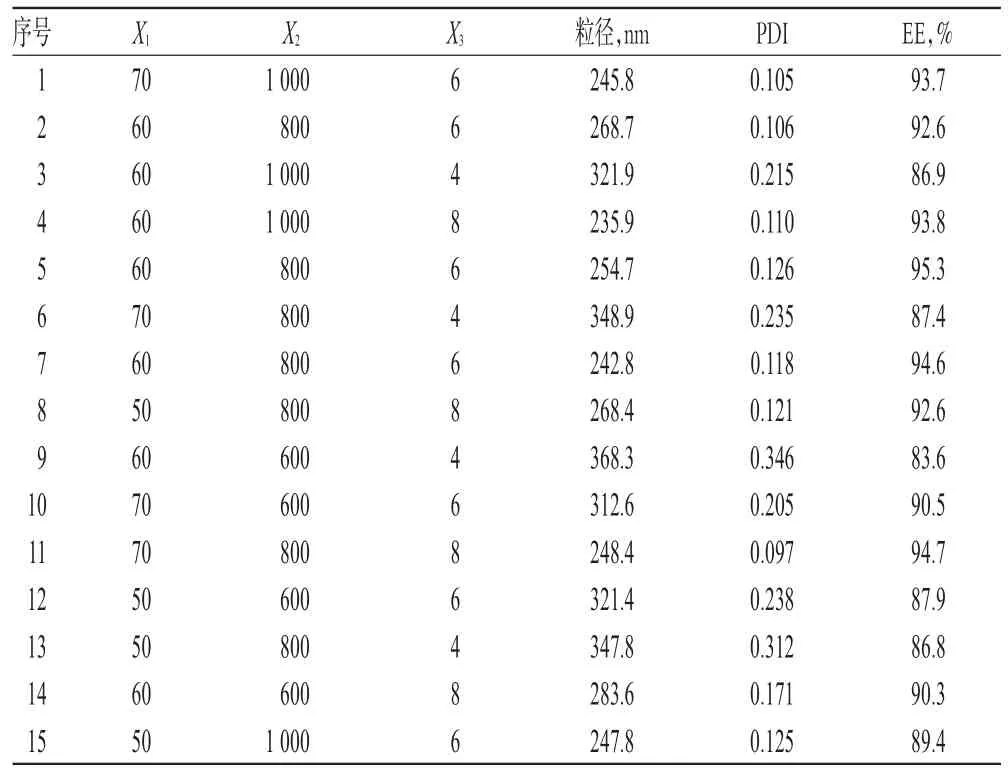
表3 试验设计与效应值Tab 3 Experimental design and effect value
2.4 EE的测定
本文采用低温超速离心法[5]测定药物在微乳中的EE,方法如下:
药物总量的测定:精密吸取多西他赛微乳注射液1ml,置于50ml量瓶中,加入甲醇适量,混匀,超声,0.22μm微孔滤膜过滤,取续滤液,按“2.1”项下色谱条件测定药物总量。
水相中药物含量的测定:取多西他赛亚微乳注射液4ml,置低温超速离心机中以50000r/min离心1.5h,于温度4℃,取下层澄清溶液0.5ml,置于25ml量瓶中,以甲醇稀释定容,0.22μm微孔滤膜过滤,取续滤液,按“2.1”项下色谱条件测定水相中药物含量。计算公式:
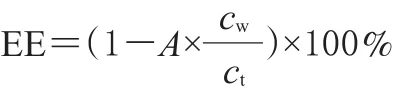
式中,A为微乳处方中水相所占比例;cw为水相中多西他赛的质量浓度;ct为多西他赛总质量浓度。
2.5 优化工艺参数验证
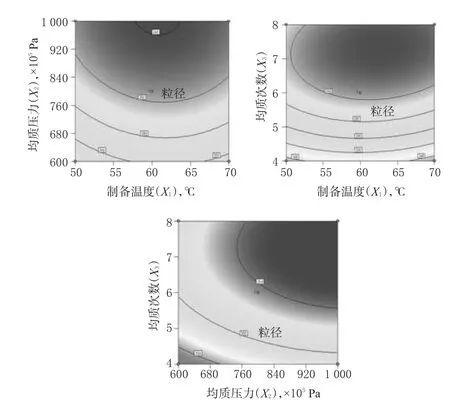
图1 自变量X与因变量粒径(Y1)的等高线Fig 1 Contour of independent variable X and the dependent variable particle size( Y1)
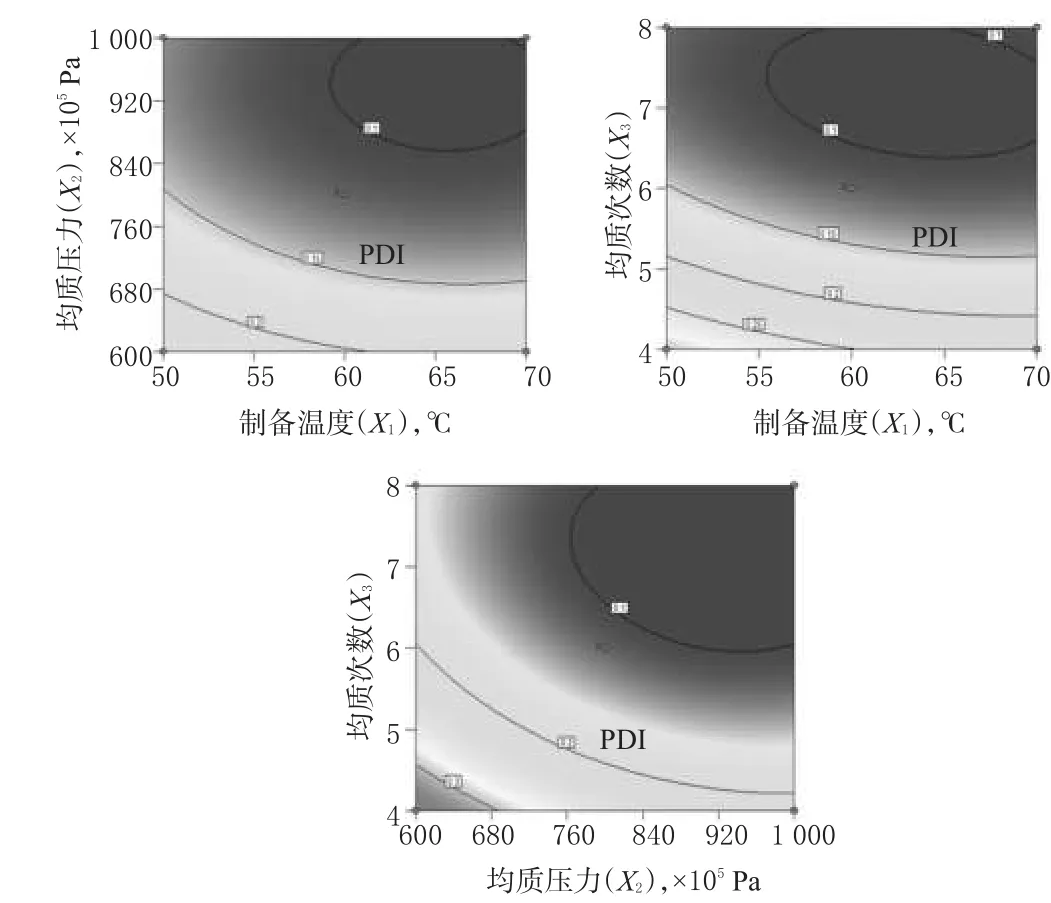
图2 自变量X与因变量PDI(Y2)的等高线Fig 2 Contour of independent variable X and the dependent variable polydispersity index( Y2)
根据“Design expert 8.0.5”试验设计软件得最佳工艺参数为:制备温度61℃,均质压力860×105Pa,均质次数7次。按照“2.2”项下方法以优化后的工艺参数制备3批微乳制剂,按照“2.4”和“2.6”项下方法测定微乳的EE、粒径及PDI。试验观测值、模型预测值及偏差见表4。
由表4可知,试验观察值和模型预测值比较接近,说明模型预测性良好。
2.6 优化后微乳粒径分布及Zeta电位测定
取多西他赛微乳溶液适量,用蒸馏水稀释50倍,采用Mastersizer粒度仪测定脂质体的粒径分布和Zeta电位,同时计算PDI,PDI=Dw/Dn(Dw为重均粒子直径,Dn为数均粒子直径)。详见图4。
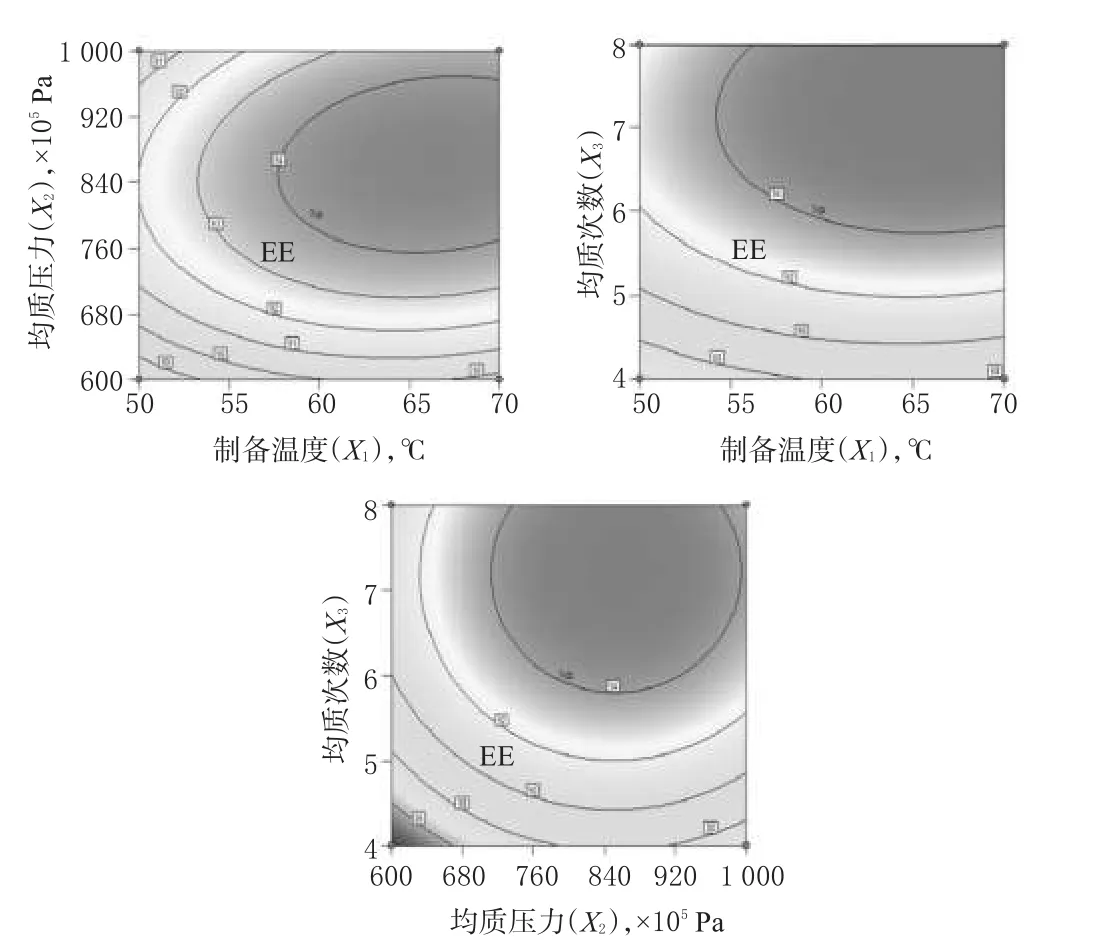
图3 自变量X与因变量EE(Y3)的等高线Fig 3 Contour of independent variable X and the dependent variable encapsulation efficiency( Y3)

表4 多西他赛微乳注射液制备工艺的验证试验结果(n=3)Tab 4 Results of verification test of preparation process of Docetaxel microemulsion injection(n=3)
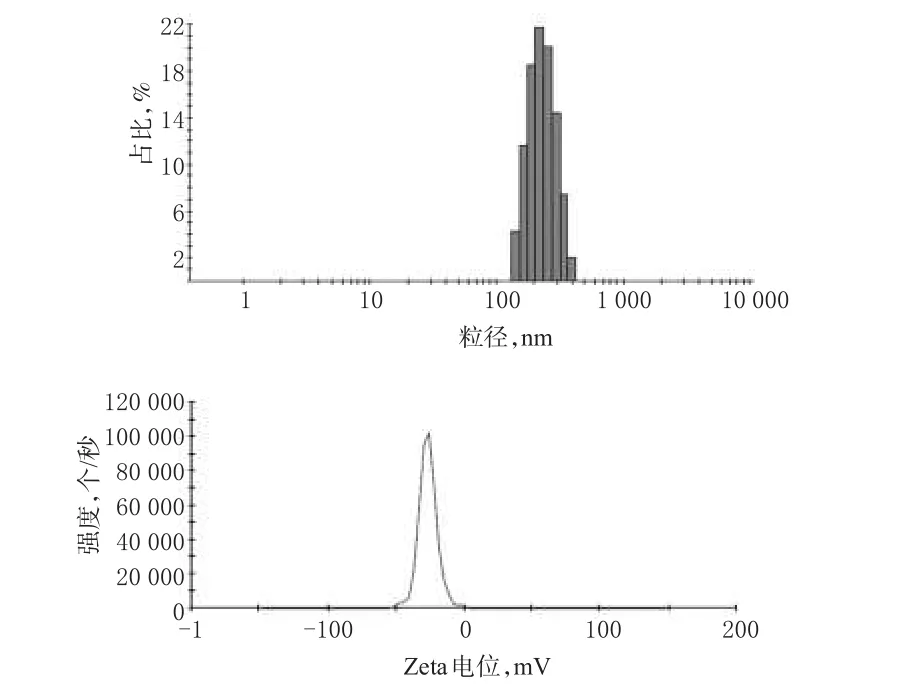
图4 多西他赛微乳注射液的粒径分布和Zeta电位Fig 4 Particle size distribution and Zeta potential of Docetaxel microemulsion injection
由图4可见,微乳平均粒径为(221.6±13.4)nm,Zeta电位为-30.3mV,计算得PDI为0.095,表明微乳制剂比较稳定。
2.7 透射电镜观察
采用磷钨酸负染法制备透射电镜样品。将样品稀释适当倍数后,取适量滴于以火棉胶作为支持膜的铜网上,浸泡于2%磷钨酸溶液中染色2~5min。待铜网干后用透射电镜观察微乳的形态结构和粒度分布,详见图5。
由图5可见,微乳大小均匀,呈圆整、规则球形,大部分粒子的粒径在200nm左右,未见过大的粒子,透射电镜观察进一步确证了粒度测定的结果。
2.8 稳定性试验
取多西他赛微乳,分别放置于2~8℃和25℃保存,进行稳定性试验,并分别在1、2、3个月取样,测定微乳的粒径分布、PDI及EE,结果见表5。
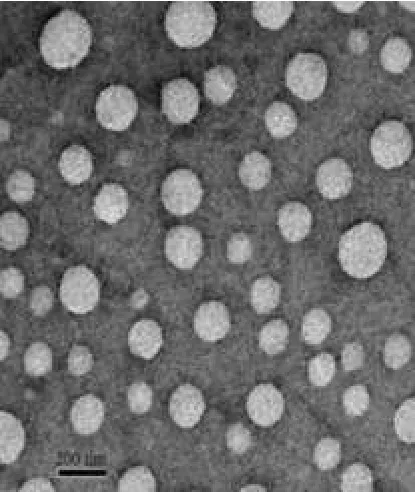
图5 多西他赛微乳注射液的透射电镜图Fig 5 TEM of Docetaxel microemulsion injection
表5 多西他赛微乳注射液的稳定性研究结果(±s,n=3)Tab 5 Stability study results of Docetaxel microemulsion injectio(n±s,n=3)
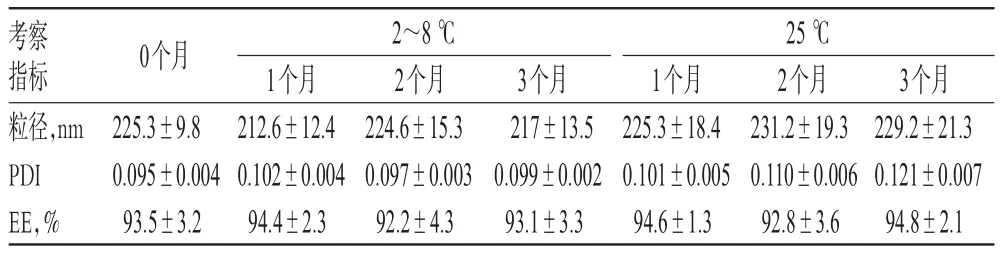
表5 多西他赛微乳注射液的稳定性研究结果(±s,n=3)Tab 5 Stability study results of Docetaxel microemulsion injectio(n±s,n=3)
考察指标粒径,nm PDI EE,%0个月2~8℃25℃225.3±9.80.095±0.00493.5±3.21个月212.6±12.40.102±0.00494.4±2.32个月224.6±15.30.097±0.00392.2±4.33个月217±13.50.099±0.00293.1±3.31个月225.3±18.40.101±0.00594.6±1.32个月231.2±19.30.110±0.00692.8±3.63个月229.2±21.30.121±0.00794.8±2.1
由表5可见,多西他赛微乳在低温(2~8℃)和室温(25℃)条件下放置3个月均较稳定,粒径、PDI及EE基本无变化。
3 讨论
多西他赛在水和油中的溶解度均较低[6],采用高压均质法制备多西他赛微乳,使多西他赛颗粒溶解并以分子形式存在于磷脂形成的高分子油水界面膜内,提高了亚微乳的载药能力,从而避免了泰素帝®中聚山梨酯80给患者带来的休克、呼吸困难、低血压、血管性水肿、风疹等不良反应。
微乳以其安全低毒、生物相容性好的特点可以作为药物的优良载体[7],但由于在热力学及动力学上均属于不稳定体系,因此物理稳定性是影响载药微乳产品开发及投向市场的重要因素。影响微乳物理稳定性的因素有很多,主要包括处方组成和工艺条件等。其中前者主要包括表面活性剂的组成及用量、油相的种类、处方的pH值等。根据文献[8-9]报道,乳剂的工艺条件如初乳的制备方法、高压均质化的压力及次数、制备温度等均会影响乳剂的粒度大小及分布并进一步影响其稳定性。本研究采用高压均质法制备微乳,通过优化均质压力、均质次数及制备温度3个重要工艺参数,将多西他赛成功制备成粒径均一、EE较高、稳定性较好的微乳制剂。
Zeta电位是微乳表面荷电性质与荷电大小的标志,是影响微乳行为的重要参数。为了得到稳定的微乳,Zeta电位一般须控制在-20~-45mV范围内,即通过荷电的稳定剂提供微粒间静电层排斥力,可以初步判断该体系是稳定的[10]。本研究制备的微乳的Zeta电位为-30.3mV,稳定性试验数据进一步表明微乳制剂比较稳定。
[1] ten Tije AJ,Verweij J,Loos WJ,et al.Pharmacological effects of formulation vehicles:implications for cancer chemotherapy[J].Clin Pharmacokinet,2003,42(7):665.
[2] Straubinger RM,Balasubrltmanian SV.Preparation and characterization of taxane-containing liposomes[J].Methods Enzymol,2005,391(3):97.
[3] 张先林.抗肿瘤药多西紫杉醇制剂的应用研究近况[J].药学进展,2006,30(11):516.
[4] 刘沙,熊非,朱家壁,等.静脉注射用载药脂肪乳的研究近况[J].药学进展,2010,34(3):104.
[5] MacFie J.The development of fat emulsion[J].Nutrition,1999,15(7/8):641.
[6] 陆彬.药物新剂型与新技术[M].北京:人民卫生出版社,2005:532-534.
[7] Zhao M,Su M,Lin X,et al.Evaluation of docetaxelloaded intravenous lipid emulsion pharmacokinetics,tissue distribution,antitumor activity,safety and toxicity[J].Pharm Res,2010,27(8):1687.
[8] Nielloud F,Marti-Mestres G.Pharmaceutical emulsions and suspensions[M].New York:Marcel Dekker Inc,2000:214-215.
[9] 苏德森,王思玲.物理药剂学[M].北京:化学工业出版社,2003:144-146.
[10] 马涛.全合一混合液的稳定性[J].中国药房,2000,11(2):88.

