双卤代均三嗪活性染料及其水解产物的HPLC分离方法的建立
胡玲玲, 范雪荣
(1. 江南大学 纺织服装学院, 江苏 无锡 214122; 2. 绍兴文理学院 纺织服装学院, 浙江 绍兴 312000)
双卤代均三嗪活性染料及其水解产物的HPLC分离方法的建立
胡玲玲1,2, 范雪荣1
(1. 江南大学 纺织服装学院, 江苏 无锡 214122; 2. 绍兴文理学院 纺织服装学院, 浙江 绍兴 312000)
为研究双卤代均三嗪活性染料的水解反应,采用反相离子对高效液相色谱对双卤代均三嗪活性染料及其水解产物进行了色谱分离。从双卤代均三嗪活性染料的选择、色谱柱的选择、流动相的选择和优化、柱温的确定等方面,探讨了对称结构双卤代均三嗪活性染料及其水解产物的HPLC分离方法的建立过程,利用该方法对双一氟均三嗪活性染料活性红LS-2G及双一氯均三嗪活性染料活性红KE-3B的水解产物进行了分离,得到了较好的分离效果。
活性染料; 双卤代均三嗪活性染料; 水解; 动力学; 高效液相色谱法
活性染料的水解活性通常通过测定染料的水解速率进行研究。由于活性染料水解主要发生在活性基团上,而活性基团并不是发色团的典型部分,且不是影响UV-VIS染料吸收光谱的主要部分,因此,测定染浴中水解染料量不能借助于光谱学的方法。研究工作者相继采用了薄层层析法[1]、滴定总碱度法[2]、氟/氯离子选择电极滴定法[3]和比色测定法[4]等测定活性染料的水解反应速率,但这些方法局限性较大,有的灵敏度不高,有的操作极不方便,难以推广,给研究工作带来一定的困难。
使用高效液相色谱法(HPLC)对活性染料及其水解产物进行定性及定量分析,具有简单、快速、准确等优点,目前已成为测试活性染料水解量的主要方法。HPLC研究的首要问题是确定色谱分离的条件。由于HPLC在印染行业应用较晚,对染料及其反应产物的色谱分离缺乏积累,因此可供参考的分离方法很少,又由于实验条件和样品的不确定性,导致多数情况下需要开发新的色谱分离方法。但由于HPLC在方法开发时涉及影响因素较多,需要大量探索性实验,如果没有系统的理论和经验给予指导,将会耗费大量的时间、金钱和精力。鉴于目前HPLC在印染行业的应用现状,系统地了解和掌握色谱方法开发过程中的影响因素,快速建立有效的研究方法,提高实验的准确性和精度可能比实验本身更为重要。本文以双一氟均三嗪活性染料活性红LS-2G和双一氯均三嗪活性染料活性红KE-3B及其水解产物的色谱分离为例,分析了双卤代均三嗪活性染料及其水解产物的色谱分离方法的建立过程,为其应用提供了理论依据。
1 实验部分
1.1 实验药品与仪器
药品:活性红KE-3B(C.I.活性红120),活性红LS-2G(C.I.活性红268),四丁基溴化铵C16H36BrN,磷酸二氢铵NH4H2PO4,氢氧化钠NaOH,碳酸氢钠NaHCO3,磷酸氢二钠Na2HPO4·12H2O,磷酸二氢钠NaH2PO4·2H2O,盐酸HCl,均为分析纯;乙腈,色谱纯;新制去离子水,18.3 MΩ·cm。
仪器:Ultimate3000高效液相色谱仪,美国DIONEX(戴安)公司;UV-3600紫外可见近红外分光光度计,日本岛津公司;L-12C恒温振荡水浴,厦门RAPID(瑞比)公司;SK7210HP超声波清洗器,上海科导超声仪器有限公司;PHS-3C精密pH计,上海虹益仪器仪表有限公司;MS204S电子天平,瑞士Metter Toledo公司。
1.2 染料水解实验
在250 mL锥形瓶中加入150 mL pH=11.0的缓冲溶液(缓冲溶液由500 mL浓度为0.05 mol/L的NaHCO3和227 mL浓度为0.1 mol/L的NaOH混合后加水稀释至1 000 mL而成),置于恒温振荡水浴中,预热至指定温度,加入0.6 g染料,进行水解反应。在指定的时间间隔,用移液管移取2.5 mL水解液,分置于已加入20 mL pH=6的缓冲溶液(该缓冲溶液由123 mL浓度为0.2 mol/L的Na2HPO4·12H2O和877 mL浓度为0.2 mol/L的NaH2PO4·2H2O混合而成)的25 mL容量瓶中,终止水解反应,定容并冷却至室温后进行色谱分析。
2 双卤代均三嗪活性染料的选择
由于具有对称结构的双卤代均三嗪活性染料在该类型染料中的比例达90%以上[5],故本文选择具有对称结构的双卤代均三嗪活性染料进行研究,使研究结果具有更广泛的适应性。对称结构双卤代均三嗪活性染料的选择也将使实验结果的分析和讨论得到简化,这是因为其第一步水解反应无论发生在哪个活性基上,所得的一卤代一羟基双均三嗪染料形式均是相同的结构,如果忽略染料的降解,水解反应过程中最多只有3种物质,即双卤代均三嗪染料形式a、一卤代-羟基双均三嗪染料形式b、双-羟基均三嗪染料形式c,见图1,这将避免增加分离的困难。
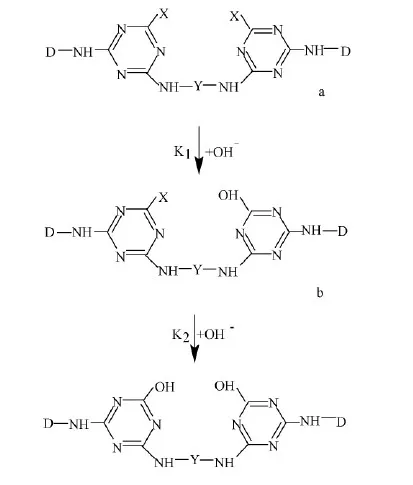
注:X为卤素;Y为连接基团。图1 对称结构的双-氯均三嗪活性染料在碱性缓冲溶液中的亲核取代反应Fig.1 Nucleophilic substitution of bis(halogeno-s-trazine) reactive dye with symmetrical chemical structure in alkali buffer solution
非对称结构的双卤代均三嗪活性染料在第1步水解时将出现2个峰(为水解产物),这2个峰在进一步的水解过程中又各自衍生出1种水解产物,导致整个过程有5种物质存在。初始染料a、半水解染料b和完全水解染料c在结构上只有1个或2个取代基的差异,它们在色谱柱中的保留时间非常接近,本身就不好分离,组分增多会使分离更加困难。
3 色谱条件的确定
3.1 色谱柱的选择
在色谱分析方法中,色谱柱的选择是方法成功与否的关键,也是提高样品分离度的关键。活性染料及其水解产物本身均是强极性的有机化合物,不适合用正相色谱进行分离。目前使用最多的是反相离子对高效液相色谱法[6-8],该方法已被证实对活性染料及其水解产物的分析是一种快速有效的方法[9-11]。在反相离子对色谱分离过程中,采用非极性的疏水固定相,含有对离子M+的甲醇-水或乙腈-水溶液作为极性流动相。流动相中待分离的活性染料离子D-与固定相或流动相中带相反电荷的对离子M+结合,形成离子对化合物M+D-,混合物中的各组分在固定相和流动相之间进行分配,当流动相中所含混合物经过固定相时,就会与固定相发生作用。由于各组分在性质和结构上的差异与固定相发生作用的大小、强弱也有差异,因此在同一推动力的作用下,不同组分在固定相中的滞留时间不同,因而按先后不同的次序从固定相中流出,达到分离的效果[12]。
反相离子对色谱在选择色谱柱时需要考虑以下几个方面:
1) 烷基的碳原子数:常用的反相色谱柱有C8~C18键合的硅胶柱,活性染料样品均采用水溶液进行HPLC分析,键合的烷基链越长,烷基疏水作用越强,色谱柱的分离效果越好,故在活性染料分析中多采用C18键合的硅胶柱ODS-2。
2)色谱柱的长短和填料的粒径:在填料和内径一定的情况下,色谱柱越长,分离度越大,但柱长、柱压和样品的保留时间也会相应增大,这意味着系统要承受更高的压力和消耗更多的流动相,因此在满足分离要求的情况下,柱长越短越好。相同长度的色谱柱,填料的粒径越小,理论塔板数越高,分离效果越好,故一般采用3 μm的粒径,短柱就可达到很好的分离效果。对称结构的双卤代均三嗪活性染料及其水解产物,主要成分只有3种,采用长150 mm,5 μm粒径的短柱基本可达到分离要求。
3)色谱柱的内径:色谱柱的内径越大,样品分散程度越差(即样品无法在到达柱头时呈现均匀面状分布),峰的对称性将下降,分离度变差,但内径大的,柱容量增大,意味着进样体积增大。目前市场上通用的4.6 mm内径的色谱柱,基本能满足活性染料色谱分离的需要。
综上所述,对色谱柱的选择主要看分离成分的复杂性和极性的大小。待分离成分多,最好选择长一点的柱子,分离的成分少,建议选择短柱,长柱不能满足分离要求的,可以选择更小的填料粒径。
色谱柱确定后,还需确定相应的流速。150 mm×4.6 mm,粒径为5 μm的C18键合硅胶柱ODS-2,流速为1 mL/min,而250 mm×4.6 mm,粒径5 μm的C18键合硅胶柱,流速为1.5 mL/min。流速越大,系统压力越高,流动相流经色谱柱的时间越短,出峰越早。样品出峰保留时间一般在8~15 min为宜(但有时为了提高分离的效率,也可适当缩短分离时间至6~8 min,尤其是在梯度洗脱时)。需注意的是太大的流速有时会影响样品的分离度,因此合适的流速应同时兼顾分离度和分离效率。
3.2 检测器及检测波长的选择
双卤代均三嗪活性染料水解产物的3种形式有相同的母体结构,在可见光区具有相近的最大吸收波长,在最大吸收波长处3种染料形式的摩尔消光系数相近,因此一般选择紫外可见检测器,在染料的最大吸收波长处对其进行检测[13-14]。使用时要注意仪器的检测限或灵敏度,样品的进样量应在仪器的检测范围内,避免出现检不出或超限的情况,在符合仪器检测限要求的情况下,应尽量选择低的样品浓度,这样可以提高检测的灵敏度,峰形也会更好。
3.3 流动相的选择
3.3.1 有机溶剂的选择
流动相是有机溶剂和离子对缓冲溶液的混合液。活性染料HPLC分析中常用的有机溶剂是甲醇和乙腈,相对甲醇而言,虽然乙腈具有分子质量大,黏度高,不易产生气泡,洗脱能力比甲醇强等优点,但国内多选择甲醇做有机相,主要是因为乙腈的价格较高,毒性较大。本实验发现,以甲醇/水的体积比=70∶30对双卤代均三嗪活性染料及其水解产物进行分离,即使1 h也不能出峰,而换做乙腈/水溶液体积比=50∶50时10 min左右即能出峰,说明对双卤代均三嗪活性染料而言,甲醇的洗脱能力明显不足,故选择乙腈较为合适。
3.3.2 对离子的选择
常用带正电的离子对试剂有四甲基溴化铵、四乙基溴化铵和四丁基溴化铵等。离子对试剂烷基碳原子数越多,染料样品在色谱柱上的保留越多,样品的分离效果也越好,因此采用反相离子对液相色谱对染料样品进行分析时,一般均采用碳原子数最多的四丁基溴化铵。对离子的浓度是控制反相离子对色谱溶质保留值的主要因素,可在较大范围内改变分离的选择性,其具体浓度需经实验确定。
3.3.3 洗脱体系的确定
在进行色谱分离时,设计洗脱程序的一个原则是能用等度洗脱时就不用梯度,必须采用梯度时也要尽可能用一步梯度,而不要用多步梯度,这样可以大大提高仪器的稳定性。对称结构的双卤代均三嗪活性染料及其水解产物待分离成分虽然只有3种,但由于3种物质结构上只相差1个原子或原子团,分子的极性相差不大,故导致3种物质紧邻出峰,采用梯度洗脱能较易分离。
在设计梯度时,比较快捷的方法是参照已有类似样品的色谱方法进行实验,在没有现成方法可参照时,先进行探索性实验,然后根据实验结果中色谱峰的峰高、半峰宽、理论塔板数、分离度和对称性等参数进行多次调整,最终获得最适色谱条件。以双一氟均三嗪活性染料活性红LS-2G及其水解产物的色谱分析为例,染料在80 ℃, pH=11.0条件下水解30 min后,水解液用Acclaim C18键合硅胶ODS-2,5 μm, 250 mm×4.6 mm色谱柱进行分析,检测波长为502 μm,流速为1.500 mL/min,柱温为30 ℃,进样量为20 μL,紫外可见检测器,流动相A为100%乙腈溶液,流动相B为含30%的0.025 mol/L的四丁基溴化铵的乙腈溶液和70%的0.05 mol/L的磷酸二氢铵溶液的混合液,梯度洗脱体系如表1所示。所得谱图如图2所示。

表1 梯度洗脱体系1Tab.1 Gradient elution system 1
色谱峰的质量由峰高H、半峰宽W、理论塔板数N、分离度R和不对称因子S等参数来衡量[15]。图2中峰的参数见表2。
从表2数据可看出,3种物质已达到完全分离,保留时间TR在7~10 min之间,不对称因子S也在可接受的范围内,但峰形稍矮胖(峰高H较矮,半峰宽W较大),理论塔板数N也有待提高。半峰宽大,意味着待分离成分的流出时间较长,应增加有机相的比例使流动相洗脱能力增强。因出峰时间是在7 min后,故初始流动相比例不变,从7 min开始提高A∶B比例至50∶50,梯度洗脱体系2如表3所示。由梯度洗脱体系2所得色谱峰见图3。图3中峰的参数见表4。
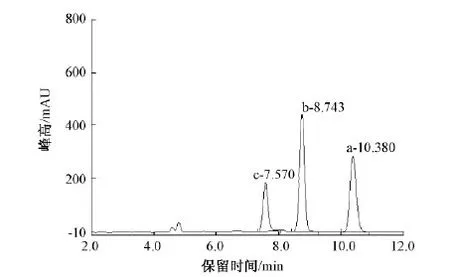
图2 由梯度洗脱体系1所得谱图Fig.2 Chromatogram obtained from gradient elution system 1
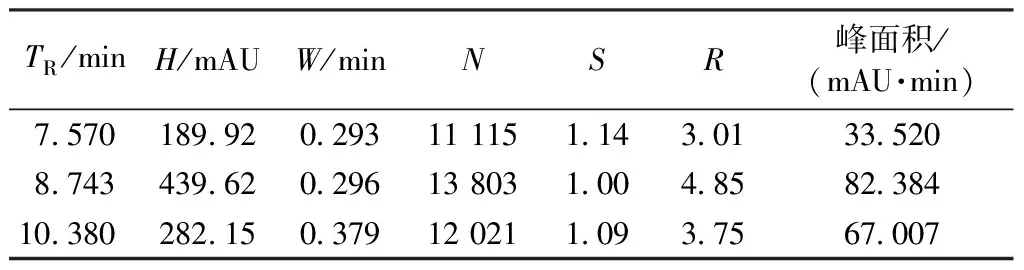
TR/minH/mAUW/minNSR峰面积/(mAU·min)7570189920293111151143013352087434396202961380310048582384103802821503791202110937567007

表3 梯度洗脱体系2Tab.3 Gradient elution system 2
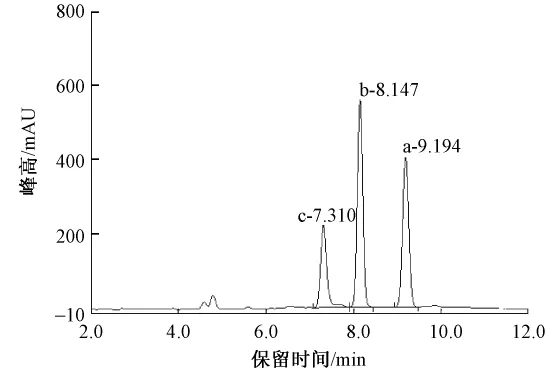
图3 由梯度洗脱体系2所得谱图Fig.3 Chromatogram obtained from gradient elution system 2
从图3和表4可看出,用梯度洗脱体系2对样品进行分析,在完全分离的情况下,3种染料出峰时间均有所提前,峰高H增加,半峰宽W减小,理论塔
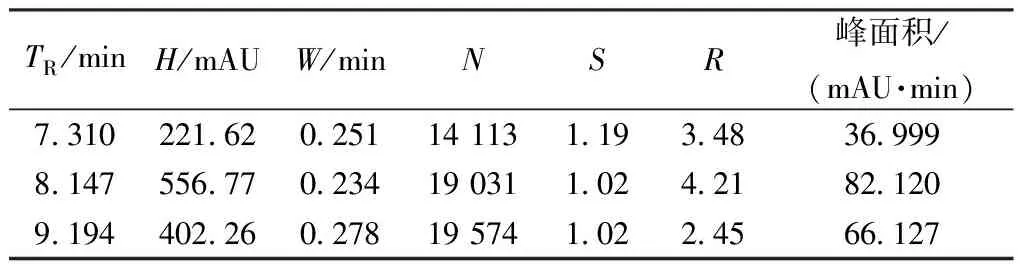
表4 图3的峰参数表Tab.4 Parameters of peaks in Fig.3
板数N增加,但并不理想。2~7 min对目标物质的分离几乎无影响,要分离的3个峰是在7 min后出峰,即A/B的比例为50∶50后才出峰。为缩短分析时间,从2 min开始即将梯度变化到A/B的比例为50∶50,重新进行实验,梯度洗脱体系3如表5所示。由梯度洗脱体系3所得谱图见图4。图4中峰的参数见表6。

表5 梯度洗脱体系3Tab.5 Gradient elution system 3

图4 由梯度洗脱体系3所得谱图Fig.4 Chromatogram obtained from gradient elution system 3
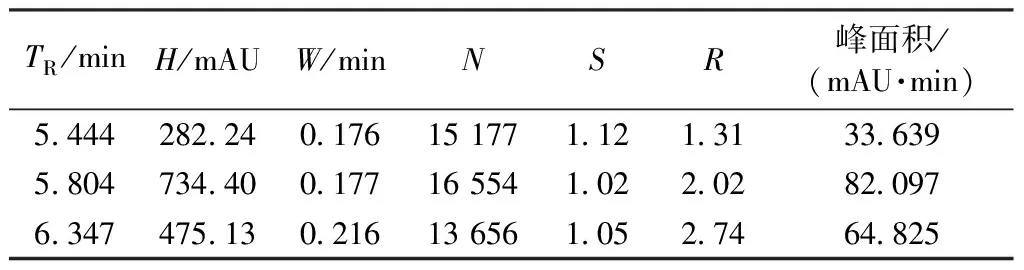
TR/minH/mAUW/minNSR峰面积/(mAU·min)544428224017615177112131336395804734400177165541022028209763474751302161365610527464825
从图4和表6可看出,从2 min开始增加有机相的比例,3种染料出峰时间明显缩短,峰高H明显增加,半峰宽W减少到0.2 min以内,理论塔板数N也增加,柱效在很大程度上得到了提高。但完全水解染料c和部分水解染料b没有完全分开,完全水解染料峰有拖尾现象,其右侧积分方式变为垂直积分,而非底到底积分,进而影响到b峰左边的积分方式也变为垂直积分,积分面积也有相应变化。这说明梯度变化过快,流动相洗脱能力过强,因此延长第一步梯度时间到5 min重新进行实验梯度洗脱体系4如表7所示。由梯度洗脱体系4所得谱图见图5。图5中峰的参数见表8。

表7 梯度洗脱体系4
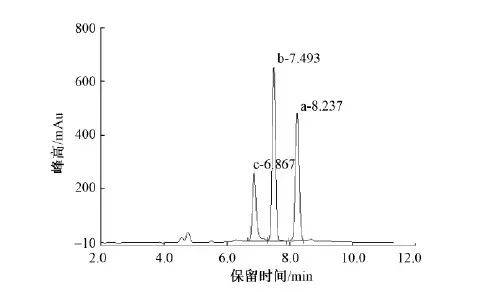
图5 由梯度洗脱体系4所得谱图Fig.5 Chromatogram obtained from gradient elution system 4
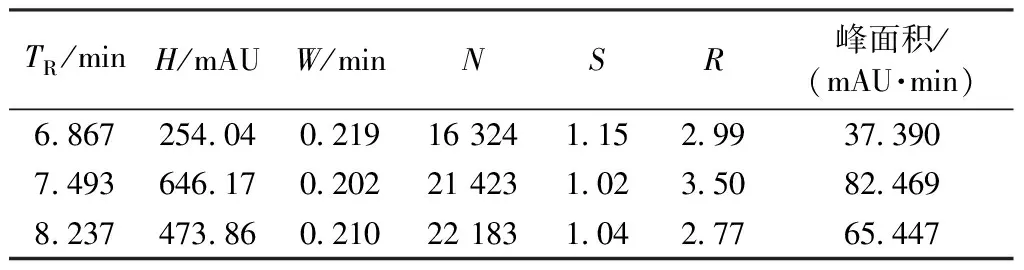
TR/minH/mAUW/minNSR峰面积/(mAU·min)686725404021916324115299373907493646170202214231023508246982374738602102218310427765447
由图5和表8可知,由梯度洗脱体系4所得各峰的峰型对称性都较好,半峰宽W小,理论塔板数N高,是较合适的梯度程序。
对比4个梯度洗脱体系可以看出,流动相中有机相含量多,洗脱能力增强,出峰时间缩短,峰形变好,但分离度变差;有机相含量少,洗脱能力差,出峰时间增加,峰形也差。因此设计梯度时要结合各方面因素进行综合考虑,在达到完全分离的前提下应尽可能使峰高、理论塔板数增加,半峰宽降低。
3.4 柱温的确定
合适的柱温能较好地控制压力,调节保留时间,提高分离度。采用3.3章节所确定梯度,调整柱温在室温、30、40、50、60℃条件下分别进样分析,考察柱温对分离的影响,所得各参数如表9所示。
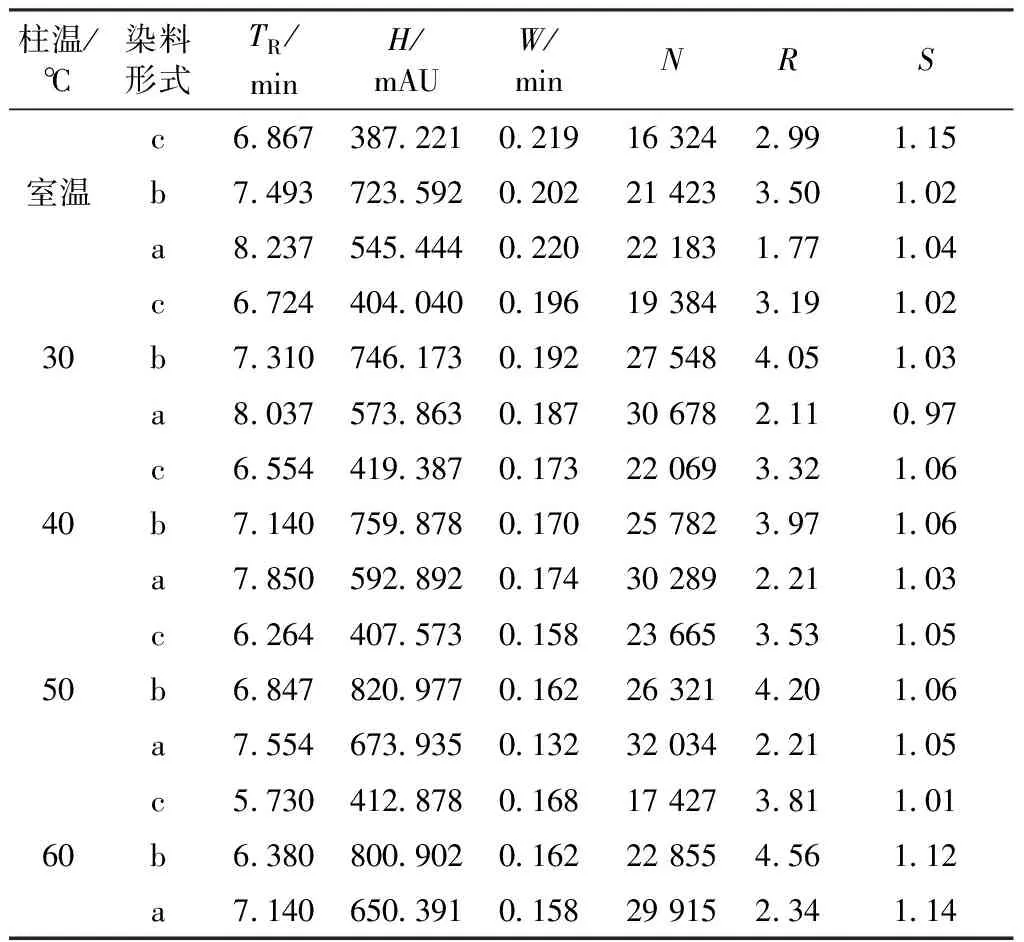
表9 不同柱温下峰参数表Tab.9 Parameters of peaks at different column temperatures
从表9数据可发现,随着柱温升高,各物质峰的保留时间TR均逐渐提前,这可能是由于温度升高使化合物在两相之间的分子运动加快引起。半峰宽W则随着温度升高逐渐减小,但0.2 min时的半峰宽都在可接受的范围内。理论塔板数N基本随着温度升高而增大,但在60 ℃反而变小。分离度R在室温时较差,其他温度下影响不大。不对称性因子S除室温和60 ℃较大外,其他均较好,因此30~50 ℃范围内均为适合的柱温。
3.5 方法的应用
由范德华体积、氢键作用力和被分离组分静电作用力的差别决定分离的选择性并获得理想分离是反相离子对色谱分离的主要特征[16]。不同染料及其水解产物的色谱分离因其染料分子结构间的差异,往往需要分别摸索分离的条件。但本文所述具有对称结构的、双偶氮类的、双卤代均三嗪活性染料及其水解产物,应可参考本文的分析方法,从而简单快速地建立色谱分离的条件。
如下例所示,采用AcclaimC18键合硅胶柱ODS-2,5 μm,150 mm×4.6 mm,及3.3章节所述梯度洗脱体系4,检测波长为536 nm,流速为1.000 mL/min,柱温为30 ℃;进样量为 20 μL;紫外可见检测器,对双一氯均三嗪活性染料活性红KE-3B在90 ℃,pH=11.0条件下水解60 min后的水解产物进行色谱分离,获得了较好的分离效果。所得产物的色谱图见图6。图6中峰的参数见表10。
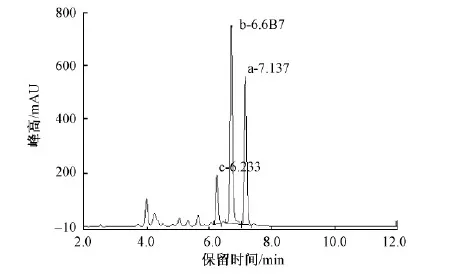
图6 双一氯均三嗪染料及其水解产物的色谱图Fig.6 Chromatogram of bis(monochloro-s-trazine) reactive dye and its hydrolysates

染料形式TR/minH/mAUW/minNRSc624318496701432116322101b669774764501434932322109a715355328901440985458108
从表10数据可看出,各峰的峰高H、半峰宽W、理论塔板数N、分离度R及峰对称性S均较好。说明该方法应用在双卤代均三嗪活性染料及其水解产物的液相色谱分离中有一定的适用性。尤其采用150 mm长的色谱柱分离双一氯均三嗪染料活性红KE-3B,即使其分子质量比双一氟均三嗪活性染料活性红LS-2G更大,但分离的时间却更短,说明对称结构的双卤代均三嗪活性染料及其水解产物的分离在150 mm色谱柱上可达到分离效果。
4 结 论
采用本文所述色谱分离方法,具有对称结构的双一氟均三嗪活性染料活性红LS-2G及双一氯均三嗪活性染料活性红KE-3B及其水解产物均得到较好的分离效果。该分离方法的建立对其他具有类似结构的染料或化合物的色谱分离方法的建立具有一定指导意义。参考该方法时应注意,若使用不同牌号的色谱柱,即使标明了相同的规格,所得分析结果也可能不同,因为不同牌号的色谱柱在填充剂及填料方式上存在较大不同,即使有微小的差异也可能导致分析结果的不同,若想得到分析结果的重现性,也须注意填装同一批填料,在定性分析时,最好先做比对实验。
FZXB
[1] 李桂贞,乐一鸣.薄层色谱法测定乙烯砜型活性染料的水解产物[J]. 色谱, 1989, 7(5): 285-288. LI Guizhen, LE Yiming. Thin-layer chromatographic analysis of hydrolysates of vinyl sulfone reactive dyes [J]. Chromatograph, 1989, 7(5): 285-288.
[2] 黄旭明,金雅,蔡再生. 液体活性染料的水解性分析及水解控制[J]. 纺织科技进展,2005,(6):17-19. HUANG Xuming,JIN Ya,CAI Zaisheng. The hydrolyze analysis and control of liquid reactive dye[J]. Progress in Textile Science & Technology,2005(6):17-19.
[3] 杭伟明. 二氟一氯嘧啶活性染料水解率测定[J]. 印染,1999(7):35-37. HANG Weiming. Determination of hydrolytic ratio of difluorochloropyrimidine reactive dyes[J]. Dyeing & Finishing, 1999(7):35-37.
[4] 吴圳燚,周凉仙,陈凤萍.活性染料中水解染料相对标准含量测定的改进[J]. 针织工业, 2010(2): 49-50. WU Zhenyan, ZHOU Liangxian, CHEN Fengping. Impro-vement of determination of hydrolysates of reactive dyes[J]. Knitting Industries, 2010(2): 49-50.
[5] 最新染料使用大全编写组. 最新染料使用大全[M].北京:中国纺织出版社,2001:381-382. Writing group of the newest use of dyestuffs. The Newest Use of Dyestuffs[M]. Beijing: China Textile & Apparel Press, 2001:381-382.
[8] 李萍,邵敏,邵建中.活性嫩黄K-6G的水解及醇解动力学研究[J].纺织学报,2009, 30(7): 83-88. LI Ping,SHAO Min,SHAO Jianzhong. Study on hydrolysis and alcoholysis kinetics of Reactive Brill Yellow K-6G[J]. Journal of Textile Research, 2009, 30(7): 83-88.
[9] KEITH R, BECK CINDY T, SALLEY.Adavances in HPLC analysis of reactive dyes[J]. AATCC Review, 2008 (8): 46-48.
[11] 丁燕,邵建中,邵敏. 高效液相色谱研究C.l.Reactive Blue 194的水解性能[J].浙江理工大学学报,2011,28(3): 328-332. DING Yan, SHAO Jianzhong,SHAO Min. A study on hydrolysis of C.I. Reactive Blue 194 by high performance liquid chromatography[J]. Journal of Zhejiang Sci-Tech University,2011,28(3): 328-332.
[12] 朱明华, 胡坪. 仪器分析[M]. 北京: 高等教育出版社, 2008: 72-73. ZHU Minghua, HU Ping. Instrumental Analysis[M]. Beijing: Higher Education Press, 2008: 72-73.
[13] 王正佳,邵敏,邵建中. 乙烯砜型活性染料水解动力学的HPLC研究[J]. 纺织学报, 2006, 27(9): 9-13. WANG Zhengjia,SHAO Min,SHAO Jianzhong. Study on the hydrolysis kinetics of vinylsulfone reactive dyes with HPLC analysis[J]. Journal of Textile Research, 2006, 27(9): 9-13.
[14] 张蓉,沈一峰,林素玲,等. C.I.活性蓝19在低温下的水解性能研究[J]. 浙江理工大学学报, 2008, 25(2): 132-136. ZHANG Rong, SHEN Yifeng, LIN Suling, et al. Study on the hydrolysis kinetics of C.I. Reactive Blue 19 at low-temperature with HPLC analysis[J]. Journal of ZheJiang Sci-Tech University,2008, 25(2): 132-136.
[15] SNYDER L R, KIRKLAND Joseph J, GIAJCH Joseph L. 实用高效液相色谱法的建立[M]. 2版. 张玉奎, 王杰, 张维冰,译.北京: 华文出版社, 2001: 25, 39, 222. SNYDER L R, KIRKLAND Joseph J, GIAJCH J L. Practical HPLC Method Development[M]. 2nd ed. ZHANG Yukui, WANG Jie, ZHANG Weibing, Translating.Beijing: Sino-Culture Press, 2001: 25, 39, 222.
[16] 邹汉法,张玉奎,卢佩章. 离子对高效液相色谱法[M]. 郑州:河南科学技术出版社,1994: 6,76-78. ZOU Hanfa, ZHANG Yukui, LU Peizhang. Ion-Pair High-Performance Liquid Chromatography[M]. Zhengzhou: Henan Science and Technology Press, 1994: 6,76-78.
Establishment of HPLC separation method for bis(halogeno-s-triazine) reactive dyes and their hydrolysates
HU Lingling1,2, FAN Xuerong1
(1.CollegeofTextile&Clothing,JiangnanUniversity,Wuxi,Jiangsu214122,China;2.CollegeofTextile&Clothing,UniversityofShaoxing,Shaoxing,Zhejiang312000,China)
In order to study the hydrolysis reaction of bis(halogeno-s-triazine) reactive dyes, the reversed-phase ion-pair high performance liquid chromatography was employed to separate the bis(halogeno-s-triazine) reactive dyes and their hydrolysis products. The establishing procedure of HPLC separation method that is appropriate for bis(halogeno-s-trazine) reactive dyes and their hydrolysis products was discussed in terms of selection of bis(halogeno-s-triazine)reactive dyes and chromatographic column, selection and optimization of mobile phase, determination of column temperature and so on. By this method the bis(monofluo-s-triazine) reactive dye Reactive Red LS-2G and bis(monochloro-s-triazine) reactive dye Reactive Red KE-3B and their hydrolysis products were separated completely.
reactive dye; bis(halogeno-s-triazine) reactive dye; hydrolysis; kinetics; HPLC
0253- 9721(2013)09- 0077- 07
2012-08-17
2012-12-11
浙江省科技厅公益技术项目(2011C21071)
胡玲玲(1977—),女,博士生。研究方向为多组分纤维纺织品的染整加工技术及理论。范雪荣,通信作者,E-mail:wxfxr@163.com。
TS 193.632
A

