2-羟基-4'-氯-4-二异戊烯氧基查尔酮的合成工艺研究
潘成燕,唐立明,赵水莲,关丽萍
(浙江海洋学院食品与医药学院,浙江舟山 316022)
天然查尔酮类化合物属于黄酮类化合物,查尔酮类基本化学结构为1,3-二苯基丙烯酮,主要存在于甘草、红花等药用植物中。天然查尔酮多为含酚羟基,如甘草中的异甘草素、红花中的红花苷元等。因为查尔酮类化合物分子具有较大的柔性,可以与不同的受体结合,表现为多方面的生物学活性。查尔酮作为黄酮类化合物家族的一员,具有广泛的生物活性,如抗菌、抗氧化、降血脂、抗炎等作用[1-2]。查尔酮是合成天然黄烷酮化合物的重要有机中间体[3],是多种药用植物的有效成分之一。查尔酮类化合物是一种多活性化合物在新型药物的研究与开发上受到广泛的应用,因此近年来引起了化学工作者们浓厚的研究兴趣。许多文献报道了多种查尔酮衍生物的合成方法及应用。如,早在1967年LALIBERTE[4]就报道了查尔酮具有抗蛲虫作用,2000年VINCENZO等[5]发现黄酮化合物中的查尔酮具有抗肿瘤活性,何克勤等[6]也报导了某些查尔酮的化合物具有抗过敏作用。
近年来,还有文献报道查尔酮的共轭效应使其电子流动性非常好,且具有不对称的结构,所以是优越的有机非线性光学材料,可以作为光储存、光计算、激光波长转换材料[7-8]。此外,查尔酮还可用作光化学中的光交联剂、荧光材料和液晶材料等[9-10]。
天然异戊烯基类化合物主要分布在桑科植物中,据文献报道,从桑科植物分离出超过6 500个黄酮类化合物,其中至少有400个化合物是异戊烯基和香叶基黄酮类化合物,异戊烯基侧链的存在大大加强了这类天然产物的生理及药理活性。该类化合物具有广泛的生理活性,比如抗肿瘤、抗细胞毒素、抗疟疾、抗艾滋病毒、抗白血病、抑制酪氨酸酶、抑制5 a还原酶[11-17]。研究在查尔酮的芳环上引入异戊烯基的方法,对合成这类化合物具有重要的应用和学术价值[18]。
目前,查尔酮衍生物的合成方法越来越多,但是主要是以取代苯乙酮与取代苯甲醛在碱性醇溶液中或以强酸为催化剂进行缩合反应得到[19]。另外还有多种合成查尔酮的新方法如金属化合物催化合成[20-21]、微波超声波催化合成[22]、相转移催化剂合成[23]、绿色合成[24]等。随着科学研究不断地进展,合成查尔酮及其衍生物的方法越来越多,产率也越来越高。
本文采用两种方法合成异戊烯氧基查尔酮,第一种方法采用经典的查尔酮的合成方法:采用氯甲基甲醚羟基保护、在强碱性下醛酮缩合、酸催化水解及异戊烯基取代四步合成,此方法也是实验室中最为常用的方法,但相对操作步骤较长,相对操作复杂,而且收率随苯环上取代基的变化从10%到70%不等[25]。第二种方法只有两步,异戊烯基取代和羟醛缩合反应就可以得到目标化合物,此方法缩短操作步骤,而且方法简单,操作容易,产率相对比较高,适合于工业化生产。两种合成路线如下:
合成方法一:

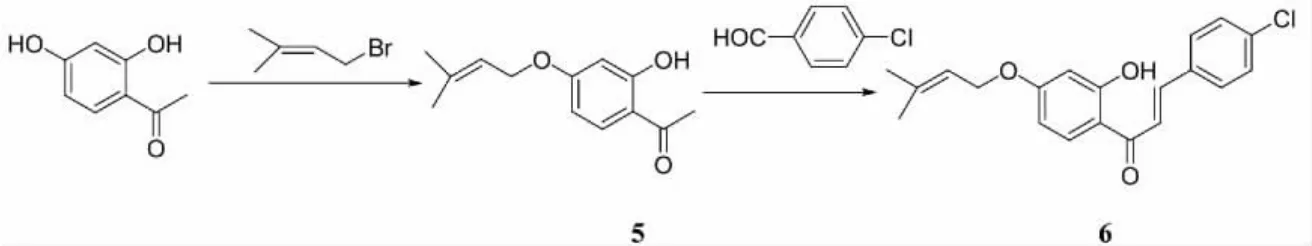
合成方法二:
1 实验部分
1.1 主要仪器与试剂
WRS-1B型数字熔点仪(上海精密科学仪器有限公司);BS323S型精密天平(赛多利斯科学仪器有限公司);RE-2000型旋转蒸发仪(上海亚荣生化仪器厂);DHG-9023A型电热恒温鼓风干燥箱(上海亚荣生化仪器厂);85-2型磁力搅拌器(常州国华电器有限公司);SHB-IIIA型循环水式多用真空泵(河南省太康科教器材厂);FI-1730型红外光谱仪(KBr压片,日本岛津公司);Bruker AV-300核磁共振仪(CCl3D为溶剂,TMS为内标,美国惠普公司);HP1100LC/MS型质谱仪(美国惠普公司)。其他试剂均为市售分析纯。
1.2 2-羟基-氯-4-异戊烯氧基查尔酮的合成(合成方法一)
1.2.1 2 -羟基-4-甲氧甲氧基苯乙酮(1)
将0.5 g(3.29 mmol)2,4-二羟基苯乙酮,0.95 g(6.88 mmol)无水K2CO3,30 mL无水丙酮加入100 mL两口瓶中,于50℃油浴条件下剧烈搅拌1 h后。慢慢滴加0.65 mL ClCH2OCH3(8.56 mmol),TLC监测反应到原料点消失后,过滤用少量丙酮淋洗残杂,旋干滤液,以石油醚/乙酸乙酯[V(石油醚)/V(乙酸乙酯)]=10:1柱层析分离得无色油状液体[26]0.51 g,产率78.5%。
1.2.2 2 -羟基-4-甲氧甲氧基-2',4'-二氯查尔酮的合成(2)
在氮气流保护下,100 mL两口圆底烧瓶中加入0.51 g(2.6 mmol)2-羟基-4-甲氧甲氧基苯乙酮(1),0.55 g(3.1 mmol)4-氯苯甲醛,在搅拌下滴加由48 mL无水乙醇和6.8 g KOH配成14%KOH的溶液,室温搅拌15 h,析出大量的黄色固体,TLC跟踪反应到原料点消失,停止反应,抽滤得黄色固体物质,用少量水洗涤后,用乙醇重结晶得到黄色针状结晶[26]0.64 g,产率:70%。
1.2.3 2 ,4-二羟基-4'-氯查尔酮的合成(3)
0.64 g(1.59 mmol)2-羟基-4-甲氧甲氧基-4'-氯查尔酮(2)放置于100 mL的两口瓶中后,加入30 mL甲醇,回流溶解后,滴加6 mL稀盐酸(5 mol/L),回流,TLC跟踪反应直到原料点消失,停止反应。冷却析出微细深黄色针状结晶(经TLC分析很纯),抽滤后,抽真空干燥后得黄色固体[26]0.39 g,产率70%。
1.2.4 2 -羟基-4'-氯-4-异戊烯氧基查尔酮的合成(4)
将0.39 g(1.2 mmol)2,4-二羟基-4'-氯查尔酮(3),0.35 g(2.5 mmol)无水碳酸钾置于50 mL圆底烧瓶中,加入20 mL无水丙酮溶解。在油浴50℃条件下剧烈搅拌一小时后滴加0.24 g(1.6 mmol)异戊烯基溴和2 mL无水丙酮的混合液,5 min滴完后,TLC监测反应到原料点消失后,滤除碳酸钾固体,丙酮淋洗残杂,旋干丙酮后,用硅胶柱层析(V(石油醚)/V(乙酸乙酯)=10:1)洗脱得到黄色固体0.29 g,产率78%,m.p.86~87 ℃.IR(KBr)cm-1:3212,1641,1582,1221,971.1H NMR(CDCl3,300 MHz):δ 1.69(s,3H,-CH3),1.74(s,3H,-CH3),4.50(d,2H,J=9 Hz,-CH2),5.41(t,1H,J=9 Hz,=CH),6.41-7.78(m,3H,-C6H3),7.49(d,1H,J=15.1 Hz,-=CH),7.19-7.36(m,4H,-C6H4),7.75(d,1H,J=15.4 Hz,=CH),13.31(s,1H,-OH).MS m/z 343(M+1).
1.3 2-羟基-2',4'-二氯-4-异戊烯氧基查尔酮的合成(合成方法二)
1.3.1 2 -羟基-4-异戊烯氧基苯乙酮的合成(5)
将 0.5 g(3.29 mmol)2,4-二羟基苯乙酮置于圆底烧瓶中,加入 0.95 g(6.88 mmol)K2CO3,加无水丙酮30 mL使其溶解。于50℃下搅拌反应1 h,然后缓慢滴加0.628 g(4.22 mmol)溴代异物烯,TLC跟踪到原料点消失,停止反应,滤除碳酸钾固体,丙酮淋洗残杂,旋干丙酮后,得白色固体0.827 g,用甲醇重结晶,干燥,得白色固体0.7 g。
在氮气保护下,在 100 mL两口圆底烧瓶中加入 0.7 g(3.18 mmol)白色固体,0.665 g(3.8 mmol)4-氯苯甲醛,在搅拌下滴加由48 mL无水乙醇和6.8 g KOH配成14%KOH的溶液,室温反应5 h后。有大量黄色固体析出,TLC跟踪反应到原料点消失,停止反应。将反应液倒入100 mL冰水中,用3 mol/L HCl调pH至中性,过滤得到黄色固体,干燥,粗产品用95%乙醇重结晶,得黄色晶体0.97g。产率产率65.4%,m.p.86-87℃.IR(KBr)cm-1:3211,1640,1580,1220,973.1H NMR(CDCl3,300 MHz):δ 1.66(s,3H,-CH3),1.71(s,3H,-CH3),4.51(d,2H,J=9 Hz,-CH2),5.43(t,1H,J=9 Hz,=CH),6.40-7.70(m,3H,-C6H3),7.45(d,1H,J=15.1 Hz,-=CH),7.20-7.39(m,4H,-C6H4),7.73(d,1H,J=15.4 Hz,=CH),13.32(s,1H,-OH).MS m/z 343(M+1).
2 结果与讨论
本实验采用两种方法合成得到的目标化合物4和6的结构经IR、1HNMR和MS确证,证明为同一种物质,即2-羟基-4′-氯-4-异戊烯氧基查尔酮。红外光谱分析产物经IR(KBr压片)测定:3212(或3211)cm-1吸收峰是羟基的伸缩振动;1641(或1640)cm-1是羰基键C=O的伸缩振动;1582(或1580)cm-1吸收峰归属于苯环 C=C键的面内振动;1221(或1220)cm-1吸收峰归属于C-O-C的伸缩振动;971(或973)cm-1吸收峰归属于苯环面外弯曲振动。经核磁共振氢谱产物可见证明氢的归属,综上所述,可以判定产物为目标化合物查尔酮。
本实验采用两种合成方法合成目标化合物2-羟基-4′-氯-4-异戊烯氧基查尔酮,合成方法一采用经典的合成方法,首先是采用氯甲基甲醚对羟基进行保护,目的增强反应活性。然后在强碱作用下进行醛酮缩合,也就是经历了经典的克莱森-史密斯缩合反应。而后在HCl作用下进行水解反应,脱去保护基氯甲基甲醚。最后采用异戊烯基取代等四步反应得到目标化合物。此合成过程相对比较复杂,且收率与苯环上取代基的不同相对不高,不适合大批量生产。
为此,在本文中我们对合成方法进行了优化,采用将原料直接与溴代异物烯进行亲核取代反应,然后与4-二氯苯甲醛进行醛酮交叉缩合(克莱森-史)密斯反应得到目标化合物,此方法后处理简单,收率高同时降低了成本,适合大批量生产。在合成2-羟基-4-异戊烯氧基苯乙酮时,反应物的投料比对产量以及产物纯度有明显的影响,而2,4-二羟基苯乙酮中4位羟基反应活性较2位高,可以很好的获得4位酚羟基醚化的产物,实验对投料比2,4-二羟基苯乙酮:溴代异物烯=1:1,1:1.3,1:1.5均进行了试验研究,结果表明投料比为1:1.3为合适。这是因为,溴代异物烯对温度敏感,而采用无水丙酮/K2CO3体系,在搅拌下滴加溴代异戊烯,可以使其迅速的参与反应,使转化率和后处理都达到了很好的效果[27-28]。
另外,合成目标化合物2-羟基-4′-氯-4-异戊烯氧基查尔酮时,是在碱性坏境中醛酮缩合反应,反应过程中是负离子化的酮和无α-氢的醛进行反应,因此要控制反应条件,即需要在无水和氮气保护下,滴加14%的KOH无水乙醇溶液。反应大约在5 h出现大量黄色固体。但是要注意反应过程中碱的浓度要控制在10%~14%,因为,碱的浓度太高会引起羟醛缩合反应,产生大量的副产物,使产率下降,而碱浓度太低则反应时间延长、产率降低[29],为此在反应时注意碱的浓度和加入的速度等。
3 结论
查尔酮类化合物作为一种多活性化合物,在医药、生物、化工等领域都将有广阔的发展前景,对查尔酮类化合物的研究将越来越多地受到人们的关注和重视。本实验采用改进的方法可经过两步制得目标化合物,而且后处理简单,产品的产率和纯度都有所提高,为生产提供可行的合成工艺。
[1]SANTOS L,CURI PEDROSA R,CORREA R,et al.Biological evaluation of chalcones and analogues as hypolipidemic agents[J].Arc Pharm(Weinheim),2006,339:541-546.
[2]ARAICO A,TERENCIO M C,ALCARAZ M J,et al.Phenylsulphonyl urenyl chalcone derivatives as dualinhibitors of cyclooxygenase-2 and 5-lipoxygenase[J].Life Sci,2006,78:2 911-2 918.
[3]曾平莉,王 东,冯 驸.查尔酮的合成应用研究进展[J].化工生产与技术,2005,12(3):23-24.
[4]LALIBERTE R.Anthelm intic activihes of chalcone sand related compounds[J].Can J Pharm Sci,1967,2(2):37-43.
[5]DE VINCENZO R,FERLINI C,DISTEFANO M,et al.In vitro evaluation of newly developed chalcone analogues in hum an cancer cells[J].Cancer chemother Pharmacol,2000,46(4):305-312.
[6]何克勤,程桂芳,奚凤德,等.查耳酮类化合物对过敏性慢反应物质拮抗作用的构效关系[J].药学学报,1996,31(11):878-880.
[7]MARTIN C R.Structure,function,and regulation of the chalconesynthease[J].1993,147:233-284.
[8]方 正,唐伟方,徐 芳.萘丁美酮的合成工艺改进[J].中国药科大学学报,2004,35(1):90-91.
[9]楼定忠,朱 坡,刘泽贵.萘丁美酮合成路线图解[J].中国医药工业杂志,1996,27(5):238-239.
[10]艾亨俭,李文玉.萘普酮的又一合成法[J].中国医药工业杂志,1985,16(11):509-510.
[11]DASKIEWICZ J B,DEPEINT F,VIORNERY L,et al.Effects of flavonoids on cell prolifera tion and caspase activation in a colonic cell line HT 29,SAR study[J].J Medicine Chemical,2005,48(8):2 790-2 804.
[12]COMTE G,DASKIEWICZ J B,BAVET C,et al.Rearrangement o f 5-O-preny l flavones:Areg ioselective access to 6-C-(1,1-dimethylallyl)and 8-C-(3,3-dimethylallyl)-flavones[J].J Medicine Chemical,2001,44:763-768.
[13]NA M,JANG J,JAMEN D N,et al.Preny lated flavonoids with PTP1B inhibitory activity from the root bark of erythrinamildbraedii[J].J Nature Product,2006,69:1 572-1 576.
[14]ZhOU J M,GENG G Y,BATIST G,et al.Syntheses and potential anti-prostate cancer activities of ionone-based chalcones[J].Bioorg Med Chem Lett,2009,19:1 183-1 186.
[15]SYAH Y M,ACHMAD S A,GHISALBERTI E I,et al.Artoindonesianins G-I,three new isoprenylated flavones from Artocarpus lanceifolius[J].Fitoterapia,2001,72(7):765-773.
[16]NOMURA T,ANO Y,AIDA M.Isoprenoid-substituted flavonoids from Artocarpus plants(M oraceae)[J].Heterocycles,1998(47):1 179.
[17]BOONLAKSIRI C,OONANANT W,KONGSAEREE P,et al.An antimalarial stilbene from Artoearpus integer[J].Phytochemical,2000(54):415.
[18]赵艳敏,杨金会.对羟基苯甲醛的异戊烯烷基化反应[J].合成化学,2010,18(6):735-737.
[19]郭宏雄,臧庶声,李文科,等.查尔酮的制备[J].兰州医学院学报,1998,24(2):12-13.
[20]陆文兴,颜朝国,顾惠芬.查尔酮的KF-A12O3催化合成[J].化学试剂,1995,17(4):253-254.
[21]李良助,赵志刚,袁音芳,等.应用芳基锂合成查尔酮[J].高等学校化学学报,1992,13(8):1 071-1 074.
[22]LI J T,YANG W Z,WANG S X,et a1.Improved synthesis of chalcones under ultrasound irradiation[J].Ultrasonic Sonochem,2002,9:237-239.
[23]蒋新宇,赵爱丽.聚乙二醇相转移催化法合成查尔酮[J].广州化工,2006,31(3):126-129.
[24]段宏昌,姜 恒,宫 红.查尔酮衍生物的绿色合成[J].中国药业,2006,15(15):30-31.
[25]石秀梅,邓士英,邹桂华,等.3,5-二羟基查尔酮的合成[J].化学工程师,2008,153(6):8-9.
[26]ZHAO D H,SUI X,QU Y L,et al.Synthesis and Studies on Antidepressant Effect of 5,7-Dihydroxyflavanone Derivatives[J].Asian Journal of Chemistry,2011,23(3):1 129-1 132.
[27]王 倩,何侃侃,侯自杰.三种O-异戊烯基苯丙素类天然产物的首次合成[J].有机化学,2003,23(3):182-186.
[28]LI M,HAN X,YU B.Facile synthesis of flavonoid 7-O-glycosides[J].J Org Chem,2003,68(17):6 842-6 845.
[29]党 珊,刘锦贵,王国辉.室温下2-羟基查尔酮的合成[J].合成化学,2008,16(4):460-463.

