美沙拉秦引起的免疫性溶血性贫血1例报道
黄月华,李 骥 ,赵 淼 ,彭 茜 ,任 翃 ,杨秀锦,杨 红
中国医学科学院北京协和医学院北京协和医院1.内科;2.消化内科,北京100730
病例 患者,27岁,男,2012年4月16日主因腹痛2年,加重3个月入院。患者于2年前无明显诱因出现脐上疼痛,进食后明显,疼痛逐渐加重,当地行结肠镜检查提示回盲部溃疡,转入外科行“右半结肠切除术+吻合术”,病理诊断为克隆恩病,此后腹痛缓解,未予药物治疗。曾查血常规:WBC:9.5×109/L,RBC:4.56×1012/L,HGB:140 g/L,PLT:315 ×109/L。生化:TBil:11.28 μmol/L,DBil:4.33 μmol/L,ALT:11 U/L,ALP 55 U/L,GGT:12 U/L,Cr:60 μmol/L。手术 1 个月后无明显诱因出现右下腹胀痛,以进食后为主,伴有里急后重,排气少,呃逆较多。于中国医学科学院就诊,行结肠镜检查(见图1A)提示吻合口溃疡,病理:(吻合口周围)炎性渗出物、坏死物、肉芽组织及结肠黏膜慢性炎。外院手术病理、中国医学科学院会诊并且结合临床症状考虑诊断为克罗恩病。2012年4月6日开始给予美沙拉秦1 g,1次/d治疗,查血常规:WBC:6.85×109/L,RBC:3.86 × 1012/L,HGB:111g/L,PLT:317 × 109/L,RET%:1.43%;生化:TBil:28.3 μmol/L,DBil:9.4 μmol/L,ALT:9 U/L,ALP:57 U/L,GGT:11 U/L,Cr:67 μmol/L。口服美沙拉秦2 周后腹痛症状缓解不明显。于2012年4月24日加用泼尼松50 mg qd po(折算为1 mg/kg体质量),患者自觉腹痛缓解。
患者于2012年5月8日起泼尼松减量至45 mg,5月10日左右发现巩膜发黄,无发热、皮疹,无畏寒寒战,无恶心、呕吐,无头痛及腰背痛,当地医院查肝肾功:TBil:66.2 μmol/L,DBil:21.9 μmol/L,ALT:8 U/L,Cr:53 μmol/L,患者继续服用美沙拉秦治疗。查血常规:WBC:11.17×109/L,RBC:3.25×1012/L,HGB:113 g/L,PLT:191 ×109/L,RET%:8.03%;生化:TBil:88.2 μmol/L,DBil:10.1 μmol/L,ALP:47 U/L,GGT:14 U/L。铁蛋白:Fe:175.9 μg/dl↑,TRF:1.94 g/L↓,TIBC:288 μg/dl,IS:61.2%↑,TS:64.3%↑,Fer:178 ng/ml。血清叶酸3 ng/ml↓,VB12:210 pg/ml。抗人球蛋白试验+分型:阴性。血涂片基本正常。红细胞渗透性EOF(含对照):STH(n)0.48%,STH(p)0.48%,CTH(n)0.28%,CTH(p)0.28%。骨髓涂片:增生明显活跃,M∶E=1.09∶1.1。粒系各阶段比例大致正常。红细胞大小不等,大红细胞及嗜多色性红细胞易见。淋巴细胞及单核细胞比例形态正常。巨核细胞及血小板不少。考虑溶血性贫血,原因可能与药物相关,入院后停美沙拉秦。停药后于2012年6月11日复查血常规:WBC:13.31×109/L,RBC:3.89×1012/L,HGB:139 g/L,PLT:277 ×109/L,RET%:3.45%。但美沙拉秦为克罗恩病必须用药,纤维素膜控释载体美沙拉秦制剂与艾迪莎为美沙拉秦不同载体的剂型,副作用可能不同,故于2012年6月13日开始更换为纤维素膜控释载体美沙拉秦制剂,期间多次查血常规+网织红细胞、胆红素未见异常。2012年7月26日复查腹盆增强CT+小肠重建 (见图2B)与2012年4月18日腹盆CT+小肠重建(见图2A)比较:末段回肠及回盲部增厚伴异常强化,较前减轻、范围缩小;肠系膜区多发淋巴结,部分较前缩小;双侧腹股沟多发淋巴结,较前部分缩小。行结肠镜(见图1B)显示:吻合口周围可见不规则溃疡,较上次吻合口溃疡缩小,接触出血,周围可见黑色手术缝线及隆起充血结节。患者于2012年8月28日再次无明显诱因出现皮肤巩膜黄染,当地查 TBil:59.9 μmol/L,IBil:45.8 μmol/L,血常规RBC:3.79×1012/L,HGB:124 g/L。电话随访嘱患者停纤维素膜控释载体美沙拉秦制剂。9月20日当地复查,RBC:4.16×1012/L,HGB:143 g/L,TBil:15.6 μmol/L,IBil:9.5 μmol/L。2012年11月27日随访,一般情况良好,无腹痛、腹胀等临床症状,体质量增加3 kg。查血常规检查:WBC:9.35×109/L,RBC:5.05×1012/L,HGB:165 g/L,PLT:243×109/L。生化:TBil:28.6 μmol/L,DBil:8.3 μmol/L,ALT:13 U/L,ALP:56 U/L,GGT:16 U/L,Cr:69 μmol/L,血沉:2 mm/h,hsCRP:0.45 mg/L。
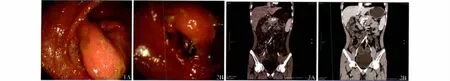
图1 结肠镜检查 A:治疗前,吻合口溃疡;B:治疗后,溃疡较前缩小;图2 腹盆增强CT+小肠重建 A:治疗前,末段回肠及回盲部增厚伴异常;B:治疗后,末段回肠及回盲部病变与A图比较有所减轻Fig 1 Colonoscopy results A:Pre-treatment,anastomotic ulcer;B:Post-treatment,the ulcer lessened;Fig 2 Abdominal and pelvicenhancement CT+intestinal reconstruction A:Pre-treatment,thickening of the terminal ileum and ileocealjunction with abnormal enhancement;B:Post-treatment,the lesions of the terminal ileum and ileocecaljunction were alleviated compared with figure A
讨论 炎症性肠病(IBD)是一类不明原因的慢性非特异性肠道炎症性疾病,主要包括溃疡性结肠炎(UC)和克罗恩病(CD)。该病在中国患病率呈增长趋势,在过去14年中我国患病率以3~4倍的速度增长,因此对于该病诊治和并发症预防非常重要。文献报道IBD可伴有贫血、凝血功能异常等多种血液学改变[1-3]。IBD合并贫血中,出现溶血性贫血相对比较少见,其原因之一考虑为疾病本身诱发,文献报道UC合并免疫性溶血性贫血的患病率0.2% ~1.7%[2],克罗恩病有个案报道[3]。而IBD合并免疫性溶血性贫血的机制在于非红细胞抗原在病变的肠道吸收,而后交叉反应对产生红细胞抗体、自身抗体吸附于红细胞表面而引起的一种溶血性贫血。IBD合并免疫性溶血性贫血另外一个原因,考虑由于治疗药物引起,如有报道柳氮磺吡啶可以诱发药物性溶血性贫血。
本报道中的患者,临床诊断后给予治疗的过程中出现了黄疸、贫血,提示临床医师要积极考虑贫血的原因,该患者临床表现为黄疸、间接胆红素增高为主,血红蛋白轻度下降,胆管酶(ALP、GGT)和肝脏谷草转氨酶、谷丙转氨酶均正常,因此在黄疸的鉴别诊断中我们首先考虑溶血性黄疸可能性大,因此对患者进行了一系列的溶血方面的检查。而通过该患者的实验室结果考虑:有红细胞破坏过多的直接证据和间接证据。其中红细胞破坏过多的直接证据有:总胆红素及间接胆红素升高。间接证据有:骨髓红系增生显著,网织红细胞比例升高,停药后胆红素、网织红细胞降至正常范围及贫血纠正。但是临床问题在于:患者有红细胞破坏证据,但是Coombs实验阴性是否能诊断溶血性贫血?目前有文献报道发现约2%~11.5%的温抗体型AIHA直接Coombs试验假阴性[4]。因此综合判断该患者溶血的证据是肯定的,可以明确诊断合并免疫性溶血性贫血。
下一步我们思考的问题是溶血性贫血的原因是什么,因为原因的寻找决定了下一步的治疗方案,如果疾病本身诱发的免疫性溶血性贫血,治疗方案还有待进一步加强,如果是其他原因如药物诱发的免疫性溶血性贫血,治疗方案需要停药等相应的改变。患者在激素减量过程中出现黄疸和贫血,首先考虑是否为CD合并溶血性贫血。然而从该患者的诊治疗效分析,患者于2012年3月查结肠镜显示病变较大,而2012年7月复查结肠镜显示回肠末段病变较前明显缩小,提示患者治疗有效。这个结果给疾病本身诱发溶血性贫血的观点就提出了疑问,另外一个不支持点在于患者血红蛋白和胆红素随美沙拉秦用药和停药而波动。再者要考虑药物诱发所致免疫性溶血性贫血,患者仅服用了美沙拉秦和激素,美沙拉秦是否会引起免疫性溶血性贫血?检索药物说明书和文献未能发现相关的报道,再者患者第1次溶血性贫血出现时已经服用美沙拉秦1个月余,唯一的方法是停药后观察。在本病例研究中由于贫血在停药后缓解、服类似药物后再发作,证实了患者溶血性黄疸的原因是药物所致。
美沙拉秦是轻、中度炎症性肠病治疗的首选药物,也是炎症性肠病患者常用药物,在临床工作中绝大多数患者服药后副作用较小,这容易让我们忽视对药物副作用的重视,另外由于IBD在中国尚不属于常见病的范围,中国人群IBD的合并症、肠外表现、对药物的疗效及副作用等方面的了解尚需深入,因此在诊治过程中会出现一些起伏,这就提示临床医师要注重细节、仔细观察病情和辅助检查的变化,不断总结经验,提高临床的认识。
本例患者克罗恩病诊断明确,诊治过程中美沙拉秦诱发了药物性溶血性贫血,由于我们积极寻找病因,及时停药避免了患者受到更大的伤害,目前患者在随访中,于2012年11月27日随访,腹痛等症状消失,实验室检查均正常。
[1]Quera R,Shanahan F.Thromboembolism-an important manifestation of inflammatory bowel disease[J].Am J Gastroenterol,2004,99(10):1971-1973.
[2]Plikat K,Rogler G,Schölmerich J.Coombs-positive autoimmune hemolytic anemia in Crohn’s disease[J].Eur J Gastroenterol Hepatol,2005,17(6):661-666.
[3]Giannadaki E,Potamianos S,Roussomoustakaki M,et al.Autoimmune hemolytic anemia and positive Coombs test associated with ulcerative colitis[J].Am J Gastroenterol,1997,92(10):1872-1874.
[4]Zhang ZN,Hao YS,Zhao YQ,et al.Hematology[M].2nd ed.Beijing:People’s Medical Publishing House,2011:426.张之南,郝玉书,赵永强,等.血液病学[M].2版.北京:人民卫生出版社,2011:426.

