基于检测铜离子的香豆素水合肼希夫碱荧光探针的研究
申有名, 李 林, 陈超男, 刘敏迪, 奉少东, 赵 菁, 张向阳, 郑清云, 张春香
基于检测铜离子的香豆素水合肼希夫碱荧光探针的研究
申有名*1,2, 李 林1, 陈超男1, 刘敏迪1, 奉少东1, 赵 菁1, 张向阳1, 郑清云1, 张春香1
(1. 湖南文理学院 化学化工学院, 湖南 常德, 415000; 2. 湖南师范大学 化学生物学及中药分析教育部重点实验室, 湖南 长沙, 410081)
设计合成了一种基于新型香豆素水合肼希夫碱荧光探针, 结构经1H NMR表征. 利用荧光光谱研究了该探针分子对铜离子的识别作用. 实验表明, 该探针对铜离子具有较好的选择性识别能力, 加入铜离子后, 该探针的荧光发射强度显著减弱, 并且荧光发射强度随着Cu2+浓度的增加而减弱. 通过荧光离子滴定实验对其选择性和抗干扰能力进行了系统研究, 发现加入其他常见金属离子(如Al3+、Ca2+、Co2+、Cr3+、Fe3+、K+、Mg2+、Na+、Ni2+、Zn2+等), 荧光强度没有发生变化, 并且上述各种离子分别与铜离子共存时, 对其没有干扰. 结果表明, 香豆素水合肼希夫碱荧光探针对铜离子具有较高选择性识别.
铜离子; 香豆素; 希夫碱; 荧光探针
铜离子是生命系统中重要的微量元素和必需的营养素, 它在生物体内以及化学反应过程中起着十分重要的作用, 在人体内如果铜元素缺乏会导致生长和代谢的紊乱[1—2]. 但是当铜在细胞中浓度平衡的改变会导致抑制神经性疾病, 如Parkinson’s Menke’s和Alzheimer’s等疾病[3-5]. 因此, 实时监测铜离子的含量引起了人们的极大兴趣. 相对于传统的检测铜离子的方法, 如原子发射光谱法、电感耦合等离子体-质谱法、电化学方法等[6-7], 近几年发展起来的荧光探针法, 具有高选择性和灵敏度, 非破坏性的分析和检测系统易操作性等优点, 在环境、化学、生物和医学等领域存在着广泛的应用, 针对金属离子的荧光探针受到人们的广泛关注[8-10]. 目前, 虽然有关于铜离子荧光探针方面的研究报道比较多, 但也存在如合成复杂、选择性不好等缺点. 因此, 设计合成新型简单、具有高选择性的铜离子探针分子显得十分必要.
香豆素类荧光基团具有较高的荧光量在产率、光量子稳定性、较大的Stokes位移等优点, 被广泛用来设计荧光探针[11-13]. 基于以上考虑, 本文以香豆素作为荧光团, 设计合成了一种简单的香豆素水合肼希夫碱荧光探针, 利用荧光光谱研究了其对铜离子的识别过程.
1 实验部分
1.1 实验仪器与试剂
核磁共振仪(德国Bruke公司, TMS为内标); F-4500型荧光分光光度仪(日本岛津公司); E-201-C型精密PH计(雷磁上海精密科学仪器有限公司); 4-N, N-二乙基氨基水杨醛(天津市大茂化学试剂厂); 85%水合肼(国药集团上海化学试剂公司); 丙二酸二乙酯(国药集团上海化学试剂公司), 三氯氧磷(上海晶纯试剂有限公司); 其他试剂均为分析纯. 所有的荧光测定在Hitachi F-4500荧光光度计上进行(激发狭缝宽: 5 nm; 发射狭缝宽: 5 nm).
1.2 探针分子的合成
1.2.1 化合物1的合成

图1 化合物1
在100 mL的三颈烧瓶中加入1.93 g(10 mmol)4-N, N-二乙基氨基水杨醛、3.200 g (20 mmol)丙二酸二乙酯、30 mL无水乙醇、1.0 mL六氢吡啶, 加热回流反应6 h, 冷却至室温, 旋干, 然后加入20 mL浓盐酸和20 mL冰醋酸, 回流反应12 h. 反应液冷至室温后, 倒入冰水中, 用20%NaOH溶液调节溶液的pH值至5, 有大量的土黄粉末析出, 过滤, 水洗, 真空干燥, 得到1.75 g化合物1, 如图1所示, 产率为80%.1H NMR δ: 7.94-6.32 (m, 5H ), 3.54 (q, 4H), 1.31(t, 6H).
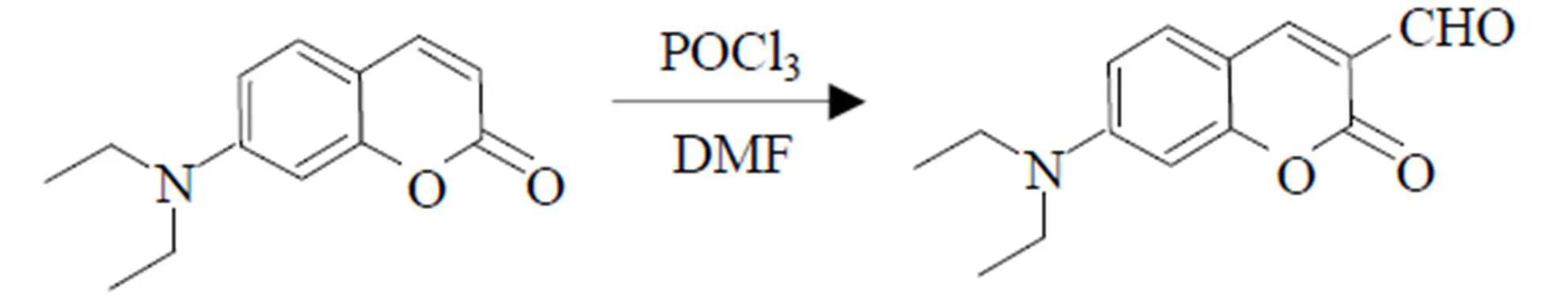
图2 化合物2
1.2.2 化合物2的合成
氮气保护下, 向100 mL三颈瓶中加入8 mL POCl3, 冰浴冷却并搅拌下, 逐滴滴加8 mL新蒸的DMF, 滴加完毕, 混合物反应1 h, 待反应液变成深红色后, 加入含有3.1 g化合物1的1, 2-二氯乙烷溶液20 mL, 反应加热回流12 h, 冷却, 用20% NaOH溶液调节pH值为5~6, 有固体析出, 过滤, 硅胶柱柱层析(乙酸乙酯:石油醚= 1∶8), 得1.78 g化合物2, 如图2所示, 产率73%.1H NMR δ: 10.23(s, 1H), 8.16 -6.61 (s, 1H ), 3.61 (q, 4H), 1.23(t, 6 H).
1.2.3 化合物3的合成
在25 mL单口瓶中, 加入0.245 g(1 mmol)化合物2、1 mL水合肼、5 mL无水乙醇, 氮气保护下回流反应2 h, 冷却, 减压抽滤, 用无水乙醇洗涤2~3次, 得到2.15 g黄色固体3, 如图3所示, 产率83%.1H NMR δ: 9.04 (s, 1H) , 8.21 -6.54(s, 1H ), 3.55(q, 4H), 1.18(t, 6 H).

图3 化合物3
1.3 溶液的配置步骤
探针化合物3的母液(1 × 10–4mol/L)配置是将化合物3溶于乙腈中. 各种金属离子的母液(1 × 10–2mol/L)配置是将适量的金属盐溶于去离子水中. 探针化合物3的测试溶液配置是取0.5 mL探针母液, 2 mL PBS溶液, 和适当量的各种金属离子母液加入到5 mL的容量瓶中, 然后用PBS溶液定容. 摇匀后, 用435 nm激发波长激发, 测定荧光发射光谱.
2 结果与讨论
2.1 光谱性质
图1记录的是探针化合物3 (CH3CN:PBS= 1: 9, pH = 7.0)在室温条件下, 不断改变Cu2+溶液时所得的荧光光谱图. 从图4中可以看出: 在没有加入Cu2+时, 探针化合物3在485 nm处具有较强的荧光, 随着加入的Cu2+浓度的增加, 荧光发射波长在485 nm处的荧光强度逐渐减弱. 当Cu2+浓度达到2 eq时荧光基本猝灭. 这可能是Cu2+与化合物3形成了配合, 促使化合物荧光下降.
2.2 离子选择性
为测试探针化合物3对Cu2+的选择性, 分别在样品池中加入已配好的各种测试液, 实验结果如图5所示. 从图5中可以看出: 当在探针溶液中加入Cu2+的溶液, 荧光发生猝灭, 而加入其它金属离子如Al3+、Ca2+、Co2+、Cr3+、Fe3+、K+、Mg2+、Na+、Ni2+、Zn2+等, 探针的荧光都没有发生明显变化. 这表明, 探针化合物3对Cu2+的识别具有很高的选择性. 在手持紫外灯的照射下, 探针溶液加入各种金属离子后的颜色变化如图6所示, 实验结果表明, 荧光探针能较好的对Cu2+具有选择性猝灭能力.

图4 不同浓度的铜离子存在时化合物3 (10 μM) 的荧光发射光谱图. 铜离子的浓度自上而下依次是0, 0.05, 0.25 , 0.5, 1, 3, 5, 6, 8, 9,10, 20 μmol/L.

图5 探针化合物4(50 µM)对各种金属离子的选择性. 从左至右离子依次是Cu2+、Al3+、Ca2+、Co2+、Cr3+、Fe3+、K+、Mg2+、Na+、Ni2+、Zn2+.
2.3 共存离子的干扰性
为了进一步确定探针化合物3对Cu2+的高选择性, 我们测试了在探针溶液中加入2 eq Cu2+后, 分别依次与Al3+、Ca2+、Co2+、Cr2+、Fe3+、K+、Mg2+、Na+、Ni2+、Zn2+共存的干扰性实验. 空白实验是在同样的条件下, 在探针化合物3溶液中只加入2 eq Al3+、Ca2+、Co2+、Cr2+、Fe3+、K+、Mg2+、Na+、Ni2+、Zn2+进行测试的; 结果如图7所示. 从图7中可以看出, 在探针溶液中加入2 eq Cu2+后, 再加入其它离子, 探针分子荧光仍然发生荧光猝灭, 这表明, 在其它离子共存下, 对Cu2+的识别具有很好的抗干扰性.
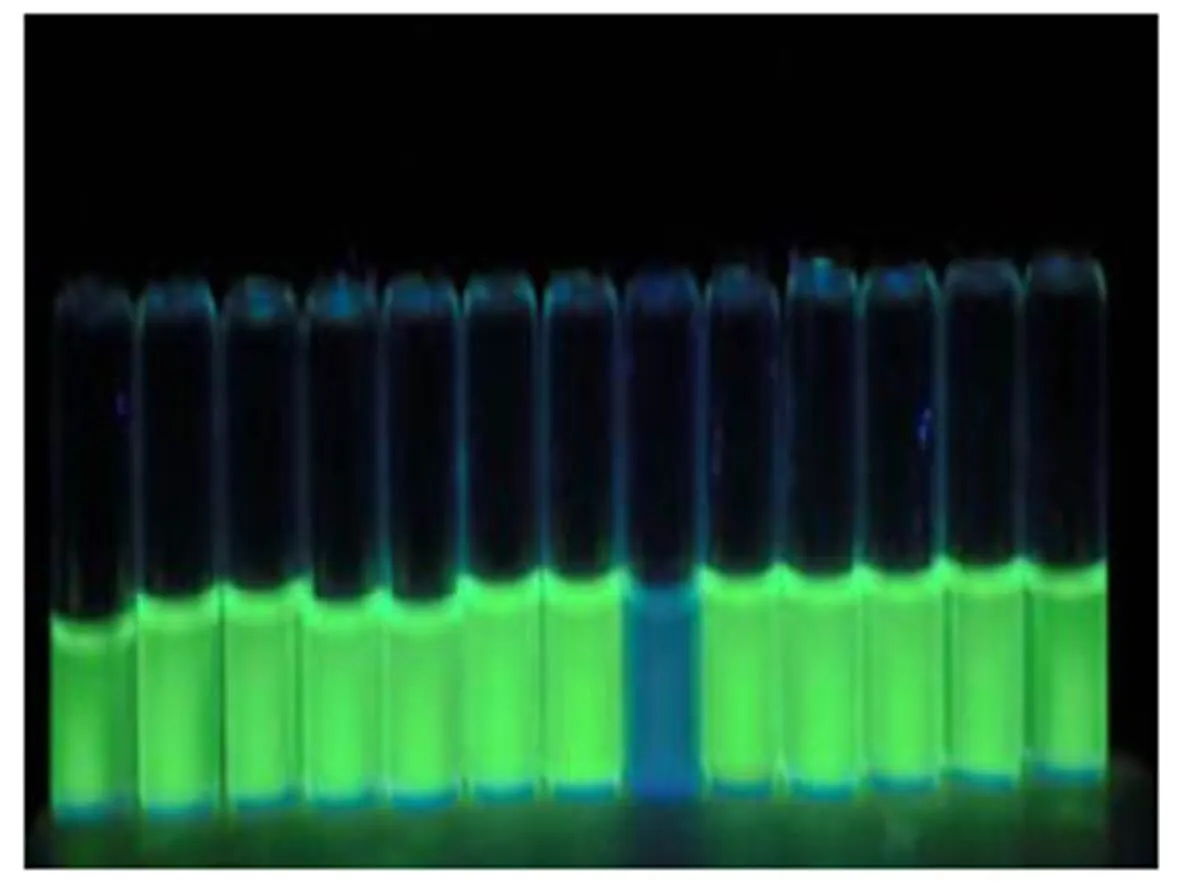
图6 分别加入各种离子后探针化合物3溶液(10 µM)在485 nm紫外灯照射下的颜色变化. 从左至右依次是Al3+、Ca2+、Co2+、Cr3+、Fe3+、K+、Mg2+、Cu2+、Na+、Ni2+、Zn2+、Hg2+、Ag+.
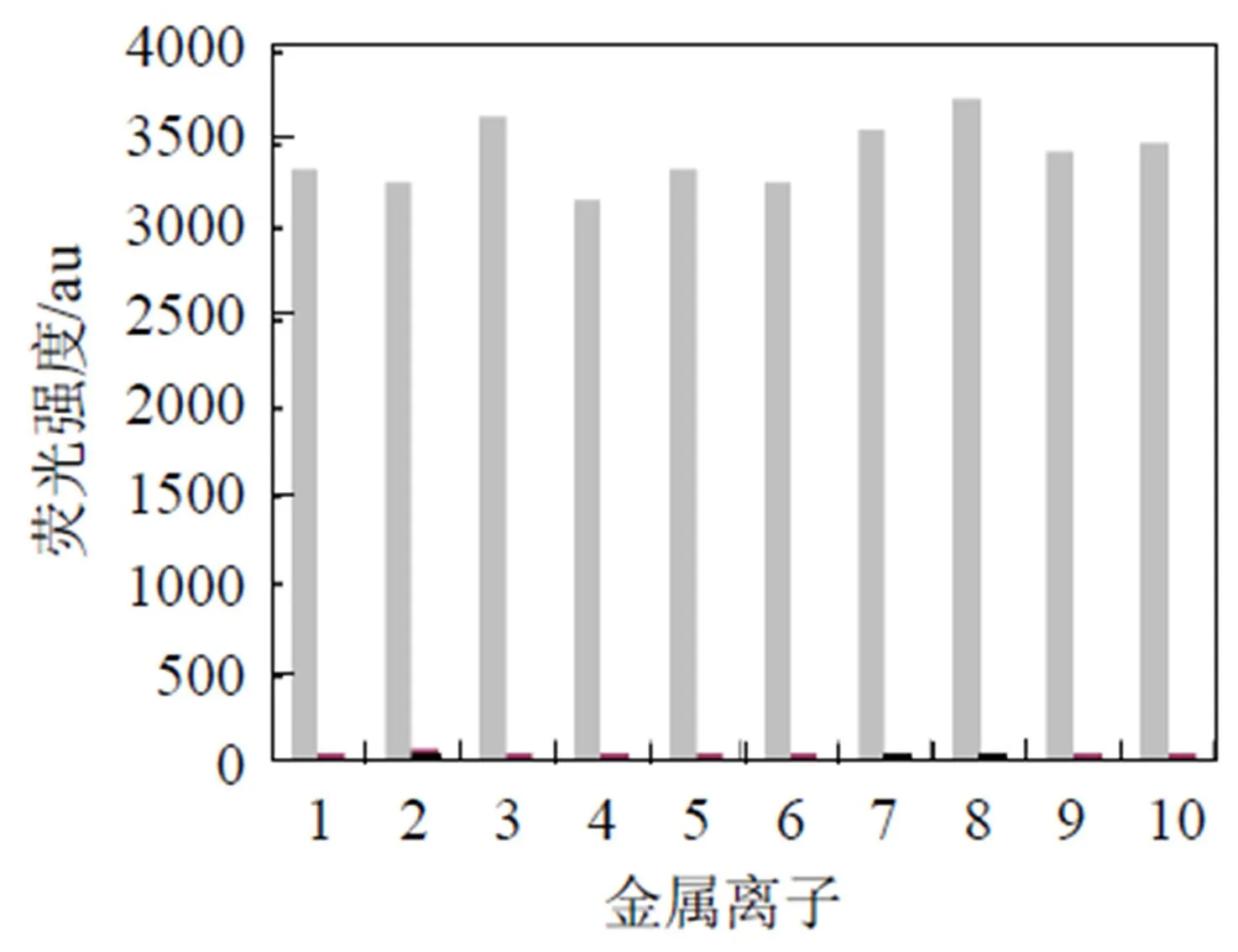
图7 探针化合物3(10 µM)对共存金属离子的抗干扰性. 从左至右依次是Al3+、Ca2+、Co2+、Cr3+、Fe3+、K+、Mg2+、Cu2+、Na+、Ni2+、Zn2+、Hg2+、Ag+.
3 结论
本工作设计合成了一种新型香豆素水合肼希夫碱探针, 该探针结构简单、易于合成, 同时对其结构用核磁共振光谱进行了表征. 在利用荧光光谱的测试中, 该探针具有高选择性检测Cu2+和较好的抗干扰能力.
[1] Fan C, Dai X, Yang W, et al. A quinoline derivated chemosensor for Cu2+recognition[J]. Chemical Research in Chinese Universities, 2009, 25( 5): 620—623.
[2] Li Y, Zhang X, Zhu B, et al. A simple but highly sensitive and selective colorimetric and fluorescent probe for Cu2+in aqueous media[J]. Analyst, 2011, 136: 1124—1128.
[3] Waggoner D J, Bartnikas T B, Gitlin J D, et al. The role of copper in neurodegenerative disease[J]. Neurobiol Dis, 1999, 6(4): 221—230.
[4] Vulpe C, Levinson B, Whitney S, et al. Isolation of a candidate gene for Menkes disease and evidence that it encodes a copper−transporting ATPase[J]. J Nat Genet, 1993, 3(1): 7—13.
[5] Lee, J C, Gray H B, Winkler J R. Copper(II) Binding to α-Synucleinthe Parkinson’s Protein[J]. J Am Chem Soc, 2008, 130(22): 6898—6899.
[6] Butler O T, Cook J M, Harrington C F, et al. Atomic spectrometry update. Environmental analysis[J]. J Anal At Spectrom, 2006, 21: 217—243.
[7] Li Y, Chen C, Li B, et al. Elimination efficiency of different reagents for the memory effect of mercury using ICP-MS[J]. J Anal At Spectrom, 2006, 21: 94—96.
[8] Lakowicz R J. Topics in Fluorescence Spectroscopy: Probe Design and Chemical Sensing[M]. New York: Kluwer Academic Publishers, 2002.
[9] De Silva A P, Gunaratne H Q N, Gunnlaugsson T, et al. Signaling Recognition Events with Fluorescent Sensors and Switches[J]. Chem Rev, 1997, 97(5): 1515—1566.
[10] Valeur B, Leray I. Design principles of fluorescent molecular sensors for cation recognition[J]. Coord Chem Rev, 2000, 205(1): 3—40.
[11] Li N, Xiang Y, Tong A. Highly sensitive and selective “turn-on” fluorescent chemodosimeter for Cu2+in water via Cu2+-promotedhydrolysis of lactone moiety in coumarin[J]. Chemical Communications, 2010, 46: 3363—3365.
[12] He G, Zhao X, Zhang X, et al. A turn-on PET fluorescence sensor for imaging Cu2+in living cells[J]. New Journal of Chemistry, 2010, 34: 1055—1058.
[13] Lü X, Liu J, Liu Y, et al. Ratiometric fluorescence detection of cyanide based on a hybrid coumarin-hemicyanine dye: the large emission shift and the high selectivity[J]. Chemical Communications, 2011, 47: 12843—12845.
Study on a coumarin hydrazine schiff base fluorescent probefor copper ion detection
SHEN You-ming1,2, LI Lin1, CHEN Chao-nan1, LIU Ming-di1, FENG Shao-dong1, ZHAO Jing1, ZHANG Xiang-yang1, ZHENG Qing-yun1, ZHANG Chun-xiang1
(1. Departement of Chemistry, Hunan University of Arts And Scince, Changde 415000, China; 2. Key Laboratory of Chemical Biology and Traditional Chinese Medicine Research of Ministry of Education, Hunan Normal University, Changsha 410081, China)
A novel coumarin derivative was synthesized facilely by the condensation reaction of coumarin and hydrazine hydrate, and its structure was characterized by1H NMR. The recognition properties of the target compound 3 with Cu2+had been investigated by the fluorescence spectrophotometry. The results showed that the probe 3exhibited the selective recognition of Cu2+. Upon addition of the concentration of Cu2+to the solution of compound 3, decreasing fluorescence was observed. The selective and interference of compound 3 were discussed. The fluorescence intensity of compound 3 was no chang when the compound 3 was joined other metal ion (such as Al3+、Ca2+、Co2+、Cr3+、Fe3+、K+、Mg2+、Na+、Ni2+、Zn2+, etc.). The interference was found,when other metal and Cu2+coexist in solution of compound 3. Experiments showed that probe 3 was selective recognition of Cu2+.
copper ion; coumarin; hydrazine hydrate; schiff base; fluorescence probe
10.3969/j.issn.1672-6146.2013.04.004
O 631.3
1672−6146(2013)04−0017−04
email: ymshen79@163.com.
2013-10-16
湖南省教育厅项目(11C0917); 湖南师范大学化学生物学及中药分析教育部重点实验室开放基金(KLCBTC MR 2011-05); 湖南文理学院大学生创新项目; 湖南文理学院博士启动基金; 湖南省十二五重点建设学科--应用化学资助.
(责任编校:刘晓霞)

