单纯性肥胖成人血浆纤维蛋白原与胰岛素抵抗的相关性研究
郑 青,黄娇珍,李国栋,钟祥旭,符先先,王永卿
随着社会经济的飞速发展和人民生活水平的提高,肥胖症的发病率呈逐年上升趋势,世界范围内有11亿人超重和肥胖,在一部分工业化国家,接近三分之二的人群超重或肥胖[1]。美国成人肥胖发生率为30%以上,女性则高达52.1%,并且增长速度较快[2]。在我国肥胖的发生率虽不足5%,但在一些城市中肥胖的发生率却高达20%[3]。单纯性肥胖是指没有发生明显的内分泌和代谢疾病的肥胖,Hotamisligil[4]首次提出,肥胖是由不同炎性因子诱导产生的一种全身性的慢性炎症性疾病,与糖尿病、高血压、冠心病、高血脂等密切相关。纤维蛋白原(fibrinogen,FIB)既是一种凝血因子,也是一种炎性标志物,是肝脏对循环白介素6(IL-6)产生应答而合成的急性期蛋白。胡怡等[5]研究发现,体质指数(body mass index,BMI)超标能够引起凝血方面的异常,并与肥胖程度呈正相关。但FIB与胰岛素抵抗(insulin resistance,IR)之间的关系,国内尚罕见报道。本研究通过检测FIB、血脂等生化指标,探讨单纯性肥胖成人FIB、血脂水平与IR的关系。
1 资料与方法
1.1一般资料所有受试者均来自海口市人民医院2012年9月—2013年3月体检人群。根据2002年世界卫生组织亚太地区肥胖诊断标准[6],选择单纯性肥胖成人78例,按BMI分为Ⅰ度肥胖组34例,BMI(25.0~29.9)kg/m2,男15例,女19例,平均年龄(37±9)岁;Ⅱ度肥胖组30例,BMI(30.0~34.9)kg/m2,男14例,女16例,平均年龄(37±7)岁;Ⅲ度肥胖组14例,BMI(35.0~40.0)kg/m2,男6例,女8例,平均年龄(38±10)岁。单纯性超重组35例,BMI(23.0~24.9)kg/m2,男19例,女16例,平均年龄(38±8)岁;健康对照组67例,BMI(18.5~22.9)kg/m2,男30例,女37例,平均年龄(37±8)岁。所有入选者均接受75 g口服葡萄糖耐量试验(OGTT),证实为正常糖耐量,同时,肝、肾功能正常,无心血管疾病,亦无其他引起肥胖的疾病,排除妊娠、哺乳期或长期口服避孕药者。各组在年龄、性别方面均衡,具有可比性。
1.2研究方法
1.2.1体格指标检测测量受试者身高、体质量、腰围(肋骨下缘至髂前上嵴之间连线的中点经线)、臀围(股骨粗隆水平经线),并计算BMI和腰臀比(waist-hip-ratio,WHR),BMI (kg/m2)=体质量/(身高)2,WHR=腰围/臀围。
1.2.2标本采集所有受试者均禁食8~12 h后于次晨空腹静脉采血8 ml,2支干燥试管各注入3 ml血液,用于检测生化指标及空腹胰岛素(FIN),1支1∶9枸橼酸钠抗凝全血2 ml,用于测定FIB,3 000 r/min(离心半径为14.2 cm)离心10 min分离上清,2 h内检测所有指标。
1.2.3相关指标检测血清总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)等生化指标均采用酶法,空腹血糖(FBG)采用葡萄糖氧化酶电极法,上述项目测定均采用美国贝克曼Dxc800型全自动生化分析仪及其配套试剂。血清FIN测定:电化学发光法,罗氏Cobas e601全自动电化学发光仪及其配套试剂。FIB测定:Sysmex CA-7000全自动血凝仪及其配套试剂。
1.3IR评估基础状态法:FBG与FIN比值作为胰岛素敏感指数,自我平衡模型分析法(homeostasis model assessment,HOMA)。HOMA-IR=(FIN×FBG)/22.5。
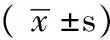
2 结果
2.1单纯性肥胖、超重与健康对照组的临床和实验室资料5组在BMI、WHR、FBG、FIN、HOMA-IR、TC、TG、HDL-C、LDL-C、FIB上差异均有统计学意义(P<0.01,见表1)。FBG、FIN、HOMA-IR、TC、TG、LDL-C、FIB水平随着BMI的升高呈逐渐上升的趋势,而HDL-C则逐渐降低(见图1)。
2.2各指标的相关性经Pearson相关性分析,FIB与BMI、WHR、FIN、FBG、HOMA-IR、TG、TC、LDL-C呈正相关(P<0.01),与HDL-C呈负相关(P<0.01);HOMA-IR与FIB、BMI、WHR、FIN、FBG、TG、TC、LDL-C呈正相关(P<0.01),与HDL-C呈负相关(P<0.01,见表2)。

表1 各组间临床及实验室资料比较
注:与健康对照组比较▲P<0.01;与Ⅰ度肥胖组比较△P<0.01,*P<0.05;BMI=体质指数,WHR=腰臀比,FBG=空腹血糖,FIN=空腹胰岛素,HOMA-IR=胰岛素抵抗指数,TC=总胆固醇,TG=三酰甘油,HDL-C=高密度脂蛋白胆固醇,LDL-C=低密度脂蛋白胆固醇,FIB=纤维蛋白原
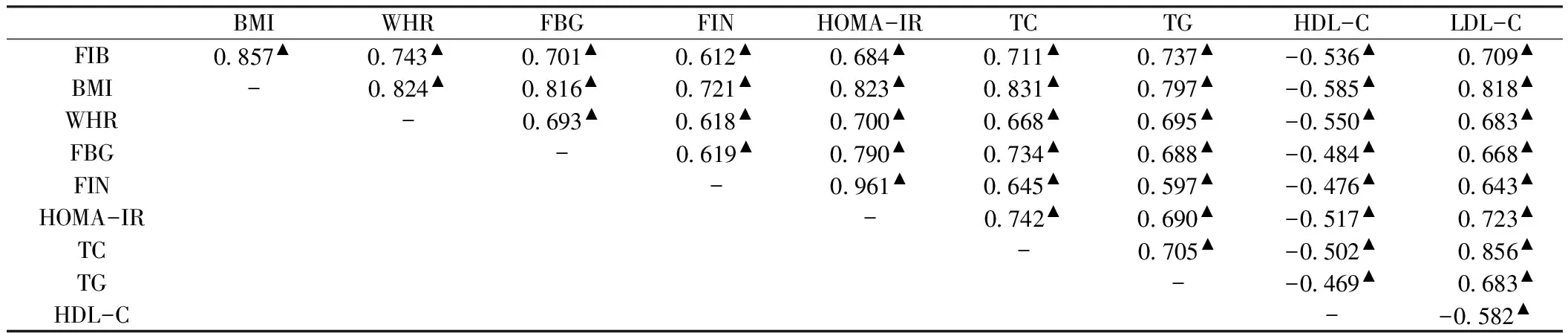
表2 受试者各指标相关性分析(r值)
注:▲P<0.01;-为无

图1 各指标均值水平趋势
2.3FIB和HOMA-IR的多元逐步回归分析分别以FIB和HOMA-IR为因变量,以BMI、HOMA-IR、FIN、FBG、血脂水平及FIB、BMI、FIN、FBG、血脂水平为自变量进行多元逐步回归分析,提示BMI、TG是影响FIB水平的独立危险因素,FIB、BMI、FIN 、FBG、LDL-C 是HOMA-IR的独立危险因素。见表3。

表3 FIB 和HOMA-IR的多元逐步回归分析
注:-为无数据
3 讨论
本研究显示,正常糖耐量单纯性肥胖成人,除脂代谢异常外(TG、TC、LDL-C明显升高,HDL-C明显下降),调节糖脂代谢的胰岛素水平亦出现明显异常,HOMA-IR与BMI呈正相关,多元逐步回归分析结果亦显示,BMI及LDL-C是HOMA-IR的独立危险因素,提示肥胖、血脂紊乱参与IR的发生发展,单纯性肥胖成人存在IR,与文献报道相符[7]。肥胖引起的IR以抑制肝脏葡萄糖输出和促进脂肪组织和肌肉葡萄糖摄取的胰岛素功能受损为特点[8],主要机制是:(1)慢性炎症机制介导IR。脂肪蓄积,尤其是内脏TG储存增加时,可引起释入血循环的游离脂肪酸(FFA)增多和到达脂肪细胞的氧量减少,二者共同作用诱导了脂肪细胞中缺氧诱导因子(HIF-1)及下游目的基因的激活和内质网应激,由此导致了脂肪细胞死亡和特异性的炎性反应,IL-6、肿瘤坏死因子ɑ(TNF-ɑ)、C反应蛋白(CRP)、FIB等炎性因子分泌增多,抑制胰岛素受体(IRS)正常的酪氨酸磷酸化,减弱了胰岛素的作用,引起肝脏、骨骼肌及脂肪组织的IR[9]。(2)氧化应激因素。活性氧自由基(ROS)过多,可以导致丝/苏氨酸激酶的活化,进而通过一系列下游信号转导,使机体对胰岛素敏感性下降。此外,氧化应激还通过抑制P13K p85亚基向质膜转运的激活,致葡萄糖转运体4(GLUT-4)表达下调、转运受阻,引发IR。(3)胰岛素信号传导障碍。糖原合成酶激酶-3(GSK-3)、磷脂酰肌醇-3激酶(PI3K)、磷酸酪氨酸磷酸酶1B(PTP1B)途径异常,均可使胰岛素刺激的组织细胞对葡萄糖的摄取发生障碍、糖原合成降低,进而导致IR。(4)肥胖使脂肪细胞数量增多,体积增大,导致其分泌激素的表达增强或减弱,从不同层次影响胰岛素的效应,导致IR。
FIB是由肝细胞合成和分泌的重要凝血因子,也是一种急性时相蛋白,是慢性炎症的标志物之一。胡怡等[5]研究发现,BMI超标能够引起凝血方面的异常,并与肥胖程度呈正相关。本研究亦证实:FIB随肥胖程度的增加而增长,与BMI呈正相关,BMI、TG是影响FIB的独立危险因素。Verschuur等[10]的动物实验研究发现,TG、TC水平较高的一组大鼠,其FIB半衰期较长,认为高血脂水平能引起血浆纤溶酶原激活物抑制剂(PAI-1)升高,从而降低纤溶酶原合成,影响FIB的清除,是FIB水平升高的关键。本研究亦发现:FIB与HOMA-IR呈正相关,并且是影响HOMA-IR的独立危险因素之一,提示FIB参与了IR的发生发展。FIB介导IR可能的机制是:(1)作为炎性因子,通过作用于胰岛素信号转导系统干扰IRS的信号转导,抑制IRS正常的酪氨酸磷酸化,减弱胰岛素的作用[8];另外能降低GLUT-4 mRNA表达水平[11],导致GLUT-4向细胞表面转运不足,从而使肌肉组织对胰岛素的刺激减弱,由此降低机体对葡萄糖的摄取能力而导致IR。(2)使内皮功能异常而导致IR,内皮功能紊乱致PAI-1增多,促使LDL-C氧化和巨噬细胞摄取氧化低密度脂蛋白,而陈晓春等[12]研究认为,FIB可诱导PAI-1 mRNA及抗原呈剂量和时间依赖性增长,PAI-1 基因表达增加,可激活NF-κB,进一步增加炎性基因的表达,与IR密切相关。朱旅云等[13]的研究亦证实:内皮功能障碍在IR的发生过程中具有重要意义。(3) FIB是肝脏对循环IL-6产生应答而合成的急性期蛋白。IL-6可使细胞因子信号抑制剂-3(SOCS-3)异位表达增加,诱导IRS的丝氨酸磷酸化,抑制IRS-1酪氨酸磷酸化及PI3K间接抑制胰岛素依赖的葡萄糖转运,抑制GLUT-4和PPAR-Y基因转录,使葡萄糖摄取减少,还能促进脂肪细胞降解,使FFA释放增加,间接诱导β细胞凋亡,使胰岛素分泌功能发生障碍[14]。
综上所述,单纯性肥胖成人较超重及体质量正常者存在更为严重的IR及高水平的FIB,FIB的过量表达参与并加重单纯性肥胖成人IR、血脂紊乱的发生和发展。
1Malena Monteverde,Kenya Noronha,Alberto Palloni,et al.Obesity and excess mortality among the elderly in the United States and Mexico [J].Demography,2010,47(1):79-96.
2Li C,Ford ES,McGuire LC,et al.Increasing trends in waist circumference and abdominal obesity among US adults[J].Obesity(Silver Spring),2007,15(1):216-224.
3邹大进,吴鸿.胰岛素抵抗与肥胖的关系认识[J].诊断学理论与实践,2009,8(3):237-239.
4Hotamisligil GS.Inflammatory pathways and insulin action[J].Int J Obes Relat Metab Disond,2003,27(Suppl 3):53-55.
5胡怡,陈思娇,李红燕,等.超重及肥胖对2型糖尿病患者凝血功能及代谢指标的影响研究[J].中国全科医学,2011,14(2):478-481.
6Choo V.WHO reassesses appropriate body-mass index for Asian population[J].Lancet,2002,360(9328):235.
7李国栋,郑青.单纯性肥胖成人血清高敏C反应蛋白、血脂水平与胰岛素抵抗的相关性研究[J].国际检验医学杂志,2011,33(17):1587-1589.
8Saltiel AR,Kahn CR.Insulin signalling and the regulation of glucose and lipid metabolism[J].Nature,2001,414(6865):799-806.
9张世卿,佟丽.胰岛素抵抗作用发生机制及实验模型的研究进展[J].中药新药与临床药理,2012,23(3):364-367.
10Verschuur M,Bekkers M,Van Erck MG,et al.Influnce of plasma triglyceride and plasma cholesterol levels on the clearance rate of fibrinogen [J].Ann N Y Acad Sci,2001,936:639-642.
11Loos RJ,Lindgren CM,Li S,et a1.Common variants near MC4R are associated with fat mass,weight and risk of obesity[J].Nature Genet,2008,40(6):768-775.
12陈晓春,黄春,蓝玉福,等.纤维蛋白原对内皮细胞t-PA 和PAI-1 mRNA 表达的影响[J].中华内科杂志,2000,39(5):305-308.
13朱旅云,胡丽叶,李晓玲,等.内皮功能障碍与胰岛素抵抗和肥胖关系研究的七年随诊观察[J].中国糖尿病杂志,2009,17(9):679-682.
14李林娟,樊霞.炎症因子与胰岛素抵抗的关系[J].医学信息,2011,24(3):331-332.

