柳氮磺胺吡啶中一个杂质的结构测定
姚旭波 沈莉 许爱红
(上海中西三维药业有限公司 上海 200331)
柳氮磺胺吡啶(sulfasalazine,1)作为一个使用历史悠久的传统药,有抗炎和抗菌的双重作用,口服后很少吸收,在肠壁中分解起治疗作用,多用于溃疡性结肠炎的治疗[1-2]。近年的许多资料表明,它还能抑制免疫复合物及类风湿因子的合成,从而对类风湿关节炎的免疫病理损伤发生影响[3-5]。该药用于治疗炎性肠病及类风湿关节炎已有40多年的历史。20世纪70年代后期的试验证明,该药可改善类风湿关节炎的临床症状并能使C反应蛋白和血沉有不同程度下降[6-7]。
柳氮磺胺吡啶是由磺胺吡啶和水杨酸经重氮偶合反应而合成的(图1)。

图1 1的合成路线
基于自由基机理的重氮偶合反应复杂、副产物多,因此柳氮磺胺吡啶成品所含杂质比较多,且通过后期的精制方法很难去除。我们在对本公司生产的柳氮磺胺吡啶原料药杂质进行研究时,发现其中一个未知杂质的含量在0.06%~0.08%之间。根据人用药物注册技术要求国际协调会议(ICH)技术指导原则的要求,对于柳氮磺胺吡啶这个日服用量超过6 g、未知杂质超过0.05%的药品必须确认结构。所以,我们分离提纯了这个杂质(2),并确定其结构。
1 仪器与试剂
1.1 仪器
AV500型核磁共振仪和micrOTOF II质谱仪(瑞士Bruker公司);Agilent 1200高效液相色谱仪(美国Agilent公司)。
1.2 试剂
1(上海中西三维药业有限公司,批号201204045,纯度97.7%);薄层色谱硅胶H(青岛海洋化工厂出品);甲醇为色谱纯,其它试剂均为分析纯,水为超纯水。
2 有关物质的分离与制备
2.1 色谱条件
按照欧洲药典EP7.7标准中的有关物质分析方法分析。色谱柱为以十八烷基硅烷键合硅胶(5 μm)为固定相的不锈钢柱,柱长25 cm×4.6 mm。检测波长320 nm,流速1.0 ml/min,柱温25 ℃,进样量20 µl。流动相A:pH 4.8的磷酸盐缓冲液(取磷酸二氢钠1.13 g和醋酸钠2.5 g,加水900 ml,用冰醋酸调pH至4.8,并用水稀释至1 000 ml);流动相B:流动相A-甲醇(10:40,v/v)的混合液。洗脱条件见表1。

表1 柳氮磺胺吡啶有关物质液相色谱流动相洗脱条件
2.2 方法与结果
取1适量,用稀氨溶液(氨水7.8 ml,加水稀释至1 000 ml)配制浓度为1 mg/ml的供试品溶液,进样量20 µl,记录色谱图。在上述色谱条件下,1主峰保留时间为23.070 min,杂质2的保留时间为15.862 min(图2)。
2.3 2的分离制备
取我公司柳氮磺胺吡啶的精制母液,溶剂经旋转蒸发浓缩至褐色黏稠液。取5 g溶于100 ml氯仿-丙酮-甲酸(60:20:2)的混合液中,再加入10 g薄层色谱硅胶H粉,混匀,置旋转蒸发仪上蒸除混合溶剂,得吸附了样品的混合硅胶H湿粉。将此湿粉放入鼓风烘箱内烘干,得吸附了样品的棕黄色混合硅胶H干粉,重约13 g。将此混合硅胶H干粉加入已装有薄层色谱硅胶H的色谱柱(5 cm×60 cm)中,用氯仿-丙酮-甲酸(60:20:2)洗脱(必要时可增加甲酸的比例),并用硅胶薄层色谱(以氯仿-丙酮-甲酸=60:30:5为展开剂,在紫外光254 nm下检视)跟踪检测洗脱液,收集Rf值约为0.45的洗脱液,将其中的溶剂蒸发除尽,得棕色油状物2的粗品。该粗品中尚混有残余的柳氮磺胺吡啶(Rf值约为0.7),需按上述方法经过反复几次柱层析,才能去除柳氮磺胺吡啶。最后得到浅黄色粉末状固体2,HPLC含量为99.3%。

图2 柳氮磺胺吡啶的有关物质色谱图
3 杂质2的结构解析
2在ESI质谱条件下的质谱主峰为m/z 482.096 2[M+H]+,与推测的分子式为C22H19N5O4S2的分子量481.087 8相符,可以确定2的分子式为C22H19N5O4S2。
从核磁共振氢谱和碳谱可以看出该结构是完全对称的结构(表2),存在两个对位取代的苯环和两个类似于吡啶环的结构。

表2 2的1H NMR、13C NMR和2D相关谱数据
在1H-1H COSY实验中,δH7.74和δH7.18相关,这8个氢可以确定为两个对位取代苯环上的氢;δH8.03与δH6.85相关,δH6.85同时又与δH7.66相关,δH7.66同时和δH7.09相关,根据化学位移和耦合常数规律,可以确定δH8.03为芳香环上N邻位的氢,即为H-6,6’,δH6.85 归属为 H-5,5’,δH7.66 归属为 H-4,4’,δH7.09 归属为 H-3,3’。
HSQC实验中,δH9.16和δH11.60的氢没有对应的相关碳的信号,可以确定为活泼氢的信号。δH9.16归属为H-14, δH11.60归属为H-13,13’,谱图中δH11.60的峰积分值偏小,是因为这个峰比较宽导致积分值不准确。
NOESY实验中δH9.16和δH7.18相关,可以确定δH7.18 为 H-9,9’,11,11’的信号 , 而 δH7.74 就可以确定为H-8,8’,12,12’的信号。
HSQC实验中,δH7.74与δC128.47相关,δC128.47归属为 C-8,8’,12,12’; δH7.18 与 δC116.27 相关,δC116.27 归属为 C-9,9’,11,11’; δH8.03 与 δC144.74 相关,δC144.74 归属为 C-6,6’; δH6.85 与 δC115.88 相关,δC115.88归属为C-5,5’;δH7.66与δC139.36相关,δC139.36归属为 C-4,4’;δH7.09与 δC113.06相关,δC113.06 归属为 C-3,3’。
HMBC 实验中,δH7.66和 δH8.03与 δC153.14相关,δC153.14归属为 C-2,2’;δH7.74与δC145.33相关,δC145.33归属为 C-10,10’;δH7.18与 δC132.75相关,δC132.75 归属为 C-7,7’。
综合以上信息,将2的结构解析为双{4-[(2-亚氨基吡啶-1(2H)-基)磺酰]苯基}胺(图3)。
致谢
本文中的质谱委托复旦大学检测,核磁共振谱委托上海医药集团中央研究院检测,结构解析得到了上海睿智化学研究公司的帮助,特此鸣谢。
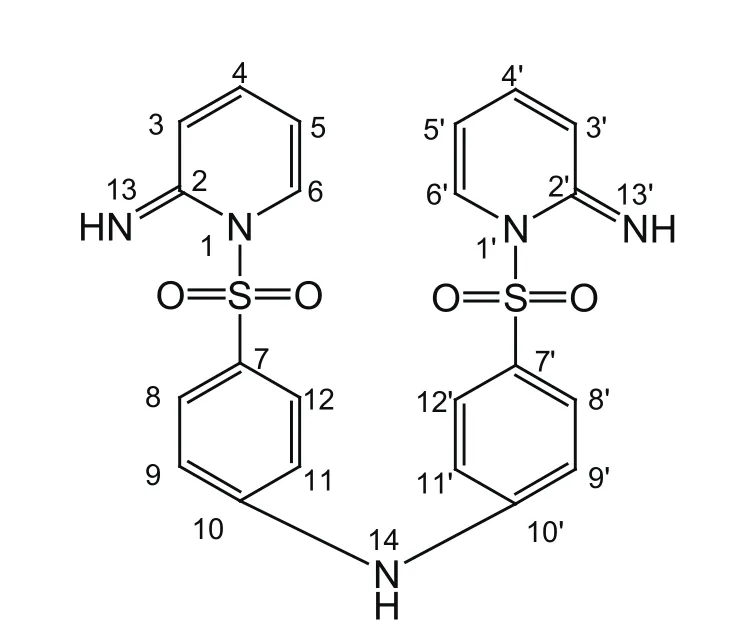
图3 2的化学结构
[1] Sircar JC, Schwender CF, Carethers ME. Inhibition of soybean lipoxygenase by sulfasalazine and 5-aminosalicylic acid: a possible mode of action in ulcerative colitis[J].Biochem Pharmacol, 1983, 32(1): 170-172.
[2] 濮永杰, 柳汝明, 唐尧. 奥沙拉嗪与柳氮磺吡啶治疗溃疡性结肠炎疗效与安全性的系统评价[J]. 中国药房, 2010,21(20): 1899-1902.
[3] Neumann VC, Grindulis KA. Sulfasalazine in rheumatoid arthritis: an old drug revived[J]. J R Soc Med, 1984, 77(3):169-172.
[4] Pullar T. Sulfasalazine and related drugs in rheumatoid arthritis [J]. Pharmacol Ther, 1989, 42(3): 459-468.
[5] Weinblatt ME, Reda D, Henderson W,et al. Sulfasalazine treatment for rheumatoid arthritis: a metaanalysis of 15 randomized trials [J]. J Rheumatol, 1999, 26(10): 2123-2130.
[6] 王鸣军, 陈志伟, 沈月平, 等. 来氟米特与柳氮磺吡啶治疗强直性脊柱炎疗效观察[J]. 苏州大学学报(医学版),2008, 28(2): 277-279.
[7] Chen J, Liu C. Is sulfasalazine effective in ankylosing spondylitis? A systematic review of randomized controlled trials[J]. J Rheumatol, 2006, 33(4): 722-731.

